Способ восстановления альфа-галогенкетонов до вторичных альфа-галогенспиртов
Иллюстрации
Показать всеИзобретение относится к способу получения α-галогенспирта общей формулы I, который применяется для получения эпоксидов. Способ получения включает стадию взаимодействия одного или более α-галогенкетонов общей формулы I
Формула I
где каждый из "X" независимо означает атом галогена за исключением фтора, атом водорода и "Z" означает атом галогена за исключением фтора; с молекулярным водородом в присутствии гетерогенного катализатора, содержащего переходный металл, где катализатор представляет собой соль металла, которой пропитан носитель катализатора, где металл включает иридий, рутений или их смесь, причем металл катализирует гидрирование по существу всех карбонильных групп α-галогенкетонов до спиртовых групп при температуре от 1 до 200°С и давлении, по меньшей мере, 14 абс.фунт/кв. дюйм с образованием одного или более α-галогенспирта общей формулы II
Формула II
.
Кроме того, изобретение относится к способу получения эпоксидов (варианты), к способу получения эпигалогенгидрина (варианты) и к способу получения пропиленоксида (варианты). 11 н. и 22 з.п. ф-лы, 3 табл.
Реферат
Настоящее изобретение относится к способу получения α-галогенспиртов из α-галогенкетонов. В частности, настоящее изобретение относится к способу синтеза α-галогенспиртов посредством гидрирования α-галогенкетонов, α-галогенспирты, полученные способом по настоящему изобретению, применяются для получения эпоксидов.
Существует множество кетонов, известных из уровня техники, и гидрирование кетонов не является чем-то необычным. Однако α-галогенкетоны по причине наличия неустойчивых связей галоген-углерод, являются более реакционно-способными, чем другие кетоны, и специалистам в данной области известно, что очень трудно осуществить селективное гидрирование α-галогенкетонов до α-галогенспиртов. Поэтому до сих пор существует необходимость в экономичном и эффективном способе гидрирования α-галогенкетонов.
α-галогенкетоны, известные из уровня техники, могут быть превращены в α-галогенспирты разнообразными известными способами. Например, в некоторых литературных ссылках описано восстановление α-галогенкетонов с использованием гомогенных каталитических систем. Например, патент США № 4024193 описывает способ гомогенного гидрирования с использованием активной формы рутенийтрифенилфосфина, представленного следующей формулой RuHCl(PR3)3, для восстановления активированных карбонильных соединений, включающих α-хлоркетоны, такие как 1,3-дихлорацетон и α-хлорацетофенон. Выходы и селективности реакций в патенте США № 4024193 не указаны.
Патент Японии № 63-297333 описывает способ получения 1,3-дихлор-2-пропанола из 1,3-дихлорацетона с использованием алюминийизопропоксида в качестве гомогенного катализатора с избытком изопропанола в качестве реагента переноса водорода. Селективности в 95 процентов или ниже могут быть получены при использовании способа по патенту Японии № 63-297333, но не может быть использовано количество алюминийизопропоксида менее 0,01 эквивалента.
Патент Японии № 09-104648 описывает способ гидрирования α-галогенкетонов, включающих α-хлоркетоны, такие как 1,3-дихлорацетон, с образованием 1,3-дихлор-2-пропанола при использовании гомогенного комплекса рутения, содержащего циклопентадиеноновый лиганд. При использовании способа по патенту Японии № 09-104648 достигаются селективности от 91 процента до 98 процентов в отношении 1,3-дихлор-2-пропанола и менее 10.000 обращений установлено при последовательном периодическом добавлении α-галогенкетона.
WO 9800375 A1 и EP 295890 A2 описывают способы асимметрического гидрирования α-галогенкетонов, таких как хлорацетон, с получением хиральных спиртов с использованием гомогенных комплексов рутения, иридия, родия, рения, кобальта, никеля, платины, палладия, содержащих хиральные лиганды.
Также хорошо известно, что α-галогенспирты используют для синтеза эпоксидов. Например, вышеупомянутые патент Японии № 09-104648 и патент Японии № 63-297333 описывают способ получения эпихлоргидрина способом, включающим три следующие стадии:
(1) α-хлорирование ацетона молекулярным хлором в присутствии иодсодержащего промотора и литийхлорида, приводящее к образованию 1,3-дихлорацетона;
(2) гидрирование 1,3-дихлорацетона в присутствии гомогенного катализатора, приводящее к образованию 1,3-дихлор-2-пропанола; и
(3) циклизацию 1,3-дихлорпропанола с основанием, приводящую к образованию эпихлоргидрина.
Ограничение всех вышеуказанных способов составляет потребность в гомогенном катализаторе для выполнения селективного восстановления α-галогенкетонов. Применение гомогенного катализатора в вышеуказанных способах ограничивает режимы работы реактора; а отделение катализатора и повторное использование составляют непростую задачу. Кроме того, желательно обеспечить гетерогенный катализатор, позволяющий выполнять восстановление α-галогенкетона с селективностями, сопоставимыми с восстановлением α-галогенкетона в присутствии гомогенных катализаторов, но обладающий дополнительными преимуществами при использовании на носителе, в гетерогенной форме. Желательно, чтобы гетерогенный катализатор позволял осуществлять способ восстановления с использованием катализатора без необходимости отделения катализатора.
Поэтому задача настоящего изобретения состоит в разработке технически выполнимого и легко регулируемого способа эффективного восстановления α-галогенкетона, приводящего к образованию α-галогенспирта, при использовании гетерогенного катализатора.
Другая задача настоящего изобретения состоит в разработке улучшенного способа гидрирования для получения α-галогенспиртов из α-галогенкетонов при использовании гетерогенного катализатора.
Также задачей настоящего способа является разработка такого способа, при котором используемые давления и температуры позволяют легко осуществлять эксплуатацию более экономичным образом.
Также к задачам настоящего изобретения относится развитие уровня техники; прочие задачи станут очевидны в дальнейшем.
Одним из аспектов настоящего изобретения является способ получения α-галогенспирта, включающего стадию взаимодействия α-галогенкетона с гидрирующим агентом, таким как элементарный водород, в присутствии гетерогенного катализатора, содержащего переходный металл, при таких условиях, в которых образуется α-галогенспирт.
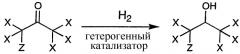
Способ по настоящему изобретению может быть представлен следующим общим уравнением:
Вторым аспектом настоящего изобретения является способ получения эпоксидов, включающий стадии:
(1) гидрирования α-галогенкетона с образованием α-галогенспирта, как указано в первом аспекте настоящего изобретения; и
(2) циклизацию α-галогенспиртов для получения эпоксидов.
Способ по настоящему изобретению основан на использовании гетерогенного катализатора, что таким образом упрощает режим работы реактора и облегчает отделение/повторное использование катализатора.
Один из ключевых аспектов настоящего изобретения состоит в обнаружении гетерогенного катализатора, который позволяет выполнять такое гидрирование селективно. Способ по настоящему изобретению также пригоден для синтеза эпоксидов из α-галогенспиртов.
В настоящее время α-галогенспирт может быть успешно и эффективно получен промышленно удобным способом и из легкодоступных материалов.
Катализатор, используемый в способе по настоящему изобретению, является твердым веществом и поэтому легко может быть выделен из реакционной смеси и легко отделен от продукта.
Способ по настоящему изобретению позволяет получать α-галогенспирты из α-галогенкетонов. α-галогенкетоны по настоящему изобретению представлены следующей формулой I.
Формула I
где каждый из "X" независимо означает атом галогена за исключением атома фтора, атом водорода или органическую группу и "Z" означает атом галогена за исключением атома фтора. 1,3-дихлорацетон является одним из примеров α-галогенкетона формулы I.
α-галогенспирты по настоящему изобретению представлены следующей формулой II.
Формула II
где каждый из "X" независимо означает атом галогена за исключением атома фтора, атом водорода или органическую группу и "Z" означает атом галогена за исключением атома фтора. 1,3-дихлор-2-пропанол является одним из примеров α-галогенспирта формулы II.
Примеры подходящих α-галогенкетонов, пригодных для настоящего изобретения, включают: 1-хлорацетон, 1,3-дихлорацетон; 1,3-дибромацетон; 1,1,3-трихлорацетон и их смеси. α-галогенкетоны, используемые по настоящему изобретению, наиболее предпочтительно означают 1,3-дигалогенацетон для получения 1,3-дигалоген-2-пропанола и 1-галогенацетон для получения 1-галоген-2-пропанола. 1,3-дигалогенацетон представлен следующей формулой.
Формула III
где каждый из "X" независимо означает галоген за исключением фтора. "X" в приведенной выше формуле III предпочтительно означает иод, хлор или бром и наиболее предпочтительно хлор.
Гидрирование α-галогенкетона осуществляют путем взаимодействия с гидрирующим агентом. Гидрирующим агентом, полезным по настоящему изобретению, может быть, например, молекулярный водород, спирт либо их комбинация. Гидрирующий агент означает предпочтительно молекулярный водород. Примерами подходящих спиртов, полезных по настоящему изобретению, могут служить первичные или вторичные спирты, такие как метанол, этанол и C3-C10- первичные или вторичные спирты. Предпочтительно спирт означает метанол. Примеры других вторичных спиртов, полезных по настоящему изобретению, описаны в патенте США № 2860146.
При взаимодействии по настоящему изобретению потребляется один моль гидрирующего агента на моль получаемого α-галогенспирта. Обычно, по меньшей мере, 0,6 молей гидрирующего агента на моль α-галогенкетона расходуется в ходе взаимодействия, предпочтительно, по меньшей мере, 0,75 молей гидрирующего агента на моль α-галогенкетона расходуется в ходе взаимодействия, еще предпочтительней, по меньшей мере, 0,9 молей и наиболее предпочтительно, по меньшей мере, 1 моль расходуется в ходе взаимодействия. Когда менее 1 моля гидрирующего агента на моль α-галогенкетона расходуется в ходе взаимодействия, полная конверсия α-галогенспирта достигнута быть не может. Однако не весь гидрирующий агент необходимо поставлять в начале взаимодействия. Гидрирующий агент можно добавлять постепенно или непрерывно по мере протекания реакции. В таком случае реакционная смесь в некоторый отдельный период времени может содержать стехиометрический избыток α-галогенкетона по отношению к гидрирующему агенту. В качестве одного из вариантов выполнения настоящего изобретения избыток требуемого гидрирующего агента может быть использован для завершения превращения α-галогенкетона в α-галогенспирт в ходе взаимодействия. Обычно, например, может быть использован избыток гидрирующего агента от 10 до 20 процентов.
Максимальное количество источника гидрирующего агента не играет решающей роли и определяется практическими соображениями, такими как давление, эффективность реактора и безопасность. Когда источник гидрирующего агента является газообразным, то количество гидрирующего агента предпочтительно должно быть, по меньшей мере, достаточным для обеспечения требуемого давления. Однако в большинстве случаев реактор предпочтительно содержит не более 1.000 молей молекулярного водорода на моль α-галогенкетона и более предпочтительно содержит не более 100 молей молекулярного водорода на моль α-галогенкетона. Газообразные источники гидрирующего агента, такие как молекулярный водород, предпочтительно используют согласно известным способам для смешивания газообразного реагента с жидкой реакционной смесью, таким как барботирование газа через смесь при перемешивании или растворение водорода под давлением.
Взаимодействие по настоящему изобретению происходит в присутствии гетерогенного катализатора, содержащего переходный металл. Переходным металлом, используемым в гетерогенном катализаторе по настоящему изобретению, может служить один или более металлов, выбираемых из групп IB, IIB или IIIA-VIIIA периодической таблицы элементов, как в настоящее время принято согласно Международному союзу теоретической и прикладной химии (ИЮПАК). Металлы катализатора, пригодные по настоящему изобретению, выбирают так, чтобы в условиях взаимодействия металлы катализировали гидрирование всех карбонильных групп молекулы α-галогенкетона до спиртовых групп, по существу не затрагивая галогены, связанные с молекулой α-галогенкетона. Металл катализатора предпочтительно выбирают из группы VIIIA принятой ИЮПАК периодической таблицы, включающей, например, железо, кобальт, никель, рутений, родий, палладий, осмий, иридий, платину и их смеси. Более предпочтительно металл катализатора выбирают из группы, включающей рутений, иридий, родий, палладий, платину и их смеси. Наиболее предпочтительно металл катализатора выбирают из группы, включающей рутений, иридий или их смеси.
Иллюстративным примером катализатора по настоящему изобретению могут служить, например, смешанные металлические катализаторы иридий/рутений, описанные в опубликованной европейской патентной заявке 1140751. Атомное соотношение металла иридия и металла рутения в катализаторе обычно составляет от 0,02 до 15, предпочтительно от 0,05 до 10, более предпочтительно от 0,15 до 8 и наиболее предпочтительно от 0,3 до 2,0.
Гетерогенным катализатором, полезным по настоящему изобретению, может служить, например, переходный металл, осажденный на нерастворимом носителе или адсорбированный нерастворимым носителем, таким как диоксид кремния, силилированный диоксид кремния, углерод, оксид алюминия, оксид титана, диоксид циркония, оксид магния и другие общепринятые носители, известные из уровня техники, как описано в Poncelet et al. editors, Preparation of Catalysts III, New York, 1983; P.N. Rylander, Hydrogenation Methods, Academic Press, London, 1985; P.N. Rylander, Catalytic Hydrogenation Over Platinum Metals, Academic Press, New York, 1967; P. Rylander, Catalytic Hydrogenation in Organic Syntheses, Academic Press, New York, 1979. Гетерогенным катализатором по настоящему изобретению может быть также переходный металл, координационно-связанный с лигандами, химически соединенными с полимерной смолой, например рутений на фосфинированном полистироле. Катализатор представлен обычно в форме гранул или таблеток. Количество активного катализатора на носителе составляет обычно от 0,1 процента (процентное) до 25 процентов и предпочтительно от 0,5 до 15 процентов.
Одно из преимуществ употребления гетерогенного катализатора в способе по настоящему изобретению состоит в возможности выделять катализатор из реакционного раствора различными способами, такими как фильтрация.
Идеальное соотношение катализатора и реагентов, используемых по настоящему способу, варьируется в зависимости от скорости потока, величины слоя, температуры, требуемой степени конверсии, реагентов и других факторов, определяющих данный способ. Обычно слой гетерогенного катализатора содержит от 0,0001 до 100 молей металла катализатора на каждый моль проходящего через слой α-галогенкетона в час.
Взаимодействие по настоящему изобретению необязательно, но предпочтительно осуществляют в присутствии растворителя. Используемый растворитель предпочтительно является инертным в отношении всех реагентов в условиях взаимодействия. Растворитель может быть выбран так, что: (1) растворитель не кипит в условиях взаимодействия, и (2) α-галогенспирт может быть выделен из растворителя, например, путем перегонки, экстракции или любыми другими известными способами выделения.
Примеры подходящих растворителей, пригодных по настоящему изобретению, включают ароматические и алифатические углеводороды, хлорированные углеводороды, простые эфиры, глимы, простые гликолевые эфиры, сложные эфиры, спирты, амиды и их смеси. Конкретные примеры растворителей, полезных по настоящему изобретению, включают толуол, циклогексан, гексан, метиленхлорид, диоксан, диметиловый эфир, диглим, 1,2-диметоксиэтан, этилацетат, метанол, NMP и их смеси. Количество растворителя, используемого по настоящему изобретению, не имеет решающего значения и определяется в первую очередь практическими соображениями, такими как эффективность реактора. Обычно количество растворителя, присутствующего в реакционной смеси, изменяется в пределах от 0 до 99,99 массовых процентов.
В наиболее предпочтительных случаях реакционная смесь по настоящему изобретению преимущественно содержит, по меньшей мере, 5 массовых процентов α-галогенкетона, желательно 10 массовых процентов и наиболее предпочтительно, по меньшей мере, 20 массовых процентов. Реакционная смесь может быть чистой (то есть реакционная смесь может содержать, по существу, 100 массовых процентов α-галогенкетона), но если используют растворитель в дополнение к α-галогенкетону, реакционная смесь предпочтительно содержит не более 90 массовых процентов α-галогенкетона и более желательно - не более 80 массовых процентов α-галогенкетона.
Когда реакционная смесь содержит спирт, взаимодействие предпочтительно осуществляют в условиях по существу отсутствия сильных минеральных кислот, таких как соляная кислота, которые могут приводить к снижению селективности и выходов. "По существу отсутствие" сильных минеральных кислот означает, что концентрация таких кислот является ниже достаточного уровня, так что кислоты не катализируют образование со значительными выходами кеталей из α-галогенкетона и спирта. Например, уровни кеталей, образующихся при катализируемом кислотой взаимодействии между α-галогенкетоном и спиртом в реакционной смеси могут быть обычно ниже 50 массовых процентов, предпочтительно ниже 20 массовых процентов и наиболее желательно ниже 1 процента.
Не вдаваясь в теоретическое обоснование, считается, что сильная кислота катализирует взаимодействие α-галогенкетона со спиртом, приводящее к образованию нежелательного кеталя. В случаях, когда реакционная смесь содержит незначительные количества соляной кислоты, предпочтительно осуществлять взаимодействие в присутствии акцептора кислоты, если в реакционной смеси присутствует спирт, для предупреждения образования кеталя.
Примеры подходящих акцепторов кислот, используемых по настоящему изобретению, включают: карбонаты щелочных металлов; бикарбонаты щелочных металлов; карбоксилаты щелочных металлов; аммоний- и фосфонийкарбоксилаты, бикарбонаты и карбонаты; эпоксиды и смеси указанных соединений. Конкретные примеры акцепторов кислот включают карбонат натрия, бикарбонат натрия, аммонийбикарбонат, этиленоксид, пропиленоксид, бутиленоксид, эпихлоргидрин и их смеси. Эпихлоргидрин является предпочтительным эпоксидом, служащим акцептором кислоты.
Температура взаимодействия не имеет решающего значения при условии, что все реагенты и катализатор находятся в тесном контакте друг с другом. Однако низкие температуры требуют более длительного осуществления реакции. Реакционная температура составляет предпочтительно, по меньшей мере, -10°C, более предпочтительно, по меньшей мере, 20°C и наиболее предпочтительно, по меньшей мере, 50°C. Температура реакции составляет предпочтительно ниже 250°C, более предпочтительно не выше 150°C и наиболее предпочтительно не выше 120°C. Температура реакции предпочтительно составляет от 0 до 200°C и более предпочтительно от 50 до 120°C.
Давление реакции не имеет решающего значения до тех пор, пока обеспечивается достаточное количество гидрирующего агента, такого как водород, для протекания взаимодействия в реакционной смеси. Давление составляет предпочтительно, по меньшей мере, 14 фунтов на квадратный дюйм в абсолютном значении (абс.фунт/кв.дюйм) (97 килоПаскалей (кПа), 1 атмосфера) и более предпочтительно, по меньшей мере, 50 абс.фунт/кв.дюйм (340 кПа, 3,4 атмосферы). Давление предпочтительно составляет не выше 3.000 абс.фунт/кв.дюйм (21 МПа, 204 атмосферы). Увеличение давления ведет к сокращению времени взаимодействия.
Обычно время взаимодействия при реакции гидрирования по настоящему изобретению составляет менее 72.000 секунд и преимущественно от 36.000 до 180 секунд достаточно для достижения конверсии, близкой к теоретической, 1 грамма α-галогенкетона до α-галогенспирта на грамм катализатора.
В предпочтительных технологических условиях α-галогенкетоны каталитически взаимодействуют с избытком водорода при температуре от 0 до 200°C за время взаимодействия от 36.000 до 180 секунд для 1 грамма α-галогенкетона на грамм катализатора с последующим выделением требуемого продукта реакции.
Продуктом взаимодействия по данному изобретению является α-галогенспирт со структурой, производной от α-галогенкетона. Продукт может быть выделен известными способами, такими как экстракция или перегонка. Продукт может быть выделен с такими низкими выходами, как 2 процента, однако в экономических целях продукт обычно выделяют, по меньшей мере, с 60 процентными выходами (в расчете на исходное количество α-галогенкетона) и предпочтительно выделяют, по меньшей мере, с 80 процентными выходами, более предпочтительно, по меньшей мере, с 90 процентными выходами и наиболее предпочтительно, по меньшей мере, с 95 процентными выходами.
α-галогенспирт, полученный способом по настоящему изобретению, является важным промежуточным продуктом реакции. Способ получения α-галогенспирта по настоящему изобретению составляет, в частности, полезную стадию общего способа получения эпоксидов. Сразу после получения α-галогенспирта с использованием реакции восстановления/гидрирования по настоящему изобретению α-галогенспирт может быть циклизован с целью получения эпоксида хорошо известными из уровня техники способами. Например, α-галогенспирты используются для получения эпоксидов путем обработки α-галогенспирта основанием. Поэтому настоящее изобретение может быть использовано для способа синтеза эпоксидов, таких как эпихлоргидрин и пропиленоксид, например, общепринятым способом, включающим следующие стадии:
(1) гидрирование α-галогенкетона с образованием α-галогенспирта и
(2) циклизацию α-галогенспирта под действием основания, приводящую к образованию эпоксида.
По другому варианту получения эпоксида перед стадией гидрирования α-галогенкетон может быть получен галогенированием кетона, приводящим к образованию α-галогенкетона.
Ключевой стадией способа по настоящему изобретению является селективное гидрирование α-галогенкетона до α-галогенспирта, осуществляемое так, что связи углерод-хлор α-галогенкетона остаются незатронутыми в ходе гидрирования.
В частности, способ по настоящему изобретению может быть использован в качестве одной из стадий способа получения, например, эпигалогенгидрина или пропиленоксида из ацетона. В качестве иллюстрации способа, например, способ получения эпигалогенгидрина может быть подробно представлен следующим образом.
На стадии (1) способа получения эпигалогенгидрина ацетон галогенируют, получая 1,3-дигалогенацетон. Эта стадия получения 1,3-дихлорацетона описана, например, в патенте США № 4251467 и JP 9255615.
На стадии (2) способа по настоящему изобретению 1,3-дигалогенацетон гидрируют с образованием 1,3-дигалоген-2-пропанола. Предпочтительные варианты выполнения такой стадии (2) описаны в настоящей заявке выше. Например, один из вариантов выполнения способа по настоящему изобретению включает стадию взаимодействия 1,3-дигалогенацетона, по меньшей мере, со стехиометрическим количеством молекулярного водорода в присутствии рутенийсодержащего, иридийсодержащего или смешанного рутений-иридий-металлсодержащего катализатора и соответствующего растворителя, такого как диоксан, что приводит к образованию 1,3-дигалоген-2-пропанола.
На стадии (3) рассматриваемого способа 1,3-дигалоген-2-пропанол превращают в эпигалогенгидрин. Такая стадия (3) хорошо известна в области получения эпигалогенгидрина. Реакционную стадию (3) обычно осуществляют путем взаимодействия 1,3-дигалоген-2-пропанола с сильным основанием, таким как водный гидроксид щелочного металла, включая, например, гидроксид натрия. Примеры взаимодействия на стадии (3) описаны в патенте США № 2860146 и в патенте Австралии № 630238.
Способы получения эпоксидов с использованием настоящего изобретения могут содержать в дополнение к стадии (2) одну или более из вышеуказанных стадий (1), (2) и (3). Способы получения эпоксидов предпочтительно включают стадии (1) и (2), более предпочтительно включают стадии (1), (2) и (3).
В способах получения эпоксидов, таких как эпигалогенгидрин или пропиленоксид, можно исходить из смеси, содержащей α-галогенкетон вместе с другими кетонами, изомерами или реагентами. В таких случаях предпочтительно, чтобы выбранный α-галогенкетон, такой как 1,3-дигалогенацетон для получения эпигалогенгидрина или такой как 1-галогенацетон для получения пропиленоксида, был преимущественным кетоном и чтобы преимущественно образующимся продуктом являлся эпигалогенгидрин или пропиленоксид соответственно. Поскольку существует возможность, что образующийся продукт будет представлять собой смесь эпигалогенгидрина и пропиленоксида, желательно регулировать количества используемых в способах α-галогенкетонов, чтобы обеспечить требуемый продукт в достаточном количестве. Под "преимущественным" здесь понимается, что требуемый продукт присутствует в количестве свыше 50 массовых процентов или более в смеси двух основных α-галогенкетоновых компонентов и свыше 40 массовых процентов или более в смеси из трех основных α-галогенкетоновых компонентов. Например, при смеси исходных соединений, такой как 70 процентов 1,3-дигалогенацетонов и 30 процентов 1-галогенацетона, продукт будет содержать по существу 1,3-дигалоген-2-пропанол.
Следующие примеры приведены исключительно в иллюстративных целях и не могут рассматриваться как ограничивающие рамки объема настоящего описания или приложенных пунктов. Если не оговорено особо, все части и проценты являются массовыми.
Общие экспериментальные методики
Синтез катализатора: катализаторы получают, пропитывая диоксид кремния водными растворами солей металлов, содержащими IrCl3·3H2O и RuCl3·H2O. Системы смешанных металлов получают совместной пропиткой диоксида кремния двумя солями металлов или пропиткой солью одного металла (и высушиванием) с последующей пропиткой солью другого металла. Катализаторы сушат на воздухе и затем предварительно восстанавливают в токе H2/N2 (5 процентный водород) при 473K (200°C). После чего катализаторы хранят и обрабатывают на воздухе.
Система реактора A: реактор включает резервуар в виде трубы 6,35E-3 м Ч 3,05E-1 м (0,25 дюйма Ч 12 дюймов) из Hastelloy сплава, обернутой ленточным электронагревательным элементом и изоляционным материалом, водокольцевой насос и два регулятора расхода, обеспечивающие подачу 3,55E6 Па (500 фунтов на квадратный дюйм, калиброванное (psig)) водорода и азота. Исходная смесь газообразного и жидкого сырья поступает в реактор со дна и выходит через верхнюю часть; после чего сырьевая смесь поступает через регулятор давления всасывания в систему отбора при давлении окружающей среды и затем в каустический скруббер.
Действие реактора А: катализатор загружают в реактор, удаляя выпускной трубопровод реактора при сброшенном давлении, добавляют 7,5E-7 м3 Sigma стеклянных бус (425-600 микрон, промытых кислотой), затем в резервуар добавляют 1E-3 кг катализатора и в реактор добавляют еще 7,5E-7 м3 стеклянных бус. Подсоединяют выпускной трубопровод и реактор продувают азотом при давлении окружающей среды в течение одного часа, затем реактор нагревают до 358K (85°C). После чего реактор наполняют водородом до давления 3,55E6 Па (500 фунт на кв. дюйм, к.) и спустя 1/2 часа начинают подачу жидкости.
Описание системы реактора B и действие: в этом случае используют резервуар реактора Парра из Hastelloy C сплава емкостью 300 мл. В реактор вносят загрузку катализатора и резервуар реактора вакуумируют и трижды продувают азотом. Смесь растворитель/α-галогенкетон дегазируют, барботируя азот, и добавляют в реактор Парра с помощью шприца. В реактор впускают/выпускают азот до давления 250/20 фунт на кв. дюйм, к. (1,8 мПа/241 кПа) и водород до давления 100/20 фунт на кв. дюйм, к. (793 кПа/241 кПа), затем оставляют под давлением водорода 100 фунт на кв. дюйм, к. (793 кПа) и нагревают до 35°C. Пробы отбирают шприцом после снижения давления реактора до величины менее 15 фунт на кв. дюйм, к. (207 кПа).
Анализ: пробы анализируют методом газовой хроматографии (ГХ), используя Hewlett Packard HP-6890 газовый хроматограф, оборудованный 30 м Rtx-5 капиллярной колонкой с щелевой инжекцией. Приблизительно 120 мкл реакционной смеси растворяют в 5E-6 м3 (5 мл) o-дихлорбензола, содержащего известное количество хлорбензола в качестве ГХ-стандарта (обычно 0,05 массовых процента). "Селективность" определяют как отношение α-галогенспирта к полученным комбинированным продуктам.
Пример 1
Пример 1 демонстрирует действие катализатора 8 процентный Ir/2 процентный Ru/диоксид кремния в отношении гидрирования 1,3-дихлорацетона.
В реакторе A, в реактор загружают, как описано выше в общих экспериментальных методиках, 1,0 г катализатора 8 процентный Ir/2,0 процентный Ru/диоксид кремния. Получают жидкое сырье, состоящее из смеси 10,2 массовых процента 1,3- дихлорацетона/диоксан, и барботируют азотом. Скорость подачи составляет 2,2E-9 м3/с (0,132 куб.см/минута), что соответствует времени взаимодействия 4,440 секунд, как указано ранее. Как указано в общих экспериментальных методиках, 85°C и 500 фунт на кв. дюйм, к. (3,55E6 Па) H2 составляют стандартные условия взаимодействия. В течение 80,5 часов периодически отбирают пробы реакционной смеси и анализируют. Результаты анализа представлены в приведенной ниже таблице I, где "селективность" определяется как отношение 1,3-дихлор-2-пропанола к полученным комбинированным продуктам.
| Таблица I | ||
| Анализ ГХ | ||
| Время (минуты) | Конверсия в процентах | Селективность в процентах |
| 1,5000 | 100,00 | 95,000 |
| 5,2500 | 100,00 | 94,000 |
| 21,420 | 100,00 | 94,000 |
| 28,000 | 100,00 | 94,000 |
| 47,000 | 100,00 | 94,000 |
| 80,500 | 99,000 | 93,000 |
Пример 2
Пример 2 демонстрирует действие катализатора 8 процентный Ir/2 процентный Ru/диоксид кремния в отношении гидрирования 1-хлорацетона.
В реакторе A, в реактор загружают, как описано выше в общих экспериментальных методиках, 1,0 г катализатора 8,0 процентный Ir/2,0 процентный Ru/диоксид кремния. Получают жидкое сырье, состоящее из смеси 7,1 массовых процентов 1-хлорацетона/диоксан, и барботируют азотом. Скорость подачи составляет 3,0E-9 м3/с (0,182 куб.см/минута), что соответствует времени взаимодействия 4,675 секунд. Как указано в общих экспериментальных методиках, 85°C и 500 фунт на кв. дюйм, к. (3,55E6 Па) H2 составляют стандартные условия взаимодействия. В течение 68,25 часов периодически отбирают пробы реакционной смеси и анализируют. Результаты анализа представлены в приведенной ниже таблице II, где "селективность" определяется как отношение 1-хлор-2-пропанола к полученным комбинированным продуктам.
| Таблица II | ||
| Анализ ГХ | ||
| Время (минуты) | Конверсия в процентах | Селективность в процентах |
| 2,2500 | 100,00 | 95,000 |
| 4,2500 | 100,00 | 95,000 |
| 21,330 | 100,00 | 95,000 |
| 26,000 | 100,00 | 93,000 |
| 51,000 | 100,00 | 93,000 |
| 68,250 | 100,00 | 94,000 |
Пример 3
Пример 3 дает возможность сравнения гетерогенного катализатора на основе оксида платины (Pt) (катализатор Adams'а) с катализатором 8 процентный Ir/2 процентный Ru/диоксид кремния. Катализатор Adams'а описан ранее в патенте США № 3189656 для гидрирования 1,3-дихлор-1,1,3,3-тетрафторацетона до 1,3-дихлор-l,1,3,3-тетрафтор-2-пропанола.
В реактор B загружают либо 0,025 г катализатора Adams'а, либо 0,25 г катализатора 8 процентный Ir/2 процентный Ru/диоксид кремния и резервуар реактора вакуумируют и трижды продувают азотом. 1,3-дихлорацетон (2,5 г), растворенный в 1,4-диоксане (50 мл), дегазируют, барботируя азот, и добавляют в реактор Парра с помощью шприца. В реактор впускают/выпускают азот до давления 250/20 фунт на кв. дюйм, к. (1,8 мПа/241 кПа) и водород до давления 100/20 фунт на кв. дюйм, к. (793 кПа/241 кПа), затем оставляют под давлением водорода 100 фунт на кв. дюйм, к. (793 кПа) и нагревают до 35°C. После 8 часов взаимодействия пробу отбирают шприцем и анализируют ГХ после снижения давления реактора до величины менее 15 фунт на кв. дюйм, к. (207 кПа). Результаты анализа для данного примера 3 приведены ниже в таблице III. Приведенные в таблице III результаты демонстрируют, что катализатор Adams'а хуже по сравнению с катализатором 8 процентный Ir/2 процентный Ru/диоксид кремния по настоящему изобретению, предназначенным для гидрирования не содержащих фтор α-галогенкетонов, таких как 1,3-дихлорацетон.
| Таблица III | |||
| Анализ ГХ | |||
| Катализатор | Конверсия в процентах1,3-дихлорацетона | Выход в процентах1,3-дихлор-2-пропанола | Селективность в процентах в отношении1,3-дихлор-2-пропанола |
| Пример сравнения А: оксид Pt (катализатор Adams'а) | 38,7 процента | 3,0 процента | 7,8 процента |
| 8 процентный Ir/2 процентный Ru/диоксид кремния | 16,2 процента | 11,6 процента | 71,6 процента |
1. Способ получения α-галогенспирта, включающий стадию взаимодействия одного или более α-галогенкетонов следующей общей формулы I:
где каждый из "X" независимо означает атом галогена, за исключением фтора, атом водорода и "Z" означает атом галогена, за исключением фтора; с молекулярным водородом в присутствии гетерогенного катализатора, содержащего переходный металл, где катализатор представляет собой соль металла, которой пропитан носитель катализатора, где металл включает иридий, рутений или их смесь, причем металл катализирует гидрирование по существу всех карбонильных групп α-галогенкетонов до спиртовых групп, при температуре от 1 до 200°С и давлении по меньшей мере 14 абс.фунт/кв. дюйм с образованием одного или более α-галогенспирта следующей общей формулы II:
где каждый из "X" независимо означает атом галогена, за исключением фтора, атом водорода и "Z" означает атом галогена, за исключением фтора.
2. Способ по п.1, где α-галогенкетон выбирают из группы, включающей 1,3-дихлорацетон; 1,3-дибромацетон; 1-бром-3-хлорацетон; 1-хлорацетон, 1-бромацетон или их смеси.
3. Способ по п.1, где α-галогенкетон означает 1,3-дихлорацетон, и образующимся α-галогенспиртом является 1,3-дихлор-2-пропанол.
4. Способ по п.1, где α-галогенкетон означает 1-хлорацетон, и образующимся α-галогенспиртом является 1-хлор-2-пропанол.
5. Способ по п.4, где соотношение молекулярного водорода и α-галогенкетона равно, по меньшей мере, 0,75:1.
6. Способ по п.4, где соотношение молекулярного водорода и α-галогенкетона равно, по меньшей мере, 0,6:1.
7. Способ по п.1, где катализатор содержит иридий и рутений при атомном отношении иридия к рутению от 0,02 до 15.
8. Способ по п.7, где атомное отношение иридия к рутению составляет от 0,15 до 8.
9. Способ по п.8, где атомное отношение иридия к рутению составляет от 0,3 до 2.
10. Способ по п.1, где катализатор включает промотор-ион металла группы I или переходного металла.
11. Способ по п.10, где промотор-ион выбирают из группы, в основном состоящей из Li, Na, К, Cs, Mo, W, V, Re, Mn и их смесей.
12. Способ по п.1, где катализатор дополнительно содержит координационно-связывающий лиганд.
13. Способ по п.12, где лиганд выбирают из группы, в основном состоящей из фосфинов, 1,5-циклооктадиена (COD), арсинов, стибинов, моноксида углерода, простых эфиров, циклопентадиенила, сульфоксидов, ароматических аминов и их смесей.
14. Способ по п.13, где лиганд означает фосфин.
15. Способ по п.1, где гетерогенный катализатор нанесен на носитель, выбранный из группы, в основном состоящей из углерода, диоксида кремния, оксида алюминия, оксида титана, диоксида циркония, сшитого полистирола и их комбинаций.
16. Способ по п.1, где гетерогенный катализатор существует в форме слоя гетерогенного катализатора в реакторе и где гетерогенный катализатор присутствует в реакционной смеси при соотношении от 0,0001 до 100 молей металла катализатора на каждый моль проходящего через слой α-галогенспирта в час.
17. Способ по п.1, где реакционная смесь дополнительно содержит растворитель.
18. Способ по п.17, где растворитель выбирают из группы, в основном состоящей из ароматических углеводородов, алифатических углеводородов, хлорированных углеводородов, простых эфиров, глимов, простых гликолевых эфиров, сложных эфиров, спиртов, амидов, воды и их смесей.
19. Способ по п.17, в котором присутствует раст