Способ получения солей 5'-трифосфатов дезоксирибо- и рибоолигонуклеотидов
Иллюстрации
Показать всеИзобретение относится к способу получения солей 5'-трифосфатов дезоксирибо- и рибоолигонуклеотидов общей формулы, указанной в описании. Исходный реагент тетраалкиламмониевую или триалкиламмониевую соль 5'-монофосфата дезокси- или рибоолигонуклеотида в виде 0,1-0,5 М раствора активируют в среде растворителя, представляющего смесь диметилсульфоксида и диметилформамида в соотношении 2:1, пяти-пятнадцатикратным избытком окислительно-восстановительной смеси трифенилфосфина и дипиридилдисульфида, взятых в соотношении 1:1, в присутствии 50-80 кратного избытка 1-метилимидазола или N,N-диметиламинопиридина в течение 5-10 минут, а далее добавляют 10-20 кратный избыток раствора бис-трибутиламмонийной соли пирофосфата в ацетонитриле и выдерживают реакционную смесь в течение 15-30 минут с последующим выделением и очисткой целевого продукта. Способ обеспечивает повышение выхода целевых продуктов, сокращение избытка используемых реагентов и объемов растворителей. 1 ил., 3 табл.
Реферат
Изобретение относится к области биоорганической химии, в частности к усовершенствованному способу получения 5'-трифосфатов дезоксирибо- и рибоолигонуклеотидов общей формулы:
где В - Thy, Ade, Cyt, Gua, Ura или другое гетероциклическое основание;
R - Н или ОН;
n-≥1.
5'-Трифосфаты дезоксирибо- и рибоолигонуклеотидов применяются в молекулярно-биологических и генно-инженерных исследованиях, однако коммерчески малодоступны из-за отсутствия универсального и эффективного способа синтеза этих соединений. Доступность 5'-трифосфатов дезоксирибо- и рибоолигонуклеотидов позволит широко использовать эти соединения при изучении процессов нуклеинового обмена (например, процессинга пре-мРНК).
Известен способ получения 5'-трифосфатов рибодинуклеотидов (Tomasz J., Simoncsits A., Kajtar M., Krug R.M., Shatkin A.J. // Nucleic Acids Res. 1978. V.5. P.2945-2957), заключающийся в обработке исходного рибодинуклеозид(3'-5"')фосфата хлорокисью фосфора с последующей обработкой водным аммиаком (введение первого фосфата и образование активированного монофосфорилированного производного). Полученный 5'-моноамидофосфат рибодинуклеозид(3'-5')фосфата обрабатывают пирофосфатом с целью получения трифосфатного производного.
Недостатком этого способа является то, что при обработке исходного динуклеотида хлорокисью фосфора на первой стадии синтеза происходит полная изомеризация межнуклеотидной фосфодиэфирной связи с образованием смеси 2'(3')-5'-фосфодиэфирных связей, что снижает выход целевого соединения в 2 раза и усложняет процедуру его очистки.
Известен также способ получения 2',5'-триаденилил-5'-трифосфата (Seto Y., Abe К., Itoh M., Sawai H. // 2002. Bioconjugate Chem. V.13. Р.303-308), заключающийся в полимеризации имидазолида 5'-аденилилфосфата в присутствии ионов Pb2+ с последующим получением 5'-трифосфатного производного олигорибонуклеотида ферментативным путем.
Недостатком этого способа является то, что он не пригоден для получения 5'-трифосфатов олигорибонуклеотидов с природными 3'-5'-фосфодиэфирными связями. Кроме того, с помощью указанного способа можно синтезировать только производные аденозина.
Наиболее ближайшим к заявляемому способу - прототипом, является способ получения 5'-трифосфатов дезоксиолигонуклеотидов (Lebedev A.V., Koukhareva I.I., Beck Т., Vaghen M.M. Preparation ofoligodeoxynucleotide 5'-triphosphates using solid support approach. // Nucleosides, Nucleotldes and Nucleic Acids. 2001. V.20(4-7). P.1403-1409), заключающийся в следующем. На первой стадии в дезоксиолигонуклеотид вводят первый фосфат с одновременным получением активированного монофосфорилированного производного дезоксиолигонуклеотида, для чего соответствующим образом защищенный дезоксиолигонуклеотид (защитные группы на гетероциклических основаниях нуклеозидов и межнуклеотидных фосфатных группах, свободная 5'-оксигруппа дезоксиолигонуклеотидной цепи), ковалентно связанный с носителем в процессе твердофазного синтеза олигонуклеотидов, обрабатывают раствором 2-хлоро-4Н1,3,2-бензодиоксафосфорин-4-она в смеси 1,4-диоксана с пиридином. На второй стадии промежуточный активированный фосфитилированный продукт обрабатывают раствором бис-трибутиламмонийной соли пирофосфата в смеси ацетонитрила с пиридином. На третьей стадии трехвалентный атом фосфора в продукте окисляют в пятивалентный с помощью раствора йода, продукт отщепляют от твердого носителя и деблокируют. Целевой продукт очищают с помощью анионообменной ВЭЖХ. В результате получают pppdT2, pppdT3, pppdT9, pppdT15, pppd(ACTGT) и pppdC2. Выходы продуктов после очистки составляют 15-30%.
Недостатками указанного способа являются:
1) Использование огромных избытков реагентов (до 3000-х кратного для 2-хлоро-4Н1,3,2-бензодиоксафосфорин-4-она и до 6000-ти кратного для пирофосфата), а также больших объемов растворителей в расчете на мкмоль исходного соединения.
2) Низкие выходы целевых соединений - 15-30%.
3) Малое количество получаемого продукта, не превышающего 2-5 мкмоль (2-5 мг), и трудности в масштабировании процесса.
4) Наличие значительных количеств побочных продуктов.
Технической задачей изобретения является повышение выхода целевых продуктов, сокращение избытка используемых реагентов и растворителей, а также расширение функциональных возможностей способа за счет обеспечения возможности получения 5'-трифосфатов олигонуклеотидов не только дезоксирибо, но и риборяда
Поставленная техническая задача достигается предлагаемым новым способом получения 5'-трифосфатов олигонуклеотидов как дезксирибо-, так и риборяда с формулой pppN(pN)n, заключающимся в следующем.
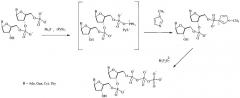
На чертеже представлена схема синтеза 5'-трифосфата дезоксирибо- и рибоолигонуклеотида на примере синтеза 5'-трифосфата дезоксидинуклеотида, где В - Ade, Gua, Cyt, Thy.
Синтез осуществляют в две стадии в растворе при комнатной температуре. На первой стадии исходный реагент - тетраалкиламмониевую или триалкиламмониевую соль 5'-монофосфата дезокси- или рибоолигонуклеотида в виде 0,1-0,5 М раствора активируют в органическом растворителе, в качестве которого используют смесь диметилсульфоксида (ДМСО) и диметилформамида (ДМФ) в соотношении 2:1, пяти-пятнадцатикратным избытком окислительно-восстановительной смеси трифенилфосфина с дипиридилдисульфидом (Ph3Р/(PyS)2), взятых в соотношении 1:1, в присутствии 50-80-кратного избытка нуклеофильного катализатора, преимущественно 1-метилимидазола или N,N-диметиламинопиридина, в течение 5-10 мин с получением активированного производного 5'-монофосфата дезокси- или рибоолигонуклеотида. На второй стадии в раствор активированного монофосфорилированного олигонуклеотида добавляют 10-20 кратный избыток раствора бис-трибутиламмонийной соли пирофосфата в ацетонитриле и выдерживают смесь в течение 15-30 минут. На момент окончания реакции 5'-трифосфаты дезоксирибо- и рибоолигонуклеотидов находятся в виде смеси тетраалкиламмониевых или триалкиламмониевых солей (целевые продукты). Коммерческие (конечные формы целевых продуктов) продукты получают преимущественно в виде литиевых солей, поскольку они наиболее стабильны при хранении. Для этого, после завершения реакции целевой продукт, а также избыток пирофосфата, осаждают десятикратным объемом 6% раствора перхлората лития в ацетоне. Осадок промывают ацетоном и серным эфиром и высушивают.Очистку целевого продукта проводят с помощью двух последовательных анионообменных хроматографий на сорбенте Полисил СА и ДЕАЕ-Сефадексе А-25. Чистота полученных соединений более 95% по данным аналитической высокоэффективной жидкостной хроматографии (ВЭЖХ).
Выходы целевых 5'-трифосфатов дезокси- и рибоолигонуклеотидов после очистки составляют 52-92% в зависимости от нуклеотидной последовательности и длины олигонуклеотида. Количество получаемых продуктов составляет 10-100 мкмоль (10-100 мг) и выше. Выходы 5'-трифосфатов дезокси- и рибоолигонуклеотидов приведены в Таблице 1, а выходы солевых форм целевых продуктов в Таблице 3.
Строение полученных соединений подтверждено с помощью 31P- и 1Н-ЯМР-спектроскопии. Данные по некоторым соединениям приведены в Таблицах 2 и 3.
5'-Монофосфорилированные олигонуклеотиды могут быть получены в больших количествах (до несколько граммов) с помощью триэфирного метода синтеза олигонуклеотидов по одной из известных методик (например, Абрамова Т.В., Комарова Н.И., Мундус Д.А., Перебоева О.С.// Изв. СО. АН СССР, сер. хим. наук. 1990. Вып.5. Стр.45-51). Перевод 5'-монофосфорилированного дезоксирибо- или рибоолигонуклеотида в тетраалкиламмониевую или триалкиламмониевую соль (исходный реагент) проводят с помощью пропускания раствора, преимущественно литиевой, соли исходного олигонуклеотида в 40%-ном водном этаноле через колонку с сорбентом Dowex 50W×2 в соответствующей форме согласно рекомендациям изготовителя сорбента (Dow, США) или, в частности, осаждением цетилтриметиламмониевой соли олигонуклеотида из водного раствора путем добавления эквивалентного количества 8% раствора цетилтриметиламмоний бромида в воде. Концентрацию олигонуклеотида в растворе определяют спектрофотометрически на длине волны 260 нм, используя известные молярные коэффициенты экстинкции ε260 для мононуклеотидов и формулу расчета для олигонуклеотидов (Cavaluzzi M.J., Borer P.N. // Nucleic Acids Res. 2004 V.32. e13).
Определяющими отличиями предлагаемого способа от прототипа, являются:
1. Синтез проводят в растворе, при этом в качестве исходного реагента используют 0.1-0.5 М раствор тетраалкиламмониевой или триалкиламмониевой соли 5'-монофосфата дезокси- или рибоолигонуклеотида, что позволяет избежать высоких избытков реагентов, а также больших объемов растворителей в расчете на мкмоль исходного реагента, а также легко масштабировать процесс, что обеспечивает получение больших (милимолярных) количеств продукта. В прототипе получение продукта осуществляют в твердофазном варианте, а в качестве исходного реагента используют соответствующим образом защищенный дезоксиолигонуклеотид (защитные группы на гетероциклических основаниях нуклеозидов и межнуклеотидных фосфатных группах, свободная 5'-оксигруппа дезоксиолигонуклеотидной цепи), взятый непосредственно из реакционной смеси в процессе синтеза олигонуклеотида. Таким образом, в заявляемом способе получения 5'-трифосфатов дезокси- и рибоолигонуклеотидов стадии введения 5'-монофосфата в олигонуклеотид и активации фосфомоноэфирной группировки разделены, что позволяет проводить синтез без применения защитных групп на гетероциклических основаниях нуклеозидов и межнуклеотидных фосфатных группах.
2. Исходный реагент активируют в органическом растворителе, представляющем смесь диметилсульфоксида и диметилформамида в соотношении 2:1, пяти-пятнадцатикратным избытком окислительно-восстановительной смеси трифенилфосфина и дипиридилдисульфида (соотношение 1:1) в присутствии 50-80-кратного избытка нуклеофильного катализатора, преимущественно 1-метилимидазола или N,N-диметиламинопиридина, в течение 5-10 минут, что позволяет селективно активировать только концевую моноэфирную фосфатную группу, не затрагивая межнуклеотидных фосфодиэфирных связей и гетероциклических оснований, и использовать в качестве исходных соединений деблокированные и очищенные 5'-монофосфорилированные дезокси- или рибоолигонуклеотиды.
В прототипе в качестве активирующего реагента используют 3000-кратный избыток 2-хлоро-4Н1,3,2-бензодиоксафосфорин-4-она.
3. Активированный монофосфорилированный олигонуклеотид обрабатывают 10-20 кратным избытком раствора бис-трибутиламмонийной соли пирофосфата в ацетонитриле, и выдерживают реакционную смесь в течение 15-30 минут, что позволяет повысить выход целевого продукта и существенно сократить расход пирофосфата. В прототипе используют 6000-кратный избыток пирофосфата.
Способ иллюстрируется следующими примерами конкретного выполнения.
Пример 1.
Получение 5'-[2'-дезокситимидин-(3'-5')-2'-дезокситимидилил]трифосфата.
В круглодонную колбу вместимостью 50 мл загружают 20 мл раствора цетилтриметиламмониевой соли 5'-[2'-дезокситимидин-(3'-5')-2'-дезокситимидилил]фосфата (pdT2) концентрацией 42 О.Е./мл в 40%-ном водном этаноле. Раствор упаривают на ротационном испарителе при пониженном давлении при температуре 40°С досуха, добавляют к остатку в колбе 10 мл сухого ацетонитрила, упаривают раствор досуха. Повторяют эту операцию дважды. Остаток в колбе растворяют в 10 мл смеси диметилсульфоксида и диметилформамида (2:1) (концентрация дезоксидинуклеотида 0.5 М), добавляют в раствор 65,6 мг трифенилфосфина, 55,1 мг дипиридилдисульфида (пятикратный избыток пары Ph3Р/(PyS)2) и 0,213 мл (50-кратный избыток) 1-метилимидазола. Реакционную смесь перемешивают 5 минут при комнатной температуре, затем в раствор добавляют 1 мл 0.5 М раствора бис(трибутил)аммонийной соли пирофосфата (10-кратный избыток) в сухом ацетонитриле. Перемешивание продолжают 30 минут, затем реакционную смесь выливают в 100 мл 6% раствора перхлората лития в ацетоне. Осадок отделяют фильтрованием, промывают ацетоном и серным эфиром и высушивают в вакууме. После высушивания осадок растворяют в 20 мл воды, раствор наносят на колонку 4.6×250 мм с анионообменным сорбентом Полисил СА (НПО Вектор, Россия). Элюцию осуществляют в линейном градиенте сульфата аммония (0-0,8 М) в течение 1.5 часов со скоростью 2 мл/мин в 20% водном ацетонитриле. Фракции, содержащие целевой продукт, разбавляют в 10 раз водой. Раствор наносят на колонку 3×9 см с ДЭАЭ-сефадексом А-25 (Pharmacia, Швеция). Элюцию осуществляют в линейном градиенте бикарбоната аммония (0-1 М) в 20% водном этаноле. Объем градиента 600 мл. Фракции, содержащие целевой продукт, упаривают в вакууме с помощью ротационного испарителя при температуре 40°С. Остаток упаривают несколько раз с водным этанолом для удаления следов буфера. Продукт - 5'-[2'-дезокситимидилил-(3'-5')-2'-дезокситимидин]трифосфат pppd(TT) - растворяют в 1 мл воды и осаждают добавлением 10 мл 6% раствора перхлората лития в ацетоне. Осадок отделяют центрифугированим или фильтрованием, промывают ацетоном и высушивают до постоянного веса в вакууме. Выход pppd(TT) 37.0 мг, 46 мкмоль, 92% (в виде литиевой соли).
Пример 2.
Получение 5'-[уридилил-(3'-5')-уридин]трифосфата (pppUU) проводят также, как в примере 1, за исключением того, что в качестве исходного соединения берут 5'-[уридилил-(3'-5')-уридин]фосфат pU2 в виде тетрабутиламмониевой соли. В качестве нуклеофильного катализатора применяют N,N-диметиламинопиридин. Из 960 ОЕ260 (50 мкмоль) 5'-монофосфата 5'-[уридилил-(3'-5')-уридин]фосфата pU2 получают 34 мг pppUU (в виде литиевой соли, 42 мкмоль, выход 84%).
Пример 3.
Получение 5'-трифосфата дезокситридекануклеотида pppd[Т(СТ)6] проводят аналогично примеру 1, со следующими отличиями. В качестве исходного соединения берут цетилтриметиламмониевую соль 5'-монофосфатдезокситридекануклеотида pd[Т(СТ)6]. Концентрация исходного соединения в реакционной смеси 0.1 М. Избыток активирующей окислительно-восстановительной пары Ph3Р/(PyS)2 15-кратный. Избыток нуклеофильного катализатора 1-метилимидазола 80-кратный. Стадию активации проводят в течение 10 минут. Избыток бис-трибутиламмониевой соли пирофосфата 20-кратный, при этом реакционную смесь выдерживают 15 минут. Из 10 мкмоль исходного 5'-монофосфатдезокситридекануклеотида pd[Т(СТ)6] получают 20 мг 5'-трифосфат pppd[Т(СТ)6] (в виде литиевой соли, 4.85 мкмоль, выход 48%).
Пример 4.
Получение 5'-трифосфата риботетрацитидилата ррр(С)4 проводят аналогично примеру 3, за исключением того, что в качестве исходного соединения берут трибутиламмониевую соль 5'-монофосфата тетрацитидилата р(С)4. Из 10 мкмоль исходного р(С)4 получают 12 мг ррр(С)4 (в виде литиевой соли, 8.5 мкмоль, выход 85%).
Пример 5.
Получение 5'-[2'-дезокситимидин-(3'-5')-2'-дезокситимидилил]трифосфата проводят аналогично примеру 1, за исключением того, что для осаждения целевого продукта берут 6% раствор перхлората натрия в ацетоне. Выход pppd(TT) 38.3 мг, 45 мкмоль, 90% (в виде натриевой соли).
Пример 6.
Получение 5'-[2'-дезокситимидин-(3'-5')-2'-дезокситимидилил]трифосфата проводят аналогично примеру 1, за исключением того, что остаток после упаривания с водным этанолом высушивают до постоянного веса в вакууме. Выход pppd(TT) 37.7 мг, 45 мкмоль, 90% (в виде аммониевой соли).
Таким образом, разработан универсальный способ получения 5'-трифосфатов дезокси- и рибоолигонуклеотидов в милимолярных количествах с высокими выходами, меньшим избытком реагентов и объемов растворителей, необходимых при синтезе.
| Способ получения 5-трифосфатов дезоксирибо- и рибоолигонуклеотидовТаблица 1 | |||||
| Олигонуклеотид | pppd(AA) | pppd(AC) | pppd(AG) | pppd(AT) | pppd(CA) |
| Выход, в %, | 61 | 58 | 52 | 69 | 59 |
| Олигонуклеотид | pppd(GG) | pppd(GT) | pppd(TA) | pppd(TC) | pppd(TG) |
| Выход, в % | 56 | 56 | 54 | 88 | 62 |
| Олигонуклеотид | pppd(CC) | pppd(CG) | pppd(CT) | pppd(GA) | pppd(GC) |
| Выход, в % | 87 | 73 | 91 | 54 | 61 |
| Олигонуклеотид | ррр(ТТ) | ppp(UU) | ррр(СА) | ррр(С)4 | pppd(CA)2 |
| Выход, в % | 92 | 84 | 73 | 85 | 78 |
| Таблица 3. | |||
| Продукт | Солевая форма (противоион) | Выход, % | 31P, δ(ppm) |
| ррр(ТТ) | Литиевая соль | 92 | 1.23 (s, 1P, PТТ,); -7.17 (d, 1P, Pγ, Jβγ, 20); -9.10 (d, 1P, Pα, Jαβ, 19.5); -20.21 (t, 1P, Pβ) |
| Натриевая соль | 90 | 1.22 (s, 1P, PTT,); -7.15 (d, 1P, Pγ, Jβγ, 20); -9.14 (d, 1P, Pα, Jαβ, 19.5); -20.20 (t, 1Р, Рβ) | |
| Аммониевая соль | 90 | 1.25 (s, 1P, PTT,); -8.95 (d, 1P, Pγ, Jβγ, 20); -10.15 (d, 1P, Pα, Jαβ, 19.5); -20.50 (t, 1P, Pβ) |
Способ получения солей 5'-трифосфатов дезокси- и рибоолигонуклеотидов, заключающийся в том, что исходный реагент тетраалкиламмониевую или триалкиламмониевую соль 5'-монофосфата дезокси- или рибоолигонуклеотида в виде 0,1-0,5 М раствора активируют в среде растворителя, представляющего смесь диметилсульфоксида и диметилформамида в соотношении 2:1, пяти-пятнадцатикратным избытком окислительно-восстановительной смеси трифенилфосфина и дипиридилдисульфида, взятых в соотношении 1:1, в присутствии 50-80-кратного избытка 1-метилимидазола или N,N-диметиламинопиридина в течение 5-10 мин, а далее добавляют 10-20-кратный избыток раствора бис-трибутиламмонийной соли пирофосфата в ацетонитриле и выдерживают реакционную смесь в течение 15-30 мин с последующим выделением и очисткой целевого продукта.