Способ получения гидроксиламинсульфата
Иллюстрации
Показать всеИзобретение относится к способу производства гидроксиламинсульфата (ГАС) методом восстановления моноокиси азота (NO) водородом (Н2) на катализаторе в среде серной кислоты. По этому методу концентрированную моноокись азота смешивают с чистым водородом и в среде 19%-ной серной кислоты на суспензированном платиновом катализаторе синтезируют ГАС. Одновременно протекают побочные реакции, обогащающие газовую фазу в реакторах, которая с водородом может образовывать взрывоопасную смесь. В целях безопасности процесса из реакторов синтеза ГАС выводят газы, содержащие не более 10,5÷11,5 об.% N2O. Эти хвостовые газы также содержат 60÷70% водорода, 8÷14 об.% NO. Изобретение направлено на извлечение NO из хвостовых газов (не менее 80%) и возврат его в процесс. Для абсорбции NO рекомендуется использовать 15÷26% раствор FeSO4 с температурой процесса при абсорбции 10÷35°С и давлении 0,1÷0,4 МПа абсолютных. После десорбции, проводимой при температуре 85÷95°С и давлении 0,105 МПа, получается концентрированный NO (не ниже 94%), либо - NO-содержащий газ при десорбции, проводимой при температуре 30-40°С током водорода. Для поддержания концентрации закиси азота вне пределов взрываемости на стадии абсорбции вводят азот в количестве, равном поглощенному NO. Предлагаемый способ позволяет достичь комплексного решения проблем удешевления производства, снижения загрязнения атмосферы окислами азота, а для действующих предприятий - увеличения производства капролактама с минимальными капитальными затратами без расширения действующих технологических установок для выработки концентрированной NO. 5 з.п. ф-лы, 2 ил., 2 табл.
Реферат
Настоящее изобретение относится к способу производства гидроксиламинсульфата - полупродукта для получения капролактама - методом восстановления моноокиси азота (NO) водородом (H2) на катализаторе в среде серной кислоты.
Изобретение может быть использовано как для интенсификации действующих производств капролактама, так и при строительстве новых.
В производствах капролактама гидроксиламинсульфат (далее ГАС) получают преимущественно методом восстановления NO водородом в среде серной кислоты. В России и странах СНГ этот метод применен на всех действующих производствах капролактама.
По этому методу производят конверсией аммиака кислородом концентрированную моноокись азота (92,5÷93,5% NO об.), смешивают с чистым водородом и в среде 19%-ной серной кислоты на суспензированном платиновом катализаторе синтезируют ГАС по реакции:
Одновременно протекают такие основные побочные реакции:
Побочные реакции (3) и (4) обогащают газовую фазу в реакторах N2O, которая с водородом может образовать взрывоопасную смесь при определенных концентрациях (16% N2O и выше).
В целях безопасности из реакторов синтеза ГАС выводят газы, содержащие не более 10,5÷11,5 об.% N2O; при содержании 12% производство останавливают.
Эти хвостовые газы содержат 60÷70 об.% водорода, 8÷14,0 об.% NO и сжигаются на факельной установке. Часовой расход хвостовых газов и содержание в них NO и N2O носит переменный характер в зависимости от целого ряда факторов (активность и селективность катализатора, нагрузка, содержание NO в исходном газе и др.).
Усреднено потери NO с хвостовыми газами могут достигать более 10%.
Помимо прямых убытков от таких потерь сжигание хвостовых газов, содержащих значительное количество NO и N2O, неизбежно приводит к загрязнению атмосферы оксидами азота, так как достичь полного восстановления NO и N2O до азота в пламени факела (и даже в других специальных горелочных устройствах для утилизации тепла сгорания хвостовых газов) невозможно.
Техническая задача, на решение которой направлено настоящее изобретение, заключается в извлечении из хвостовых газов и возврате в производство не менее 80% NO, что позволяет достичь комплексного решения проблем удешевления производства, снижения загрязнения атмосферы окислами азота, а для действующих предприятий - увеличения производства капролактама с минимальными капитальными затратами без расширения действующих технологических установок для выработки концентрированной NO.
Анализ патентной литературы по производству гидроксиламинсульфата методом восстановления моноокиси азота водородом (авторские свидетельства СССР №1214584, №1237629, №1599302 от 15.10.1990, заявка ЕПВ №945401, опубликованная в 1999 г., патенты РФ №2045471, №2241662, №2257339) показал, что все они решают определенные вопросы усовершенствования способа производства гидроксиламинсульфата, но не затрагивают проблемы извлечения и возврата NO из хвостовых газов и, как следствие, снижения загрязнения атмосферы окислами азота.
Поэтому все известные способы производства ГАС методом восстановления NO могут служить прототипом способа по настоящему изобретению и подтверждают его новизну и патентоспособность (Овчинников В.И., Производство капролактама, М., «Химия», 1974 г. - 264 с., А.с. СССР №1599302, №1214584, №1237629, №1599302, Патенты РФ №2045471, №2241662, №2257339).
В качестве прототипа принят способ по авторскому свидетельству СССР SU 1599302 С01В 21/14, 15.10.1990 г., позволяющий уменьшить количество хвостовых газов за счет повышения степени превращения сырья в гидроксиламинсульфат. Способ включает получение концентрированной моноокиси азота конверсией аммиака, синтез гидраксиламинсульфата методом восстановления NO водородом при молярном соотношении Н2:NO=(10÷20):1 на суспензированном платиновом катализаторе. Но по прототипу сохраняется необходимость вывода хвостовых газов со стадии синтеза на сжигание, т.к. степень превращения моноокиси азота в ГАС даже в лабораторных условиях не превышает 92,5%. Таким образом, кардинально проблемы загрязнения среды оксидами азота данный способ не решает, а потери NO с хвостовыми газами весьма существенны. Наши технико-экономические исследования показали, что для извлечения NO из хвостовых газов и возвращения их в процесс получения ГАС как с технической, так и экономической точек зрения целесообразно использовать известную способность ряда растворов солей двухвалентного железа поглощать NO. На основе известных литературных данных и наших исследований (С.Н Ганз, Е.И.Кузнецов. «Очистка промышленных газов», Киев, Наукова думка, 1967; Автореферат, канд. диссертация, Зубов В.В. «Исследование поглощения окислов азота солевыми растворами», Ленинград, 1964; Автореферат, докт. диссертация, Терещенко Л.Я. «Исследование процессов взаимодействия окислов азота с растворами некоторых кислот и солей», Ленинград, 1971) была проанализирована возможность и применение водных растворов этих солей. Практически все эти растворы пригодны для промышленного использования в процессе поглощения NO из газов указанного выше состава.
С учетом особенностей процесса синтеза гидроксиламинсульфата приоритетным согласно настоящему изобретению является применение водных растворов сульфата двухвалентного железа. Недостаток солей двухвалентного железа - переход железа из двухвалентной в трехвалентную форму с потерей абсорбционных свойств раствора, - в данном процессе малосущественен, так как хвостовые газы процесса синтеза ГАС не содержат кислорода, а подсос воздуха исключается проведением процесса абсорбции под избыточным давлением. Для выделения из раствора трехвалентного железа предлагается пропускать раствор через железосодержащую насадку. В связи с этим в независимый пункт формулы изобретения включено использование для абсорбции NO только солей двухвалентного железа и проведение процесса абсорбции и десорбции при давлении выше атмосферного, чтобы исключить подсос воздуха из атмосферы. При этом преимущественно желательно использовать водный раствор сульфата железа.
В циркулирующем растворе солей неизбежно присутствие следов серной кислоты при применении сульфата железа или соляной кислоты - при применение хлорида железа, а также, возможно, и азотной кислоты. Сочетание соляной и азотной кислоты, даже в незначительной концентрации, предъявляет жесткие требования к материалу аппаратуры и трубопроводов, в то время как при присутствии в растворе примеси азотной и серной кислот возможно применение широко распространенных кислотостойких сталей типа Х18Н10Т.
Дополнительным неблагоприятным фактором в случае применения хлорида железа является повышенная летучесть соляной кислоты, и как следствие, опасность попадания на платиновый катализатор ионов хлора, являющимся для него ядом. Поэтому в формулу изобретения входит конкретизирующий независимый пункт формулы, пункт о преимущественном применении 15÷26%-ного водного раствора сульфата железа.
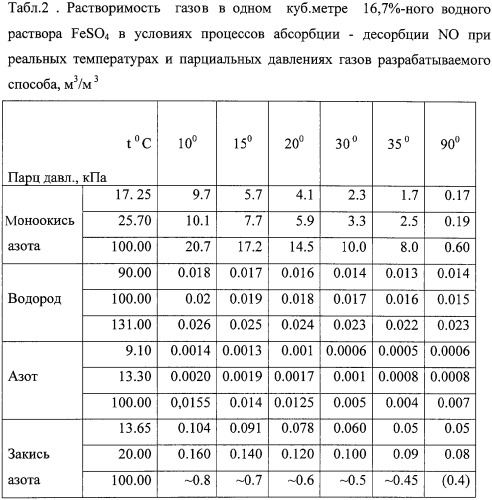
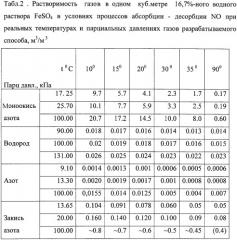
Параметры абсорбционного раствора (концентрация и температура) приняты на основе исследований по растворимости NO в водных растворах FeSO4 разной концентрации и температуре 10÷35°С в диапазоне давления хвостовых газов 0,1÷0,4 МПа абсолютных.
| Табл.1Максимальная растворимость СУЛЬФАТА ЖЕЛЕЗА закисного | |
| Температура, °С | мас.% |
| 0 | 13.6 |
| 10 | 17.2 |
| 20 | 20.8 |
| 30 | 24.7 |
| 40 | 28.6 |
| 80 | 30.4 |
При давлении в процессе абсорбции, незначительно превышающем атмосферное (до 0,2 МПа), следует применять раствор с концентрацией в диапазоне 15÷23 мас.% FeSO4 и температуру процесса 10÷30°С; при более высоком давлении - температуру процесса можно повысить до 35°С и концентрацию раствора до 26 мас.% (например, при давлении на стадии синтеза ГАС порядка 0,4 МПа абс.).
В диапазоне указанных температур и давлений растворимость других газов, входящих в состав хвостовых газов, незначительна, что обеспечивает получение высококонцентрированного NO после термической десорбции (не ниже 94 об.%) или практически бинарную смесь NO и Н2.
В процессе многократного повторения циклов абсорбции и десорбции, охлаждения и нагревания, уноса брызг не исключено снижение поглощающей способности раствора солей как вследствие уменьшения концентрации, так и перехода Fe+2 в Fe+3.
Для поддержания стабильной поглощающей способности раствора и снижения величины подпитки цикла свежим раствором согласно изобретению производят фильтрацию циркулирующего раствора через фильтрующий железосодержащий крупнопористый материал. Присутствие в растворе свободной серной кислоты обеспечивает переход железа в раствор и его «подпитку» солью двухвалентного железа.
Учитывая чувствительность платинового катализатора синтеза гидроксиламинсульфата к отравлению различными ядами с потерей активности согласно изобретению предусматривается очистка десорбированной из раствора моноокиси азота или ее смеси с водородом от брызг раствора и аэрозольных частиц солей фильтрованием через фильтрующие тонковолокнистые материалы или путем водной промывки газа.
С целью сохранения существующего уровня безопасности эксплуатации производства согласно изобретению предусматривается подача азота или водорода в очищаемые от NO хвостовые газы при содержании больше 10,5 об.% N2O в количестве, равном количеству поглощаемого NO.
Десорбция NO из раствора согласно изобретению может осуществляться током водорода при более низкой нежели при термической десорбции температуре до 40°С, которая оптимально должна быть на 1÷5°С выше температуры раствора на стадии абсорбции и зависит от степени его насыщения моноокисью азота и общего давления. Необходимый расход водорода на десорбцию определяется на основе равновесных данных и общего давления по стандартной методике расчета процесса отгонки. По условиям безопасности производства расход водорода должен не менее чем в 2 раза превышать количество десорбированного NO по объему. Максимальный расход водорода, используемого в процессе синтеза гидроксиламинсульфата, на десорбцию NO из насыщенного раствора теоретически может быть любым и лимитируется общим расходом водорода на процесс синтеза гидроксиламинсульфата. Практически расход водорода на десорбцию ограничивается технически и экономически целесообразными решениями по доле водорода от общего его расхода на производство ГАС, направляемого на десорбцию NO.
Пример 1 осуществления способа.
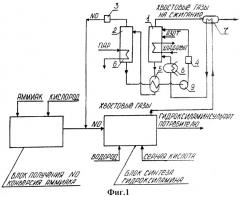
Иллюстрация осуществления способа производства гидроксиламинсульфата по настоящему изобретению представлена на Фиг.1.
Аммиак и кислород поступают в блок получения концентрированной 92,0÷94,0%-ной моноокиси азота известным способом окисления аммиака кислородом в среде водяного пара на платиновом катализаторе. После охлаждения и конденсации водяных паров из нитрозных газов концентрированную моноокись азота направляют на синтез гидроксиламинсульфата известным способом восстановления NO водородом в 19%-ном растворе серной кислоты.
Водный раствор гидроксиламинсульфата направляют потребителю.
Хвостовые газы с давлением 0,14÷0,15 МПа в количестве, например, 4500 м3/ч сухого газа, содержащего 782 кг NO, 264 кг H2, 864 кг N2O, 550 кг N2, насыщенные водяными парами при температуре около 45°С после промывки хвостовых газов от брызг серной кислоты и гидроксиламинсульфата (на Фиг.1 не показана), после последовательного охлаждения до плюс 10°С в газовом теплообменнике 7 и холодильнике 8, поступают в абсорбционную колонну 1, орошаемую 16,7%-ным раствором FeSO4 в количестве 100÷110 м3/ч с температурой 10°С. В колонне поглощается примерно 85% содержащейся в исходных хвостовых газах NO, т.е. 665 кг NO.
Хвостовые газы из абсорбционной колонны, подогретые встречным потоком исходных газов до 30°С, направляются на сжигание в факеле или в печах производства капролактама для сжигания жидких отходов. В примере принято, что исходные хвостовые газы содержат более 10 об.% N2O, а поэтому в процессе абсорбции в них подают азот в количестве, равном поглощенному NO. Циркулирующий раствор абсорбента после нагрева в рекуперационном теплообменнике 5 поступает в колонну 2, в которой под давлением около 0,105 МПа NO десорбируется при нагреве раствора водяным паром в испарителе 6 до 85÷95°С.
Десорбированная NO содержит до 5 об.% H2, N2O и N2 в сумме. После очистки в фильтре 3 от брызг и аэрозольных частиц концентрированная NO направляется на смешение с потоком NO из блока конверсии аммиака (вместо очистки в фильтре 3 может быть применена водная промывка, см.. Пример 2, Фиг.2, поз.15).
Циркулирующий раствор после десорбера 2 охлаждается в системе теплообменников 5 до температуры плюс 10°С и подается насосом 9 на фильтрацию в железосодержащем пористом фильтре 4.
Пример 2 осуществления способа.
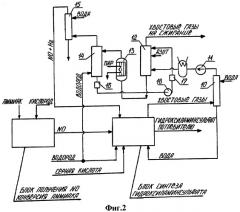
Иллюстрация примера 2 осуществления способа производства гидроксиламинсульфата по настоящему изобретению с десорбцией NO из циркулирующего раствора водородом представлена на Фиг.2.
Хвостовые газы с давлением 0,15 МПа в количестве, например, 4500 м3/час, содержащие 782 кг NO, 264 кг Н2, 864 кг N2O, 550 кг N2, насыщенные водяными парами при температуре приблизительно 45°С над раствором ГАС, после промывки от примесей серной кислоты и ГАС в скруббере 10 поступают на всасывающий трубопровод газодувки 11, где сжимаются до давления 0,24 МПа. Сжатый хвостовой газ поступает в абсорбционную колонну 12, орошаемую 23%-ным раствором FeSO4 в количестве 200÷220 м3/ч с начальной температурой 30°С и конечной 32°С. В колонне поглощается до 80% содержащейся в исходных хвостовых газах NO.
Очищенные газы из абсорбционной колонны с температурой около 30°С направляются на сжигание в факеле или в печах производства капролактама для сжигания жидких отходов. В примере принято, что исходные хвостовые газы содержат более 10 об.% N2O, поэтому в конце процесса абсорбции для разбавления в них подают азот или водород в количестве, равном поглощенному NO.
Насыщенный раствор из абсорбера под действием разницы давлений поступает в подогреватель 13, где раствор нагревается до 33°С и далее - в десорбционную колонну 14, в которой при давлении 0,105 МПа моноокись азота отгоняется с водородом.
Десорбированный газ содержит NO около 10,0 об.%, а остальное Н2, с небольшими примесями N2O, N2, брызг раствора FeSO4 в сумме менее 1% и пары воды.
После очистки в скруббере 15 от брызг и аэрозольных частиц FeSO4 смесь NO и водорода в соотношении около 1:9 направляется в производство ГАС. Орошение скруббера 15 проводят 5 м3/ч обессоленной воды с последующим возвращением ее в цех водоподготовки на стадию осветления вместе с «продувочным» раствором FeSO4 из сборника раствора 16. (Вместо водной очистки может быть применен фильтр, см. Фиг.1, поз.3)
Циркулирующий раствор FeSO4 с помощью насоса 18 подвергается фильтрации на железосодержащем пористом фильтре 17, охлаждению и возвращается на орошение абсорбера 12 при температуре 30°С.
Приведенные примеры иллюстрируют осуществление способа по всем существенным признакам изобретения, изложенным в формуле изобретения.
При использовании других солей двухвалентного железа и других параметрах процессов абсорбции и десорбции (например, повышении давления хвостовых газов выше 0,24 МПа, снижении содержания N2O и др. изменениях) отдельные зависимые пункты формулы изобретения могут не использоваться с полным решением технической задачи по настоящему изобретению.
1. Способ производства гидроксиламинсульфата, включающий получение концентрированной моноокиси азота окислением аммиака кислородом в присутствии водяного пара, синтез гидроксиламинсульфата восстановлением NO водородом в среде водного раствора серной кислоты на платиновом катализаторе, вывод хвостовых газов, содержащих NO, H2, N2O, N2, CH4 и водяной пар, из реакторов синтеза, отличающийся тем, что из хвостовых газов извлекают моноокись азота абсорбцией растворами солей двухвалентного железа (Fe+2) под давлением выше атмосферного, затем при давлении выше атмосферного NO десорбируют из раствора нагреванием или током водорода и возвращают в поток концентрированной моноокиси азота или в реактор синтеза гидроксиламинсульфата, а регенерированный раствор солей железа - на стадию абсорбции NO из хвостовых газов.
2. Способ по п.1, отличающийся тем, что NO абсорбируют преимущественно 15÷26%-ным раствором сульфата железа (FeSO4) при температуре 10÷35°С в зависимости от давления газов на стадии абсорбции, с предварительной их очисткой от примесей серной кислоты и гидроксиламинсульфата.
3. Способ по п.1, отличающийся тем, что циркулирующий раствор солей двухвалентного железа фильтруют от нерастворимых примесей через пористый материал, содержащий железо.
4. Способ по п.1, отличающийся тем, что десорбированный высококонцентрированный NO или газ, содержащий NO после продувки насыщенного раствора водородом при температуре 30÷40°С, очищают от брызг раствора и аэрозольных частиц фильтрацией через тонковолокнистые пористые материалы или водной промывкой.
5. Способ по п.1, отличающийся тем, что для обеспечения содержания N2O не выше 10,5 об.% в хвостовые газы после извлечения из них моноокиси азота на стадии абсорбции при необходимости подают азот или водород.
6. Способ по п.1, отличающийся тем, что хвостовые газы после абсорбции NO направляют на сжигание в факельную установку или на установку с утилизацией тепла их сгорания.