Профилактическое и терапевтическое применение гидроксистероидов
Иллюстрации
Показать всеИзобретение относится к лекарственным средствам и касается применения 3-гидрокси-7-гидроксистероидов для защиты против ишемического поражения периферических органов и для лечения поражения спинного мозга, индуцированного повреждением спинного мозга, где стероид представляет собой соединение формулы (I) и его фармацевтически приемлемые соли и сложные эфиры. Также раскрывается способ защиты млекопитающего против индуцированного ишемией поражения ткани в периферических органах или против индуцированного повреждением спинного мозга поражения спинного мозга введением эффективного количества 3-гидрокси-7-гидроксистероида или его фармацевтически приемлемого сложного эфира. Данное изобретение позволяет расширить арсенал средств для защиты против ишемического нарушения в тканях периферических органов. 2 н. и 15 з.п. ф-лы, 6 ил., 4 табл.
где каждый из R1, R2, Ra, Rb, А и n имеет указанные в описании значения,
Реферат
Данное изобретение имеет отношение к применению для профилактики и терапии определенных новых соединений 3-гидрокси-7-гидроксистероидов и их некоторых кетонных производных, а точнее к применению указанных соединений для предупреждения или лечения нарушений, вызванных ишемическим стрессом периферических органов, таких как сердце или почки, а также для лечения повреждения спинного мозга.
С использованием специальной модели нейропротекции, было продемонстрировано, что соединения указанного типа обладают нейропротекторной активностью. В настоящее время заявителями установлено, что тот же самый способ действия, который приводит к упомянутому нейропротекторному эффекту, также реализуется в тканях периферических органов, таких как сердце и почки, и, таким образом, соединения также характеризуются кардиопротекторным действием и способностью предупреждать ишемическое поражение почек.
Таким образом, данное изобретение предусматривает применение 3-гидрокси-7-гидроксистероида или 3-оксо-7-гидроксистероида или их фармацевтически приемлемого сложного эфира для производства лекарственного средства для защиты против ишемического нарушения в тканях периферических органов (то есть в любой функциональной ткани в организме, за исключением мозга и спинного мозга), особенно поражения сердца и почек, и для лечения поражения спинного мозга, индуцированного повреждением в спинном мозге.
Особым классом соединений, которые предпочтительны для применения в данном изобретении, являются 7β-гидроксистероиды, а из числа указанных - соединения, которые представляют исключительный интерес для данного изобретения, представляют собой 3β,7β-дигидроксистероиды и их фармацевтически приемлемые сложные эфиры.
Предпочтительные сложные эфиры представляют собой сложные эфиры карбоновых кислот и аминокислот.
Примерами необязательно замещенных 3β,7β-дигидроксистероидов и их фармацевтически приемлемых сложных эфиров и других производных, которые могут быть использованы в данном изобретении, являются соединения формулы (I)
в которой R1 и R2 являются одинаковыми или отличаются друг от друга и каждый означает атом водорода, алкильную группу, содержащую от 1 до 6 атомов углерода, алкенильную группу, содержащую от 2 до 6 атомов углерода, алкинильную группу, содержащую от 2 до 6 атомов углерода, арильную группу, содержащую от 6 до 10 атомов углерода, формильную группу, алкилкарбонильную группу, содержащую от 2 до 7 атомов углерода, алкенилкарбонильную группу, содержащую от 3 до 7 атомов углерода, алкинилкарбонильную группу, содержащую от 3 до 7 атомов углерода, арилкарбонильную группу, содержащую от 7 до 11 атомов углерода, аралкилкарбонильную группу, содержащую от 8 до 15 атомов углерода, аралкенилкарбонильную группу, содержащую от 9 до 15 атомов углерода, остаток аминокислоты или гетероциклическую карбонильную группу, которая описана ниже;
один из Ra и Rb представляет собой группу формулы -Rc, предпочтительно в β-конфигурации, а другой означает атом водорода, или Ra и Rb вместе означают оксогруппу;
Rc означает алканоильную группу, содержащую от 1 до 6 атомов углерода, арилкарбонильную группу, в которой арильная часть представляет собой ароматическую карбоциклическую группу, содержащую от 6 до 10 атомов углерода в кольце, гетероциклическую карбонильную группу, которая описана ниже, или группу формулы -OR4, в которой R4 означает любую одну из групп и атомов, определенных выше для R1 и R2;
кольцо А представляет собой кольцо бензола или циклогексана;
если кольцо А представляет собой кольцо циклогексана, пунктирная линия в кольце В означает одинарную или двойную связь углерод-углерод, а n равно 1, или если кольцо А представляет собой кольцо бензола, пунктирная линия в кольце В означает одинарную связь углерод-углерод, а n равно 0;
указанная гетероциклическая карбонильная группа представляет собой группу формулы R3-CO, в которой R3 означает гетероциклическую группу, содержащую от 3 до 7 атомов в кольце, из которых от 1 до 3 являются гетероатомами, выбранными из атомов азота, атомов кислорода и атомов серы, а оставшийся атом или атомы, из которых имеется, по меньшей мере, один, является или являются атомами углерода;
указанные алкильные, алкенильные и алкинильные группы и алкильный, алкенильный и алкинильный фрагменты указанных алкилкарбонильной, алкенилкарбонильной и алкинилкарбонильной групп являются незамещенными или содержат, по меньшей мере, один из следующих заместителей ψ:
заместители ψ: гидроксигруппы, меркаптогруппы, атомы галогенов, аминогруппы, алкиламиногруппы, содержащие от 1 до 6 атомов углерода, диалкиламиногруппы, в которых каждая группа алкила содержит от 1 до 6 атомов углерода, карбамоильные группы, нитрогруппы, алкоксигруппы, содержащие от 1 до 6 атомов углерода, алкилтиогруппы, содержащие от 1 до 6 атомов углерода, карбоксигруппы, алкоксикарбонильные группы и незамещенные арильные группы, содержащие от 6 до 10 атомов углерода;
указанные арильные группы, указанные гетероциклические группы и арильные фрагменты указанных арилкарбонильных групп и указанные аралкилкарбонильные группы являются незамещенными или содержат, по меньшей мере, один из следующих заместителей ξ:
заместители ξ: любой из заместителей ψ и алкильные группы, содержащие от 1 до 6 атомов углерода, гидроксиалкильные группы, содержащие от 1 до 6 атомов углерода, и галогеналкильные группы, содержащие от 1 до 6 атомов углерода,
и их фармацевтически приемлемые соли и сложные эфиры.
Активность соединений данного изобретения иллюстрируют с помощью сопровождающих чертежей, в которых
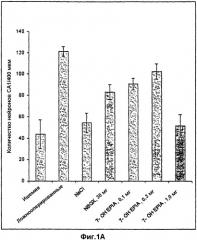
на фиг.1А показаны данные, имеющие отношение к примеру 22, представленные как среднее количество ± SEM (средняя квадратичная ошибка) интактных нейронов на 400 мкм длины области CA1;
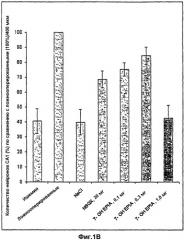
на фиг.1В представлены данные примера 22, выраженные как процент интактных нейронов на 400 мкм длины области CAl по сравнению с ложнооперированными животными, рассматриваемыми как 100%;
на фиг.1С показаны данные примера 22, представленные как абсолютный процент нейропротекции, если количество выживших нейронов в ишемической группе принимали за нуль, а количество выживших нейронов в ложнооперированной группе - за 100%;
на фиг.2 показан размер инфаркта согласно примеру 23 в контрольных, обработанных наполнителем сердцах и обработанных 7β-ОН-EPIA сердцах до, во время и после региональной ишемии; 7β-ОН-EPIA добавляли в перфузат на 25 минуте, региональную ишемию проводили на 55 минуте, ишемическую область повторно перфузировали на 85 минуте;
на фиг.3 представлен коронарный кровоток согласно примеру 23 в контрольных, обработанных наполнителем сердцах и сердцах, обработанных 7β-ОН-EPIA, перед, во время и после региональной ишемии; 7β-ОН-EPIA добавляли в перфузат на 25 минуте, региональную ишемию проводили на 55 минуте, ишемическую область повторно перфузировали на 85 минуте;
на фиг.4 представлена частота сердечных сокращений согласно примеру 23 контрольных, обработанных наполнителем сердец и сердец, обработанных 7β-ОН-EPIA, перед, во время и после региональной ишемии; 7β-ОН-EPIA добавляли в перфузат на 25 минуте, региональную ишемию проводили на 55 минуте, ишемическую область повторно перфузировали на 85 минуте;
на фиг.5 продемонстировано наблюдаемое давление левого желудочка согласно примеру 23 в контрольных, обработанных наполнителем сердцах и сердцах, обработанных 7β-ОН-EPIA, перед, во время и после региональной ишемии; 7β-ОН-EPIA добавляли в перфузат на 25 минуте, региональную ишемию проводили на 55 минуте, ишемическую область повторно перфузировали на 85 минуте;
на фиг.6 представлено конечное диастолическое давление согласно примеру 23 в контрольных, обработанных наполнителем сердцах и сердцах, обработанных 7β-ОН-EPIA, перед, во время и после региональной ишемии; 7β-ОН-EPIA добавляли в перфузат на 25 минуте, региональную ишемию проводили на 55 минуте, ишемическую область повторно перфузировали на 85 минуте.
В описанных выше соединениях формулы (I) группа -OR2 в положении 7 может быть в α- или β-конфигурации, однако предпочтительной является β-конфигурация.
Более предпочтительно в соединениях формулы (I)
R1 и R2 являются одинаковыми или отличаются друг от друга и каждый означает атом водорода, алкильную группу, содержащую от 1 до 6 атомов углерода, необязательно замещенную фенильную группу, формильную группу, алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, арилкарбонильную группу, содержащую от 7 до 11 атомов углерода, аралкилкарбонильную группу, содержащую от 8 до 15 атомов углерода, остаток аминокислоты или гетероциклическую карбонильную группу, которая описана ниже; особенно предпочтительно, что R1 и R2 оба должны представлять собой атомы водорода;
один из Ra и Rb представляет собой алканоильную группу, содержащую от 1 до 6 атомов углерода, или группу формулы -OR4, в которой R4 означает любую одну из групп и атомов, описанных выше для R1 и R2, предпочтительно в β-конфигурации, а другой представляет собой атом водорода, или Ra и Rb вместе означают оксогруппу; особенно предпочтительно, что Ra и Rb должны вместе означать оксогруппу, или что один из Ra и Rb должен означать атом водорода, а другой должен представлять собой гидроксигруппу или алканоильную группу, содержащую от 1 до 4 атомов углерода, особенно гидроксигруппу или ацетильную группу;
указанная гетероциклическая карбонильная группа представляет собой группу формулы R3-CO, в которой R3 соответствует гетероциклической группе, содержащей от 3 до 7 атомов в кольце, из которых 1-3 являются гетероатомами, выбранными из атомов азота, атомов кислорода и атомов серы, а оставшийся атом или атомы, из которых имеется, по меньшей мере, один, является или являются атомами углерода.
Наиболее предпочтительными соединениями формулы (I) являются такие соединения, в которых
R1 и R2 оба представляют собой атомы водорода и
Ra и Rb вместе означают оксогруппу, или один из Ra и Rb представляет собой атом водорода, а другой означает гидроксигруппу или алканоильную группу, содержащую от 1 до 4 атомов углерода, особенно предпочтительна гидроксигруппа или ацетильная группа,
и их фармацевтически приемлемые сложные эфиры.
Примерами 3-оксо-7β-гидроксистероидов, которые можно использовать в данном изобретении, являются соединения формулы (II)
в которой Ra, Rb и R2 являются такими, как описано выше, и предпочтительно Ra и Rb вместе представляют собой оксогруппу или один из Ra и Rb означает атом водорода, а другой представляет собой гидроксигруппу, предпочтительно в β-конфигурации, или ацетильную группу,
и их фармацевтически приемлемые сложные эфиры.
В вышеприведенных соединениях формулы (II) группа -OR2 в положении 7 может быть в α- или β-конфигурации, однако предпочтительной является β-конфигурация.
Более предпочтительно в соединениях формулы (II)
R2 представляет собой атом водорода, алкильную группу, содержащую от 1 до 6 атомов углерода, необязательно замещенную фенильную группу, формильную группу, алкилкарбонильную группу, содержащую от 2 до 5 атомов углерода, арилкарбонильную группу, содержащую от 7 до 11 атомов углерода, аралкилкарбонильную группу, содержащую от 8 до 15 атомов углерода, или гетероциклическую карбонильную группу, которая описана ниже; особенно предпочтительным является то, что R2 должен представлять собой атом водорода;
один из Ra и Rb представляет собой алканоильную группу, содержащую от 1 до 6 атомов углерода, или группу формулы -OR4, в которой R4 означает любую одну из групп и атомов, описанных выше для R2, предпочтительно в β-конфигурации, а другой представляет собой атом водорода, или Ra и Rb, вместе означают оксогруппу; особенно предпочтительно, что Ra и Rb вместе должны представлять собой оксогруппу или что один из Ra и Rb должен означать атом водорода, а другой должен представлять собой гидроксигруппу или алканоильную группу, содержащую от 1 до 4 атомов углерода, в особенности гидроксигруппу или ацетильную группу;
указанная гетероциклическая карбонильная группа представляет собой группу формулы R3-CO, в которой R3 соответствует гетероциклической группе, содержащей от 3 до 7 атомов в кольце, из которых от 1 до 3 являются гетероатомами, выбранными из атомов азота, атомов кислорода и атомов серы, а оставшийся атом или атомы, из которых имеется, по меньшей мере, один, означает или означают атомы углерода;
и их фармацевтически приемлемые сложные эфиры.
Наиболее предпочтительными соединениями формулы (II) являются те соединения, в которых
R2 означает атом водорода и
Ra и Rb вместе представляют собой оксогруппу или один из Ra и Rb является атомом водорода, а другой представляет собой гидроксигруппу или алканоильную группу, содержащую от 1 до 4 атомов углерода, в особенности гидроксигруппу или ацетильную группу,
и их фармацевтически приемлемые сложные эфиры.
В соединениях данного изобретения, в которых R1, R2, R4 или заместитель ξ представляет собой алкильную группу, это может быть алкильная группа с прямой или разветвленной цепью, содержащей от 1 до 6 атомов углерода, и примеры включают в себя группы метила, этила, пропила, изопропила, бутила, изобутила, втор-бутила, трет-бутила, пентила, 1-метилбутила, 2-метилбутила, 3-метилбутила, 1-этилпропила, 2-этилпропила, 1,1-диметилпропила, гексила, 1-метилпентила, 2-метилпентила, 3-метилпентила, 4-метилпентила, 1-этилбутила, 2-этилбутила, 3-этилбутила, трет-гексила и 1,1-диметилпентила, из которых предпочтительными являются группы, содержащие от 1 до 4 атомов углерода, группы метила и этила являются наиболее предпочтительными.
В которых R1, R2 или R4 представляет собой алкенильную группу, которая может быть алкенильной группой с прямой или разветвленной цепью, содержащей от 2 до 6 атомов углерода, а примеры включают в себя группы винила, 1-пропенила, аллила, изопропенила, металлила, 1-, 2-, 3-бутенила, изобутенила, 1-, 2-, 3-, 4-пентенила и группы 1-, 2-, 3-, 4-, 5-гексенила, из которых предпочтительными являются группы алкенила, содержащие от 2 до 4 атомов углерода, наиболее предпочтительны группы винила и аллила.
В которых R1, R2 или R4 представляет собой алкинильную группу, которая может быть алкинильной группой с прямой или разветвленной цепью, содержащей от 2 до 6 атомов углерода, а примеры включают в себя группы этинила, 1-, 2-пропинила, 1-, 2-, 3-бутинила, изобутинила, 1-, 2-, 3-, 4-пентинила и 1-, 2-, 3-, 4-, 5-гексинила, из которых предпочтительными являются группы алкинила, содержащие от 2 до 4 атомов углерода.
В которых R1, R2, R4 или заместитель ψ представляет собой арильную группу, указанная группа представляет собой ароматическую карбоциклическую группу, содержащую от 6 до 10 атомов углерода. Примеры таких групп включают в себя группы фенила, 1-нафтила, 2-нафтила и инденила, из которых предпочтительной является группа фенила. Кроме заместителя ψ, упомянутые группы могут быть замещенными или незамещенными. В случае замещенной группы количество заместителей ограничено только количеством замещаемых положений, и возможно, в некоторых примерах, пространственными ограничениями. Таким образом, в случае фенильных групп максимальное количество заместителей составляет 5, в случае нафтильных групп максимальное количество заместителей составляет 7 и так далее. Однако предпочтительное количество заместителей составляет от 1 до 3, а заместители являются такими, как описано в дальнейшем.
В которых R1, R2 или R4 представляет собой алкилкарбонильную группу, указанная группа представляет собой алканоильную группу, которая может быть группой с прямой или разветвленной цепью, содержащей от 2 до 7 атомов углерода (то есть от 1 до 6 атомов углерода в алкильном фрагменте), а примеры включают в себя группы ацетила, пропионила, бутирила, изобутирила, валерила, изовалерила, пивалоила, гексаноила и гептаноила, из которых предпочтительными являются группы, содержащие от 2 до 5 атомов углерода, наиболее предпочтительными являются группы ацетила и пропионила. Алкильная часть указанной группы может быть замещенной или незамещенной, и, если замещена, заместителей выбирают из заместителей ψ. Примеры таких заместительных групп включают в себя группы аланила, β-аланила, фенилаланила, аспарагинила, цистеинила, гликолоила, глицила, метионила, орнитила, глицероила, тропоила, глутаминила, глутамила, гомоцистеинила, серила, гомосерила, треонила, лактоила, лейцила, изолейцила, норлейцила, лизила, валила, норвалила и саркозила.
В которых R1, R2 или R4 представляет собой алкенилкарбонильную группу, указанная группа может быть алкенилкарбонильной группой с прямой или разветвленной цепью, содержащей от 3 до 7 атомов углерода, а примеры включают в себя группы акрилоила, метакрилоила, кротоноила, изокротоноила, 3-бутеноила, пентоноила и гексеноила, из которых предпочтительными являются алкенилкарбонильные группы, содержащие от 3 до 5 атомов углерода, наиболее предпочтительными являются группы акрилоила и метакрилоила.
В которых R1, R2 или R4 представляет собой алкинилкарбонильную группу, указанная группа может быть алкинилкарбонильной группой с прямой или разветвленной цепью, содержащей от 3 до 7 атомов углерода, а примеры включают в себя группы пропиолоила, 3-бутинилкарбонила, пентинилкарбонила и гексинилкарбонила, из которых предпочтительными являются те алкинилкарбонильные группы, которые содержат от 3 до 5 атомов углерода.
В которых Rc, R1, R2 или R4 представляет собой арилкарбонильную группу, арильная часть указанной группы может быть любой из арильных групп, описанных и приведенных в качестве примера выше. Предпочтительные арилкарбонильные группы включают в себя группы бензоила, o-, м- или п-толуоила, o-, м- или п-анизоила, o-, м- или п-гидроксибензоила, пикрила, галлоила, протокатехоила, ваниллоила, вератроила, антранилоила, 1-нафтоила и 2-нафтоила.
В которых R1, R2 или R4 представляет собой аралкилкарбонильную или аралкенилкарбонильную группу, группа арила и, в зависимости от обстоятельств, алкила или алкенила может быть любой из указанных групп, описанных и приведенных в качестве примера выше. Специальные примеры таких групп включают в себя группы фенилацетила, 3-фенилпропионила, бензилоила, тирозила, атропоила, гидратропоила и циннамоила.
В которых Rc, R1, R2 или R4 представляет собой гетероциклическую карбонильную группу, которая является группой формулы R3-CO-, в которой R3 представляет собой гетероциклическую группу, содержащую от 3 до 7 атомов в кольце, из которых от 1 до 3 являются атомами азота, кислорода или серы, остальные являются атомами углерода. По меньшей мере, один из атомов в кольце должен быть атомом углерода. В соединениях, в которых имеется 3 гетероатома, предпочтительно, что, по меньшей мере, один является атомом азота. Примеры таких групп включают в себя группы 2- и 3-фуроила, 2- и 3-теноила, 2-пиридинкарбонила, никотиноила, изоникотиноила, пролила, пиперидинкарбонила, пиперазинкарбонила и морфолинкарбонила.
В которых R1 и/или R2 представляют собой остаток аминокислоты, указанный остаток может быть любой аминокислотой, в которой гидроксигруппа удалена или карбокси (-СООН) группой. Примеры таких аминокислотных остатков включают в себя группы аланила, β-аланила, цистатионила, цистила, глицила, гистидила, гомосерила, изолейцила, лантионила, лейцила, лизила, метионила, норлейцила, норвалила, орнитила, пролила, саркозила, серила, треонила, тиронила, тирозила, валила, цистеинила, гомоцистеинила, триптофила, α-аспартила, β-аспартила, аспартоила, аспарагинила, α-глутамила, γ-глутамила и глутаминила.
В которых Rc представляет собой группу алканоила, указанная группа может быть группой с прямой или разветвленной цепью, содержащей от 1 до 6 атомов углерода, а примеры таких групп включают в себя группы формила, ацетила, пропионила, бутирила, изобутирила, валерила, изовалерила, пивалоила, гексаноила и гептаноила, из числа которых предпочтительными являются группы, содержащие от 2 до 5 атомов углерода, более предпочтительными являются группы ацетила и пропионила, а наиболее предпочтительной является ацетильная группа.
В которых заместитель ψ или заместитель ξ представляет собой алкиламиногруппу, содержащую от 1 до 6 атомов углерода, алкильная часть может быть любой из групп алкила, описанных и приведенных в качестве примеров выше. Предпочтительные примеры таких алкиламиногрупп включают в себя группы метиламино, этиламино, пропиламино, изопропиламино, бутиламино, изобутиламино, втор-бутиламино, трет-бутиламино, пентиламино, изопентиламино, неопентиламино, трет-пентиламино, гексиламино и изогексиламино, из числа которых предпочтительны группы, содержащие от 1 до 4 атомов углерода, наиболее предпочтительными являются группы метиламино и этиламино.
В которых заместитель ψ или заместитель ξ представляет собой диалкиламиногруппу, каждая алкильная часть содержит от 1 до 6 атомов углерода, а две алкильные группы могут быть одинаковыми или отличаться друг от друга. Алкильные группы могут быть любыми из групп алкила, описанных и приведенных в качестве примеров выше. Предпочтительные примеры таких диалкиламиногрупп включают в себя группы диметиламино, метилэтиламино, диэтиламино, метилпропиламино, дипропиламино, диизопропиламино, этилбутиламино, дибутиламино, ди-трет-бутиламино, метилпентиламино, дипентиламино, диизопентиламино и дигексиламино, из числа которых предпочтительными являются группы, содержащие от 1 до 4 атомов углерода в каждой алкильной группе, наиболее предпочтительными являются группы диметиламино и диэтиламино.
В которых заместитель ψ или заместитель ζ представляет собой алкоксигруппу, указанная группа может быть алкоксигруппой с прямой или разветвленной цепью, содержащей от 1 до 6 атомов углерода, а примеры таких групп включают в себя группы метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси, изопентилокси, неопентилокси, трет-пентилокси, гексилокси и изогексилокси, из числа которых предпочтительны группы, содержащие от 1 до 4 атомов углерода, наиболее предпочтительными являются группы метокси и этокси.
В которых заместитель ψ или заместитель ζ представляет собой алкилтиогруппу, содержащую от 1 до 6 атомов углерода, алкильная часть может быть любой из групп алкила, описанных и приведенных в качестве примеров выше. Предпочтительные примеры таких алкилтиогрупп включают в себя группы метилтио, этилтио, пропилтио, изопропилтио, бутилтио, изобутилтио, втор-бутилтио, трет-бутилтио, пентилтио, изопентилтио, неопентилтио, трет-пентилтио, гексилтио и изогексилтио, из числа которых те группы, которые содержат от 1 до 4 атомов углерода, являются предпочтительными, наиболее предпочтительны группы метилтио и этилтио.
В которых заместитель ψ или заместитель ζ представляет собой алкоксикарбонильную группу, указанная группа может быть алкоксикарбонильной группой с прямой или разветвленной цепью, содержащей от 2 до 7 атомов углерода, а примеры таких групп включают в себя метоксикарбонильную, этоксикарбонильную, пропоксикарбонильную, изопропоксикарбонильную, бутоксикарбонильную, изобутоксикарбонильную, втор-бутоксикарбонильную, трет-бутоксикарбонильную, пентилоксикарбонильную, изопентилоксикарбонильную, неопентилоксикарбонильную, трет-пентилоксикарбонильную, гексилоксикарбонильную и изогексилоксикарбонильную группы, из числа которых предпочтительными являются группы, содержащие от 1 до 4 атомов углерода, наиболее предпочтительными являются метоксикарбонильные и этоксикарбонильные группы.
В которых заместитель ζ представляет собой группу гидроксиалкила, содержащую от 1 до 6 атомов углерода, алкильная часть может быть любой из групп алкила, описанных и приведенных в качестве примеров выше. Предпочтительные примеры таких групп гидроксиалкила включают в себя группы гидроксиметила, 1- и 2-гидроксиэтила, 1-, 2- и 3-гидроксипропила, 1,2-дигидроксиэтила, 1,2,3-тригидроксипропила, 4-гидроксибутила, 5-гидроксипентила и 6-гидроксигексила.
В которых заместитель ζ представляет собой группу галогеналкила, содержащую от 1 до 6 атомов углерода, предпочтительно от 1 до 4 атомов углерода, алкильный фрагмент может быть таким, как описанные и приведенные в качестве примера выше, а атомом галогена предпочтительно является хлором, фтором, бромом или йодом. Примеры таких групп включают в себя группы фторметила, хлорметила, бромметила, йодметила, дихлорметила, дифторметила, трихлорметила, трифторметила, 2,2,2-трихлорэтила, 2-хлорэтила, 2-фторэтила, 2-бромэтила, 2-йодэтила, 2,2-дибромэтила, 2,2,2-трибромэтила, 3-фторпропила, 3-хлорпропила, 4-бромбутила, 4-фторбутила, 5-фторпентила и 6-фторгексила.
Следует оценить, что когда соединение содержит группу формулы -OR, в которой R представляет собой любую из групп и атомов, описанных выше относительно R1 и так далее, возможно, активным типом является соединение, содержащее свободную гидроксигруппу. Соответственно, любую группу, которая может in vivo превращаться в гидроксигруппу, можно использовать вместо гидроксигруппы.
Специальные примеры соединений, которые можно применять в данном изобретении, включают в себя следующие:
Из числа приведенных выше соединений предпочтительными являются 7β-изомеры.
Когда соединения данного изобретения содержат гидроксигруппу, их можно превращать в соответствующие соли или сложные эфиры, что хорошо известно в данной области, и не существует никакого особого ограничения относительно природы образованной соли или сложного эфира. Если указанные соли или сложные эфиры предназначены для введения пациенту, они должны быть фармацевтически приемлемыми. Однако, если соединения предназначены для некоторых других целей, например для использования в виде интермедиата в другом синтезе, даже в таком случае упомянутое ограничение не является необходимым. Соли и сложные эфиры могут быть выбраны из солей и эфиров, хорошо известных в данной области для описанного типа соединения. Предпочтительными сложными эфирами являются сложные эфиры карбоновых кислот и сложные эфира аминокислот, таких как, например, аланин, β-аланин, цистатионин, цистин, глицин, гистидин, гомосерин, изолейцин, лантионин, лейцин, лизин, метионин, норлейцин, норвалин, орнитин, пролин, саркозин, серин, треонин, тиронин, тирозин, валин, цистеин, гомоцистеин, триптофан, аспарагиновая кислота, аспарагин, глутаминовая кислота и глутамин.
Соединения данного изобретения можно получать, начиная с исходных стероидов, с помощью целого ряда способов, хорошо известных специалистам. Например, их можно получать по способам, описанным в литературе, упомянутой выше, которые дают смесь 7β- и соответствующих 7α-соединений, которые, если желательно, затем можно разделить с помощью известных технологий. Однако при некоторых обстоятельствах может быть необходимо или удобно использовать смесь 7α- и 7β-изомеров без разделения их.
Например, 7α-гидрокси-EPIA и 7β-гидрокси-EPIA можно получать из DHEA в результате окисления аллила после защиты 3β-гидроксигруппы и 17-кетонной группы, используя общепринятые способы. Затем продукт восстанавливают катализатором, растворимым соединением металла (таким как гидрид натрия) и снимают защиту с 3β-гидрокси- и 17-кетонных групп. Потом 7α-гидрокси- и 7β-гидроксиэпимеры можно разделить по общепринятым способам, например методом колоночной хроматографии, а 7α-гидрокси-EPIA и 7β-гидрокси-EPIA для очистки можно кристаллизовать.
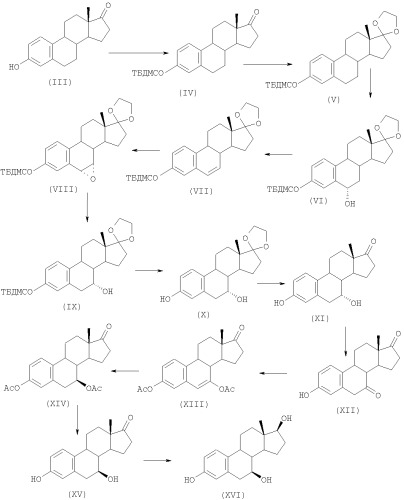
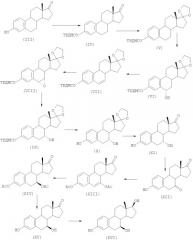
Альтернативный способ синтеза представлен в следующей схеме реакций:
В вышеприведенных формулах ТБДМСО означает трет-бутилдиметилсилилокси, а Ас означает ацетил. При использовании в дальнейшем указанные сокращения имеют такие же значения.
На первой стадии вышеприведенной схемы реакций соединение формулы (III), эстрон, защищают трет-бутилдиметилсилилоксигруппой обычным способом, чтобы получить защищенное соединение формулы (IV). Затем полученное соединение вводят в реакцию с этиленгликолем в присутствии кислотного катализатора (такого как п-толуолсульфоновая кислота), чтобы защитить кетогруппу в положении 17 и получить соединение формулы (V). Затем гидроксигруппу вводят в положение 6, что иллюстрируют в дальнейшем в примере 3, чтобы получить соединение формулы (VI), которое потом дегидратируют для получения соединения формулы (VII). Последнее эпоксидируют с получением соединения формулы (VIII), которое затем восстанавливают до соединения формулы (IX) с 7α-гидроксигруппой. Защитную группу трет-бутилдиметилсилила удаляют, получая соединение формулы (Х), а полученное соединение нагревают с каталитическим количеством кислоты, чтобы получить 7α-гидроксиэстрон (XI), который можно использовать в данном изобретении. Потом полученное соединение можно окислить, например, используя хромовую кислоту/фосфорную кислоту, чтобы получить 7-кетоэстрон (XII), который затем вводят в реакцию с уксусным ангидридом для получения соединения формулы (XIII). Полученное соединение гидрируют, используя, например, водород в присутствии палладиевого катализатора, чтобы получить соединение формулы (XIV), и наконец удаляют ацетильные группы, чтобы получить 7β-гидроксиэстрон (XV), соединение данного изобретения. Если требуется, полученное соединение можно восстановить, чтобы получить 7β-гидроксиэстрадиол (XVI), также соединение данного изобретения. Соответствующее 7α-соединение можно получать аналогичным способом из 7α-гидроксиэстрона (XI).
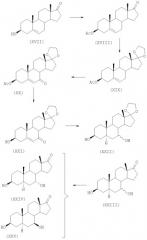
Другие 7α- и 7β-гидроксисоединения данного изобретения можно получать подобным способом, например 7β-гидрокси-DHEA может быть получен, как показано с помощью следующей схемы реакции:
По приведенной схеме реакций DHEA (XVII) ацетилируют, чтобы получить соответствующий ацетат формулы (XVIII), который затем вводят в реакцию с этиленгликолем для получения кеталя формулы (XIX). Затем кеталь (XIX) окисляют, как описано в примере 16, чтобы получить соответствующее 7-кетосоединение (ХХ), которое потом деацетилируют с получением соединения формулы (XXI). Полученное соединение восстанавливают, чтобы получить 7-гидрокси-17-кеталь-EPIA формулы (XXII), который затем обрабатывают кислотой, чтобы удалить группу кеталя и получить 7-гидрокси-EPIA, который, в конце концов, разделяют на 7β- и 7α-изомеры методом хроматографии, чтобы получить 7α-гидрокси-EPIA (XXIV) и 7β-гидрокси-EPIA (XXV).
Каждая из стадий приведенных выше схем реакций в отдельности хорошо известна и может быть осуществлена с использованием известных растворителей и катализаторов (если уместно) и при известных реакционных условиях, например, временные и температурные условия.
Описанные выше соединения характеризуются нейропротективным действием. В соответствии с данным изобретением установлено, что указанные соединения также обладают кардиопротективным действием, и поэтому их можно применять для предупреждения или лечения заболеваний сердца, развивающихся в результате ишемического поражения, например инфаркта миокарда. Соединения также обладают способностью защищать против ишемического поражения почек, например гломерулонефрита или острой почечной недостаточности. Вообще, на основании продемонстрированной активности можно предсказать, что соединения будут оказывать подобное защитное действие на ткани других периферических органов.
Действительно, соединения данного изобретения также можно использовать для лечения повреждения спинного мозга.
Соединения данного изобретения можно применять пациенту, если предполагают, что у пациента существует опасность ишемии, особенно инфаркта миокарда или ишемического поражения почек. Такое профилактическое применение может быть очень эффективным. Однако также продемонстрировано, что соединения данного изобретения оказывают эффективное действие, даже если применять их после ишемического события, но следует принимать во внимание, что предпочтительно вводить соединения, как только становится возможным, чтобы насколько возможно избежать поражения миокарда или ткани почек. При некоторых обстоятельствах может быть необходимым введение повторных доз, особенно когда у пациента сохраняется опасность ишемии.
Соединения также можно вводить профилактически при антиципации повреждения спинного мозга или можно применять для лечения такого повреждения после его появления.
Для того чтобы достигнуть насколько возможно желаемого результата, подходящими способами введения обычно является инъекция. Таким образом, внутривенная инъекция оказывается особенно предпочтительной.
Доза соединения данного изобретения будет изменяться в зависимости от многих факторов, включая возраст, массу тела и общее состояние пациента, а также способа, частоты и пути введения. Однако обычно рекомендуют дозу от 0,01 до 50 мг/кг массы тела, доза от 0,05 до 20 мг/кг является более предпочтительной. Дозу можно вводить в виде однократной дозы или в виде разделенной общей дозы.
В дальнейшем изобретение иллюстрируют следующими, не ограничивающими изобретение примерами, из которых примеры 1-20 иллюстрируют получение соединений данного изобретения, а примеры 21-23 демонстрируют их активность. В примерах 1-20 римские цифры относятся к формулам в представленных выше схемах реакций.
ПРИМЕР 1
3-трет-Бутилдиметилсилилэстрон (IV)
4,25 г трет-бутилдиметилсилилхлорида (28,2 ммоль, 3 экв.) добавляли к раствору 50 мл диметилформамида (ДМФ), содержащему 2,54 г эстрона (III) (9,41 ммоль, 1 экв.) и 3,84 г имидазола (56,5 ммоль, 6 экв.), в трехгорлой колбе на 100 мл. Затем смесь оставляли на ночь при комнатной температуре в атмосфере азота. 10% мас./об. водный раствор карбоната калия добавляли в реакционную смесь, которую затем экстрагировали этилацетатом. Органическую фазу промывали водой, а потом высушивали над безводным сульфатом натрия и выпаривали досуха. Получали 3,76 г 3-трет-бутилдиметилсилилэстрона (IV) (9,41 ммоль, 100%).
ПРИМЕР 2
17-Кеталь-3-трет-бутилдиметилсилилэстрон (V)
Раствор 60 мл толуола, содержащий 3 г 3-трет-бутилдиметилсилилэстрона (IV) (7,50 ммоль), 3 мл этиленгликоля и каталитическое количество п-толуолсульфоновой кислоты, нагревали до кипения с обратным холодильником с перегонкой с водяным паром, используя аппарат Дина-Старка (Dean-Stark), в течение 24 часов. Затем реакционную среду вливали в 50 мл 10% мас./об. водного раствора карбоната калия. Органическую фазу сливали. Водную фазу экстрагировали этилацетатом. Органические фазы объединяли и выпаривали досуха. Получали 3,16 г 17-кеталь-3-трет-бутилдиметилсилилэстрона (V) (7,12 ммоль, 95%).
ПРИМЕР 3
6α-гидрокси-17-кеталь-3-трет-бутилдиметилсилилэстрон (VI)
В 1-литровой трехгорлой колбе проводили дегазацию 100 мл раствора безводного тетрагидрофурана (ТГФ) промывкой азотом и охлаждали до -80°C. В реакционную среду добавляли диизопропиламин (20 мл,