Инъекционная лекарственная форма, обладающая нейропротекторными свойствами
Иллюстрации
Показать всеИзобретение относится к области медицины, конкретно к лекарственному препарату - деанола ацеглумату. Предложена инъекционная лекарственная форма деанола ацеглумата, содержащая следующие компоненты: деанол ацеглумат, сахара (сорбит, ксилит и др.), аминоуксусную кислоту, трилон Б, необязательно янтарную, яблочную кислоты, N-диметиламиноэтанол. Показано, что инъекционная лекарственная форма деанола ацеглумата обладает нейропротекторной активностью и может применяться при острых нарушениях мозгового кровообращения и препятствует развитию ишемических повреждений мозга. Технический результат представляет собой создание стабильной стерильной инъекционной лекарственной формы деанола ацеглумата, пригодной для использования больными диабетом. 2 н. и 1 з.п. ф-лы, 2 табл., 2 ил.
Реферат
Изобретение относится к области медицины, конкретно к лекарственному препарату, обладающему нейропротекторными свойствами, в качестве которого предлагается деанола ацеглумат: 2-(диметиламино) этанола N-ацетил-L-глутамат формулы I и его инъекционной лекарственной форме.
Деанола ацеглумат известен как малотоксичный ноотропный препарат [Машковский М.Д., Лекарственные средства, М., 14-е изд., 2000 г, т.1, с.110].
По своей химической структуре он близок к естественным метаболитам мозга (ГАМК, глутаминовая кислота). Препарат обладает церебропротективными свойствами с отчетливым ноотропным, психостимулирующим и психогармонизирующим действием. Кроме того, установлено, что деанола ацеглумат обладает гепатопротекторными свойствами [Патент РФ №2068408, 1992. Патент РФ №2111747, 1996]. Клинические исследования препарата деанола ацеглумата под названием нооклерин позволили рекомендовать его в качестве эффективного антиастенического средства [П.В.Морозов. Новый отечественный ноотропный препарат «Нооклерин»», Ж. «Психиатрия и психофармакотерапия», том 05, №6, 2003]. В ходе проведения доклинических и клинических испытаний препарат известен под названиями Деманол, Нооклер, Глютабианц, Нооклерин.
Ввиду крайней гигроскопичности субстанцию деанола ацеглумата не хранят в свободном состоянии, а готовят и используют в виде водного раствора для перорального применения.
Зарубежные лекарственные формы для перорального применения препаратов на основе деанола ацеглумата содержат весьма значительное количество сахара (до 40%), что не обеспечивает необходимую стабильность препарата при хранении, а также делает практически невозможным их использование больными диабетом.
Во Всероссийском научном центре по безопасности биологически активных веществ разработана оригинальная лекарственная форма в виде водного раствора для перорального применения, выгодно отличающаяся от зарубежных аналогов и содержащая вместо сахара ксилит или сорбит [Патент РФ №1561256 (1990).].
Однако жидкая лекарственная форма деанола ацеглумата для перорального применения не может быть использована для инъекций, поскольку не является стерильной и содержит в своем составе такие консерванты, как эфиры 4-оксибензойной кислоты, которые нежелательны для инъекционного использования.
Целью предлагаемого изобретения является создание инъекционной лекарственной формы деанола ацеглумата и применение ее по новым показаниям в качестве нейропротектора, препятствующего развитию ишемических повреждений мозга.
В литературе не описана инъекционная лекарственная форма деанола ацеглумата и отсутствуют данные о применении деанола ацеглумата в качестве нейропротектора для профилактики и лечения нарушений мозгового кровообращения ишемического генеза.
Особенность и сложность создания инъекционной лекарственной формы деанола ацеглумата заключается в создании стерильного стабильного раствора, пригодного для применения в виде инъекций. Кроме того, необходимо, чтобы раствор для инъекций с таким активным компонентом, как деанола ацеглумат, имеющим кислую реакцию (pH водного раствора чистого вещества имеет от 3,5 до 4,0), обладал определенной величиной pH в интервале от 4,0 до 5,0.
В связи с этим нами были изучены различные вспомогательные вещества, стабилизирующие субстанцию деанола ацеглумата в разбавленном растворе, и вещества, биологически приемлемые для использования в виде инъекций.
В качестве вспомогательных веществ были исследованы разнообразные консерванты: сахара (сорбит, ксилит, манит и др.), комплексообразователи, антиоксиданты и др.
В качестве веществ основного характера для стабилизации pH раствора были исследованы различные органические и неорганические основания (аминоспирты, карбонаты щелочных и щелочноземельных металлов и др.), обеспечивающие pH раствора от 4,0 до 5,0.
В результате экспериментальных исследований были выбраны вспомогательные вещества, обеспечивающие стабильность деанола ацеглумата в разбавленных растворах различных концентраций (0,5-10,0%).
Предлагаемая инъекционная лекарственная форма деанола ацеглумата содержит: деанола ацеглумат, сахара, трилон Б, аминоуксусную кислоту, при необходимости янтарную и яблочную кислоты при следующем соотношении компонентов, мас.%:
| Деанола ацеглумат | 0,5÷10,0 |
| Сахара | 1,0÷5,0 |
| Аминоуксусная кислота | 0,2÷2,0 |
| N-диметиламиноэтанол | 0,0÷1,0 |
| Трилон Б | 0,01÷0,1 |
| Янтарная кислота | 0÷2,0 |
| Яблочная кислота | 0÷3,0 |
В качестве сахаров-консервантов используют преимущественно сорбит, ксилит, манит.
Следующие примеры иллюстрируют изобретение.
Пример 1. В колбу загружают 800-850 мл стерильной воды для инъекций, добавляют последовательно 20,0 г деанола ацеглумата, 10,0 г сорбита, 2,0 г аминоуксусной кислоты, 0,64 г N-диметиламиноэтанола, 0,1 г трилона Б, 5,0 г янтарной кислоты. Массу перемешивают до полного растворения компонентов, доводят объем до 1000 мл. Раствор деанола ацеглумата подвергают стерилизующей фильтрации и разливают в ампулы по 2 мл. Полученный раствор отвечает всем требованиям Госфармакопеи XI издания (см. таблицу 1).
Пример 2. Получение раствора деанола ацеглумата осуществляют по примеру 1 исходя из 5,0 г деанола ацеглумата, 0,46 г N-диметиламиноэтанола, 10,0 г ксилита, 10,0 г аминоуксусной кислоты, 0,5 г трилона Б, 5,0 г яблочной кислоты. Получают раствор деанола ацеглумата, отвечающий всем нормативным требованиям (см. таблицу 1).
Пример 3. Получение раствора деанола ацеглумата осуществляют аналогично примеру 1 исходя из 50,0 г деанола ацеглумата, 20,0 г манита, 15,0 г аминоуксусной кислоты, 1,0 г трилона Б, 30,0 г яблочной кислоты. Получают раствор деанола ацеглумата, отвечающий всем нормативным требованиям (см. таблицу 1).
Пример 4. Получение раствора деанола ацеглумата осуществляют аналогично примеру 1 исходя из 100,0 г деанола ацеглумата, 10,0 г N-диметиламиноэтанола 50,0 г сорбита, 20,0 г аминоуксусной кислоты, 1,0 г трилона Б, 10,0 г янтарной кислоты. Получают раствор деанола ацеглумата, отвечающий всем нормативным требованиям (см. таблицу 1).
Полученный раствор деанола ацеглумата отвечает всем требованиям Госфармакопеи СССР XI издания и нормативным требованиям на препарат деанола ацеглумат (см. таблицу 1) и сохраняет свою стабильность в течение не менее двух лет (в соответствии с требованиями, предъявляемыми к лекарственным препаратам).
Фармакологические исследования инъекционной лекарственной формы деанола ацеглумата в качестве нейропротектора
Наиболее близким аналогом деанола ацеглумата по нейропротекторной активности является препарат пикамилон, который был использован при фармакологических исследованиях в качестве препарата сравнения, учитывая при этом, что недостатком пикамилона является его свойство снижать артериальное давление в постишемическом периоде, что может провоцировать ишемические повреждения мозга [Гусев Е.И., Никифоров А.С., Гехт А.Б. Лекарственные средства в неврологической клинике: Руководство для врачей. - М.: МЕДпресс-информ, 2003. - 416 с.].
Эксперименты выполнены на 70 беспородных крысах-самцах массой 200-220 г. Нейропротекторную активность деанола ацеглумата оценивали путем сравнения с пикамилоном - нейропротетором с ноотропным типом действия.
Циркуляторную гипоксию моделировали с помощью гравитационных перегрузок в кранио-каудальном направлении. Градиент нарастания и спада нагрузки составлял 0,30-0,33 ед. в сек. Бодрствующих крыс помещали в специальные контейнеры-пеналы, укрепленные к концам рычагов центрифуги, а мощный двигатель в течение 10 с создавал необходимую степень гравитации. Критерием противогипоксического действия являлся % выживания животных в сравнении с контролем. Деанола ацеглумат и пикамилон в дозах 1 мг/кг, 10 мг/кг и 50 мг/кг вводили профилактически (за 30 мин до моделирования гипоксии).
В качестве модели ишемии мозга использовали одностороннюю окклюзию левой сонной артерии в течение 3-х суток. Эксперименты проведены на 3-х группах лабораторных животных: контрольной (1 группа) и опытных, которым вводили терапевтически деанола ацеглумат (2 группа) и пикамилон (3 группа) в суточной дозе 10 мг/кг (однократно) в течение 3-х суток. Контрольной группе вводили физиологический раствор в эквивалентных объемах. На 4-й день у животных под уретано-хлоралозным наркозом делали забор крови из сагиттального синуса.
Концентрацию вторичных продуктов ПОЛ в мозге в пересчете на малоновый диальдегид (МДА) проводили по тесту с тиобарбитуровой кислотой. Структурно-функциональные свойства мембран эритроцитов оценивали по изменению накопления в них концентрации МДА. Биоантиоксидантную защиту мозга определяли по каталазной и супероксиддисмутазной активности. Активность каталазы и супероксиддисмутазы определяли спектрофотометирически. Содержание пировиноградной кислоты (ПВК) в крови производили модифицированным методом Умбрайта. Содержание молочной кислоты (МоК) в крови определяли по Балоховскому-Наточину.
Статистическую обработку результатов проводили внутри серий по t-критерию Стьюдента (методом попарных сравнений), между сериями - по критерию инверсий Вилкоксона-Манна-Уитни.
На фиг.1 и 2 представлены данные фармакологического изучения деанола ацеглумата в сравнении с пикамилоном.
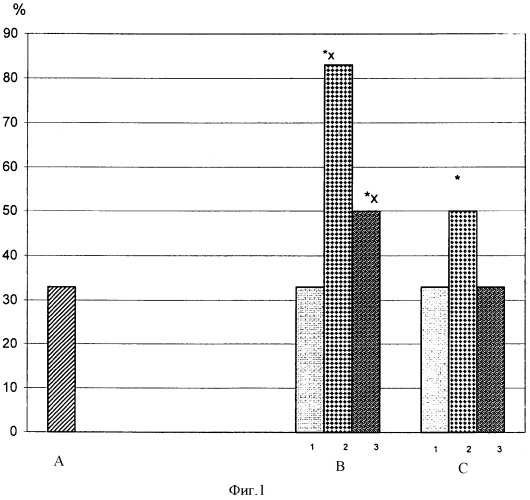
Наиболее выраженное увеличение выживаемости белых крыс (до 83%) в условиях гравитационных перегрузок было отмечено при применении деанола ацеглумата в дозе 10 мг/кг (фиг.1).
Препарат сравнения пикамилон повышал выживаемость экспериментальных животных лишь в дозе 10 мг/кг (50%), а деанола ацеглумат в дозах 10 и 50 мг/кг. Таким образом, нейропротекторная активность деанола ацеглумат на модели тотальной ишемии мозга существенным образом превосходила активность пикамилона.
При анализе эффективности терапевтического применения деанола ацеглумата и пикамилона в условиях ишемического повреждения мозга установлено, что деанола ацеглумат активирует процесс утилизации глюкозы мозгом, блокирует гипопротеинимею и существенным образом ограничивает процессы перокисдации липидов мозга. Так, в опытах с деанола ацеглуматом констатировали снижение вторичных продуктов пероксидации - ТБК-активных продуктов - как в правом (на 26,6%), так и в левом (на 44,5%) полушариях мозга относительно контрольных опытов (табл.2).
Терапевтическое введение пикамилона не способствовало угнетению образования ТБК активных продуктов в правом полушарии мозга, более того, в зоне повреждения - левом полушарии, изучаемый показатель был выше, чем в контрольных опытах на 58,0% (табл.2).
Таким образом, терапевтическое применение деанола ацеглумата ограничивает процессы пероксидации липидов на стадии образования первичных продуктов ПОЛ. Действие пикамилона на процессы пероксидации липидов менее выражено, и оно связано с воздействием на процесс перехода первичных во вторичные продукты ПОЛ (табл.2).
Об эффективности применения деанола ацеглумата при ишемических повреждениях мозга свидетельствует и тот факт, что у животных, которым был введен данный препарат, уровень средних молекул был на 37,7% ниже, чем в контроле (табл.2). Введение пикамилона в той же дозе менее выраженно препятствует развитию эндогенной интоксикации (на 23,1%) (табл.2).
Таким образом, выраженность токсемии в опытах с пикамилоном на 14% превышает выраженность данного процесса при введении деанола ацеглумата.
В опытах с деанола ацеглуматом и пикамилоном активность каталазы была существенно ниже активности СОД (фиг.2). Так, увеличение активности фермента, обезвреживающего перекись водорода, в опытах с деанола ацеглуматом была на 15±2,4%, а в опытах с пикамилоном на 25±3,1% выше, чем в контрольных опытах (табл.2). В то время как активность фермента, воздействующего на супероксиданион, существенным образом повышалась, чем в контроле: на 123,2±24,6% при применении АКФ 90-7 и на 53,9±15,6% при использовании деанола ацеглумата (табл.2).
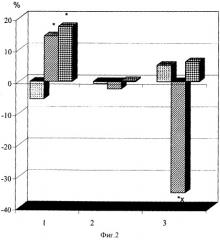
При анализе утилизации мозгом глюкозы и его основных метаболитов - пирувата и лактата - установлено, что применение деанола ацеглумата и пикамилона препятствует вызванной ишемией утилизацию глюкозы мозгом. Это является важным прогностическим моментом, так как для мозга глюкоза является основным источником АТФ. Установлено также, что деанола ацеглумат существенным образом угнетает утилизацию лактата мозгом, в то время как пикамилон не оказывает влияния на данный показатель (фиг.2).
Проведенное исследование свидетельствует, что терапевтическое применение деанола ацеглумата в дозе 10 мг/кг в условиях ишемии мозга, вызванной односторонней окклюзией левой сонной артерии, более эффективно, чем применение пикамилона. Применение деанола ацеглумата препятствует развитию ишемических повреждений мозга.
Краткое описание чертежей
Фиг.1 - Влияние деанола ацеглумата и пикамилона на выживаемость животных (в %) при гравитационных перегрузках в кранио-каудальном положении
А - контроль, В - деанола ацеглумат, С - пикамилон
1 - доза 1 мг/кг; 2 - доза 10 мг/кг; 3 - доза 50 мг/кг.
Обозначены статистически значимые изменения (Р<0,05) относительно:
* - контрольных опытов, x - опытов с пикамилоном.
Фиг.2 - Утилизация мозгом (в %) глюкозы, пирувата и лактата в контрольных опытах и при применении деанола ацеглумата и пикамилона 1 - утилизация глюкозы, 2 - утилизация пирувата, 3 - утилизация лактата
Контрольные опыты
Опыты с деанола ацеглуматом
Опыты с пикамилоном
Обозначены статистически значимые изменения (Р<0,05) относительно:
* - контрольных опытов, х - опытов с пикамилоном.
| Таблица 1 | |||||
| Показатель | Норма | Пример 1 | Пример 2 | Пример 3 | Пример 4 |
| 1 | 2 | 3 | 4 | 5 | 6 |
| 1. Описание | Бесцветная или слегка окрашенная жидкость. | Бесцветная жидкость | Бесцветная жидкость | Слегка окрашенная жидкость | Бесцветная жидкость |
| 2. Прозрачность | Препарат должен быть прозрачным (ГФ XI, вып.1, с.198). | Прозрачен | Прозрачен | Прозрачен | Прозрачен |
| 3. Цветность | Окраска раствора не интенсивнее эталона №7б (ГФ XI, вып.1, с.194). | Не интенсивнее эталона №7б | Не интенсивнее эталона №7б | Не интенсивнее эталона №7б | Не интенсивнее эталона №7б |
| 4. Посторонние примеси | Глутаминовая кислота не более 0,5% | менее 0,5% | менее 0,5% | менее 0,5% | менее 0,5% |
| 5. Стабильность | 2 года при 20°С | 2 года | 2 года | 2 года | 2 года |
| Таблица 2 | |||
| Изменения биохимических показателей в контрольных опытах и в опытах с деанола ацеглуматом и пикамилоном у животных с ишемией мозга | |||
| Изучаемые показатели | Контрольные животные | Изменения в % относительно контрольных опытов | |
| в опытах с деанола ацеглуматом | в опытах с пикамилоном | ||
| Каталаза в сыворотке, мг Н2О2/мин | 0,041±0,020 | +22,7±6,4* | +15,3±5,6* |
| СОД в сыворотке, ЕД/мг белка | 1,32±0,030 | +123,2±24,6*x | +53,9±15,6* |
| Белок в сыворотке, ммоль/л | 54,2±8,6 | +69,2±8,2 | +83,4±9,9* |
| ПВК в артериальной крови, мкмоль/л | 0,176± | -2,9±5,6 | -10,6±3,6* |
| ПВК в венозной крови, мкмоль/л | 0,174± | +0,5±5,7 | -10,1±4,2* |
| МоК в артериальной крови, ммоль/л | 0,70±0,02 | -5,4±5,0 | +4,3±6,3 |
| МоК в венозной крови, ммоль/л | 0,68±0,03 | +29,4±7,8*x | +5,4±5,5 |
| Глюкоза в артериальной крови, ммоль/л | 3,4±0,14 | +44,1±9,6* | +33,3±6,3* |
| Глюкоза в венозной крови, ммоль/л | 3,6±0,20 | +16,7±4,6* | +4,8±6,5 |
| Средние молекулы, у.е. | 0,53±0,003 | -37,7±7,0* | -23,1±5,1* |
| ТБК-мозга правое полушарие, нмоль/г | 15,4±0,2 | -26,6±7,1*x | -8,4±5,3 |
| ТБК- мозга продукты левое полушарие, нмоль/г | 16,40±0,3 | -44,5±7,2x* | +58,1±7,6* |
| Обозначены статистически значимые изменения (Р<0,05) относительно: | |||
| * - контрольных опытов; х - опытов с пикамилоном. |
1. Инъекционная лекарственная форма деанола ацеглумата, обладающая нейропротекторной активностью, отличающаяся тем, что содержит деанола ацеглумат, сахара, аминоуксусную кислоту, трилон Б, при необходимости N-диметиламиноэтанол, янтарную и яблочную кислоты при следующем соотношении компонентов, мас.%:
| Деанола ацеглумат | 0,5÷10,0 |
| Сахара | 1,0÷5,0 |
| Аминоуксусная кислота | 0,2÷2,0 |
| N-диметиламиноэтанол | 0,0÷1,0 |
| Трилон Б | 0,01÷0,1 |
| Янтарная кислота | 0÷2,0 |
| Яблочная кислота | 0÷3,0 |
| Стерильная вода для инъекций | Остальное |
2. Лекарственная форма по п.1, отличающаяся тем, что в качестве сахаров содержит сорбит, ксилит, манит.
3. Применение лекарственной формы по пп.1 и 2 в качестве лекарственного средства при острых нарушениях мозгового кровообращения и препятствующего развитию ишемических повреждений мозга.