Способ фотометрического определения железа (iii) в растворах чистых солей
Иллюстрации
Показать всеГруппа изобретений относится к аналитической химии, а именно к фотометрическому определению малых концентраций железа (III) в растворах чистых солей. Способ осуществляют путем переведения железа (III) в окрашенное комплексное соединение в слабокислой среде, причем к раствору железа (III) добавляют 2 мл ацетатного буферного раствора с рН 4,7-5,7, 0,7-1 мл раствора поверхностно-активного вещества, содержащего 0,2% раствора полиоксиэтилен сорбитан моноолеата, 0,2% раствора моноалкилфенилового эфира полиэтиленгликоля на основе полимердистиллята и воду в соотношении 1:1:1, и 90-110-кратный избыток алюминона, затем полученный раствор доводят водой до 4 мл, нагревают на водяной бане при температуре 80-98°С в течение 2-3 минут и фотометрируют при длине волны 364 нм. По другому варианту осуществления способа к раствору железа (III) добавляют 2 мл ацетатного буферного раствора с рН 4,3-4,8, 0,1-0,2 мл раствора поверхностно-активного вещества, содержащего 0,2% водный раствор полиоксиэтилен изооктилфенилового эфира, и 8-12-кратный избыток ксиленолового оранжевого, затем полученный раствор доводят водой до 10 мл, нагревают на водяной бане при температуре 80-98°С в течение 2-3 минут и фотометрируют при длине волны 490 нм. Достигается повышение чувствительности и селективности анализа. 2 н.п. формулы, 10 ил.
Реферат
Изобретение относится к области аналитической химии, а именно к фотометрическому методу анализа, и может быть использовано для определения содержания железа (III) в растворах чистых солей, содержащих железо (III) в малой концентрации.
Известен способ фотометрического определения железа (III) с помощью алюминона (εMR≈10000), заключающийся в добавлении к анализируемому раствору буферного раствора с определенным значением рН (слабокислая среда) и действии органического реагента [А.К.Бабко, А.Т.Пилипенко. Фотометрический анализ. Общие сведения и литература. - М.: Химия, 1968. - С.283].
Известен способ фотометрического определения железа (III) с помощью ксиленолового оранжевого (εMR≈26600), заключающийся в добавлении к анализируемому раствору буферного раствора с определенным значением рН (слабокислая среда) и действии органического реагента (М.И.Булатов, И.П.Калинкин. Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа. - М.: Химия, 1972. - С.338; О.А.Татаев, К.Н.Багдасаров. Применение органических реагентов в электрофотометрии. Ч.1. - Махачкала: Изд-во Дагестанского университета, 1971. - с.43).
Недостатком известных способов является невысокая чувствительность и избирательность определения.
Технический результат заключается в повышении чувствительности фотометрического определения железа (III) и избирательности при осуществлении способа.
Технический результат достигается тем, что в способе фотометрического определения железа (III) в растворах чистых солей путем переведения железа (III) в окрашенное комплексное соединение в слабокислой среде, к раствору железа (III) добавляют 2 мл ацетатного буферного раствора с рН 4,7-5,7, 0,7-1 мл раствора поверхностно-активного вещества, содержащего 0,2% раствора полиоксиэтилен сорбитан моноолеата, 0,2% раствора моноалкилфенилового эфира полиэтиленгликоля на основе полимердистилята и воду в соотношении 1:1:1, и 90-110-кратный избыток алюминона, затем полученный раствор доводят водой до 4 мл, нагревают на водяной бане при температуре 80-98° в течение 2-3 минут и фотометрируют при длине волны 364 нм.
В способе фотометрического определения железа (III) в растворах чистых солей путем переведения железа (III) в окрашенное комплексное соединение в слабокислой среде, к раствору железа (III) добавляют 2 мл раствора ацетатного буферного раствора с рН 4,3-4,8, 0,1-0,2 мл раствора поверхностно-активного вещества, содержащего 0,2% водный раствор полиоксиэтилен изооктилфенилового эфира, и 8-12-кратный избыток ксиленолового оранжевого, затем полученный раствор доводят водой до 10 мл, нагревают на водяной бане при температуре 80-98°С в течение 2-3 минут и фотометрируют при длине волны 490 нм.
В первом варианте максимальная интенсивность окраски достигается при рН 4,7-5,7 ацетатного буферного раствора. Вне этих интервалов комплекс распадается. Максимальная интенсивность окраски комплексного соединения достигается при 90-110 - кратном избытке реагента алюминона. При меньшей или большей кратности реагента интенсивность окраски падает и комплекс не обнаруживается, не существует. Максимальная интенсивность окраски комплексного соединения, следовательно, и высокая чувствительность реакции наступает при добавлении 0,7-1 мл раствора поверхностно-активного вещества (ПАВ-1). При меньшем или большем количестве ПАВ-1 от оптимально найденного чувствительность уменьшается. Максимальное развитие окраски достигается при нагревании полученного раствора 2-3 мин на водяной бане при температуре 80-98°С. Снижение температуры водяной бани менее 80°С требует более продолжительного нагревания. Если нагревать полученный раствор при выбранном интервале температуры меньше 2 мин, максимальное развитие окраски не достигается, более 3 мин - нерациональная трата времени, так как этим чувствительность реакции не повысить, т.е. интенсивность окраски более интенсивной не станет.
Раствор ПАВ-1 готовят следующим образом: к 0,2% раствору полиоксиэтилен сорбитан моноолеату добавляют 0,2% раствор моноалкилфенилового эфира полиэтиленгликоля на основе полимердистиллята и воду в соотношении 1:1:1.
Polyoxyethylene sorbitan monooleate [Tween - 80] [9005 - 65 - 6] nD20 1,4720. d. 1.064 Fp>230°F (110°C) Merk Index 13, 7664 R & S 1(1),761 H RTECS # WG 2932500 Average Mn ca. 1,310. HLB 15.0 IL 41.50 [Алдрич. Справочник химических реактивов и оборудования. - Россия Евро, Российская федерация, Москва, 105062, а/я 102, Сигма - Sigma, 2003 - 2004. - с.1894; 27, 436-4].
Моноалкилфениловый эфир полиэтиленгликоля на основе полимердистиллята [ОП - 7] [СnН2n+1С6Н4O(С2Н4O)mН1 1, где n=8÷10, m=6÷7. Состав %: OB 99, влаги 0,5] [Поверхностно-активные вещества: Справочник / Абрамзон А.А., Бочаров В.В., Гаевой Г.М. и др.; под ред. А.А.Абрамзона и Г.М.Гаевого. - Л.: Химия, 1979. - 376 с. - с.305].
Пример 1. Определение железа (III) с алюминоном в присутствии ПАВ - 1.
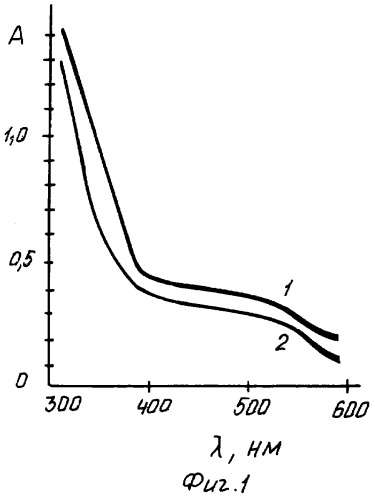
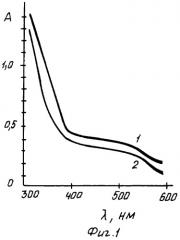
а) Зависимость А - длины волны. В пробирки помещают по 0,1 мл 10-4 М раствора железа (III), ацетатных буферных растворов с переменным значением рН, по 0,5 мл раствора ПАВ-1, по 0,2 мл 10-2 М раствора алюминона, воду до Vобщ=4 мл, μ=1. При изменении порядка сливания реагентов комплекс все равно образуется. Нагревают на водяной бане (t=80-90°С) в течение 2 мин. Фотометрируют пару растворов с наибольшей разницей в интенсивностях окрасок относительно воды (фиг.1 - спектры светопоглощения комплекса железа (III) с алюминоном (I) и алюминоном (2) в присутствии ПАВ-1). Получают λопт=364 нм.
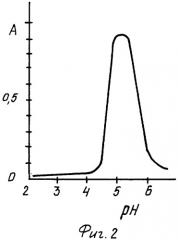
б) Зависисмость А - рН. Приготовленные в а) растворы фотометрируют при λопт относительно растворов сравнения (фиг.2 - зависимость А - рН комплекса железа (III) с алюминоном в присутствии ПАВ-1). рНопт для MR 4,3-6,3; рНmax=5,0.
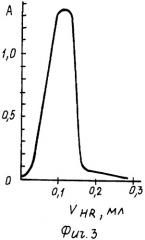
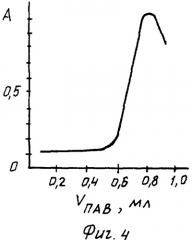
в) Зависимость А - Vпав и А - VHR. Комплекс образуется при 100-кратном избытке алюминона (фиг.3 - зависимость A-VHR для комплекса железа (III) с алюминоном в присутствии ПАВ-1) в присутствии 0,8 мл раствора ПАВ-1, (фиг.4 - зависимость А-Vпав для комплекса железа (III) с алюминоном в присутствии ПАВ-1) при 2-минутном нагревании на водяной бане при температуре 80-90°С. Окраска комплекса устойчива во времени. Молярный коэффициент светопоглощения комплексного соединения εMR=560000.
г) Зависимость А - VFe.
В градуированные пробирки помещают по Vмл 10-4 М раствора железа (III), по 2 мл ацетатных буферных растворов с рН 5, по 0,8 мл раствора ПАВ-1, по 0,1 мл 10-2 М раствора алюминона, доводят водой до 4 мл, нагревают на водяной бане при температуре 80-98°С в течение 2 минут, фотометрируют при длине волны 364 нм относительно раствора сравнения, не содержащего железо (III), е=1 см.
Линейность градуировочного графика соблюдается в интервале концентраций железа (III) (0,5-2) 10-6 М.
Во втором варианте максимальная интенсивность окраски достигается при рН 4,3-4,8 ацетатного буферного раствора. Вне этих интервалов комплекс распадается. Максимальная интенсивность окраски комплексного соединения достигается при 8-12-кратном избытке реагента ксиленолового оранжевого. При меньшей или большей кратности реагента интенсивность окраски падает и комплекс не обнаруживается. Максимальная интенсивность окраски комплексного соединения и чувствительность реакции наступает при добавлении 0,1-0,2 мл раствора поверхностно-активного вещества (ПАВ-2). При меньшем или большем его количестве от оптимально найденного чувствительность уменьшается. Максимальное развитие окраски достигается при нагревании полученного раствора 2-3 мин на водяной бане при температуре 80-98°С. Снижение температуры водяной бани менее 80°С требует более продолжительного нагревания. Если нагревать при выбранном интервале температуры меньше 2 мин, максимальное развитие окраски не достигается, более 3 мин - нерациональная трата времени, так как этим чувствительность реакции не повысить, т.е. интенсивность окраски еще более интенсивной не станет.
Раствор ПАВ-2: 0,2% водный раствор полиоксиэтилен изооктилфениловый эфир.
Polyoxyethelene isooctylphenyl ether [Triton x - 100, Ferak Berlin [9002-93-1] 4 - (С8Н17)С6Н4(ОСН2СН2)nОН, n˜10 nD20 1.4900 d 1.070 Fp>230°F (110°C) Merck. Index 13.6793 FT-IR(1) 1163C Safety 2.3 544D R & S 1(1) 1351N RTECS #, MD 0907700. R: 22-41 S: 23-26-36 Constains<3% polyethylene glycol] [Алдрич. Справочник химических реактивов и оборудования. - Россия Евро, The Sigma - Aldrich, 2003-2004. - С.1888, 23, 472-9].
Пример 2. Определение железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2.
а) Зависимость А - λ, нм. В пробирки помещают по 0,2 мл 10-4 М раствора железа (III), по 2 мл ацетатных буферных растворов с переменным значением рН, по 0,2 мл раствора ПАВ-2, по 0,2 мл 10-3 М раствора ксиленолового оранжевого, доводят водой до 10 мл, нагревают 2 мин на водяной бане при t=80-98°С. Комплекс бурого цвета, раствор сравнения желтый. Фотометрируют пару растворов с наибольшей разницей в интенсивностях окрасок относительно воды (фиг.5 - спектры светопоглощения комплекса железа (III) с ксиленоловым оранжевым (1) и ксиленоловым оранжевым (2) в присутствии ПАВ-2); λmaxMR=490 нм; μ=0,6.
б) Зависимость А - рН. Приготовленные растворы фотометрируют при λmax относительно растворов сравнения (фиг.6 - зависимость А-рН комплекса железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2). рН для MR 3,9 - 5,2; рНmax=4,6.
в) Зависимость А - Vпав и А - VHR. Комплекс образуется при 10-кратном избытке ксиленолового оранжевого в присутствии 0,15 мл раствора ПАВ-2 (фиг.7 - зависимость A-VHR для комплекса железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2) (1) и (фиг.8 - зависимость А-Vпав для комплекса железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2), при 2-минутном нагревании на водяной бане при температуре 80-98°С. Окраска комплекса устойчива во времени. Молярный коэффициент светопоглощения комплексного соединения εMR=122000.
г) Зависимость А - VFe.
В градуированные пробирки помещают по V мл 10-4 М раствора железа (III), по 2 мл ацетатного буферного раствора с рН 4,6; по 0,15 мл раствора ПАВ-2, по 0,2 мл 10-3 М раствора ксиленолового оранжевого, доводят водой до 10 мл, нагревают на водяной бане при температуре 80-98°С в течение 2 минут, фотометрируют при длине волны 490 нм относительно раствора сравнения, не содержащего железа (III), е=0,5 см.
Линейность градуировочного графика соблюдается в интервале концентраций железа (III) (1,8-3)·10-6 М.
Молярный коэффициент погашения комплексного соединения железа (III) с алюминоном в присутствии ПАВ-1 в 56 раз больше той же величины для комплексного соединения железа (III) с алюминоном в отсутствие ПАВ-1 и в 11 раз больше самого большого из известных молярных коэффициентов поглощения для комплексных соединений железа (III) с органическими реагентами (с дифенилкарбазоном εMR=50300) [М.И.Булатов, И.П.Калинкин. Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа. - М.: Химия, 1972. - с.330].
Молярный коэффициент погашения комплексного соединения железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2 в 4,5 раза больше той же величины для комплексного соединения железа (III) с ксиленоловым оранжевым в отсутствии ПАВ-2. Из [М.И.Булатов, И.П.Калинкин. Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа. - М.: Химия, 1972. - С.330] известен окрашенный комплекс железа (III) с дифенилкарбазоном, имеющий наибольшее значение εMR=50300 из всех известных комплексных соединений железа (III) с органическими реагентами.
Предложенный способ определения железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2 позволяет определять железо (III) в растворах в еще меньшей концентрации, чем с дифенилкарбазоном, так как молярный коэффициент погашения комплекса железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2 в 2,4 раза больше той же величины для комплексного соединения железа (III) с дифенилкарбазоном (известный способ). Кроме того, в реакции получения комплексного соединения железа (III) с дифенилкарбазоном используют растворитель толуол, оказывающий вредное влияние на организм человека. В предложенном способе применяют в качестве растворителя воду.
В обоих вариантах предложенного способа поверхностно-активные вещества - ПАВ-1 и ПАВ-2 повышают чувствительность фотометрических реакций в связи с тем, что константа устойчивости комплексного соединения в присутствии ПАВ больше, чем в их отсутствие, что показано на примере реакции комплексообразования комплексного железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2 [фиг.9(1) - определение константы устойчивости комплексов железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2], и в его отсутствие [фиг.9(2) - определение константы устойчивости комплексов железа (III) с ксиленоловым оранжевым в отсутствие ПАВ-2]. Фиг.9(2) выполнен в тех же условиях, что и фиг.9(1), только в отсутствие ПАВ - 2.
Методом пересечения кривых [М.И.Булатов, И.П.Калинкин. Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа. - М.: Химия, 1972 год - 408 с.- С.208] рассчитаны константы устойчивости комплексов железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2 [фиг.9(1)] и в отсутствие ПАВ-2 [фиг.9(2)]. Константа устойчивости комплекса железа (III) с ксиленоловым оранжевым в присутствии ПАВ-2 равна 3,04·109, в отсутствие последнего - 2,25·109. Из расчетов видно, что константа устойчивости осталась неизменной.
1. Способ фотометрического определения железа (III) в растворах чистых солей путем переведения железа (III) в окрашенное комплексное соединение в слабокислой среде, отличающийся тем, что к раствору железа (III) добавляют 2 мл ацетатного буферного раствора с рН 4,7-5,7, 0,7-1 мл раствора поверхностно-активного вещества, содержащего 0,2% раствора полиоксиэтилен сорбитан моноолеата, 0,2% раствора моноалкилфенилового эфира полиэтиленгликоля на основе полимердистиллята и воду в соотношении 1:1:1, и 90-110-кратный избыток алюминона, затем полученный раствор доводят водой до 4 мл, нагревают на водяной бане при температуре 80-98°С в течение 2-3 мин и фотометрируют при длине волны 364 нм.
2. Способ фотометрического определения железа (III) в растворах чистых солей путем переведения железа (III) в окрашенное комплексное соединение в слабокислой среде, отличающийся тем, что к раствору железа (III) добавляют 2 мл ацетатного буферного раствора с рН 4,3-4,8, 0,1-0,2 мл раствора поверхностно-активного вещества, содержащего 0,2% водный раствор полиоксиэтилен изооктилфенилового эфира, и 8-12-кратный избыток ксиленолового оранжевого, затем полученный раствор доводят водой до 10 мл, нагревают на водяной бане при температуре 80-98°С в течение 2-3 мин и фотометрируют при длине волны 490 нм.