Способ оценки тяжести эндогенной интоксикации при неотложной абдоминальной патологии в раннем послеоперационном периоде
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к клинической биохимии, и предназначено для оценки тяжести эндогенной интоксикации при неотложной абдоминальной патологии в раннем послеоперационном периоде. Способ осуществляется путем клинико-биохимического исследования параметров антиоксидантной и оксидантной систем в крови на фоне стандартных гематологических и клинико-биохимических тестов и обработки его результатов с помощью математического критерия, позволяющего оценить совокупность вкладов отдельных параметров в нарушение метаболических процессов у больных. Изобретение позволяет более доказательно характеризовать эндогенную интоксикацию по совокупному вкладу отдельных параметров в нарушение метаболических процессов в организме больного, служит завершающим этапом применения методологии доказательной клинико-биохимической оценки эндотоксикоза у больных с неотложной абдоминальной патологией. 1 з.п. ф-лы, 10 табл.
Реферат
Область применения
Изобретение относится к медицине, в частности к клинической биохимии, и предназначено для оценки тяжести эндогенной интоксикации при неотложной абдоминальной патологии в раннем послеоперационном периоде путем биохимического исследования и обработки его результатов с помощью математического критерия, позволяющего оценить совокупность вкладов отдельных параметров в нарушение метаболических процессов у больных.
Уровень техники
В настоящее время разработаны различные методологические подходы к клинико-биохимическому мониторингу тяжести эндогенной интоксикации у больных при неотложных состояниях, предусматривающие применение шкал и расчетных критериев. Для характеристики состояния больных с абдоминальной патологией применяются различные шкальные системы. Шкальная система предполагает числовую оценку клинических, физиологических, лабораторных и биохимических параметров. Наличие клинических симптомов или отклонение физиологического либо биохимического параметра от нормы определяется числом, и значения, относящиеся к одному пациенту, суммируются в общую шкалу. Полученное число соответствует определенному диагнозу или степени тяжести течения болезни [1, 2, 3, 4, 5].
Согласно [6] интегральная и количественная оценка тяжести системной воспалительной реакции при гнойно-септической патологии предполагает применение двух типов шкал:
1) шкалы оценки состояния больных, например APACHE, SAPS (цель - прогноз, результат - оценка риска летального исхода);
2) шкалы оценки полиорганной дисфункции, например MODS, SOFA (цель - описание синдрома, результат - оценка осложнения).
В [7] было предложено классифицировать системы оценки тяжести состояния больных хирургического профиля с сепсисом на три группы:
1) методы, основанные на сборе объективных клинических и лабораторных данных (APS; SAPS; APACHE I, II, III; SOFA);
2) методы, основанные на статистическом моделировании, - система МРМ;
3) системы, оценивающие тяжесть состояния больных по количеству и сложности методов исследования и лечения, необходимых для его ведения, - система TISS.
Использование объективных систем-шкал определения тяжести состояния больных позволяет прогнозировать исход заболевания и оптимизировать лечебную тактику.
Однако в соответствии с существующими шкальными системами оценки тяжести состояния больных с абдоминальной патологией при неотложных состояниях требуется определять достаточно обширное количество клинико-лабораторных тестов, что зачастую вызывает объективные трудности их применения в современных условиях в связи с отсутствием необходимого оборудования, реактивов и т.п.
Кроме того, в доступной нам литературе мы не встретили шкалы оценки эндотоксикоза у больных с неотложной абдоминальной патологией. На практике, как правило, применяются только расчетные критерии индексного типа.
При перитоните в оценке тяжести состояния больных получил международное признание Мангеймский перитонеальный индекс (МИП). Вместе с тем этот критерий не является показателем, характеризующим степень эндогенной интоксикации, которая во многом определяет исход заболевания при разлитом перитоните [8].
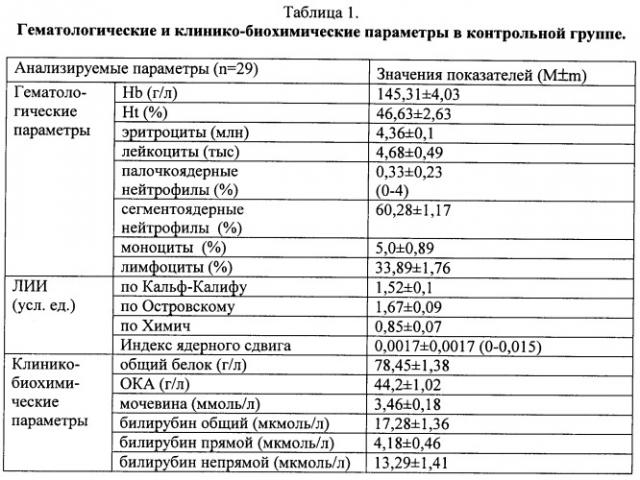
Одними из расчетных показателей, характеризующих степень выраженности эндотоксикоза, являются лейкоцитарные индексы интоксикации (ЛИИ). Использование ЛИИ позволяет оценить активность воспалительных процессов. Наиболее широко используются ЛИИ по Кальф-Калифу, Островскому и Химич. Расчет их осуществляется следующим образом [27]:
1. ЛИИ по Кальф-Калифу=[(сег+2юн+3пал+4миел)×(пл+1)]/[(мо+ли)/(эоз+1)].
2. ЛИИ по Островскому=(ней+пл)/(мо+ли+эоз).
3. ЛИИ по Химич=[0,1лей(тыс)хней(в %)]/[100-ней].
4. Индекс ядерного сдвига=(юн+пал+миел)/сег.
Согласно [9] достоинством ЛИИ по Кальф-Калифу является возможность перевода гемограмм в числовые показатели, отражающие эндогенную интоксикацию, в том числе при сепсисе, перитоните, гнойном остром панкреатите и холецистите. Высокий лейкоцитоз и повышение ЛИИ по Кальф-Калифу до 10 служит признаком септического шока. ЛИИ по Кальф-Калифу характеризуется как простой, доступный и достаточно информативный показатель. Авторы отмечают, что использование только одного этого параметра не дает полной оценки степени эндотоксикоза, а отражает, в основном, степень воспалительного ответа организма.
Наряду с вышеизложенным следует отметить: принципы, методические приемы и формы разработки шкальных систем и расчетных критериев методологически обоснованы с позиций доказательной медицины. Их анализ позволяет предложить весьма универсальный подход выведения шкальной системы оценки биохимических проявлений эндотоксикоза у больных с абдоминальной патологией при неотложных состояниях исходя их реальных возможностей клинических экспресс-лабораторий.
На этапе внедрения в практику доказательных оценочных клинико-биохимических подходов изучения метаболизма организма хирургических больных с абдоминальной патологией при неотложных состояниях одной из наиболее распространенных форм служит использование индексных параметров. Анализ представленных в литературе индексов оценки тяжести эндогенной интоксикации и состояния больных позволяет выделить следующие особенности их выведения.
Для построения индексных зависимостей выбираются маркерные тесты биохимической, гематологической, клинико-биохимической направленности.
Известен способ диагностики тяжести эндогенной интоксикации при острых гнойно-септических заболеваниях у детей (патент РФ № 2122739) путем электрофоретического исследования, отличающийся тем, что исследованию подвергается сыворотка крови и при наличии на электрофореграмме белковых компонентов с мол. м. менее 12 к Да диагносцируют тяжелую эндогенную интоксикацию с формированием органной недостаточности.
Недостатком данного способа является то, что не в каждой лаборатории имеются технические возможности для осуществления электрофоретического исследования, он достаточно длителен (в среднем время анализа составит около 8-9 ч).
Известен способ оценки эндогенной интоксикации организма (патент РФ № 2082971) путем изучения и подсчета форменных элементов периферической крови, отличающийся тем, что исследуют эритроциты и определяют индекс интоксикации ИИ по формуле, включающей в себя количество эхиноцитов, пойкилоцитов, гемолизирующих форм, дискоцитов, стоматоцитов.
Данный способ также сложен в исполнении, что является его недостатком.
Известен способ диагностики эндогенной интоксикации при тяжелой механической травме (патент РФ № 2195652) по показателям крови и балльной оценке шокогенности травмы, отличающийся тем, что измеряют хемилюминесценцию цельной крови и хемилюминесценцию популяции моноцитов и определяют индекс интоксикации ИИ по формуле, включающей в себя балл шокогенности травмы; хемилюминесценцию цельной крови и моноцитов, индуцированных зимозаном, мВ.
Способ требует применения дорогостоящих реактивов (в том числе зимозана), метод хемилюминесеценции можно осуществить не в каждой диагностической лаборатории в связи с отсутствием необходимого лабораторного оборудования - все это можно считать его недостатками.
Математическое выражение, служащее тем или иным расчетным индексом, может представлять собой отношение значений параметров (или их группы) друг к другу, как правило, в случае взаимонаправленного действия, сумму или произведение, чаще всего в случае однонаправленного действия или при необходимости подчеркнуть отношение показателей к анализу одной биологической жидкости. В этом случае преимуществом использования индексов служит простота расчета.
Известен способ определения оксидантной/антиоксидантной активности раствора анализируемого вещества (заявка РФ №2002130523), включающий оценку оксидантной/антиоксидантной активности по электрохимическим параметрам раствора анализируемого вещества, отличающийся тем, что предварительно готовят исходный раствор, в который вводят медиаторную систему, содержащую одновременно окисленную и восстановленную формы реагента, а оценку оксидантной/антиоксидантной активности проводят по изменению окислительно-восстановительного потенциала раствора, определенного до и после введения в исходный раствор анализируемого вещества. Концентрацию (активность) оксидантов/антиоксидантов в растворе рассчитывают по формуле как отношение концентрации окисленной формы медиатора к концентрации восстановленной формы медиатора.
Данный способ требует использования реактивов, имеющихся не в каждой лаборатории, в том числе в связи с их высокой стоимостью, а также необходимой измерительной аппаратуры, что можно считать недостатками метода.
Известен биохимический способ определения эндогенной интоксикации [14], заключающийся в определении уровня молекул средней массы в сыворотке крови. Молекулы средней массы являются интегральным биохимическим маркером эндогенной интоксикации [15].
Данный способ включает забор крови натощак, отделение сыворотки от форменных элементов крови путем центрифугирования, получение безбелковой пробы путем прибавления к 1 мл сыворотки крови 0,5 мл 10% трихлоруксусной кислоты и центрифугирования в течение 30 минут при 3000 об/мин. Далее к 0,5 мл надосадочной жидкости прибавляют 4,5 мл дистиллированной воды и определяют оптическую плотность пробы на спектрофотометре при длине волны 254 нм. По величине оптической плотности пробы определяют содержание молекул средней массы и по их уровню судят о наличии эндогенной интоксикации.
Однако этот метод достаточно длителен в исполнении (центрифугирование осуществляется в течение 30 минут) и требует большого количества сыворотки крови (1 мл), необходимого для проведения исследования, которое не всегда можно получить у больного, особенно в практике экспресс-лабораторий отделений реанимации и интенсивной терапии, когда перед клиницистом встает вопрос о выборе необходимого комплекса лабораторных тестов, что ограничивает применение этого способа.
Из уровня техники известен способ определения эндогенной интоксикации (патент РФ № 2193780), включающий забор крови, отделение сыворотки от форменных элементов крови, депротеинезацию, центрифугирование, прибавление к 0,5 мл надосадочной жидкости 4,5 мл дистиллированной воды, спектрофотометрию пробы при длине волны 254 нм и диагностику по уровню молекул средней массы, отличающийся тем, что перед депротеинезацией сыворотку крови разводят в 10 раз физиологическим раствором, пробу центрифугируют в течение 10 мин и при значении более 0,136 единиц оптической плотности судят о наличии эндогенной интоксикации у больных.
Данный способ характеризует только уровень молекул средней массы в крови - это пул веществ различного происхождения (в том числе продукты перекисного окисления липидов) - и не позволяет оценить вклады различных веществ, составляющих пул, в формирование эндотоксикоза, что можно считать недостатками метода. В [10] была отмечена особая ценность оценки сбалансированности реакций ПОЛ и АОС, степень которой можно определить по величине интегрального коэффициента (К) дисбаланса в системе ПОЛ/АОС:
К=[(ДКi/ДКn)·(МДАi/МДАn)·(СОi/СОn)]/[(ТФi/ТФn)·(ЦПi/ЦПт)],
где ДК - диеновые коньюгаты, МДА - малоновый диальдегид, СО - степень окисленности липидов сыворотки крови, ТФ - α-токоферол, ЦП - церулоплазмин, обозначения с индексом i соответствуют исследуемому образцу, а обозначения с индексом n - среднему значению в норме.
Этот способ оценки сбалансированности реакций ПОЛ и АОС с применением соответствующего индекса включает в себя определение веществ различных уровней каскада реакций СРО в совокупности с активностью антиоксидантов: это положительная сторона метода. Однако в условиях обычной клинической лаборатории сложно провести идентификацию всех составляющих интегрального коэффициента (К) дисбаланса в системе ПОЛ/АОС в связи с необходимостью наличия дорогостоящих реактивов и оборудования: это недостаток метода.
Предложили и апробировали [11] при остром панкреатите индекс эндогенной интоксикации (ИЭИ) по следующим параметрам: уровню общего белка крови Б (г/л); мочевины М (ммоль/л); веществ средней молекулярной массы пептидной природы МСМ (по Лоури); аланинаминотрансферазы АлАТ (ммоль/ч·л):
.
Недостатком этого индекса эндогенной интоксикации (ИЭИ) можно считать следующее: в расчетную формулу включены параметры, имеющие разные единицы измерения. В данном случае требуется перевод значений используемых клинико-лабораторных тестов в относительные величины, например, путем деления величины каждого показателя на его норму (при этом единицы измерения сокращаются).
В качестве составляющих индексов могут браться те или иные регрессионные или корреляционные зависимости изучаемых критериев. В данном случае актуальным является большее соответствие полученного математического выражения реальным характеристикам вариационного ряда.
В [12] был предложен ряд индексов интоксикации.
Индекс интоксикации 1, который включает в себя показатели катаболизма белка, функциональной активности печени, количество лейкоцитов и лимфоцитов в крови и отражает такую функцию организма как детоксикационная. Для оценки состояния формулы периферической крови использован индекс интоксикации 2. Состояние антиоксидантного статуса в крови и уровень транспортной функции альбумина характеризует индекс интоксикации 3. Индекс интоксикации 4 объединяет параметры, входящие в состав индексов интоксикации 2 и 3.
В основу расчета индексов интоксикации (Y или ИИ) была положена формула, предложенная М.Н.Тарелкиной [13]:
где Ар - реальные значения i-го признака, Ан - среднее значение i-го признака у доноров, δ - дисперсия i-го признака у доноров.
Интервальная оценка приближенных значений индексов интоксикации при односторонней доверительной вероятности (tβ) с надежностью β=0,95 проводилась по следующим формулам:
ИИmax=М+ε,
где tβ - величина, определяющая число среднеквадратичных отклонений, которые нужно отложить вправо или влево от центра рассеивания (при односторонней доверительной вероятности) для того, чтобы вероятность попадания случайной величины Х в полученный интервал была равна β (значения tβ взяты из соответствующих таблиц распределения Стьюдента).
Так как некоторые факторы связаны значимой и даже сильной корреляционной зависимостью, расчет общей (суммарной) дисперсии производили по формуле
Эти индексы можно считать аналогами заявляемого способа. Однако они также имеют ряд недостатков: расчет коридора значений величины индексов проводится только в сторону максимума, минимальные значения индексов не рассчитываются; необходим расчет корреляции параметров, для чего требуется время для набора группы обследованных.
Задачей заявляемого изобретения является предложить комплексную систему оценки развития эндогенной интоксикации у больных с неотложной абдоминальной патологией на основе исследования диапазонов изменений исследуемых блоков гематологических и клинико-биохимических тестов и разработки методологического подхода выведения расчетных индексов, характеризующих степень сбалансированности исследуемых метаболических цепочек.
Технический результат изобретения состоит в том, что способ позволяет более доказательно характеризовать эндогенную интоксикацию по совокупному вкладу отдельных параметров в нарушение метаболических процессов в организме больного, служит завершающим этапом применения методологии доказательной клинико-биохимической оценки эндотоксикоза у больных с неотложной абдоминальной патологией.
Данный способ позволяет использовать математический критерий J в экспресс-лабораториях отделений реанимации, при малом времени проведения анализа, но необходимости комплексно оценить тяжесть эндогенной интоксикации при неотложной абдоминальной патологии.
Метод пригоден как для однократного исследования, так и для мониторинга тяжести эндогенной интоксикации у больных с абдоминальной патологией в раннем послеоперационном периоде.
Достижение результата
Данный технический результат достигается за счет того, что способ определения оценки тяжести эндогенной интоксикации при неотложной абдоминальной патологии в раннем послеоперационном периоде, включающий забор крови, клинико-биохимические исследования параметров антиоксидантной и оксидантной систем в крови на фоне стандартных гематологических и клинико-биохимических тестов, отличающийся тем, что применяют расчетные индексы для выявления степени сбалансированности оксидантной и антиоксидантной систем в крови, определяющиеся по следующей формуле:
причем параметрбольного характеризует параметр, полученный по данным исследований больного, а параметрнорма характеризует параметр, полученный как среднее арифметическое по данным исследований у здоровых людей.
Затем проводят расчет математического критерия J, характеризующего по блокам анализируемых тестов совокупность вкладов отдельных параметров в нарушение метаболических процессов в организме больного в соответствии с формулой:
,
где Δn - отклонение n-измерения математического ожидания величины у больного, соответствующее вкладу каждого теста в суммарный показатель J, причем J представляется в виде диапазона значений Jmin-Jmax, а Δn рассчитывают по формулам для вариационного ряда:
для минимального значения вклада параметра в суммарный показатель Jmin:
Δn=(М-m в норме) - (М-m в группе обследованных);
для максимального значения вклада параметра в суммарный показатель Jmax:
Δn=(М+m в норме) - (М+m в группе обследованных).
В основе расчета М и m лежит вариационная статистика для малых выборок с применением t-критерия Стьюдента:
Для оценки математического ожидания (М) величины I, где М и m являются вариационной статистикой для малых выборок с применением t - критерия Стьюдента и определяются по формулам:
,
где δ - среднее квадратичное отклонение, определяющееся по формуле:
, где - среднее значение величины Ii - определенного значения выборки.
Для расчета суммарного критерия J у конкретного больного данные клинико-биохимического обследования по каждому из параметров сопоставляются с математическим ожиданием или со средним значением данного параметра в контрольной группе (норма), т.е. Δn рассчитывается как разница между значением показателя М в норме и величиной параметра у больного в данный период наблюдений - это величина, соответствующая вкладу в суммарный показатель J каждого теста.
Для определения доверительного коэффициента (меры точности t) при проверке гипотезы о равенстве средних арифметических М1 и М2 параметра I в каких-либо двух группах обследованных использовалась следующая формула:
Следует отметить, что критерий J наиболее показателен при комплексном применении, хотя он может быть адаптирован к перечню применяемых клинико-биохимических параметров в конкретной клинике. Расчет вкладов отдельных блоков показателей в суммарный критерий J, кроме необходимости учета их в соответствии с формулой, позволяет комплексно интерпретировать выявляемые нарушения метаболических процессов в организме больного в раннем послеоперационном периоде. Например, при холецистите более 90% вклада в минимальное значение и около 90% вклада в максимальное значение суммарного критерия J вносят значения J по блоку биохимических параметров (показатели свободнорадикального окисления и антиоксидантной защиты, уровень молекул средней массы) и по связывающей способности альбумина. При этом имеет место преобладание вклада в значение суммарного критерия J значений J по связывающей способности альбумина (до 69%). При разлитом перитоните реактивной и токсической стадии с благоприятным исходом заболевания картина аналогичная. Однако на 3 и 5 сутки наблюдения отмечается, что при разлитом перитоните токсической стадии существенный вклад в суммарный критерий J имеется и по блоку гематологических и клинико-биохимических параметров. При разлитом перитоните терминальной стадии и при неблагоприятном исходе в раннем послеоперационном периоде эта тенденция усиливается. Так, на 5 сутки после операции при разлитом перитоните терминальной стадии 37,8% вклада в суммарный критерий J приходится на вклад блока гематологических параметров, а при неблагоприятном исходе разлитого перитонита 39,2%.
Все это позволяет сделать вывод о предпочтительном использовании всего комплекса составляющих суммарного критерия J для оценки тяжести эндогенной интоксикации в раннем послеоперационном периоде.
В случае соответствия величин суммарного критерия J значениям этого суммарного критерия при определенных диагнозах (хронический и острый холецистит, разлитой перитонит), выявляемого путем сопоставления с рассчитанными нами величинами в группах обследования, отмечается соответствующая этим нозологиям тяжесть эндогенной интоксикации организма.
Для прогноза исхода разлитого перитонита наиболее значимы диапазоны J на 1 и 3 сутки послеоперационного периода, проявившие пограничные изменения в зависимости от стадии и исхода заболевания. Значения суммарного критерия J при разлитом перитоните на 1 сутки после операции в диапазоне 9937,56-14454,89, на 3 сутки - в диапазоне 8955,13-9350,07 свидетельствуют о риске неблагоприятного исхода заболевания. При этом на 5 сутки наблюдений диапазон суммарного критерия J (10151,85-11816,29) у умерших больных перекрывался с таковым диапазоном у больных разлитым перитонитом терминальной стадии (11445,87-12491,55). Это может свидетельствовать о том, что 5 сутки послеоперационного периода являются критическим этапом наблюдений больных разлитым перитонитом терминальной стадии.
Учитывая то, что в разных клиниках имеются биохимические лаборатории различного уровня оснащения и, возможно, не в каждой из них будет иметься возможность определения всего спектра тестов, применяемых нами в работе, может быть проведена коррекция диапазонов J в соответствии с конкретным перечнем определяемых маркеров эндотоксикоза. Кроме того, в клинической биохимии принято при отработке методик проведения анализов осуществлять определение нормативных величин и сопоставлять их с указанными значениями в методиках в каждой лаборатории самостоятельно, поскольку могут иметься незначительные расхождения в результатах, например, в связи с применением разной измерительной аппаратуры.
Новизной способа является его комплексность и универсальность: при необходимости механизм расчета критерия J может быть применен к такой группе биохимических показателей, которые применяются в данной экспресс-лаборатории.
Сущность изобретения
Принципами доказательной медицины определены следующие основные требования к шкальным системам:
- методологическая обоснованность;
- объективность;
- клиническая эффективность применения.
В соответствии с этими принципами основными методическими приемами выведения шкальных систем можно считать:
- изучение теоретических предпосылок их разработки в соответствии с исторической логикой развития науки;
- исследование достоинств и недостатков существующих систем оценки тяжести состояния больных;
- анализ возможных направлений усовершенствования имеющихся шкал или разработки новых.
Учитывая вышеизложенные принципы и методы разработки шкальных систем оценки тяжести эндотоксикоза у больных с абдоминальной патологией при неотложных состояниях, формы их представления могут быть следующими:
1) таблицы диапазонов изменений исследуемых блоков тестов с балльной шкалой их оценки;
2) расчетные индексы, характеризующие степень сбалансированности исследуемых метаболических цепочек;
3) комплексные системы, включающие в себя в качестве составляющих пункты 1 и 2.
В связи с объективными трудностями применения существующих шкальных систем оценки тяжести абдоминальной патологии на основе использования их в качестве теоретического и методологического базиса была разработана авторская шкальная система мониторирования биохимических проявлений эндотоксикоза при неотложных состояниях.
Предлагаемая нами шкальная система может быть отнесена к комплексным:
- базируется на регистрации вкладов отдельных блоков исследуемых тестов (гематологических и клинико-биохимических) и выведении расчетных индексов маркерных параметров тяжести эндогенной интоксикации;
- предусматривает анализ комплексного математического критерия, характеризующего по блокам анализируемых тестов совокупность вкладов отдельных параметров в нарушение метаболических процессов в организме больного.
Преимуществом данной шкалы, по сравнению с существующими шкалами, служит возможность использования отдельных составляющих без снижения прогностической ценности, хотя применение ее в системе более обоснованно и эффективно. При этом перспективной особенностью этой шкалы являются разработанные диапазоны совокупных отклонений от нормы в динамике наблюдений исследуемых гематологических и клинико-биохимических тестов, а также ряда расчетных индексов (1, 3, 5 сутки после операционного периода).
Предлагаемая шкальная система оценки эндогенной интоксикации, представляемая в виде диапазонов значений математического критерия J, характеризующего по блокам анализируемых тестов совокупность вкладов отдельных параметров в нарушение метаболических процессов в организме больного, коррелировала с MPI - Мангеймским перитонеальным индексом - и ЛИИ.
Таким образом, нормативы этой шкалы по отдельным ее составляющим применимы для оценки биохимических проявлений эндотоксикоза у больных с абдоминальной патологией при неотложных состояниях. Однако универсальность подхода разработки, при отсутствии возможности определения ряда включенных в нее тестов, позволяет легко адаптировать данную шкалу для потребностей практики, в том числе рассмотреть возможность ее использования при других видах неотложных состояний.
Неотложные состояния сопровождаются метаболическими нарушениями различной степени выраженности. При этом в жидкостях и тканях организма в нефизиологических концентрациях накапливаются промежуточные и конечные продукты нормального и нарушенного обмена веществ, которые оказывают токсическое влияние и вызывают дисфункцию различных органов и систем.
Среди широкого круга метаболитов, обладающих способностью оказывать токсическое действие, особое место занимает пул веществ средней молекулярной массы, динамика которого отражает тяжесть эндогенной интоксикации. Другим фактором, способным оказывать существенное влияние на развитие эндотоксикоза, является интенсификация свободнорадикального окисления. Поэтому комплекс биохимических исследований, необходимых для представленной шкалы оценки эндогенной интоксикации, включал в себя анализ параметров соответствующих блоков метаболизма.
Заявляемый способ осуществляется следующим образом
Производится комплекс биохимических исследований, включающий в себя изучение параметров антиоксидантной и оксидантной систем в крови, сопоставление полученных данных с гематологическими и клинико-биохимическими тестами, оценку уровня эндотоксикоза с применением расчетных индексов.
Применяют следующие унифицированные методы анализа антиоксидантной системы и выраженности окислительных процессов в крови:
- общую антиоксидантную и оксидантную - ОАА и ООА соответственно - активность оценивают согласно [35];
- активность церулоплазмина оценивают согласно [27];
- уровень малонового диальдегида - МДА - в крови оценивают согласно [36].
Тяжесть эндотоксикоза у обследованных больных в послеоперационном периоде оценивается также с расчетом математических индексов. Эти индексы предложены нами по причине необходимости проанализировать соотношение активности составляющих антиоксидантной системы в плазме крови и эритроцитах, а также оксидантной и антиоксидантной систем в крови.
В некоторых случаях единицы измерения клинико-биохимических показателей различны (например, ОАА плазмы - %, церулоплазмин - мг %). Поэтому необходимо введение коэффициентов К для получения относительных величин индексов: значение каждого параметра нужно делить на его норму.
Для клинико-биохимических показателей, имеющих одинаковые единицы измерения, введение коэффициентов К не обязательно. Однако для достижения единообразия коэффициенты К введены во все индексы.
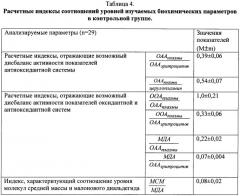
Расчетные индексы, отражающие возможный дисбаланс активности показателей антиоксидантной системы
В организме человека имеются как система генерации активных форм кислорода (АФК), так и достаточно эффективная система защиты от их повреждающего воздействия на интактные клетки.
В эритроцитах имеют место ферментативные и самопроизвольные механизмы генерации реактивных оксигенирующих радикалов (POP), которые устраняются из них в основном при помощи специфических ферментативных реакций, играющих ведущую роль в инициации процессов оксигенации гемоглобина [16, 17].
Считается, что цитотоксичность АФК крови проявляется в основном к эритроцитам, что ведет к увеличению содержания метгемоглобина, инициации процесса перекисного окисления липидов, а гемоглобин служит медиатором образования гидроксильных радикалов.
Согласно [18] первичным фактором, вызывающим повреждение и последующую элиминацию эритроцитов, является длительное повышение интенсивности процессов ПОЛ в период 1-3 сутки постреанимационного периода.
Учитывая вышеизложенное, актуально изучение соотношения общей антиоксидантной активности плазмы и эритроцитов для оценки сбалансированности реакций антиоксидантных факторов этих биологических субстратов.
Исходя из этого предлагается введение коэффициентов К, предназначенных для получения относительных величин индексов: значение каждого параметра нужно делить на его норму, так как единицы измерения клинико-биохимических показателей могут быть различны.
Например, требуется разработать индекс, отражающий возможный дисбаланс биохимического параметра 1 и показателя 2. Тогда предлагаемые расчетные индексы могут быть представлены в виде следующей общей формулы:
где величина
Соответственно общая формула предлагаемых расчетных индексов:
Нами был предложен индекс 1: характеризующий возможный дисбаланс ОАА плазмы и эритроцитов и рассчитывающийся таким образом, что берут среднее значение нормы (математическое ожидание величины) ОАА плазмы и ОАА эритроцитов и перемножают на данные ОАА плазмы и ОАА эритроцитов больного.
Например, если среднее значение нормы (математическое ожидание величины) ОАА плазмы составляет 13%, а ОАА эритроцитов 40,78%, тогда индекс 1 определяется по следующей формуле:
В сыворотке крови роль антиоксидантов выполняет ряд белков, в первую очередь церулоплазмин. В дополнение к антиоксидантной функции церулоплазмин контролирует синтез гемоглобина и ряда других железосодержащих белков, а также участвует в инактивации избытка гормонов в крови. Белок вырабатывается в печени и при увеличении в крови перекисей и других продуктов ПОЛ интенсифицируется синтез церулоплазмина и выведение его в кровь.
Церулоплазмин обладает выраженной оксидазной активностью; в плазме он также ограничивает освобождение запасов железа, активирует окисление аскорбиновой кислоты, норадреналина, серотонина и сульфгидрильных групп, а также инактивирует активные формы кислорода, предотвращая перекисное окисление липидов. Для более эффективной защиты эритроцитов от свободных радикалов на поверхности клеток имеются специальные рецепторы, способные связывать церулоплазмин [19]. Долю активности церулоплазмина в ОАА плазмы можно оценить с применением индекса 2, рассчитывающегося по следующей формуле:
Например, если среднее значение нормы (математическое ожидание величины) ОАА плазмы составляет 13%, а активности церулоплазмина 27,15 мг%, тогда индекс 2 выводится по следующей формуле:
Расчетные индексы, отражающие возможный дисбаланс активности показателей оксидантной и антиоксидантной систем
Активированные формы кислорода (АФК) выступают инициаторами интенсификации свободнорадикальных процессов в тканях и органах больного при критических состояниях любого генеза. Основные виды АФК исходно являются нормальными компонентами клеточного метаболизма и выполняют определенные биологические функции. Их реактивная агрессивность сдерживается антиоксидантной системой (АОС), присутствующей в любом живом организме, но в патологических условиях этот баланс нарушается в сторону неконтролируемой генерации реактивных оксигенирующих радикалов (POP), что приводит к формированию оксидантно-антиоксидантного дисбаланса в развитии эндотоксикоза.
Дисбаланс ООА плазмы и ОАА плазмы и эритроцитов соответственно отражают индексы 3 и 4.
Индекс 3 определяют по формуле:
Например, если среднее значение нормы (математическое ожидание величины) ООА плазмы 11,86%, ОАА плазмы 13%, то индекс 3 определяется по следующей формуле:
Индекс 4 определяют по формуле:
Коэффициент К=3,44 для индекса 4 получают следующим образом.
Среднее значение нормы (математическое ожидание величины) ООА плазмы 11,86%, ОАА эритроцитов 40,78%.
Тогда индекс 4 выводится по следующей формуле:
Активация процессов перекисного окисления липидов (ПОЛ) приводит к накоплению токсических продуктов, которые отрицательно влияют на клеточные мембраны. ПОЛ является многостадийным процессом.
Различные метаболиты этого каскада реакций в возникающих при эндотоксикозе нарушениях гомеостаза могут играть разную роль. Диеновые коньюгаты являются короткоживущими продуктами, а шиффовы основания химически инертны, поэтому полагают, что их роль в нарушениях клеточного метаболизма невелика, в основном они выступают в виде маркеров активности ПОЛ. В отличие от них малоновый диальдегид (МДА) не только является показателем активности свободнорадикальных реакций, но и обладает токсичными свойствами, поскольку способен повреждать белки, ферменты, нуклеиновые кислоты [20]. Возможно, поэтому избыточное накопление МДА значительно усугубляет эндотоксемию [21, 22].
Известно, что МДА активно взаимодействует с сывороточным альбумином и белками эритроцитов и печени [23].
Активизация в организме процессов свободнорадикального окисления, наблюдающаяся при многих заболеваниях, может заметно повлиять на функциональную активность сывороточных альбуминов. С другой стороны, сам альбумин считается компонентом антиоксидантной системы организма [24, 25]. Альбумин снижает образование гидроксильных радикалов в си