Способ диагностики риска развития вазопатии у больных артериальной гипертонией с метаболическим синдромом
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к кардиологии и ангиологии, и может быть использовано для диагностики риска развития вазопатии у больных артериальной гипертонией (АГ) с метаболическим синдромом (МС). Сущность способа: определяют агрегационную активность тромбоцитов с коллагеном, уровень антитромбина III, время эуглобулинового лизиса и содержание нитратов в крови пациентов до и на фоне временной венозной окклюзии. Затем вычисляют индекс антиагрегационной активности стенки сосудов (ИААСС), индекс синтеза антитромбина III в сосудах (ИСАС), индекс фибринолитической активности сосудистой стенки (ИФАСС) и нитратный индекс (НИ), рассчитываемые как отношение значений соответствующих показателей на фоне и до временной венозной окклюзии. Далее рассчитывают противотромботический индекс сосудов (ПТИС) по формуле ПТИС=(ИААСС+ИСАС+ИФАСС+НИ)/4. При его значении 2,27 и выше риск развития вазопатии отсутствует; при его значении в интервале 2,26-2,10 больные входят в группу риска по развитию вазопатии; при его значении 2,09 и ниже развивается вазопатия. Использование способа позволяет повысить эффективность ранней диагностики риска развития вазопатии у больных АГ с МС, что дает возможность своевременно назначить соответствующее лечение. 2 табл., 1 ил.
Реферат
Изобретение относится к медицине, а именно к кардиологии и ангиологии.
Известны методы исследования сосудистых функций (Баркаган З.С., Момот А.П. Основы диагностики нарушений гемостаза. М., 1999. - 214 с.), однако способ раннего выявления ослабления антитромботической активности сосудов в целом не разработан.
В клинической лабораторной диагностике применяется метод исследования антиагрегационной активности сосудистой стенки, оценивается уровень антитромбина III (AT III), активность плазминногена до и после временной венозной окклюзии и содержание оксида азота (NO) в плазме крови по уровню нитратов.
Однако никогда ранее данные методы не объединяли в единый диагностический комплекс, а полученные результаты не обрабатывали статистически с расчетом противотромботического индекса сосудов (ПТИС).
Целью изобретения является повышение эффективности ранней диагностики риска развития вазопатии у больных артериальной гипертонией с метаболическим синдромом.
Сущность заявляемого способа заключается в том, что для ранней диагностики риска развития вазопатии у больных артериальной гипертонией с метаболическим синдромом проводится следующий диагностический комплекс исследований: определяется индекс антиагрегационной активности сосудов, активность антитромбина III и эуглобулиновый лизис до и после временной венозной окклюзии с вычислением индекса синтеза AT III в сосудах и индекса фибринолитической активности сосудистой стенки, а также содержание в крови нитратов до и после временной ишемии венозной стенки, указывающее на уровень синтеза NO в стенках сосудов с вычислением нитратного индекса (НИ). Полученные результаты обрабатываются статистически с вычислением противотромботического индекса сосудов.
Способ позволяет своевременно диагносцировать риск развития вазопатии по снижению ПТИС у пациентов с АГ и МС, что дает возможность своевременно назначать соответствующее лечение, переводящее ПТИС на уровень, близкий к таковому для здоровых людей. При регулярном обследовании в последующем согласно заявляемому способу возможен контроль поддержания ПТИС в оптимальном режиме функционирования, что позволит существенно снизить риск тромботических осложнений, уменьшить число случаев временной нетрудоспособности, выходов на инвалидность и снизить смертность среди сосудистых больных.
Заявляемый способ осуществляется следующим образом.
Антиагрегационная активность сосудистой стенки определялась по методу (Балуда В.П., Лукьянова Т.И., Балуда М.В. Метод определения антиагрегационной активности стенки сосудов человека. // Лабор. дело, 1983. - № 6. - с.17-20). В основе этого метода лежит вычисление степени торможения агрегации тромбоцитов в плазме, полученной из крови после временной венозной окклюзии.
На плечо руки, из сосудов которой не производился забор крови, накладывается манжетка сфигмоманометра и создается давление на 10 мм рт.ст. выше систолического. Через 3 минуты производилось взятие 9 мл крови в 1 мл 3,8% раствора цитрата натрия. Ее немедленно центрифугировали 5 минут при 1000 об/мин для получения богатой тромбоцитами плазмы. Плазму отсасывали пипеткой и сразу же помещали в тающий лед, где хранили до начала исследований. Повторно пробу центрифугировали 20 минут при 3000 об/мин для получения бестромбоцитной плазмы. После подсчета количества тромбоцитов в богатой тромбоцитами плазме, полученной до венозного застоя (подробно описано ниже), ее разводили бедной тромбоцитами плазмой (БеТП), взятой до (1 проба) и после (2 проба) венозного застоя до концентрации 200000 тромбоцитов/мкл. Полученную смесь встряхивали и инкубировали 10 минут при 20-22°С. Затем проводили агрегацию тромбоцитов (AT) с коллагеном (разведение 1:2 основной суспензии) на стекле.
Оценка AT для проведения данного исследования осуществляется следующим способом (Шитикова А.С. Гемостаз. Физиологические механизмы, принципы диагностики основных форм геморрагических заболеваний. Под ред. Н.Н.Петрищева, Л.П.Папаян. СПб, 1999. С.49-52).
Кровь забирают с цитратом натрия 3,8% в соотношении 9:1, центрифугируют 5 мин при 1000 об/мин для получения богатой тромбоцитами плазмы (БТП). Часть плазмы отбирают, а оставшуюся центрифугируют при 3000 об/мин в течение 20 мин, получая бедную тромбоцитами плазму. БТП стандартизируют по числу тромбоцитов путем разбавления исходной БТП аутологичным образцом БеТП (полученной до венозного застоя - 1-я проба или после него - 2-я проба) до 200·109/л. Концентрация кровяных пластинок в исходной БТП подсчитывается в камере Горяева (в 50 больших квадратах). Объемы смешиваемых БТП и БеТП определяют по формуле:
VБеТП=VБТП·[(N/200000)-1],
VБеТП - объем бедной тромбоцитами плазмы,
VБТП - объем богатой тромбоцитами плазмы,
N - счетная концентрация тромбоцитов в исходной БТП (клеток/мкл).
Из отобранного объема стандартизированной плазмы на предметное стекло наносят 0,02 мл плазмы и другой пипеткой 0,02 мл р-ра индуктора коллагена в стандартной концентрации (разведение 1:2 основной суспензии). Стеклянной палочкой смешивают плазму с индукторами и включают секундомер. Смесь перемешивают так, чтобы жидкость занимала окружность диаметром около 2 см.
Покачивая стекло круговыми движениями в проходящем свете осветителя, на черном фоне следят через лупу за возникновением агрегатов. При появлении отчетливых агрегатов, просветлении раствора и прилипании части агрегатов к стеклу секундомер отключают, фиксируя время агрегации тромбоцитов.
Реакцию повторяют по 2-3 раза, находя среднее арифметическое значение.
По степени торможения агрегации тромбоцитов после временного венозного застоя судят об антиагрегационной активности плазмы крови, обусловленной поступлением в кровоток простациклина из сосудистой стенки. Индекс антиагрегационной активности сосудистой стенки (ИААСС) при исследовании AT на стекле рассчитывали по формуле:
Нормальными значениями для коллагена можно считать ИААСС 1,50-1,60.
Определение противосвертывающих свойств сосудистой стенки, зависящих от выделения из нее антитромбина III, оценивая его базальный уровнь до- и послевременной дозированной ишемии стенки вены приведены ниже (Баркаган З.С., Момот А.П. Основы диагностики нарушений гемостаза. М. 1999 - 214 с.).
Принцип метода основан на выявлении снижения активности (в отсутствие гепарина) в плазме антитромбина III, которую определяют по способности исследуемой плазмы инактивировать тромбин, для чего ее предварительно обрабатывают сорбентом гепарина, затем подвергают тепловой дефибринации и смешивают со стандартным количеством тромбина. После инкубации смеси в ней определяют остаточную коагуляционную активность тромбина. По уровню снижения активности тромбина в процентах от нормы оценивают активность AT III в исследуемой плазме.
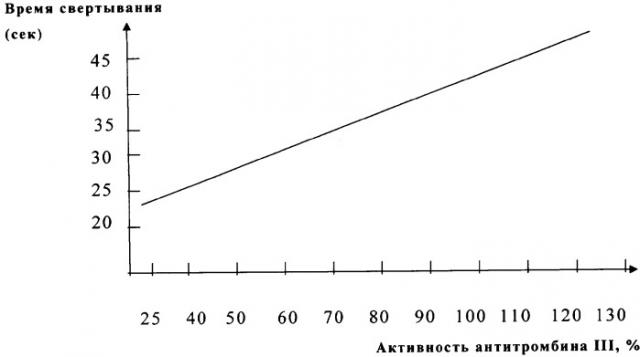
Используются следующие реактивы. 1. Трис-HCl буфер 0,05 М, рН 7,4. 2. Раствор тромбина в буфере: 0,2 мл раствора должны свертывать 0,3 мл 0,4% раствора фибриногена за 15-16 сек. Рабочий раствор тромбина готовят в пластиковой или силиконированной пробирке, хранят при комнатной температуре и используют в тесте в день исследования. 3. Сорбент гепарина Гепасорб-1 (фирма "Технология-Стандарт"). 4. Свежеприготовленный раствор фибриногена в концентрации 3,5-4,0 г/л, который применяют для тестирования остаточной активности тромбина. Допускается замена раствора фибриногена нормальной бедной тромбоцитами цитратной плазмой, разведенной буфером в 2 раза; 5. Свежая цитратная бедная тромбоцитами плазма, полученная от 6-8 здоровых людей, или лиофилизированная фирменная с известной активностью AT III, которую используют для построения калибровочного графика (см. чертеж 1).
Материалом для исследования служит цитратная бедная тромбоцитами плазма.
Для приготовления сорбированной и дефибринированной плазмы в пробирке смешивают 10 мг сорбента гепарина с 1,0 мл исследуемой плазмы. Постоянно встряхивая пробирку, перемешивают ее содержимое при комнатной температуре в течение 8 мин, исключая образование пены и осадка на ее дне. После этого смесь центрифугируют в течение 2 мин при 1000-1500 об/мин. Плазму в надосадке переносят в чистую пробирку и дефибринируют на водяной бане при 56°С в течение 6 мин, после чего вновь центрифугируют при 3000 об/мин в течение 10 мин, снимают надосадочную часть и исследуют в течение первых 2 ч.
Ход определения. В пробирку вносят 0,4 мл рабочего раствора тромбина и прогревают его на водяной бане при 37°С в течение 2 мин. Затем добавляют 0,1 мл исследуемой адсорбированной и дефибринированной плазмы, включают секундомер. Через 2 мин (точно!) 0,2 мл смеси переносят в пробирку с 0,3 мл раствора фибриногена (или разведенной нормальной плазмы), предварительно подогретой до 37°С. Немедленно включают секундомер и регистрируют время свертывания.
По калибровочной кривой находят активность AT III в процентах.
Построение калибровочной кривой проводят следующим образом. Плазму здоровых людей подвергают дефибринированию, как указано выше. Затем из нее готовят разведения для построения калибровочной кривой в соответствии с табл.1.
| Таблица 1 | |||
| Схема приготовления разведений плазмы для построения калибровочной кривой при определении активности AT III | |||
| Номер разведения | Плазма + буфер | Активность AT III, % | |
| 1 | Плазма без буфера | 100 | |
| 2 | 0,2 мл + 0,2 мл | 50 | |
| 3 | 0,1 мл + 0,3 мл | 25 |
С каждым из разведений определяют время свертывания по указанной выше методике. Все измерения проводят трижды, рассчитывают средний результат. При построении калибровочной кривой по логарифмической оси ординат откладывают время свертывания в секундах, по оси абсцисс - активность AT III в % в соответствии с указанными выше разведениями. Примерная калибровочная кривая приведена на чертеже.
Калибровочную кривую для одной серии тромбина и буфера строят однократно. Периодически контролируют лишь активность рабочего раствора тромбина.
В норме без венозной окклюзии активность AT III составляет 85-115%. При взятии крови после временной венозной окклюзии, как описано в методе по оценке антиагрегационной активности сосудов, и определении в ней AT III возможно косвенно оценить уровень выделения из стенки сосуда AT III. На фоне временной венозной окклюзии активность AT III повышается и находится в границах 120-143%. Рассчитывается индекс синтеза AT III в сосудах (ИСАС) путем деления величины активности AT III на фоне венозной окклюзии на величину AT III без нее. В норме он равен 1,20-1,45.
Активность синтеза тканевых активаторов плазминогена по времени лизиса эуглобулинового сгустка до- и послевременной венозной окклюзии оценивали следующим образом.
Принцип метода заключается в осаждении эуглобулиновой фракции плазмы, при этом основные ингибиторы фибринолиза, в частности α2-антиплазмином, остаются в надосадочной части и удаляются. Поэтому эуглобулиновый лизис отражает активность фибринолиза в условиях исключения ингибирующего действия антиплазминов. Его скорость отражает в основном количество плазминогена в плазме и степень его активации. Определяют время спонтанного лизиса сгустка, получаемого из эуглобулиновой фракции плазмы при добавлении к ней раствора хлорида кальция.
Используются следующие реактивы: 1. 1% раствор уксусной кислоты. 2. 0,277% раствор хлорида кальция. 3. Буфер Михаэлиса или трис-HCl буфер, 0.05М, рН 7,3-7,4.
Материалом для исследования служит цитратная бедная тромбоцитами плазма до и после временной венозной окклюзии.
Ход определения. Для получения эуглобулиновой фракции к 8,0 мл дистиллированной воды добавляют 0,15 мл 1% уксусной кислоты и 0,5 мл исследуемой плазмы. После 30-минутного охлаждения смеси в холодильнике при +2-8°С эуглобулины осаждают центрифугированием при 1500 об/мин в течение 7 мин. Надосадочную жидкость сливают, пробирку осушают опрокидыванием на фильтровальную бумагу. Осадок эуглобулинов разводят в 0,5 мл буфера и помещают на водяную баню (37°С). Затем, не вынимая пробирку из бани, добавляют 0,5 мл раствора хлорида кальция, осторожно перемешивают покачиванием пробирки (не встряхивая!), включают секундомер и инкубируют на водяной бане при 37°С. Регистрируют время с момента добавления хлорида кальция до полного растворения сгустка.
Результат выражают в минутах. В норме время спонтанного лизиса эуглобулинового сгустка составляет 180-240 мин. После временной венозной окклюзии время лизиса снижается, находясь в границах 126-170 мин. При делении величины длительности спонтанного лизиса эуглобулинового сгустка до окклюзии на величину после рассчитан индекс фибринолитической активности сосудистой стенки (ИФАСС), в норме равный 1,40-1,50.
Нитраты в крови определяли по методу (Емченко Н.Л., Цыганенко О.И., Ковалевская Т.В. Универсальный метод определения нитратов в биосредах организма.// Клиническая лабораторная диагностика. 1994. - № 5, - с.19-20).
Ход определения. В центрифужные пробирки вместимостью 10 мл помещают 0,25-1,50 мл 50% раствора сульфата цинка, 0,25-1,50 мл 17% раствора феррицианида железа, 1-5 мл анализируемой пробы (пипетку для отбора крови предварительно смачивают раствором цитрата натрия). Затем прибавляют 0,5-2 мл аммиачно-хлоридного буфера (рН 9,6±0,05) и от 1 до 8 мл дистиллированной воды для анализа плазмы крови.
Объемы анализируемой пробы и применяемых для ее депротеинизации реактивов представлены в табл.2.
| Таблица 2 | |||||
| Объемы (в мл) анализируемых проб и реактивов, прибавляемых для их депротеинизации | |||||
| Биосубстрат | Проба | ZnSO4 | K2Fe(CN)6 | Буфер | Дистиллированная вода |
| Кровь | 1,00 | 1,00 | 1,00 | 2,00 | 5,00 |
Общий объем смеси должен составлять 10 мл.
Полученную смесь перемешивают и центрифугируют в течение 20 мин при 2500 об/мин. Параллельно проводят холостой опыт.
Отбирают аликвоту центрифугата объемом 5 мл в колбу вместимостью 50 мл, прибавляют 2,5 мл аммиачно-хлоридного буфера, 2,5 мл дистиллированной воды, перемешивают и пропускают через колонку с губчатым кадмием вначале холостую пробу, затем испытуемую. Перед пропусканием каждой из проб колонку промывают последовательно 5 мл 1 н. HCl, 50 мл дистиллированной воды и 25 мл аммиачно-хлоридного буфера, разбавленного в соотношении 1:9. Элюат собирают в ту же мерную колбу, колонку промывают дистиллированной водой, не доводя объем раствора в колбе до метки примерно на 10 мл. Затем в колбу прибавляют 5 мл 0,25% раствора стрептоцида, 1 мл HCl (1:2) и через 5 мин - 1 мл 0,1% раствора N-нафтилэтилендиаминдигидрохлорида. Раствор доводят до метки дистиллированной водой, перемешивают и оставляют на 10 мин. По истечении этого времени пробы фотометрируют на фотоэлектроколориметре при длине волны 540 нм (зеленый светофильтр) в кювете с длиной оптического пути 5 см против холостой пробы.
Концентрацию нитратов определяют по градуированному графику, строящемуся в каждой лаборатории отдельно и самостоятельно. Для его построения в мерные колбы вместимостью 50 мл вносят 0,25, 0,5, 1, 2,5 и 5 мл раствора нитрата калия с концентрацией нитрат-иона, равной 10 мкг/мл, добавляют по 10 мл дистиллированной воды и по 5 мл аммиачно-хлоридного буфера и элюируют через кадмиевую колонку. Цветную реакцию и фотометрирование проводят, как описано выше. Оптическую плотность измеряют против нулевого раствора.
Содержание нитратов (X, мг/л) в анализируемых образцах биосред рассчитывают по формуле:
где C1 - концентрация нитрат-ионов в фотометрируемом растворе, найденная по градуировочному графику (мкг/мл); V1 - общий объем безбелкового экстракта (мл); V2 - общий объем фотометрируемого раствора (мл); V3 - объем образца, взятого для анализа (мл); V4 - объем безбелкового экстракта, взятого для анализа (в мл). В норме у здоровых людей концентрация нитритов в крови составляет 1,20-2,2 мг/л. При временном наложении жгута на плечо и создании временной ишемии стенки сосуда по описанной выше схеме отмечается усиленное выделение в кровь из сосуда оксида азота с ростом содержания в крови нитратов от 6,0 до 13,0 мг/л. Возможен расчет нитратного индекса по формуле:
В норме НИ находится в границах от 5,0 до 5,9.
ПТИС рассчитывается по формуле:
Нормальными значениями ПТИС являются значения не ниже 2,27. При ПТИС в границах 2,26-2,10 имеет место риск развития вазопатии, а при значении ПТИС 2,09 и ниже отмечается клиническая манифестация вазопатии.
Внедрение данного способа риска развития вазопатии у больных АГ с МС в практику лечебных учреждений позволит решить ряд насущных социально-экономических проблем современности. Ранняя диагностика у данной категории больных позволит своевременно начинать у них лечение вазопатии, что сократит у этих пациентов сроки временной нетрудоспособности, профилактирует инсульты и инфаркты, уменьшит число выходов на инвалидность и снизит смертность среди данного контингента больных.
Пример 1. Больная Б. 42 года, страдающая артериальной гипертонией с метаболическим синдромом на протяжении 2 лет, ведущая здоровый образ жизни, обследована во время диспансерного осмотра по поводу артериальной гипертонии. У больной была взята кровь и исследована по изложенной выше схеме с оценкой антиагрегационной активности сосудистой стенки, содержания антитромбина III, времени эуглобулинового лизиса, уровня нитратов до и после венозной окклюзии и вычислением ИААСС, ИСАС, ИФАСС, НИ и противотромботического индекса сосудов.
У пациентки не было выявлено признаков угнетения ПТИС. ИААСС составлял 1,5, ИСАС, ИФАСС, НИ составляли 1,3, 1,4, и 5,1 соответственно. ПТИС составил 2,32. Больной было рекомендовано и далее контролировать артериальное давление и вести здоровый образ жизни. Исследование функций сосудистой стенки у нее через 12 нед не выявило отрицательных изменений значения ПТИС (2,34).
Пример 2. Больная Л. 47 лет, страдающая артериальной гипертонией с метаболическим синдромом на протяжении 6 лет, обследована во время диспансерного осмотра по поводу артериальной гипертонии. У больной была взята кровь и исследована по изложенной выше схеме с оценкой антиагрегационной активности сосудистой стенки, содержания антитромбина III, времени эуглобулинового лизиса, уровня нитратов до- и послевенозной окклюзии и вычислением ИААСС, ИСАС, ИФАСС, НИ и расчетом ПТИС.
ИААСС составлял 1,36. ИСАС, ИФАСС и НИ составили 1,18, 1,37 и 4,7 соответственно. ПТИС составил 2,15. У пациентки был выявлен риск развития вазопатии. Больной было рекомендовано для адекватного контроля артериального давления и нормализации состояния сосудистой стенки вести здоровый образ жизни, принимать нормодипин 10 мг 1 раз в сутки и обследоваться ежемесячно. Так, исследование функций сосудистой стенки через 12 нед не выявило отрицательных отклонений в ИААСС - 1,51, ИСАС - 1,43, ИФАСС - 1,48, НИ - 5,4. ПТИС у нее находился на уровне нормы - 2,45.
Способ диагностики риска развития вазопатии у больных артериальной гипертонией с метаболическим синдромом, характеризующийся тем, что определяют агрегационную активность тромбоцитов с коллагеном, уровень антитромбина III, время эуглобулинового лизиса и содержание нитратов в крови пациентов до и на фоне временной венозной окклюзии, затем вычисляют индекс антиагрегационной активности стенки сосудов (ИААСС), индекс синтеза антитромбина III в сосудах (ИСАС), индекс фибринолитической активности сосудистой стенки (ИФАСС) и нитратный индекс (НИ), рассчитываемые как отношение значений соответствующих показателей на фоне и до временной венозной окклюзии, затем рассчитывают противотромботический индекс сосудов (ПТИС) по формуле ПТИС=(ИААСС+ИСАС+ИФАСС+НИ)/4, и при его значении 2,27 и выше риск развития вазопатии отсутствует; при его значении в интервале 2,26-2,10 больные входят в группу риска по развитию вазопатии; при его значении 2,09 и ниже развивается вазопатия.