Ингалятор сухого порошка
Иллюстрации
Показать всеОписан ингалятор сухого порошка, содержащий сопло, подложку, дозу лекарственного порошка, обеспечивающий дезагрегирование и рассеивание в воздух агрегатов частиц дозы лекарственного порошка. Настоящее изобретение не требует других источников энергии кроме энергии усилия вдоха, производимого пользователем, для осуществления очень высокой степени дезагрегирования и эффективного рассеивания в воздух терапевтической дозы сухого порошка. Под действием силы всасывания воздуха через сопло частицы терапевтической порошковой дозы, доступные соплу, постепенно дезагрегируются и рассеиваются в поток воздуха, поступающего в сопло. Постепенное дезагрегирование и рассеивание продуцируется эффектом срезания порошка потоком воздуха благодаря относительному движению, индуцированному между соплом и порошковой дозой. Сопло обычно располагается за пределами участка, занимаемого порошком, без доступа к порошку до тех пор, пока воздушный поток в сопло, созданный посредством всасывания, не пройдет пороговую скорость течения. Одновременно с всасыванием начинается относительное движение таким образом, что сопло постепенно пересекает порошковую дозу. Срезающее усилие и инерция воздушного потока настолько мощные, что агрегаты частиц порошковой дозы, прилежащие к входному отверстию движущегося сопла, высвобождаются, дезагрегируются до очень высокой степени и рассеиваются, а затем увлекаются в созданный воздушный поток, проходящий через сопло к пользователю, делающему ингаляцию. 6 з.п. ф-лы, 3 табл., 18 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к ингалятору сухого порошка, содержащему сопло, подложку, дозу лекарственного порошка, обеспечивающему дезагрегирование и рассеивание в воздух агрегатов частиц дозы лекарственного порошка.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
В настоящее время в медицинских службах введение лекарственных средств осуществляют целым рядом различных способов. По ряду причин, таких как необходимость местного лечения легочных заболеваний взамен инъекционной терапии и необходимость быстрого начала действия, имеется большая заинтересованность во введении лекарственных средств в легкие пациента. Разработано много различных устройств для доставки лекарственных средств в легкое, например аэрозоли под давлением (pMDI (дозирующие аэрозольные ингаляторы под давлением)), небулайзеры и сухие порошковые ингаляторы (DPI).
Несмотря на то что ингаляция лекарственных средств хорошо зарекомендовала себя для местного лечения легочных заболеваний, таких как астма, исследования по использованию легкого в качестве возможного места введения в организм системно действующих лекарственных средств продолжаются. Для местно действующих лекарственных средств предпочтительное осаждение лекарственного средства в легком зависит от локализации конкретного заболевания, поэтому осаждение в верхних, а также в нижних дыхательных путях представляет интерес. Для системной доставки лекарства осаждение лекарственного средства глубоко в легком является предпочтительным и обычно необходимо для максимальной эффективности. Под «глубоко в легком» следует понимать периферические области легкого и альвеолы, где может осуществляться прямой транспорт активного вещества в кровь.
Легкое представляет собой притягательное место для системной доставки лекарственных средств, так как оно предоставляет большую площадь поверхности (примерно 100 м2) для всасывания молекул через тонкий эпителий, что дает возможность быстрого всасывания лекарственного средства. Поэтому легочная доставка имеет преимущество по сравнению с назальной доставкой, а именно возможность достижения достаточно высокой степени всасывания без необходимости использовать усилители всасывания. Пригодность этого пути введения для конкретного лекарства зависит, например, от размера дозы и степени всасывания конкретного вещества.
Критическими факторами для осаждения вдыхаемых частиц в легком являются характер вдоха/выдоха и распределение частиц по их аэродинамическим размерам. Для максимального осаждения в легком вдох должен производится спокойно для снижения скорости воздуха и, соответственно, уменьшения осаждения в верхних дыхательных путях под действием ударной силы.
Для сухих порошковых ингаляторов существуют ограничения по аэродинамическому размеру частиц лекарственного средства для достижения приемлемого осаждения лекарственного средства внутри легкого. Если частица должна попасть глубоко в легкое, то аэродинамический размер частиц обычно должен быть меньше 3 мкм, а для местного осаждения в легком - обычно приблизительно 5 мкм. Частицы большего размера оседают в ротовой полости и в горле. Таким образом, независимо от того, является ли целью местная или системная доставка лекарственного средства, важно сохранить распределение частиц дозы по их аэродинамическим размерам в узких пределах, чтобы обеспечить высокий процент фактически осажденной дозы там, где это будет наиболее эффективно.
Дезагрегирование
Порошки с размером частиц, подходящим для ингаляционной терапии, имеют тенденцию к агрегации, то есть к образованию малых или больших агрегатов, которые сначала необходимо дезагрегировать, а затем вводить частицы в дыхательные пути пользователя. Дезагрегирование определяется как разрушение агрегированного порошка путем использования энергии, например электрической, механической, пневматической или аэродинамической энергии. Некоторые сухие порошковые ингаляторы рассчитаны на внешние источники дезагрегирующей энергии, например механической, электрической или пневматической, а некоторые рассчитаны только на силу вдоха пользователя.
Аэродинамический диаметр частицы - это диаметр сферической частицы, имеющей плотность 1 г/см3, которая обладает такими же инерционными свойствами в воздухе, как и частица, представляющая интерес. Это означает, что аэродинамический диаметр частицы определяется размером первоначальной частицы, формой этой частицы и плотностью этой частицы. Если первоначальные частицы дезагрегированы в воздухе не полностью, агрегат аэродинамически будет вести себя подобно одной большой частице. Поэтому для конкретного лекарственного вещества существует три основных, принципиально разных способа регулировать распределение частиц по их аэродинамическим размерам из сухого порошкового ингалятора (DPI): a) варьированием распределения первоначальных частиц по размерам или б) варьированием степени дезагрегирования, или в) варьированием плотности частиц (делая частицы похожими на перекати-поле).
Существующие в настоящее время ингаляционные устройства, предназначенные для лечения астмы и других легочных заболеваний, обычно доставляют рассеянное лекарственное средство в диапазоне аэродинамических размеров, подходящем для местного осаждения в легких. Такое распределение частиц по их аэродинамическим размерам часто вызвано неэффективной дезагрегацией порошка с размером первоначальных частиц в пределах 2-3 мкм. Таким образом, вдыхаемая доза состоит в основном из агрегатов частиц. Это обуславливает ряд недостатков, наиболее важными из которых являются:
- однородность распределения частиц по их аэродинамическим размерам может существенно меняться от дозы к дозе, поскольку дезагрегирование чувствительно к самым незначительным различиям в условиях вдоха от одной ингаляции к другой;
- распределение частиц доставляемой дозы по их размерам может иметь «хвост» из больших агрегатов, которые будут оседать в ротовой полости и в верхних дыхательных путях.
Лучшую, более устойчивую ситуацию получают при высокой степени дезагрегации лекарственного порошка во вдыхаемом воздухе, так как хорошее дезагрегирование дает лучшую воспроизводимость и эффективность осаждения лекарственного средства в легком. Предпочтительно дезагрегирующая система должна быть как можно менее чувствительной к силе вдоха, производимого пользователем, чтобы распределение доставляемых частиц по их аэродинамическим размерам во вдыхаемом воздухе не зависело от силы вдоха.
Поэтому для эффективной доставки лекарственных средств в легкое имеется потребность в системе, устойчиво генерирующей очень высокую степень дезагрегации лекарственного порошка в тех случаях, когда сила вдоха пациента меняется в разумных пределах. Очевидно, что для системно действующих лекарственных средств, когда необходимо глубокое осаждение в легких, а также для местно действующих лекарственных средств, когда предпочтительно в большей степени местное осаждение в легких, устойчивая высокая степень дезагрегации порошка лекарства является преимуществом. Таким путем распределение частиц по их аэродинамическим размерам будет в меньшей степени зависеть от силы вдоха пользователя. Средний размер частиц, который влияет на картину осаждения в легком, можно регулировать распределением первоначальных частиц в порошке по их размерам. Больший размер первоначальных частиц и идеальное дезагрегирование дают устойчивую систему для местной доставки в легкое.
Очень высокая степень дезагрегации предполагает необходимость следующего:
- соответствующий препарат порошка (распределение частиц по размерам, форма частиц, адгезионные силы, плотность и т.д.);
- соответственно сформированная доза порошка, адаптированная к возможностям выбранного ингаляторного устройства;
- ингаляторное устройство, обеспечивающее в дозе срезывающие усилия достаточной силы, чтобы дезагрегировать порошок (например, турбулентность, столкновение).
Что касается лекарственного препарата, то существует ряд общеизвестных методов достижения подходящего распределения первоначальных частиц по размерам, обеспечивающего возможность надлежащего осаждения в легких высокого процента дозы. Такие методы включают измельчение в струйной мельнице, распылительную сушку и сверхкритическую кристаллизацию.
Существует также целый ряд общеизвестных способов модифицирования сил между частицами и получения таким путем порошка с подходящими адгезионными силами. Такие способы включают модифицирование формы частиц и поверхностных свойств частиц, например пористые частицы и контролируемое образование гранул порошка, а также добавление инертного носителя с большим средним размером частиц (так называемая упорядоченная смесь).
Большинство местно действующих лекарственных средств для ингаляции, имеющихся в настоящее время в продаже, представляют собой довольно небольшие органические молекулы. Примерами используемых лекарственных средств являются стероиды, такие как будесонид, бронходилататоры, такие как салбутамол, и подобные им вещества.
Для многих из этих лекарственных веществ разработка фармацевтических препаратов довольно проста. С другой стороны, новые лекарственные средства как для местной, так и для системной доставки часто содержат биологические макромолекулы с совершенно новыми требованиями к приготовлению препарата.
Многие белки и пептиды потенциально подходят для ингаляционной терапии и некоторые из них находятся на разных стадиях разработки. Некоторыми примерами являются инсулин, ингибитор альфа-1-протеиназы, интерлейкин-1, паратиреоидный гормон, генотропин, колониестимулирующие факторы, эритропоэтин, интерфероны, кальцитонин, фактор VIII, альфа-1-антитрипсин, фолликулостимулирующие гормоны, агонист LHRH (рилизинг-фактор лютеинизирующего гормона) и IGF-I (инсулиноподобный фактор роста I).
Белковые и пептидные лекарственные средства (PPDs) обладают свойствами, которые создают значительные проблемы в приготовлении препарата. В частности, их химическая и ферментативная лабильность практически не допускает возможности получения традиционных лекарственных форм, таких как пероральные таблетки. Поэтому PPDs в настоящее время вводят преимущественно парентерально внутривенными, внутримышечными или подкожными инъекциями. Хотя эти пути обычно удовлетворительны для ограниченного числа введений, проблемы с долговременной терапией существуют. Частые инъекции, необходимые для лечения болезни, разумеется, не являются идеальным способом доставки лекарственного средства и часто приводят к тому, что пациенты плохо соблюдают режим лечения, так как такой режим ограничивает свободу пациента. Кроме того, многие пациенты неохотно соглашаются на инъекции по физиологическим причинам и поэтому инъецируются через большие промежутки времени, чем это требуется по медицинским показаниям.
Инсулин является примером важного пептидного лекарственного средства, когда частые парентеральные введения являются наиболее распространенным путем введения. Большой процент, может быть 5%, человеческой популяции страдает сахарным диабетом. Причиной диабета является нарушение продуцирования или недостаточное продуцирование инсулина. В норме уровень глюкозы в крови постоянно контролируется продуцированием организмом естественного инсулина, но когда в случае диабета этого не происходит, концентрация глюкозы может подняться до высоких и возможно угрожающих жизни уровней. В таких случаях для лечения болезни инсулин в соответствующих количествах должен поставляться извне.
Самостоятельное введение инсулина является немаловажной реальностью и частью повседневной жизни для многих пациентов с диабетом. Обычно пациенту требуется вводить инсулин несколько раз в сутки. Инсулин, введенный перорально, не эффективен, поскольку он разрушается в желудочно-кишечном тракте, в результате чего системные концентрации слишком малы для терапевтического эффекта.
Наиболее распространенным способом введения инсулина является подкожная инъекция, которую делает сам пациент, основываясь на строгом мониторинге уровня глюкозы. Как упомянуто выше, частые инъекции не являются идеальным способом доставки лекарственного средства. Кроме того, для использования подкожного пути существуют фармакокинетические ограничения. Всасывание инсулина после подкожной инъекции довольно медленное. Иногда вплоть до одного часа проходит до того момента, когда уровень глюкозы в крови начинает значительно снижаться. Эта естественная проблема с подкожной доставкой инсулина не может быть решена более частым введением. Для получения физиологически корректных концентраций инсулина в плазме необходимо выбирать другой путь введения.
Доставка белковых и пептидных лекарственных средств (PPDs) через носовой проход обычно характеризуется довольно низкой и вариабельной биодоступностью. Факторы, влияющие на биодоступность из носовой полости, включают ограниченную площадь поверхности (приблизительно 150 см2), большой размер молекул PPDs, мукоцилиарный клиренс и ферментативную деструкцию. Всасывание PPDs из носовой полости можно значительно улучшить с помощью агентов, усиливающих всасывание. Было исследовано довольно большое количество усилителей, и предложенные механизмы заключаются в том, что они открывают непроницаемые перегородки, разрушают мембрану или ингибируют ферменты. Однако усилители проницаемости часто вызывает местное раздражение на назальной оболочке, создавая проблему, которую, как было доказано, трудно решить.
Доставка путем ингаляции аэрозоля инсулина задокументирована еще в 1920-е годы (М.Gänsslen "Uber Inhalation von Insulin"). Естественным состоянием для инсулина в качестве лекарственного вещества все же является форма раствора, так что исторически с 1920-х годов исследования по назальному и легочному введению инсулина были сконцентрированы на различных жидких препаратах инсулина.
Способы изготовления инсулина в виде сухого порошка из жидкого состояния известны и применялись в течение более чем 50 лет, в том числе такие способы, как выпаривание, распылительная сушка и сублимационная сушка (лиофилизация). Однако отсутствовали надежные и экономичные технологии получения порошков инсулина с подходящими свойствами, с одной стороны, и подходящие аппараты для доставки порошка пользователю способом, который обеспечивает эффективную системную доставку, с другой стороны. Это мешало широкомасштабным исследованиям с использованием инсулина в сухих порошковых препаратах. Тем не менее, в начале 1990-х годов Bäckström, Dahlbäck, Edman и Johansson (Therapeutic preparation for inhalation, WO 95/00127) показали, что ингаляция терапевтического препарата, содержащего инсулин и усилитель всасывания, быстро и эффективно приводит к тому, что инсулин всасывается в нижних дыхательных путях. Очевидно, что усилитель был необходим по всей вероятности из-за недостаточной дезагрегации порошка и использования некондиционного порошкового ингалятора. В течение последнего десятилетия было опубликовано множество сообщений с описанием фармакокинетики и фармакодинамики инсулина, доставляемого в легкое человека. В большинстве известных случаев инсулин рассеивали из водного препарата. Однако в начале 1990-х годов было проведено исследование эффекта легочного введения инсулина в форме сухого порошка. Было продемонстрировано, что системная доставка сухого инсулинового порошка может быть выполнена пероральной ингаляцией и что порошок может быстро всасываться через альвеолярные области легких. Например, в US 5997848 продемонстрировано, что системная доставка сухого инсулинового порошка достигается пероральной ингаляцией и что порошок может быстро всасываться через альвеолярные области легких. Однако обратное растворение дозы по-прежнему выглядит низким. Согласно описанию дозировки инсулина имеют общую массу от самого низкого значения 0,5 мг вплоть до 10-15 мг инсулина, и инсулин присутствует в отдельных частицах в концентрации от всего лишь 5% до 99% по массе со средним размером частиц менее 10 мкм.
Ряд факторов делает доставку PPDs в легкое в виде сухих порошков заманчивой альтернативой. PPDs подвержены деструкции различными путями, в том числе деаминированием, гидролизом и окислением. Поэтому достичь приемлемой стабильности фармацевтического продукта во многих случаях может быть трудной задачей. С точки зрения стабильности, твердый препарат, который хранят в сухих условиях, обычно является наилучшим вариантом. В твердом состоянии молекулы обычно относительно стабильны в отсутствие влаги или повышенной температуры. Белки и пептиды средней молекулярной массы растворимы в слое жидкости глубоко в легком и, следовательно, растворяются, обеспечивая быстрое всасывание из легкого.
Что касается представления дозы, то в продаже имеются сухие порошковые системы двух основных классов - типа резервуара, где порошок находится в ингаляторе в виде массы сыпучего материала, и типа разовых доз, где порошок предварительно отмерен в разовые дозы. В первом случае доза отмеряется пациентом с использованием устройства, а во втором случае доза отмерена и заключена производителем в, например, желатиновые капсулы или Al-блистер.
Конкретным случаем предварительно отмеренных доз являются электростатически или электродинамически изготовленные дозы (смотри патенты авторов настоящего изобретения US 6089227, SE 9802648-7, SE 9802649-5 и SE 0003082-5; смотри также US 6063194, US 5714007, US 6007630 и WO 00/22722). Конфигурация изготовленной этим способом дозы может быть специализирована для конкретного применения. Кроме того, имеются также большие возможности для изготовления порошков с заданной внутренней структурой, такой как пористость, которая будет влиять на адгезионные силы между частицами.
Было предложено большое количество различных решений для дезагрегирования лекарственного порошка в DPI. Одним из примеров является использование спейсера, принцип действия которого основан на рассеивании частиц, равномерно распределенных в контейнере, из которого можно делать ингаляцию. В принципе, ингалятор соединен с контейнером, который имеет относительно большой объем и в который инжектируется распыленный порошок. При ингаляции из спейсера распыленный порошок эффективно достигает альвеолей. Этот способ в принципе имеет два недостатка: во-первых, трудности в контролировании количества лекарства, поступающего в легкое, так как неконтролируемое количество порошка прилипает к стенкам спейсера, и, во-вторых, трудности в эксплуатации этого относительно объемистого аппарата.
Внешние источники энергии в дополнение к энергии вдоха, который делает пользователь во время ингаляции, являются обычными в данной области средствами для улучшения технических характеристик ингалятора с точки зрения дезагрегации. Некоторые производители используют электрические пропеллеры, пьезо-вибраторы и/или механическую вибрацию для дезагрегации агломератов. Добавление внешних источников энергии усложняет и удорожает ингаляторы более чем это необходимо, а также повышает возлагаемые на пользователя требования по эксплуатации ингалятора.
Следовательно, имеется потребность в подходящих терапевтических препаратах лекарственных веществ и в способе и системе для обеспечения высокоэффективного дезагрегирования и рассеивания в воздух лекарственного порошка для введения пользователю, вдыхающему его через ингаляторное устройство нового типа.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Согласно изобретению предложен ингалятор (8) сухого порошка, содержащий:
сопло (1), имеющее входное отверстие и выходное отверстие,
подложку (140, 141), причем сопло (1) и подложка (140, 141) выполнены с возможностью перемещения друг относительно друга при всасывании воздуха через выходное отверстие сопла,
дозу лекарственного порошка (180), нанесенную на подложку (140, 141) и имеющую распределение частиц по аэродинамическим размерам, подходящее для терапевтического применения, и регулируемую пористость, отличающийся тем, что
сопло (1) выполнено с возможностью создания локальной высокоскоростной турбулентной воздушной струи, поступающей во входное отверстие сопла, выходящей через его выходное отверстие при всасывании воздуха и одновременном относительном перемещении сопла (1) и подложки (140, 141) и пересекающей при указанном относительном перемещении дозу лекарственного порошка (180), подвергая постепенно указанную дозу воздействию срезающих напряжений и силы инерции указанной воздушной струи и обеспечивая тем самым дезагрегирование и рассеивание в воздух агрегатов частиц внутри указанной дозы (180).
Согласно одному воплощению изобретения предложен ингалятор, в котором указанная доза лекарственного порошка (180) содержит инсулин в качестве фармакологически активного вещества.
Согласно еще одному воплощению изобретения предложен ингалятор, в котором указанная доза лекарственного порошка (180) содержит белок в качестве фармакологически активного вещества.
Согласно еще одному воплощению изобретения предложен ингалятор, в котором указанная доза лекарственного порошка (180) содержит пептид в качестве фармакологически активного вещества.
Согласно еще одному воплощению изобретения предложен ингалятор, в котором указанная доза лекарственного порошка (180) содержит ингибитор альфа-1-протеиназы, интерлейкин-1, паратиреоидный гормон, генотропин, колониестимулирующие факторы, эритропоэтин, интерфероны, кальцитонин, фактор VIII, альфа-1-антитрипсин, фолликулостимулирующие гормоны, агонист LHRH (рилизинг-фактор лютеинизирующего гормона) или IGF-1 (инсулиноподобный фактор роста I) в качестве фармакологически активного вещества.
Согласно еще одному воплощению изобретения предложен ингалятор, в котором указанная доза лекарственного порошка (180) содержит фармакологически активное вещество, оказывающее системное действие.
Согласно еще одному воплощению изобретения предложен ингалятор, в котором указанная доза лекарственного порошка (180) содержит фармакологически активное вещество, оказывающее местное действие в легких пользователя.
В отличие от предшествующего уровня техники настоящее изобретение не требует других источников энергии, кроме энергии от усилия вдоха, производимого пользователем, для достижения очень высокой степени дезагрегирования и эффективного рассеивания в воздух дозы сухого порошка.
Для того чтобы достичь очень высокой степени дезагрегирования и рассеивания в воздух дозы, когда она предоставляется и высвобождается пользователю, делающему ингаляцию через ингалятор нового типа, порошок в этой дозе должен иметь соответствующую пористость. Порошковый препарат, используемый в процессе формирования дозы, также должен иметь распределение частиц по их аэродинамическим размерам, подходящее для намеченного терапевтического применения. Порошок предпочтительно дозируют способами с использованием электростатического или электродинамического поля или их комбинации, но равновозможны и другие способы формирования дозы. Предпочтительно в процессе формирования дозы получают вытянутую дозу заданного размера и контура, а также с соответствующими пористостью и межчастичными адгезионными силами.
Дезагрегирование и рассеивание в воздух порошка в дозе обеспечивается методом срезания порошка потоком воздуха (a powder Air-razor method), который реализован в ингаляторном устройстве нового типа. Под действием силы, с которой пользователь всасывает воздух через ингалятор, воздух проходит через сопло, частицы в порошковой дозе становятся доступными соплу и постепенно дезагрегируются и рассеиваются в поток воздуха, поступающего в сопло. Постепенное дезагрегирование и рассеивание происходит в результате относительного движения сопла и вытянутой дозы. В предпочтительном воплощении порошок наносят на подложку, причем аккумулированный порошок вытянутой дозы обычно занимает участок большей площади, чем площадь входного отверстия сопла. Вначале сопло предпочтительно расположено за пределами занимаемого порошком участка, причем порошок не имеет доступа к соплу за счет относительного движения до тех пор, пока поток воздуха в сопло, созданный всасыванием, не пройдет пороговую скорость течения. Одновременно с всасыванием, производимым пользователем, или сразу после него начинается относительное движение таким образом, что сопло постепенно проходит участок порошковой дозы. Высокая скорость вхождения воздуха во входное отверстие сопла обеспечивает большое срезывающее усилие, турбулентность и инерцию, когда протекающий воздух сталкивается с первой выдающейся точкой границы контура участка вытянутой дозы. В результате, частицы в агрегатах частиц порошка, прилегающего к входному отверстию движущегося сопла, высвобождаются, дезагрегируются до очень высокой степени и рассеиваются, а затем увлекаются созданным потоком воздуха, проходящим через сопло и далее в дыхательные пути пользователя.
Предпочтительный способ введения лекарственной дозы терапевтического сухого порошка, содержащей по меньшей мере одно тонкоизмельченное фармакологически активное лекарственное вещество, пользователю, делающему ингаляцию через ингалятор нового типа, зависит от выбора сухого порошкового препарата, обеспечивающего подходящее распределение частиц по их аэродинамическим размерам. Кроме того, для достижения оптимальных результатов доставки пользователю дозу предпочтительно формируют таким образом, чтобы она имела вытянутый контур, подходящую пористость и дозирующие качества для использования в ингаляторе, реализующем устройство срезания порошка потоком воздуха. Тогда результатом будет доставка дозы в намеченное место действия в дыхательных путях пользователя, отличающаяся непрерывной доставкой дозы с очень высокой степенью дезагрегирования частиц, в силу чего большая часть доставляемой дозы, по массе, будет состоять из тонкодисперсных частиц.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Данное изобретение вместе с дополнительными объектами и их преимуществами можно лучше понять, обратившись к следующему ниже подробному описанию в совокупности с прилагаемыми графическими материалами, в которых
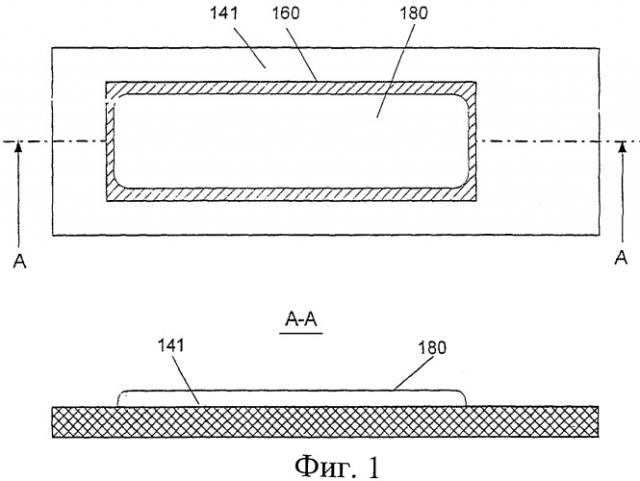
Фиг.1 иллюстрирует виды сверху и сбоку отмеренной дозы, сформированной в виде полосы на намеченном участке неперфорированной подложки;
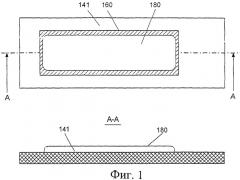
Фиг.2 иллюстрирует виды сверху и сбоку другой отмеренной дозы, сформированной в виде полосы на намеченном участке неперфорированной подложки;
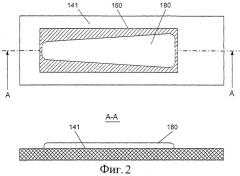
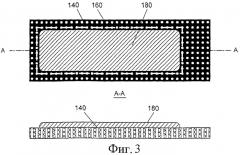
Фиг.3 иллюстрирует виды сверху и сбоку отмеренной дозы, сформированной в виде полосы на намеченном участке перфорированной подложки;
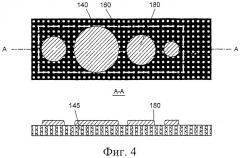
Фиг.4 иллюстрирует виды сверху и сбоку другой отмеренной дозы, сформированной в виде пятен на намеченном участке перфорированной подложки;
Фиг.5 иллюстрирует виды сверху и сбоку другой отмеренной дозы, сформированной в виде полосы на намеченном участке перфорированной подложки;
Фиг.6 иллюстрирует виды сверху и сбоку отмеренной дозы, сформированной в виде состоящей из двух частей дозы на намеченном участке, по одной части на каждой стороне перфорированной подложки;
Фиг.7 иллюстрирует дозировочный элемент в форме цилиндра с продольными канавками для множества доз;
Фиг.8 иллюстрирует дозировочный элемент в форме цилиндра с кольцевыми канавками для множества доз;
Фиг.9 иллюстрирует дозировочный элемент в форме диска с радиально расположенными канавками для множества доз;
Фиг.10 иллюстрирует дозировочный элемент в форме листа с круглыми лунками для множества доз;
Фиг.11а иллюстрирует вид в разрезе образца дозы на поверхности неперфорированной подложки и расположенного рядом с той же стороны, что и доза, сопла в стартовой позиции перед высвобождением дозы;
Фиг.11b иллюстрирует вид в разрезе образца дозы на поверхности неперфорированной подложки и расположенного рядом с той же стороны, что и доза, движущегося сопла, всасывающего частицы порошка, распыляемого в воздушный поток;
Фиг.12а иллюстрирует вид в разрезе образца отмеренной дозы, сформированной в виде состоящей их двух частей дозы, по одной части на каждой стороне перфорированной подложки, и расположенного рядом с первой стороны подложки сопла в стартовой позиции перед высвобождением дозы;
Фиг.12b иллюстрирует вид в разрезе образца отмеренной дозы, сформированной в виде состоящей из двух частей дозы, по одной части на каждой стороне перфорированной подложки, и расположенного рядом с первой стороны подложки движущегося сопла, всасывающего с обеих сторон частицы порошка, рассеиваемые в воздушный поток;
Фиг.13 иллюстрирует непористую неперфорированную подложку с порошковой дозой на ней и сопло с эллиптическим входным отверстием, расположенное рядом с той же стороны подложки, что и доза;
Фиг.14 иллюстрирует вид сбоку непористой неперфорированной подложки с порошковой дозой на ней и сопла, всасывающего по линии движения частицы порошка и рассеивающего их в воздушный поток;
Фиг.15 иллюстрирует воплощение метода срезания порошка потоком воздуха, показывающее сопло и дозировочный элемент в относительном движении друг к другу в процессе высвобождения порошковой дозы;
Фиг.16 иллюстрирует воплощение ингалятора, сконструированного для применения метода срезания порошка потоком воздуха;
Фиг.17 иллюстрирует разные силы, действующие на стационарную частицу, находящуюся в потоке воздуха; и
Фиг.18 иллюстрирует на блок-схеме основные стадии способа доставки дозы.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение раскрывает дозу терапевтического сухого порошкового препарата в виде приготовленного заранее лекарственного порошка для ингаляции, который в высокой степени дезагрегируется и увлекается во вдыхаемый воздух при использовании метода срезания порошка потоком воздуха для дезагрегирования и рассеивания частиц порошка в воздух.
Лекарственный порошок содержит одно или более фармакологически активных веществ, таких как белки или пептиды, и возможно один или более эксципиентов. В этом документе термины «порошок» или «лекарственный порошок» использованы для обозначения вещества в форме сухого порошка, который является объектом дезагрегирования и рассеивания в воздух и предназначен для осаждения на выбранной намеченной области, месте действия, дыхательных путей пользователя. Возможные эксципиенты могут подвергаться или не подвергаться дезагрегированию таким же образом, как и активное фармакологическое вещество, в зависимости от модели порошка. Например, упорядоченная смесь содержит эксципиент, характеризующийся частицами, которые значительно больше частиц фармакологически активного вещества. Дополнительными примерами фармакологически активных веществ в сухих порошковых препаратах, которые представляют интерес для введения ингаляцией, являются следующие: кетобемидон, фентанил, бупренорфин, гидроморфон, ондансетрон, гранисетрон, трописетрон, скополамин, наратриптан, золмитриптан, алмотриптан, дигидроэрготамин, соматропин, кальцитонин, эритропоэтин, фоликкулостимулирующий гормон (FSH), инсулин, интерфероны (альфа и бета), паратиреоидный гормон, альфа-1-антитрипсин, агонист LHRH.
Обратимся к Фиг.1-18 графических материалов, где одинаковыми цифрами обозначены одинаковые элементы на нескольких видах. Шесть различных воплощений доз на подложке показаны на Фиг.1-6 в качестве примеров. Каждая из Фиг.1 и 2 иллюстрирует непористую неперфорированную подложку 141 с выбранным отмеченным участком для дозы 160, на которую нанесена основная вытянутая доза порошка 180 в форме полосы, при этом доза имеет случайный контур, подходящий для данного применения. Фиг.3-6 иллюстрируют воплощения, аналогичные воплощению на Фиг.1, но вместо неперфорированной подложки 141 показана перфорированная подложка 140. Характерное различие между перфорированной или пористой подложкой 140, с одной стороны, и непористой или неперфорированной подложкой 141, с другой стороны, заключается в том, что первая пропускает воздух через подложку, включая намеченный участок дозы 160, а последняя - не пропускает воздух. Выбор типа подложки зависит от применения и от выбранного ингаляторного устройства. Проиллюстрированные дозы имеют вытянутые контуры в форме полосы за исключением Фиг.4, которая иллюстрирует вытянутую дозу, сформированную в виде серии последовательных пятен одинаковых или разных размеров. Подложка (несущий элемент) для доз 140, 141 при необходимости может быть изогнута, например, для того, чтобы поместить большой участок дозы в отведенное для этого небольшое пространство дозировочного элемента. Различные типы дозировочных элементов 10, каждый из которых способен вмещать множество доз, представлены на Фиг.7-10. Метод срезания порошка потоком воздуха проиллюстрирован на Фиг.11а, 11b-14, где различные воплощения вытянутых доз 180 соединены с различными подложками 140, 141. Эти графические материалы иллюстрируют, каким образом относительное движение v дозы и сопла 1 дает возможность срезывающим силам воздушного потока, входящего во входное отверстие сопла, постепенно дезагрегировать и рассеивать частицы порошка 101 в воздух 20. Фиг.15 иллюстрирует воплощение метода срезания порошка потоком воздуха, реализованного в ингаляторе нового типа, проиллюстрированного также на Фиг.16.
В предпочтительном воплощении, приведенном в качестве примера на Фиг.11а и 11b, метод срезания порошка потоком воздуха для порошков включает введение регулируемого относительного движения вытянутой дозы порошка 180, такого как инсулин, нанесенного на подложку 141, использованную в качестве несущего элемента для дозы, и соответствующим образом установленного сопла 1, которое собирает и направляет локальный высокоскоростной поток воздуха 20. При наведении входного отверстия сопла на массу порошка на подложке энергия воздушного потока, являющаяся результатом всасывающего усилия, дезагрегирует и рассеивает в воздух частицы 101 доступного порошка, находящегося на подложке. По мере движения сопла по направлению вытянутого контура нанесенного порошка дозы первичные частицы и агрегаты частиц постепенно становятся доступными и подвергаются воздействию срезающей силы и силы инерции потока воздуха, движущегося в сопло. Таким образом, в результате срезания потоком воздуха отдельные частицы постепенно дезагрегируются, высвобождаются, рассеиваются и увлекаются в воздух, поступающий в сопло. Тем не менее, конечный лечебный эффект во многом зависит от порошкового препарата и характеристик первоначальных частиц. Для достижения оптимального лечебного эффекта необходимо, чтобы первоначальные частицы были определенного среднего размера и имели определенное распределение по размерам и были полностью дезагрегированными при доставке. Только тогда большая доля доставляемой дозы будет оседать в намеченной области воздушных путей пользователя, то есть в месте лечебного действия. Доставку можно осуществлять назальным или пероральным введением в зависимости от того, какой тип ингаляторного устройства используется.
Степень агрегации частиц и пористость дозы играют важную роль в получении наилучшей тонкодисперсной фракции и достижении наилучшего рассеивания в воздух порошка по мере того, как он принудительно увлекается воздухом в результате высвобождения. Тонкоизмельченные лекарственные порошки с первоначальным размером частиц ниже 10 мкм исключительно текучие, но имеют тенденцию образовывать агрегаты. Поэтому тонкоизмельченные порошки, которые менее склонны образовывать агрегаты и/или требуют меньших затрат энергии на разрушение образовавшихся агрегатов, предпочтительны при использовании метода срезания порошка потоком воздуха. Например, для облегчения дезагрегирования и рассеивания в воздух активных веществ могут быть использованы пористые частицы или упорядоченные смеси, которые возможно могут содержать фармакологически приемлемые эксципиенты, используемые, например, для разбавления активного вещества или для улучшения одного или более свойств активного вещества, таких как биодоступность или электростатические свойства.
В отличи