Получение частично гидрированных анса-металлоценовых комплексов
Иллюстрации
Показать всеДанное изобретение относится к улучшенному способу получения гидрированных или частично гидрированных рацемических анса-металлоценовых комплексов путем введения во взаимодействие мостиковых или не мостиковых комплексов переходных металлов с соединениями щелочных металлов или соединениями щелочно-земельных металлов, нагревания полученной реакционной смеси до температуры в интервале от комнатной до 80°С и, по меньшей мере, частичного гидрирования продуктов реакции в присутствии подходящего катализатора в соответствующие гидрированные или частично гидрированные металлоцены, и к их использованию в качестве катализаторов, или в качестве компонента катализаторов полимеризации олефино-ненасыщенных соединений, или в качестве реагентов или катализаторов стереоселективного синтеза. 4 з.п. ф-лы.
Реферат
Настоящее изобретение относится к способу получения гидрированных или частично гидрированных рацемических анса-металлоценовых комплексов, к самим комплексам и их производным и к их использованию в качестве катализаторов, или компонента катализаторов полимеризации олефино-ненасыщенных соединений, или в качестве реагентов или катализаторов стереоселективного синтеза.
Помимо стереоспецифической полимеризации олефинов, энантиоселективный синтез предлагает все более интересные возможные применения хиральных металлоценовых комплексов металлов III-VI переходных групп периодической системы элементов. Как правило, в упомянутых применениях требуется использование металлоценового комплекса в форме рацемата, то есть без мезо-соединений. В случае смеси диастереомеров (рацемической и мезо-формы), получаемой обычно при синтезе металлоценов предшествующей области техники, мезо-форму необходимо отделять. Поэтому в прошлом были предприняты попытки разработать рацемоселективный синтез анса-металлоценов и были описаны соответствующие общие синтетические подходы, например, в WO 99/15538 и в DE 10030638. Данный рацемоселективный синтез анса-металлоценов протекает через промежуточное соединение бисфеноксид анса-металлоцена, или дифеноксид анса-металлоцена.
Гидрированные металлоцены, такие как дихлорид этилен-бис(тетрагидроинденил)циркония и дихлорид диметилсиландиил бис(тетрагидроинденил)циркония описаны в J. Am. Chem. Soc. (1996), 118, 2105, J. Mol. Katal. A. Chem. (1995), 102, 59, EPA 0643079 и JPA 07292019. Они подходят для получения полиолефинов, таких как изотактический полипропилен, сополимеров и эластомеров. Кроме того, известен ряд других гидрированных металлоценов, см. ссылку EPA 0581754, JPA 07041521. Гидрированные и частично гидрированные металлоцены были также описаны в качестве предшественников катализаторов полимеризации олефинов, см., например, ссылку EPA 0344887, ЕРА 0185918 и ЕРА 0537686. Гидрированные и частично гидрированные металлоцены обладают различной трехмерной структурой и различными полимеризационными свойствами по сравнению со своими ненасыщенными аналогами, и подобные измененные структура и свойства приводят к выгодным эффектам и возможным использованиям в конкретных применениях.
В предшествующей области техники получение гидрированных или частично гидрированных анса-металлоценов, в частности металлоценов, содержащих частично гидрированные инденильные системы в качестве лигандов, обычно проводят через получение бисинденилцирконоценовых дихлоридов, их выделение и последующее гидрирование с последующим выделением гидрированного или частично гидрированного продукта кристаллизацией (см, например, ссылку ЕР 839822 и цитированные там ссылки). Данный синтетический подход имеет ряд недостатков.
Обычно синтез анса-металлоценовых дихлоридных комплексов проводят общим способом с использованием тетрахлорида циркония в качестве источника металла: при этом анса-лиганд растворяют в толуоле, депротонируют действием сильных оснований, а затем вводят во взаимодействие с тетрахлоридом циркония, получая соответствующий дихлорид анса-металлоцена (плюс два эквивалента хлорида лития). Дихлорид анса-металлоцена, который преимущественно выпадает в осадок при образовании, отделяют от хлорида лития известными способами, а комплекс, в случае необходимости, затем очищают кристаллизацией.
У данного «классического» реакционного пути есть две существенные проблемы. Помимо желательного рацемата, в большинстве случаев в фактически эквивалентных количествах образуется зеркально-симметричный мезо-диастереомер. Кроме того, достигаемые по данной стратегии выходы смеси рац/мезо сравнительно невысоки (порядка от около 30 до 40%). Однако в случае, когда дихлорид анса-металлоцена нужно применять в качестве катализаторов полимеризации замещенных олефинов, можно использовать только рацематы (как указано выше). В рамках синтеза дихлоридов анса-металлоценов для этого часто требуется трудоемкое и невыгодное разделение рац/мезо, или даже разрушение мезо-комплекса. В результате этого конечный выход чистого дихлорида рац-анса-металлоцена обычно не превышает 15-20%.
Прочие недостатки связаны с эффективностью синтеза. Как описано выше, дихлорид анса-металлоцена нужно отделить от одновременно образующегося хлорида лития. Данная стадия часто сравнительно трудна, поскольку для отделения малорастворимого (в частности, в толуоле) дихлорида анса-металлоцена от также фактически нерастворимого (в толуоле) хлорида лития требуются большие количества растворителя и, следовательно, ограничиваются производительность и эффективность данного синтетического подхода.
Более того, вследствие малой растворимости дихлорида анса-металлоцена в углеводородных растворителях, концентрации комплекса в реакции гидрирования данного комплекса в большинстве случаев относительно невысоки. Это также ограничивает производительность и эффективность данного общего синтетического подхода.
По этой причине частично гидрированные анса-металлоцены до сих пор получались только при допущении значительных потерь в выходе и условий неэкономичного синтеза.
Задача настоящего изобретения заключается во избежании недостатков предшествующей области и обеспечении простого и экономичного, но в то же время высокоэффективного способа получения гидрированных и частично гидрированных рацемических металлоценовых комплексов, которые фактически не содержат мезо-изомера (в пределах точности измерения ЯМР). Особая задача настоящего изобретения состоит в разработке рацемоселективного синтетического подхода к гидрированным и/или частично гидрированным рацемическим металлоценовым комплексам, приводящего простым и недорогим способом к конечным продуктам, которые можно выделить в чистом виде. Еще одной задачей является получение гидрированных или частично гидрированных рацемических металлоценовых комплексов, которые можно использовать либо непосредственно в качестве катализаторов, в первую очередь, для полимеризации олефинов, либо использовать после модификации, например после замещения «вспомогательного лиганда», в катализаторах, в первую очередь, для полимеризации олефинов, или которые можно использовать в качестве реагентов или катализаторов стереоселективного синтеза.
Авторами изобретения найдено, что данная задача решается при помощи способа, определенного в формуле изобретения, конечных гидрированных или частично гидрированных рацемических металлоценовых комплексов (VI) и их использования в качестве катализаторов полимеризации олефино-ненасыщенных соединений, или в качестве реагентов или катализаторов стереоселективного синтеза.
Термин «мезо-форма», «рацемат» и, следовательно, также «энантиомеры» в контексте металлоценовых комплексов известны и охарактеризованы, например, у Rheingold et al., Organometallics 11 (1992), p. 1869-1876.
В настоящей заявке термин «фактически мезо-форма» означает, что более 80%, предпочтительно, по меньшей мере, 90% соединения находится в форме рацемата, в частности, предпочтительно, по меньшей мере, 95%.
В настоящем контексте термин «гидрированный или частично гидрированный» означает, что, по меньшей мере, одна пара или большая часть пар ненасыщенных атомов углерода, то есть sp2-гибридизованных атомов углерода, присутствующих в лиганде до стадии гидрирования, гидрируются, то есть присутствуют после гидрирования в водородно-насыщенном виде, а именно в виде sp3-гибридизованных атомов углерода.
Способ настоящего изобретения получения гидрированных или частично гидрированных рацемических анса-металлоценовых комплексов включает в себя следующие стадии:+
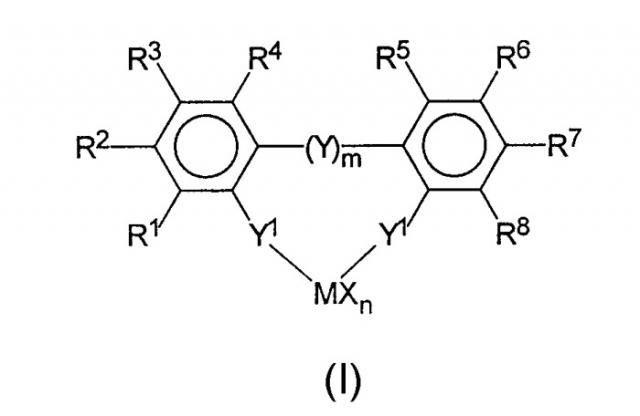
взаимодействие мостиковых или не мостиковых ароматических комплексов переходных металлов формулы I
где заместители и индексы имеют следующие значения:
М представляет собой титан, цирконий, гафний, ванадий, ниобий, тантал, хром, молибден, вольфрам, или любой элемент III переходной группы периодической системы и лантаниды;
Х являются одинаковыми или различными и каждый из них представляет собой фтор, хлор, бром, йод, водород, С1-С10-алкил, С6-С15-арил, алкиларил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, -OR10 или -NR10R11,
n является целым числом от 1 до 4 и соответствует валентности М минус 2,
R1 по R8 являются одинаковыми или различными и каждый из них представляет собой водород, галоген, С1-С20-алкил, 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильную группу в качестве заместителя, С6-С15-арил, алкиларил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, арилалкил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, где соседние радикалы от R2 по R7 могут также образовывать насыщенные, или частично ненасыщенные циклические группы, содержащие от 4 до 15 атомов углерода, Si(R9)3, -OR10, -SR10, -N(R10)2, Р(R10)2 и все вышеуказанные радикалы могут быть полностью или частично замещены гетероатомами,
R9 являются одинаковыми или различными и каждый представляет собой С1-С20-алкил, С3-С10-циклоалкил, С6-С15-арил, где упомянутые радикалы могут быть полностью или частично замещены гетероатомами,
R10 являются одинаковыми или различными и каждый представляет собой С1-С10-алкил, С6-С15-арил, С3-С10-циклоалкил, алкиларил или Si(R11)3,
R11 являются одинаковыми или различными и каждый представляет собой С1-С10-алкил, С6-С15-арил, С3-С10-циклоалкил, алкиларил,
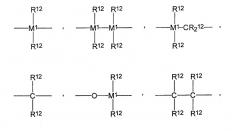
Y, Y1 являются одинаковыми или различными и каждый представляет собой
или =BR12, =AlR12, -Ge-, -Sn-, -O-, -S-, =SO, =SO2, =NR12, =CO, =PR12 или =P(O)R12, где
R12 являются одинаковыми или различными и каждый представляет собой водород, галоген, С1-С10-алкил, С1-С10-фторалкил, С6-С10-фторарил, С6-С10-арил, С1-С10-алкокси, С2-С10-алкенил, С7-С40-арилалкил, С8-С40-арилалкенил, С7-С40-алкиларил, или два радикала R12 вместе со связывающими их атомами образуют цикл,
М1 представляет собой кремний, германий или олово, а
m равен 0, 1, 2 или 3, или
Y является несвязывающим и представляет собой два радикала R' и R'', где
R' и R'' аналогичны определенным для R1 по R8, а R' и R'' вместе с соседними радикалами R4, R5 могут также образовывать насыщенные, частично насыщенные или ненасыщенные циклические группы, содержащие от 4 до 15 атомов углерода,
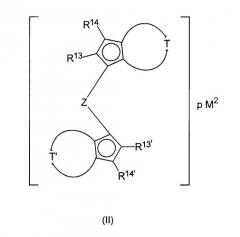
с циклопентадиенильными производными формулы II
где
представляет собой двухвалентную группу, такую как
а
представляет собой двухвалентную группу, такую как
а заместители и индексы имеют следующие значения:
R13, R13', R14, R14' являются одинаковыми или различными и каждый представляет собой водород, галоген, С1-С20-алкил, 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильную группу в качестве заместителя, С6-С15-арил, алкиларил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, арилалкил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, -OR10, -SR10, -N(R10)2, -Р(R10)2 или Si(R9)3,
Z представляет собой -[Q(R15)(R16)]q-группу, в которой
Q могут быть одинаковыми или различными и каждый представляет собой кремний, германий, олово или углерод,
R15, R16, каждый, представляет собой водород, С1-С10-алкил, С3-С8-циклоалкил или С6-С15-арил, а
q равен 1, 2, 3 или 4,
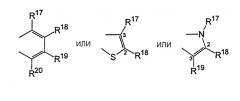
R17-R20, R17'-R20' являются одинаковыми или различными и каждый представляет собой водород, С1-С20-алкил, 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильную группу в качестве заместителя, С6-С15-арил или арилалкил, где соседние радикалы могут совместно образовывать циклические группы, содержащие от 4 до 15 атомов углерода, или Si(R11)3, и
М2 представляет собой ион щелочного металла или ион щелочно-земельного металла, а
р равен 1, если М2 представляет собой ион щелочно-земельного металла, и 2, если М2 представляет собой ион щелочного металла;
и нагревание полученной реакционной смеси до температуры в интервале от минус 78°С до 250°С с добавлением или без добавления свободных радикалов или источников свободных радикалов с получением комплекса формулы III
и, по меньшей мере, частичное гидрирования III при действии водорода в присутствии подходящего катализатора.
К удивлению, было найдено, что рацемоселективный синтез гидрированных или частично гидрированных металлоценовых комплексов можно успешно осуществить при получении комплексов переходных металлов формулы I, предпочтительно, без выделения промежуточных соединений, из соответствующих мостиковых лигандов дифеноксидного типа, или не мостиковых лигандов бисфеноксидного типа, реакцией с галогенидами переходных металлов способом, который известен как таковой, при этом данные комплексы вводят во взаимодействие с циклопентадиенильными производными формулы II, получая дифеноксид- или бисфеноксидзамещенные металлоцены, содержащие ароматические бисинденильные лиганды, или их гетероатомсодержащие аналоги, формулы III, которые затем каталитически гидрируют в реакционной смеси. Было найдено, что данный реакционный подход приводит рацемоселективно и с высокими выходами к соответствующим гидрированным или частично гидрированным, рацемическим дифеноксид- или бисфеноксидзамещенным анса-металлоценам. Таким образом избегают снижающего выход, сложного разделения диастереомеров.
Гидрированные или частично гидрированные рацемические дифеноксид- или бисфеноксидзамещенные анса-металлоцены можно использовать в качестве катализаторов либо непосредственно, либо после превращения в соответствующие частично гидрированные анса-металлоценовые дихлоридные комплексы за счет замещения феноксидных лигандов. Поскольку, в отличие от соответствующих гидрированных или частично гидрированных анса-металлоценовых дихлоридных комплексов, дифеноксид- или бисфеноксидзамещенные анса-металлоцены сравнительно легко растворимы в органических растворителях, их отделение от LiCl, или других солей, или катализатора гидрирования, значительно проще. Более того, синтез можно проводить в растворах высокой концентрации, что дополнительно повышает экономичность данного реакционного подхода.
В способе настоящего изобретения предпочтение отдают использованию мостиковых или не мостиковых ароматических комплексов с переходными металлами формулы I,
которые получают способом, известным как таковой, из соединений формулы IV
депротонированием при действии подходящих депротонирующих агентов и последующей реакцией депротонированных соединений с подходящим соединением переходного металла формулы V
MX4(основание Льюиса)k, (V)
где k равен 0, 1 или 2, причем заместители и индексы в формулах (I), (V) и (IV) имеют следующие значения:
М представляет собой титан, цирконий, гафний, в частности, цирконий; а
Х являются одинаковыми или различными и каждый представляет собой фтор, хлор, бром, йод, предпочтительно, хлор, или С1-С6-алкил, такой как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изо-бутил, предпочтительно, трет-бутил, или алкоксид -OR9, или амид -N(R9)2, где R9 являются одинаковыми или различными и каждый предпочтительно представляет собой С1-С10-алкил, С6-С15-арил, алкиларил, арилалкил, фторалкил, или фторарил, каждый из которых содержит от 1 до 10 атомов углерода в алкильном радикале и от 6 до 20 атомов углерода в арильном радикале, например метил, этил, изо-пропил, трет-бутил, фенил, нафтил, п-толил, бензил, трифторметил, пентафторфенил.
Заместители от R1 по R8 являются одинаковыми или различными и каждый из них предпочтительно представляет собой водород, фтор, хлор, бром, йод, С1-С20-алкил, -OR10, -SR10, -N(R10)2, -Р(R10)2 или Si(R9)3, где R9 и R10 являются одинаковыми или различными и каждый из них представляет собой С1-С10-алкил, С6-С15-арил, С3-С10-циклоалкил, алкиларил.
Кроме того, каждый из заместителей от R1 по R8 может представлять собой 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильный радикал, такой как метил, этил или пропил, в качестве заместителя. Примерами подобных циклоалкильных радикалов являются циклопропил, циклопентил, предпочтительно, циклогексил, норборнил. В конкретных вариантах осуществления от R1 по R8 могут также представлять собой С6-С15-арил, такой как фенил или нафтил, или алкиларил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, например, п-толил; арилалкил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, например бензил, неофил; или триорганосилил, такой как Si(R9)3, где R9 являются одинаковыми или различными и каждый из них представляет собой С1-С20-алкил, С3-С10-циклоалкил, С6-С15-арил, например триметилсилил, трет-бутилдиметилсилил, трифенилсилил. Конечно, упомянутые радикалы могут быть частично или полностью замещены гетероатомами, например S-, N-, O-, или галогенсодержащими структурными элементами. Примерами подобных замещающих радикалов от R1 по R8 являются трифторметильная, пентафторэтильная, гептафторпропильная, гептафторизопропильная и пентафторфенильная группы.
Предпочтительными заместителями R1 и R8 для мостикового Y и R1, R', R'' и R8 для не мостикового Y являются, независимо друг от друга, С1-С10-алкильные группы, такие как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил, предпочтительно, просто метил. Особое предпочтение отдают случаю, когда все заместители R1, R', R'' и R8 для не мостикового Y являются одинаковыми и каждый из них представляет собой метил и когда заместители R1 и R8 для мостикового Y являются одинаковыми и каждый из них представляет собой трет-бутильные группы.
В предпочтительных вариантах осуществления все R1, R', R'' и R8 для не мостикового Y являются метилами, при этом особенно предпочтительно, чтобы Y1 представлял собой -О-, то есть в формуле (IV) в качестве лигандов используются 2 молекулы 2,6-диметилфенола. Кроме того, использование 2,4,6-триметилфенола и 2,4-ди-трет-бутилфенола также предпочтительно согласно настоящему изобретению.
Заместители R3 и R6 могут меняться в широких пределах с целью изменения растворимости металлоценовых комплексов (III) и (VI), полученных по способу настоящего изобретения и согласно настоящему изобретению они являются одинаковыми или различными и каждый из них предпочтительно представляет собой водород, фтор, хлор, бром, йод, предпочтительно, хлор, алкоксид -OR10, тиолат -SR10, амин -N(R10)2, -Р(R10)2, или Si(R9)3, где R9 и R10 являются одинаковыми или различными и каждый из них представляет собой С1-С10-алкил, С3-С10-циклоалкил, в частности 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильный радикал, такой как метил, этил, или пропил в качестве заместителя. Примерами подобных циклоалкильных радикалов являются циклопропил, циклопентил, предпочтительно циклогексил, норборнил. Кроме того, R9 и R10 могут также представлять собой галогензамещенные алкильные или циклоалкильные радикалы, например трифторметил, пентафторэтил, гептафторпропил или гептафторизопропил.
Специалист в данной области техники выберет алкильные, циклоалкильные или ароматические заместители R3 и R6 для повышения растворимости металлоценовых комплексов в неполярных растворителях и выберет полярные заместители R3 и R6, например галоген, алкоксид, тиолат, амин и так далее, для уменьшения растворимости данных комплексов в неполярных растворителях.
В последнем случае R3 и R6 предпочтительно представляют собой атомы галогена, такие как хлор, или бром, алкоксиды -OR10, тиолаты -SR10, или амины -N(R10)2, где R10 представляет собой метил, этил, н-пропил, изопропил, трет-бутил, циклопропил, циклопентил, циклогексил, норборнил.
Особое предпочтение отдают случаю, когда R9 представляет собой метил. R3 и R6 в формуле (I) особенно предпочтительно представляют собой хлор, бром, метокси, этокси, изопропилокси, трет-бутилокси, циклопропилокси, или циклогексилокси.
Варьирование заместителей R3 и R6 в широком интервале не оказывает неблагоприятного эффекта на рацемоселективность синтеза, так что соответствующий выбор заместителей, принимая во внимание выбранные условия реакции, дает возможность повысить и улучшить выход синтеза заданным образом.
В целях настоящего изобретения все феноксиды, дифеноксиды или бисфеноксиды (или их аналогичные производные) представляют собой соединения формулы IV и их аналогичные производные, заявленные согласно настоящему изобретения, то есть как те конкретные соединения, так и лиганды, имеющие данную основную структуру, и другие элементы или группы, определенные в случае Y1 вместо фенольного атома кислорода в положении Y1.
Помимо упомянутых выше мостиков Y и Y1, предпочтительными мостиками в конкретных вариантах осуществления изобретения являются метилен -СН2-, -S-, -O-, -C(CH3)2-; особое предпочтение отдается мостикам Y1, которые являются одинаковыми и каждый из которых представляет собой кислород -О-. Кроме того, особое предпочтение отдается дифеноксидам, в которых m равен нулю, а оба Y1 являются кислородом.
В случае, когда Y является не мостиковым и представляет собой два радикала R', R'', эти радикалы предпочтительно определены, как в случае R1 по R8, включая радикалы, указанные там как предпочтительные. Кроме того, R', R'', наряду с соседними радикалами R4, R5 могут образовывать насыщенные, частично насыщенные или ненасыщенные циклические группы, содержащие от 4 до 15 атомов углерода.
Подходящие депротонирующие агенты для депротонирования (IV) представляют собой, например, н-бутиллитий, трет-бутиллитий, гидрид натрия, трет-бутилоксид калия, реагенты Гриньяра, полученные из магния, магниевые соединения, такие как ди-н-бутилмагний, (н,втор)-дибутилмагний, или другие подходящие алкильные соединения щелочно-земельных металлов или щелочных металлов.
Мостиковые или не мостиковые комплексы переходных металлов формулы (I) впоследствии вводят во взаимодействие с циклопентадиенильными производными формулы (II):
в которой заместители и индексы являются определенными выше, с использованием способов, которые обычно известны специалистам в данной области техники.
Что касается циклопентадиенильных производных формулы (II), предпочтение отдают производным, в которых
представляют собой
и в которых М2 представляет собой ион щелочного металла, или ион щелочно-земельного металла, в частности Li, Na, K, Rb, Cs, Be, Mg, Ca, Sr или Ba, где р=1 в случае Be, Mg, Ca, Sr, Ba, и р=2 в случае Li, Na, K, Rb, Cs, при этом радикалы от R17 по R20 и от R17' по R20' аналогичны определенным выше.
Было найдено, что хорошо подходящая методика является следующей, обычно осуществляемой в интервале температур от -78 до 110°С, предпочтительно первоначально примерно при 20°С, и в котором реакцию можно, при необходимости, завершить кипячением с обратным холодильником.
Сначала соединения формулы (IV) депротонируют в подходящем растворителе, или смеси растворителей, например, в толуоле, или тетрагидрофуране (ТГФ) при действии, например, гидрида натрия, или н-бутиллития, а затем добавляют соединение переходного металла, например галогенид, такой как тетрахлорид титана, тетрахлорид циркония или тетрахлорид гафния, преимущественно, в виде бис-ТГФ аддукта, или ДМЭ аддукта формулы (V). В качестве альтернативы, депротонированное соединение формулы (IV) можно добавлять к раствору соединения переходного металла. По завершении реакции продукт (I) можно, как правило, получить кристаллизацией после отделения солей. Однако предпочтение отдают использованию реакционной смеси, освобожденной от солей, для дальнейшей методики без выделения (I).
Обычно мостиковые или не мостиковые комплексы переходных металлов (I) все еще содержат от 1 до 4 эквивалентов основания Льюиса, которое, как правило, вводится синтетическим путем. Примерами таких оснований Льюиса являются простые эфиры, такие как диэтиловый эфир, или тетрагидрофуран (ТГФ), а также амины, такие как ТМЭДА. Однако возможно также получать комплексы переходных металлов (II), не содержащие оснований Льюиса, например, высушиванием при пониженном давлении или за счет выбора других растворителей для синтеза. Подобные приемы известны специалистам в данной области техники.
Комплексы переходных металлов формулы (I) вводят во взаимодействие, как описано выше для случая циклопентадиенильных производных формулы (II), при последующем нагревании полученной реакционной смеси, или без него, и в присутствии или в отсутствие свободных радикалов или источников свободных радикалов, как описано далее.
Предпочтение отдают использованию комплексов переходных металлов (I), в которых М представляет собой цирконий, а радикалы от R1 по R8 имеют описанные выше предпочтительные значения, и в которых каждый из Y1 является кислородом. Весьма подходящими комплексами являются бис(2,6-диметилфеноксид) дихлорциркония, бис(2,4,6-триметилфеноксид) дихлорциркония, бис(2,6-диметил-4-хлорфеноксид) дихлорциркония, бис(2,6-диметил-4-бромфеноксид) дихлорциркония, бис(2,6-диметил-4-метоксифеноксид) дихлорциркония, бис(2,6-диметил-4-этоксифеноксид) дихлорциркония, бис(2,6-диметил-4-трет-бутоксифеноксид) дихлорциркония, бис(2,4-ди-трет-бутилфеноксид) дихлорциркония, бис(3,5-ди-трет-бутилфеноксид) дихлорциркония, 3,3'-ди-трет-бутил-5,5'-диметокси-1,1'-ди-2-феноксид дихлорциркония, 3,3'-ди-трет-бутил-5,5'-диэтокси-1,1'-ди-2-феноксид дихлорциркония, 3,3'-ди-трет-бутил-5,5'-дипропокси-1,1'-ди-2-феноксид дихлорциркония, 3,3'-ди-трет-бутил-5,5'-диметилтио-1,1'-ди-2-феноксид дихлорциркония, 3,3'-ди-трет-бутил-5,5'-диэтилтио-1,1'-ди-2-феноксид дихлорциркония, 3,3'-ди-трет-бутил-5,5'-дипропилтио-1,1'-ди-2-феноксид дихлорциркония, их аддукты с растворителями и соединения бисфеноксида циркония и дифеноксида циркония, упомянутые в примерах.
В соответствии с настоящим изобретением реакция соединений формулы (I) с циклопентадиенильными производными формулы (II) в способе настоящего изобретения первоначально приводит известными образом к комплексам переходных металлов формулы (III)
в которой все заместители аналогичны определенным выше, включая предпочтительные заместители.
На следующей стадии способа комплексы формулы (III), по меньшей мере, частично гидрируют в присутствии подходящего катализатора, получая гидрированные или частично гидрированные рацемические анса-металлоценовые комплексы формулы (VI):
в которой все заместители и индексы имеют определенные выше значения, в частности предпочтительные значения, а
представляет собой двухвалентную группу, такую как
а
представляет собой двухвалентную группу, такую как
в которой
R13, R13', R14, R14' являются одинаковыми или различными и каждый представляет собой водород, галоген, С1-С20-алкил, 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильную группу в качестве заместителя, С6-С15-арил, алкиларил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, арилалкил, содержащий от 1 до 10 атомов углерода в алкильной части и от 6 до 20 атомов углерода в арильной части, -OR10, -SR10, -N(R10)2, -Р(R10)2 или Si(R9)3, и
Z представляет собой -[Q(R15)(R16)]q- группу, в которой
Q может быть одинаковой или различной и представляет собой кремний, германий, олово или углерод,
каждый из R15, R16 представляет собой водород, С1-С10-алкил, С3-С10-циклоалкил или С6-С15-арил, а
q равен 1, 2, 3 или 4;
R17-R20, R17'-R20' являются одинаковыми или различными и каждый представляет собой водород, С1-С20-алкил, 3-8-членный циклоалкил, который, в свою очередь, может содержать С1-С10-алкильную группу в качестве заместителя, С6-С15-арил, или алкиларил, где соседние радикалы могут, кроме того, совместно образовывать циклические группы, содержащие от 4 до 15 атомов углерода, или Si(R11)3.
Особенное предпочтение отдается
представляющим собой
где R17-R20, R17'-R20' являются одинаковыми или различными и каждый предпочтительно представляет собой водород, С1-С10-алкил, где соседние радикалы могут, кроме того, совместно образовывать циклические группы, содержащие от 4 до 15 атомов углерода.
Гидрирование можно проводить в присутствии гомогенного или гетерогенного катализатора, предпочтительно гетерогенного катализатора. Подходящими катализаторами являются Pt, Pd, Rh, Ru, Os, а также никель, никель Ренея, их оксиды, соли или комплексы, их смеси, при желании, на подходящих носителях катализаторов. Особенное предпочтение отдается проведению гидрирования в присутствии гетерогенных палладиевых катализаторов, в частности палладия на угле или на активированном угле.
Дополнительные примеры катализаторов гидрирования, подходящих для целей настоящего изобретения, представляют собой палладий на сульфате бария, палладий на оксиде алюминия, палладиевую чернь, губчатый палладий, оксид платины, платиновую чернь, губчатую платину, диоксид платины и так далее.
В принципе, подходящими катализаторами гидрирования являются такие соединения или элементы, которые не гидрируют или лишь частично гидрируют растворитель в используемых условиях гидрирования.
Каталитическое гидрирование предпочтительно проводят в интервале температуры от 0°С до 150°С, в частности в интервале от 15°С до 100°С. Используемые в реакции растворители являются подходящими устойчивыми к гидрированию растворителями, в особенности предпочтительно, не содержащими галогена растворителями. Растворители, подходящие для данной цели, представляют собой ароматические растворители, такие как бензол, толуол, ксилол (в виде смеси изомеров), о-ксилол, м-ксилол, п-ксилол, мезитилен, тетралин, анизол, кумол, 1,2-диэтилбензол, 1,3-диэтилбензол, 1,4-диэтилбензол, 1-этил-2-метилбензол, 1-этил-3-метилбензол, 1-этил-4-метилбензол. Предпочтение отдается анизолу, толуолу, бензолу, ксилолам (в виде смеси чистых соединений) и тетралину.
Кроме того, подходящими растворителями являются ароматические или алифатические простые эфиры, такие как анизол, этилфениловый эфир, изопропилфениловый эфир, диэтиловый эфир, ди-н-бутиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, диоксан и диметоксиэтан (ДМЭ). Можно также использовать сложные эфиры алифатических или ароматических карбоновых кислот, например этилацетат или пропилбутират.
Кроме того, можно также использовать галогенсодержащие растворители, такие как хлористый метилен. Однако предпочтение отдается использованию не содержащих галогена растворителям, поскольку использование галогенсодержащих растворителей в сравнительно больших количествах возможно лишь в случае следования строгим мерам безопасности и защиты окружающей среды. Кроме того, если нужно избежать реакций галогенирования, в хлорированных растворителях можно использовать только катализаторы гидрирования, обладающие низкой активностью, например платиновую чернь или диоксид платины. Реакции галогенирования приводят к разложению продукта и коррозионным проблемам в используемых аппаратах.
Гетерогенно катализируемое гидрирование в способе настоящего изобретения обычно проводят в соответствующих сосудах высокого давления, то есть автоклавах, которые заполняют газообразным водородом (Н2) под давлением. Подходящие значения давления водорода находятся в интервале до 100 бар, предпочтительно, до 30 бар, особенно предпочтительно до 20 бар.
Рацемические металлоценовые комплексы формулы (VI), которые гидрировали или частично гидрировали в соответствии с настоящим изобретением, можно использовать либо непосредственно в качестве катализаторов или в качестве компонентов катализаторов для полимеризации олефиноненасыщенных соединения, либо в качестве реагентов или катализаторов стереоселективного синтеза, или обычно можно дополнительно модифицировать.
В частности, один или два феноксидных лиганда, или единственный дифеноксидный лиганд в комплексе (VI), например, можно заменить путем замещения перед дальнейшим использованием. Подходящим способом замещения является реакция рацемических металлоценовых комплексов формулы (VI) с SOCl2, четыреххлористым кремнием, дихлоридом метилалюминия, хлоридом диметилалюминия, треххлористым алюминием, диалкилалюминийхлоридами, полуторными хлоридами алюминия, в особенности предпочтительно, дихлоридом этилалюминия, или кислотой Бренстеда, такой как галогеноводород, то есть HF, HBr, HI, предпочтительно HCl, который обычно используют как таковой или в виде раствора в воде, или любом органическом растворителе, таком как диэтиловый эфир, или ТГФ. Хорошо подходящими растворителями являются алифатические углеводороды, такие как пентан, гексан, гептан, ароматические углеводороды, такие как толуол, орто-, мета- или параксилол, или изопропилбензол (кумол), простые эфиры, такие как тетрагидрофуран (ТГФ), диэтиловый эфир, метил-трет-бутиловый эфир, или диметоксиэтан (ДМЭ), амины, такие как диизопропиламин, тетраметилэтандиамин (ТМЭДА), или пиридин.
Кроме того, подходят содержащие основание Льюиса смеси растворителей, включающие в себя углеводороды и простые эфиры, или амины, или и то, и другое, например смеси толуола и ТГФ, толуола и ДМЭ, или толуола и ТМЭДА, при этом основание Льюиса обычно присутствует в количестве 0,01-50 мол.%, предпочтительно 0,1-10 мол.%, из расчета на смесь растворителей. Особенно подходящими замещающими реагентами являются галогенангидриды карбоновых кислот, такие как ацетилхлорид, фенилацетилхлорид, 2-тиофенацилхлорид, трихлорацетилхлорид, триметилацетилхлорид, О-ацетилманделилхлорид, хлорангидрид 1,3,5-бензолтрикарбоновой кислоты, хлорангидрид 2,6-пиридинкарбоновой кислоты, трет-бутилацетилхлорид, хлорацетил