Синтез гидрида кальция в процессе электролиза водного раствора гидроксида кальция
Иллюстрации
Показать всеИзобретение относится к химии гидридов металлов и может быть использовано, например, для аккумулирования водорода в химически связанном состоянии. Гидроксид кальция, помещенный в реактор, нагревают до температуры 860°С за счет пропускания по трубам, размещенным во внутреннем объеме реактора, теплоносителя, являющегося продуктом окисления водорода кислородом в водородной горелке, температура водородного факела на выходе из которой достигает 2600°С, производят многократное впрыскивание в реактор через форсунки воды, нагретой в камере с водородной горелкой до температуры не менее 860°С, с образованием высокотемпературного водяного пара, подключают к источнику постоянного электрического тока клеммы катода, функцию которого выполняют стенки реактора, и клеммы анода, функцию которого выполняет твердооксидная сплошная пленка, нанесенная на заглушенную снизу полую трубу с множеством сквозных отверстий в стенках, предназначенных для выхода во внутреннюю полость трубы кислорода, абсорбированного твердооксидной пленкой, и осуществляют высокотемпературный электролиз водного раствора гидроксида кальция с образованием гидрида кальция у внутренних поверхностей стенок реактора. Способ позволяет синтезировать гидрид кальция в качестве надежного и безопасного хранилища химически связанного водорода. 1 ил.
Реферат
Изобретение относится к химии гидридов металлов, в частности к способам их получения методом прямого взаимодействия водорода с атомами металлов, и может быть использовано, например, для аккумулирования водорода в химически связанном состоянии.
УРОВЕНЬ ТЕХНИКИ
Известен способ получения гидридов путем гидрирования металлов при высоких температурах в атмосфере водорода в течение 1-12 часов (1).
Известны аккумуляторы водорода с капсулами, заполненными порошкообразным металлом, который способен поглощать и отдавать водород (2). Известен способ получения гидридов переходных металлов, в частности гидрида титана (3), который включает: прессование порошка титана дисперсностью 0,5-1,5 мм в виде таблеток, размещение их в герметичном водоохлаждаемом реакторе; вакуумирование реактора до достижения давления в 1 Па; заполнение реактора водородом до давления 1-5 атм. (0,1-0,5 МПа); локальное инициирование горения с помощью вольфрамовой проволоки, находящейся в контакте с металлом; развитие самораспространяющегося высокотемпературного синтеза и извлечение готового продукта. Основным недостатком способа (3) является высокая себестоимость при низкой производительности (не более 0,5 кг за один эксперимент). Кроме этого, продукт синтеза представляет собой сильно спеченный материал и требует дополнительного длительного помола для его измельчения. Для длительного хранения водорода в химически связанном состоянии разработан способ приготовления гидрида ванадия (4), по которому термическую обработку ванадия перед подачей к нему изотопов водорода проводят при 593-793 К, в процессе нагрева до температуры термической обработки и во время ее давление остаточных газов в камере поддерживают не выше 1,3 Па, и процесс взаимодействия ванадия с водородом производят при давлении от 300000 до 1000000 Па. Наиболее близким решением к заявляемому является «Электрическая печь для производства гидрида кальция» по патенту GB 176354 A (ALBIN KIESEWALTER) от 11.01.1923 года (5), в описании к которому раскрыт способ ввода водорода и оксида кальция во внутренний объем печи, где при температуре горящей электрической дуги осуществляется синтез гидрида кальция. Основным недостатком прототипа (5) является то обстоятельство, что для осуществления синтеза гидрида кальция в печь необходимо вводить не только ту массу водорода, которая требуется для гидридизации кальция, но также и дополнительную массу водорода, расходуемую на восстановление кальция из оксида кальция. Все указанные способы аккумулирования водорода путем химического связывания его в гидридах металлов требуют применения водорода и ценных металлов, при производстве которых уже осуществлены большие затраты ресурсов, а кроме этого известные технологии гидридизации металлов требуют применения сложнейшего оборудования, способного обеспечить выполнение необходимых технологических операций как при сверхнизких, так и при высоких давлениях.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
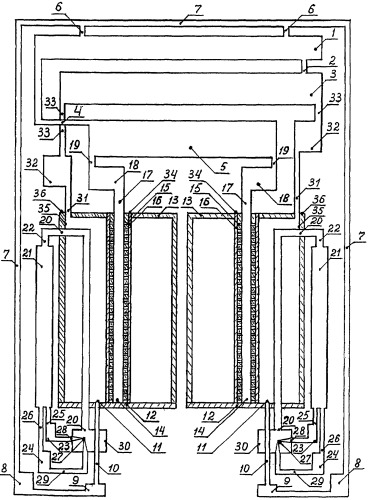
Синтез гидрида кальция в процессе электролиза водного раствора гидроксида кальция происходит в реакторе, где поддерживают высокую температуру, а самокомпримирующийся водород реагирует с кальцием. Для иллюстрации сущности процессов, в ходе которых может быть получен водород не только при электролизе водного раствора гидроксида кальция, но также и без затрат электроэнергии на осуществление электролизного процесса, на чертеже изображена блок-схема комплектов оборудования для синтеза гидрида кальция (при двух и более комплектах, в одном из них готовый гидрид кальция). Батарея топливных элементов 1 соединена трубами 2 с ресивером 3, предназначенным для хранения запаса водорода, и трубами 4 с ресивером 5, в котором должен храниться запас кислорода. Трубы 6 предназначены для отвода продуктов окисления водорода кислородом, образующихся при выработке электроэнергии в топливных элементах, в магистральный трубопровод 7, по которому эти продукты транспортируют в резервуар 8. Насос 9 предназначен для создания напора воды, которую по трубам 10 подводят к форсункам 11, размещенным в днище 12 реактора 13. На днище 12 опирается своим заглушенным концом труба 14, имеющая в стенках множество сквозных отверстий 15, предназначенных для пропуска во внутреннюю полость трубы 14 кислорода, который абсорбируется твердым электролитом 16, нанесенным на наружную поверхность трубы 14. Труба 14 за пределами реактора 13 соединена с герметичным патрубком 17, предназначенным для транспортирования кислорода из внутренней полости трубы 14 в сборник кислорода 18, с помощью которого поддерживают расчетное давление кислорода во внутренней полости трубы 14. Сборник кислорода 18 соединен трубой 19 с ресивером 5. Во внутреннем объеме реактора 13 размещены трубы 20, металлические стенки которых должны передавать тепловую энергию от теплоносителя к веществам внутри реактора. В случае использования в качестве теплоносителя водяного пара для его транспортирования в высокотемпературный электролизер 21 известной конструкции предназначены трубы 22. Для вывода образующихся продуктов электролиза: кислорода в накопитель 23, а водорода в накопитель 24 - предназначены соответственно трубы 25 и 26. Для транспортирования кислорода из накопителя 23 к водородной горелке 27 предназначены трубы 28, а для транспортирования водорода из накопителя 24 к горелке 27 предназначены трубы 29. Часть трубы с водой 10 проходит через камеру 30, внутри которой размещена водородная горелка 27. Трубы 31 предназначены для транспортирования водорода из реактора 13 в сборник водорода 32. Для транспортирования избыточного объема водорода из сборника 32 в ресивер 3 предназначены трубы 33. Для подключения к источнику постоянного электрического тока слоя твердого электролита 16, размещенного на наружной поверхности трубы 14 и являющегося анодом при осуществлении электролизного процесса в реакторе, предназначены клеммы 34, а для подключения к источнику постоянного электрического тока внутренней поверхности металлических стенок 35 реактора 13, которые являются катодом при осуществлении электролизного процесса в реакторе, предназначены клеммы 36.
Функционирование комплектов оборудования для получения водорода проиллюстрировано на примере электролиза гидроксида кальция. В процессе подготовки комплектов оборудования к работе загружают во внутреннюю полость каждого реактора 13 химически чистый гидроксид кальция и осуществляют нагрев его до температуры 860 градусов по Цельсию за счет пропуска по трубам 20 теплоносителя - водяного пара, являющегося продуктом окисления водорода кислородом в водородной горелке 27. В связи с тем, что температура водородного факела на выходе из водородной горелки 27 достигает 2600 градусов по Цельсию, водяной пар, пропущенный по трубам 20 в качестве теплоносителя, на входе в трубы 22 имеет температуру не менее 860 градусов по Цельсию и может быть использован в качестве готового электролита для высокотемпературного электролизера 21. Известные конструкции высокотемпературных электролизеров (8), которые предназначены для разделения водяного пара на водород и кислород, имеют наиболее экономичные показатели работы при вводе в них электролита в виде водяного пара при температуре 850 градусов по Цельсию. В процессе электролиза такого электролита образуется кислород и водород. Кислород из электролизера 21 транспортируют по трубам 25 в накопитель 23, а водород - по трубам 26 в накопитель 24. Для питания горелки 27 дозированные порции водорода транспортируют из накопителя 24 по трубам 29, а порции кислорода, масса которых должна быть в 8 раз больше массы каждой порции водорода, транспортируют из накопителя 23 по трубам 28. В массу гидроксида кальция, нагретую до температуры 860 градусов по Цельсию, впрыскивают расчетные порции воды через форсунки 11 для барботажа образующегося водного раствора гидроксида кальция с целью достижения однородной концентрации получаемой щелочи. В связи с тем, что воду, предназначенную для впрыскиваемая в реактор, нагревают до температуры не менее 860 градусов по Цельсию во время нахождения ее в участке трубы 10, размещенном в пределах камеры 30, внутри реактора в атмосфере высокотемпературного водяного пара происходит разрушение молекул гидроксида кальция с наименьшими затратами энергии. Молекулы гидроксида кальция диссоциируют на ионы в соответствии с законами теории электролитической диссоциации (6): положительно заряженные ионы кальция и отрицательно заряженные гидроксид-ионы. В обзоре исследований (6) приведено утверждение о том, что «...диссоциация электролита на ионы большей частью не связана с заметным выделением или поглощением тепла, поэтому небольшие изменения температуры обычно мало на ней сказываются, а диссоциация воды идет со значительным поглощением тепла: ; при нагревании степень диссоциации воды сильно увеличивается...». В описываемом реакторе дополнительную тепловую энергию, необходимую для диссоциации воды в составе щелочи, передают через стенки труб 20 за счет пропуска внутри них высокотемпературного теплоносителя в виде водяного пара. При подаче на клеммы 34 и 36 постоянного электрического тока в электропроводящей массе высокотемпературного водного раствора гидроксида кальция (щелочи) осуществляются электролизные процессы: ионы кальция движутся к поверхностям стенок 35 реактора 13, как к катоду, а гидроксид-ионы притягиваются поверхностью твердого электролита 16, как анодом. Твердый электролит 16 известного состава (7), например, из циркония, стабилизированного кальцием (Zr0,89Ca0,11 О1,89), абсорбирует атомы кислорода из гидроксид-ионов, дошедших до его поверхности, в результате чего из гидроксид-ионов высвобождаются атомы водорода, которые в ходе электрохимического взаимодействия с атомами кальция во внутреннем объеме реактора образуют молекулы гидрида кальция в соответствии с известным химическим уравнением (8):
Са+Н2=СаН2.
В ходе электролизных процессов, протекающих внутри реактора 13, только часть выделившегося водорода может вступить в химическую реакцию с кальцием при образовании гидрида кальция. Так, например, при вводе в реактор воды массой 100 килограммов для барботажа находящегося в реакторе гидроксида кальция массой 100 килограммов в процессе электролиза щелочи массой 200 килограммов твердым электролитом анода абсорбируется 132,15 килограммов кислорода, а внутри реактора останется 54,05 килограммов кальция в атмосфере водорода массой 13,8 килограммов. Для гидрирования кальция массой 54,05 килограммов потребность в водороде составляет 2,6 килограммов, а избыточно полученный водород массой 11,2 килограммов самокомпримируется внутри реактора и остается в нем до тех пор, пока автоматические приборы контроля давления водорода в реакторе не приведут в открытое положение разобщительный кран, размещенный на входе в трубу 31 (на чертеже не показан, чтобы не затемнять его деталями оборудования известной конструкции) для того, чтобы часть избыточной массы водорода из реактора попала в сборник водорода. В связи с тем, что исследованиями, результаты которых опубликованы в (1), доказана необходимость поддержания давления в водородной атмосфере внутри реактора на уровне 1 бара для получения гидридов, «близких по своему составу к стехиометрическим», избыточный водород может быть выведен из реактора. Автоматические приборы контроля давления водорода в реакторе передают управляющий импульс на перевод разобщительного крана в закрытое положение в тот момент, когда давление водорода в реакторе снизится до расчетного, после чего водород из сборника 31 транспортируют в ресивер 3, откуда его расходуют по мере возникновения необходимости для питания топливных элементов. Одновременно со сбросом части избыточной массы водорода из реактора в сборник водорода автоматические приборы контроля давления кислорода во внутренней полости трубы 14 переводят в открытое положение разобщительный кран, размещенный на входе в патрубок 17 (на чертеже не показан во избежание затемнения его деталями оборудования известной конструкции), для выравнивания давления по обе стороны пленки твердого электролита 16, нанесенного на внешнюю поверхность трубы 14. После автоматического возврата в закрытое положение разобщительного крана кислород, прошедший через патрубок 17 в сборник 18, транспортируют в ресивер 5, откуда расходуют по мере возникновения необходимости для питания топливных элементов либо в других целях. После завершения электролизных процессов внутри реактора остается гидрид кальция в атмосфере водорода. С этого момента электролизный ток отключают и внутренний объем реактора охлаждают известными способами, например, путем пропуска по трубам 20 воды. Охлажденный гидрид кальция может храниться в реакторе для того, чтобы в любой момент можно было возобновить производство водорода за счет впрыскивания через форсунки 11 воды, масса которой составляет 85,74% массы гидрида кальция. Гидрид кальция взаимодействует в реакторе с водой в соответствии с известным уравнением:
СаН2+2H2O=Са(ОН)2+2H2.
В результате осуществления этой химической реакции выделяется водород, масса которого составляет 5,128% от общей массы гидрида кальция и воды, а остальные 94,872% от общей массы гидрида кальция и воды приходятся на остающийся в реакторе химически чистый гидроксид кальция, который будет использован для приготовления раствора гидроксида кальция (щелочи) в реакторе путем впрыскивания через форсунки 11 воды с целью подготовки реактора к осуществлению электролиза щелочи при возобновлении подачи постоянного электрического тока через клеммы 34 и 35.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На изображенной на чертеже блок-схеме компоновки оборудования, предназначенного для синтеза гидрида кальция, а также для накопления водорода и кислорода, используемых в качестве топлива и окислителя в батарее топливных элементов, и для получения водорода при прекращении подачи постоянного электрического тока чрез клеммы 34 и 35 цифрами обозначены части оборудования, имеющие существенное значение для его функционирования:
1 - батарея топливных элементов;
2 - трубы для соединения батареи топливных элементов с ресивером 3;
3 - ресивер, в котором накапливают водород в процессе электролиза водного раствора гидроксида кальция, а также при извлечении водорода из гидрида кальция при прекращении энергоснабжения оборудования;
4 - трубы для соединения батареи топливных элементов с ресивером 5;
5 - ресивер, предназначенный для хранения запаса кислорода, который получают в процессе электролиза водного раствора гидроксида кальция;
6 - трубы, предназначенные для отвода продуктов окисления водорода кислородом из топливных элементов в магистральный трубопровод 7;
7 - магистральный трубопровод для транспортирования продуктов окисления водорода кислородом в резервуар 8;
8 - резервуар, предназначенный для хранения запаса воды;
9 - насос, предназначенный для создания напора воды, впрыскиваемой в реактор;
10 - трубы, предназначенные для подачи воды из резервуара 8 в реактор;
11 - форсунки, предназначенные для ввода воды в реактор;
12 - часть днища реактора, электрически изолированная от остальной массы металлического корпуса реактора;
13 - реактор, представляющий собой герметичную емкость из прочного и жаростойкого металла, предназначенную для электролиза водного раствора гидроксида кальция, а также для хранения гидрида кальция (на чертеже показан в сечении плоскостью, проходящей через ось трубы 14);
14 - труба, заглушенная снизу, предназначенная для приема кислорода из водного раствора гидроксида кальция в процессе его электролиза;
15 - сквозные отверстия в стенках трубы 14, через которые кислород из массы твердого электролита попадает во внутреннюю полость трубы 14;
16 - слой твердого электролита известного состава, предназначенный для абсорбирования кислорода из водного раствора гидроксида кальция в процессе его электролиза;
17 - герметичный патрубок, предназначенный для транспортирования кислорода из внутренней полости трубы 14 в сборник кислорода;
18 - сборник кислорода, предназначенный для приема образующегося в процессе электролиза в реакторе кислорода, а также для поддержания расчетного давления кислорода во внутренней полости трубы 14;
19 - труба, предназначенная для соединения сборника кислорода 18 с ресивером 5;
20 - трубы, размещенные во внутреннем объеме реактора 13, предназначенные для пропуска внутри них теплоносителя - продуктов окисления водорода кислородом;
21 - электролизер, предназначенный для разделения продуктов окисления водорода кислородом после пропуска их внутри труб 20;
22 - трубы, предназначенные для транспортирования продуктов окисления водорода кислородом из труб 20 в электролизер 21;
23 - накопитель кислорода, предназначенный для приема из электролизера 21 кислорода, образующегося там в процессе электролиза высокотемпературного водяного пара;
24 - накопитель водорода, предназначенный для приема из электролизера 21 водорода, образующегося там в процессе электролиза высокотемпературного водяного пара;
25 - трубы, предназначенные для пропуска кислорода из электролизера 21 в накопитель 23;
26 - трубы, предназначенные для пропуска водорода из электролизера 21 в накопитель 24;
27- водородная горелка известной конструкции, предназначенная для осуществления процесса окисления водорода кислородом;
28 - трубы, предназначенные для транспортирования кислорода из накопителя 23 к водородной горелке 27;
29 - трубы, предназначенные для транспортирования водорода из накопителя 24 к водородной горелке 27;
30 - камера, внутри которой размещена водородная горелка и часть труб 10, предназначенных для подачи воды к форсункам 11;
31 - трубы, предназначенные для транспортирования водорода из реактора 13 в сборник водорода 32;
32 - сборник водорода, предназначенный для приема водорода из реактора при автоматическом открытии разобщительного крана на входе в трубу 31;
33 - трубы, предназначенные для транспортирования избыточного объема водорода из сборника водорода 32 в ресивер 3;
34 - клеммы, предназначенные для подключения к источнику постоянного электрического тока слоя твердого электролита 16, нанесенного на внешнюю поверхность трубы 14, который при осуществлении электролизного процесса водного раствора гидроксида кальция является анодом;
35 - внутренняя поверхность металлических стенок реактора 13, которые при осуществлении электролизного процесса водного раствора гидроксида кальция являются катодом;
36 - клеммы для подключения к источнику постоянного электрического тока катода.
Лучший вариант осуществления изобретения
Одним из основных вариантов осуществления изобретения является использование его при проектировании такого оборудования, которое предназначено для извлечения водорода и кислорода из водных растворов гидроксидов металлов, в частности из водного раствора гидроксида кальция, с одновременным синтезом гидридов металлов, в частности гидрида кальция, способного длительно сохранять водород в химически связанном состоянии. Полученный гидрид может оставаться внутри реактора до того момента, когда потребуется извлечь из него водород без затрат электроэнергии, для чего в реактор необходимо ввести воду, масса которой должна составлять 85,74% массы гидрида кальция. В результате взаимодействия гидрида кальция с водой образуется водород, масса которого составляет 5,128% от общей массы гидрида кальция и воды, а остальные 94,872% от общей массы гидрида кальция и воды приходятся на выпадающий в осадок гидроксида кальция, который будет использован для приготовления водного раствора гидроксида кальция (щелочи) при осуществлении очередного цикла электролиза в реакторе. Возможность повторного использования гидроксида кальция для осуществления электролизных процессов в реакторе создает условия для улучшения экономических показателей работы оборудования. Лучшим вариантом осуществления изобретения будет проектирование таких реакторов для электролиза водного раствора гидроксида кальция, конструкция которых позволит производить перегрузку синтезированного гидрида кальция из реактора в специальные водонепроницаемые контейнеры с целью длительного хранения его до возникновения необходимости извлечь водород из гидрида кальция. В этом варианте появляется реальная возможность использования всех избыточных электрических мощностей в энергосистемах в периоды спадов в потреблении электроэнергии для накопления запасов водорода, кислорода и гидрида кальция для того, чтобы в периоды пиковых нагрузок в энергосистемах вводить в работу дополнительные батареи топливных элементов с целью производства недостающей электроэнергии.
Синтезированный гидрид кальция, перегруженный из реакторов в специальные водонепроницаемые контейнеры, может также доставляться любыми видами транспорта в те регионы, в которых после извлечения из него водорода образующийся гидроксид кальция будет использован в качестве ценного попутного продукта, например, для известкования кислых почв, для использования в качестве наполнителя в производстве красок и в других химических технологиях.
Может оказаться перспективным направлением использование гидрида кальция в качестве надежного и безопасного хранилища химически связанного водорода, предназначенного для питания топливных элементов на транспортных средствах, например на локомотивах железных дорог, где при включении между управляющими секциями локомотива специального подвижного состава (контейнеровоза для гидрида кальция массой 60 тонн и цистерны для воды массой 52 тонны) будет произведено 5700 килограмм водорода, при использовании которого в топливных элементах можно выработать 100000 киловатт-часов электроэнергии. При мощности непрерывно работающих энергетических установок локомотива 5000 киловатт топливные элементы локомотива обеспечат питание их электроэнергией за счет полученного водорода в течение 20 часов. Такой запас хода локомотива с генерированием электроэнергии в батареях топливных элементов вместо генераторов, для вращения которых необходимы двигатели внутреннего сгорания, достаточен для размещения пунктов экипировки локомотивов через 500 километров, что позволяет сохранить систему тягового обслуживания движения поездов. В пунктах экипировки локомотивов необходимо перецепить управляющие секции к загруженному гидридом кальция контейнеровозу и цистерне с водой, а отцепленный от локомотива контейнеровоз, в котором находится 106,3 тонн гидроксида кальция, освобождают от гидроксида кальция и загружают 60 тоннами гидрида кальция в процессе подготовки его к очередному рейсу. В пустую цистерну, отцепленную от управляющих секций, наливают 52 тонны воды в процессе подготовки ее к очередному рейсу. Наличие необходимого количества контейнеровозов, а также специальных водонепроницаемых контейнеров позволит синтезировать гидрид кальция в периоды спада в потреблении электроэнергии в энергосистемах, обслуживающих пункты экипировки локомотивов, и за счет этого достигнуть снижения затрат на производство гидрида кальция.
Замечательные свойства гидрида кальция, как безопасного и надежного аккумулятора водорода, позволяют прогнозировать его использование в электромобилях при применении топливных элементов с твердым электролитом в виде тонкой пленки из стабилизированного диоксида циркония. Загруженный в электромобиль гидрид кальция массой 600 килограммов в сочетании с запасом воды общей массой 520 килограммов позволяет получить 57 килограммов водорода без затрат электроэнергии. Полученное количество водорода позволяет выработать не менее 1000 киловатт-часов электроэнергии. Этой электроэнергией можно обеспечить питание тяговых электродвигателей электромобиля общей мощностью 100 киловатт при непрерывном движении на подъем в течение 10 часов. За это время электромобиль проедет около 600 километров. Такой пробег между пунктами заправки гидридом кальция может оказаться привлекательным стимулом для широкого распространения электромобилей в мире.
В случаях затруднений со строительством газопроводов и линий для электроснабжения новостроящихся домов усадебного типа может оказаться конкурентоспособным вариант замены дорогостоящей транспортировки электроэнергии и газа в эти пункты на выработку водорода из гидрида кальция для питания топливных элементов. Например, при годовом расходе электроэнергии в 100000 киловатт-часов достаточно привезти к усадьбе 60 тонн гидрида кальция, из которого при добавлении 52 тонн воды можно получить 5700 килограмм водорода и обеспечить питание им топливных элементов, вырабатывая в каждый период суток ровно столько электроэнергии, сколько ее требуется для своих электроприборов, а 106,3 тонн гидроксида кальция, который образуется в течение года, можно использовать в качестве ценного известкового удобрения почвы.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Синтез гидрида кальция в процессе электролиза водного раствора гидроксида кальция происходит в реакторе потому, что для соединения атомов кальция и водорода в молекулы гидрида кальция созданы все необходимые условия:
1) температура внутри реактора, где происходит химическая реакция, поддерживается на уровне не ниже 860 градусов по Цельсию за счет тепловой энергии, которую отдает стенкам нагревательных труб 20 водяной пар, имеющий на входе в трубы 20 температуру 2600 градусов по Цельсию, а после выхода из труб 20 этот водяной пар попадает на вход в высокотемпературный электролизер, предназначенный для получения водорода и кислорода, используемых для питания водородных горелок 27. Конструкция высокотемпературных электролизеров была разработана в последней четверти 20 века. Например, в Институте электрохимии Уральского отделения Академии наук СССР в электролизерах с твердым электролитом из (ZrO2)0,9(Y2O3)0,1 в виде пленки толщиной 1 миллиметр при температуре 850 градусов по Цельсию получена плотность тока 3 килоампер на квадратный метр с расходом электроэнергии на выработку кубометра водорода 3,25 киловатт-час;
2) давление водорода, самокомпримирующегося в ходе электролизных процессов в реакторе за счет получения избыточных в сравнении с потребностью для гидридизации кальция масс водорода, поддерживают на расчетном уровне путем автоматизации управления приборами выпуска из реактора части масс водорода и кислорода.
Имеющиеся на земном шаре запасы карбоната кальция, из которого получают гидроксид кальция, практически неисчерпаемы и не требуют больших затрат на их добычу и переработку известными способами.
Источники информации
1. Мюллер В. Гидриды металлов, Атомиздат, 1973 г.,с.44-189.
2. Заявка Японии №61 - 29881, С01В 3/00.
3. Патент SU 552293, C01G 1/00 от 30.03.77 г.
4. Патент RU 2171784 С2, С01G 31/00, С01В 6/02, опубликован 10.08.01 г.
5. Патент GB 176354 A (ALBIN KIESEWALTER) от 11.01.1923 г.
6. Б.В.Некрасов Основы общей химии, том 1, изд.3 исправленное и дополненное, издательство Химия, 1974 г., с.171-187.
7. С.Ф.Пальгуев и др. Высокотемпературные оксидные электронные проводники для электрохимических устройств, М.: Наука, 1990 г., с.173-180.
8. И.А.Зубович Неорганическая химия, М.: Высшая школа, 1989 г., с.261.
Синтез гидрида кальция, отличающийся тем, что гидроксид кальция, помещенный в реактор, нагревают до температуры 860°С за счет пропускания по трубам, размещенным во внутреннем объеме реактора, теплоносителя, являющегося продуктом окисления водорода кислородом в водородной горелке, температура водородного факела на выходе из которой достигает 2600°С, производят многократное впрыскивание в реактор через форсунки воды, нагретой в камере с водородной горелкой до температуры не менее 860°С, с образованием высокотемпературного водяного пара, подключают к источнику постоянного электрического тока клеммы катода, функцию которого выполняют стенки реактора, и клеммы анода, функцию которого выполняет твердооксидная сплошная пленка, нанесенная на заглушенную снизу полую трубу с множеством сквозных отверстий в стенках, предназначенных для выхода во внутреннюю полость трубы кислорода, абсорбированного твердооксидной пленкой, и осуществляют высокотемпературный электролиз водного раствора гидроксида кальция с образованием гидрида кальция у внутренних поверхностей стенок реактора.