Катализатор, способ его приготовления и способ получения бензойной кислоты
Иллюстрации
Показать всеИзобретение относится к области органического синтеза, а именно к способу получения бензойной кислоты (С6Н5СООН, бензолкарбоновая кислота) каталитическим окислением бензилового спирта раствором пероксида водорода, а также к катализаторам для его осуществления и способу их получения. Описан катализатор получения бензойной кислоты, представляющий собой наноструктурированный бифункциональный металлокомплексный катализатор, выполняющий функции катализатора окисления и межфазного переноса, представляющий собой комплексное соединение общей формулы Q3{PO4[W(O)(O2)2]4}, где: Q - четвертичный аммониевый катион - [(R1)3NR2]+, где: R1, R2 содержат от 8 до 24 атомов углерода. Описан способ приготовления катализатора получения бензойной кислоты растворением соединений, содержащих фосфор и вольфрам, в растворе пероксида водорода с добавлением соединения катализатора межфазного переноса, при этом в качестве соединений, содержащих фосфор и вольфрам, используют фосфорновольфрамовые гетерополикислоты структуры Кегина или Даусона, растворение проводят при мольном отношении пероксида водорода к вольфраму [H2O2]/[W]=15-50 с последующим добавлением в качестве катализатора межфазного переноса соединения четвертичного аммониевого катиона - [(R1)3NR2]+, где: R1, R2 содержат от 8 до 24 атомов углерода. Описан также способ получения бензойной кислоты окислением субстрата пероксидом водорода в присутствие описанного выше катализатора. Технический результат - увеличение эффективности процесса. 3 н. и 5 з.п. ф-лы, 2 табл., 1 ил.
Реферат
Изобретение относится к области органического синтеза, а именно к способу получения бензойной кислоты (С6H5СООН, бензолкарбоновая кислота) каталитическим окислением бензилового спирта раствором пероксида водорода, а также к катализаторам для его осуществления.
Бензойная кислота является одним из важнейших продуктов химической промышленности. Данный продукт используется в следующих отраслях: в сельском хозяйстве и пищевой промышленности (консерванты растительного сырья и пищевых продуктов, бактерицидные упаковочные материалы), в химической и нефтехимической промышленности (производство химических средств защиты растений, каучуков и резинотехнических изделий, горюче-смазочных веществ, антиобледенителей, антифризов, пластификаторов, изоляционных лаков, клеев, красителей, синтетических полимеров и волокон, препаратов аналитической химии), в целлюлозно-бумажной и текстильной промышленности (производство целлюлозы, гомогенизаторы в моющих композициях; водоотталкивающая отделка тканей), в медико-биологической и фармацевтической промышленности (производство лекарственных веществ).
В медицине ее применяют при кожных заболеваниях наружно как антисептическое (противомикробное) и фунгицидное (противогрибковое) средства, а натриевую соль (бензоат натрия) - как отхаркивающее и жаропонижающее средство. Кроме того, бензойную кислоту и бензоат натрия используют при консервировании пищевых продуктов (Е210, Е211, Е212, Е213). Бензоат натрия используют в качестве катализатора для осуществления реакции Клауса в органических средах - процесс «Clauspol-300» (Institut Français du Petrole). Сложные эфиры бензойной кислоты (от метилового до амилового), обладающие сильным запахом, применяют в парфюмерной промышленности.
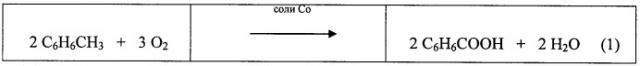
Получают бензойную кислоту окислением толуола азотной или хромовой кислотой, а также декарбоксилированием фталевой кислоты. Впервые в промышленном масштабе жидкофазное окисление толуола в бензойную кислоту было осуществлено в Германии в середине 50-х годов. Толуол окисляли кислородом воздуха при температуре 140°С и давлении 0,3 МПа (3 атм) в присутствии солей кобальта в соответствии со следующей целевой реакцией.
Из сырого продукта, содержащего около 50% бензойной кислоты, извлекали кислоту и непревращенный толуол, а побочные продукты бензиловый спирт или бензальдегид возвращали на стадию окисления. Каталитическое окисления толуола при температуре 150-170°С и давлении около 1 МПа (10 атм) является стадией одного из процессов получения капролактама, например на заводе фирмы Snia Viscosa в г.Тарвизио, Италия (Europ. Chem. News, 1976, 28, 721, p.50).
Дальнейшие попытки улучшения процесса получения бензольной кислоты путем каталитического окисления толуола сводились:
- к изменению состава катализатора, например, наряду с использованием солей кобальта в качестве катализатора применяют со-катализаторы стеараты или ацетаты лития, никеля, марганца, бензоат марганца и т.п. [SU 187767, С07с, 1966; SU 250765; SU 852857, C07C 63/06, 1980; SU 789505, C07C 63/04, 1981];
- к введению промоторов: соединения брома, иода [SU 453824, С07 51/00, 1975; SU 1026650, C07C 51/12, 1983], алкилсилоксанов с М.В. не менее 400 и др. [SU 250765, С07с, 1970];
- или к применению комбинированных окислителей [SU 262899, С07с, 1970], либо увеличению концентрации кислорода (до 76%) в воздушной смеси [SU 249363, С07с, 1969];
- или к проведению реакции под давлением кислорода (до 10 атм) [SU 1779241, C07C 63/04, 1992].
Известны также и способы получения бензойной кислоты без применения катализаторов, например путем окисления толуола кислородом воздуха при 240-275°С и давлении 7,5-15,0 МПа в присутствии воды и карбоната натрия при 2-6 н. концентрации последнего [SU 1369226, C07C 63/06, 1995]. Для повышения выхода бензойной кислоты до 91,5% в данном способе организована стадия дополнительного доокисления.
Таким образом, многочисленные способы получения бензойной кислоты путем окисления толуола требуют высоких температур 140-275°С и давления от 0,3 до 15 МПа, что делает эти процессы дорогими, требующими существенных капитальных затрат. Кроме этого используемые для этих целей катализаторы, со-катализаторы и промоторы содержат экологически неблагоприятные соединения Со, Cr, Mn, Pb, Br, I и т.п., что влияет на качество продукта и загрязнение окружающей среды.
Параллельно с целью создания эффективного процесса получения бензойной кислоты были разработаны каталитические способы окисления дибензилового эфира кислородом воздуха [US 3538165, 260-599, 1970; SU 1154261, C07C 47/54, 1985] и окисления бензила раствором пероксида водорода [SU 185885, 12о, 12С07с, 1966]. Получение бензойной кислоты путем окисления дибензилового эфира проводят при 120-145°С в присутствии катализатора общей формулы M(R'COCHCOR)n·(2L)m, где М - Со, Mn, Cr; n - 2, 3; m - 0,1; R' - СН3, С6Н5, CF3, С(СН3)3; R - С6Н5, CF3, С(СН3)3, СН3; L - Н2О, амин, или соединения хрома общей формулы [Cr3О(RCO2)6Ln]Х·m Н2О, где L - RCOOH, H2O; R - С6Н5, n-NO2 С6Н4, 3,5-(NO2)2С6Н3CO2; Х - ОН, NO3; n - 2, 3; m - 1,5.
Окисление α-дикетона - бензила 30-40% раствором пероксида водорода позволяет снизить температуру до 40°С, но реакцию осуществляют в среде органического растворителя - низшего алифатического спирта. В качестве катализатора используют кислородсодержащие производные щелочноземельных металлов, например оксиды, гидроксиды, алкоголяты. Применение органического растворителя требует организации дополнительной стадии его отгонки при выделении бензойной кислоты. Таким образом, рассмотренные процессы не лишены ранее указанных недостатков и являются экологически несбалансированными.
Большая группа патентов посвящена методам окисления спиртов молекулярным кислородом до карбонильных соединений, в том числе и до карбоновых кислот с использованием оксометаллатов - гетерополикислот, с Si, W, Ru и т.п., входящими в структуру гетерополисоединения (JP 2003261493, B01J 31/02, 2003). Исключением являются разработки Ishii Y. с сотрудниками, которые в качестве окислителя для окисления циклических олефинов и диолов использовали 30-35% растворы пероксида водорода, а в качестве катализаторов системы (Н3РМо12O40+Q) и (H3PW12O40+Q), Q - четвертичные аммониевые или фосфониевые соли. Выход бензойной кислоты, получаемой из 1-фенил-1,2-этандиола с использованием указанных систем, составил 55%. (Y.Ishii, К.Yamawaki and et al. J. Org. Chem. 1988, 53, 3587-3593; JP 1165542, C07B 61/100; B01J 31/34, 1989). Основной недостаток таких процессов - трудности с выделением катализатора из гомогенного раствора для повторного использования.
Для устранения этого недостатка в более поздних патентах разработаны способы окисления пероксидом водорода в двухфазных растворах различных органических субстратов, в т.ч. и спиртов с применением в качестве катализаторов пероксополиоксометаллатных комплексов в сочетании с катализаторами межфазного переноса - четвертичными катионами. Здесь можно выделить два направления.
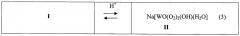
Получение карбоновых кислот путем окисления линейных и ароматических спиртов пероксидом водорода с использованием в качестве предшественника пероксополиоксокомплексов вольфрамата натрия в сочетании с четвертичной аммониевой солью (Na2WO4+[CH3(n-C8H17)3N]HSO4). Реакцию окисления осуществляют при 90°С с использованием 30% раствора пероксида водорода. Молярные соотношения: [Sub]/[Cat]=50-330, [Н2О2]/[Sub]=2,5-5. [К.Sato, J.Takagi, M.Aoki, and R.Noyori, Tetrahedron Letters 39, 1998, pp.7549-7552; R.Noyori, M.Aoki, and K.Sato, Chem. Commun., 2003, pp.1977-1986; JP 2004059451, C07C 51/285; B01J 23/30, 2004]. Катализатор синтезируется in situ путем добавления предшественников Na2WO4 и [CH3(n-C8H17)3N]HSO4 непосредственно в реакционную смесь, при этом образуются комплексы вольфрама, содержащие одну или две пероксогруппы, например:
Комплекс I неактивен в реакции окисления, но он находится в равновесии с активным комплексом II в кислом растворе при рН 0,4-3 [R.Noyori, M.Aoki, and К.Sato, Green oxidation with aqueous hydrogen peroxide, Chem. Commun., 2003, pp.1977-1986].
Для переноса комплекса в органическую фазу для осуществления реакции окисления (5) используют катализатор межфазного переноса Q-[CH3(n-C8H17)3N]+.
Несмотря на то что данный способ относится к «зеленым» процессам, стабильность таких каталитических систем недостаточна для достижения большого числа оборотов катализатора и, как следствие, требует достаточно высоких концентраций катализатора ([Sub]/[Cat]=50-330). Выход бензойной кислоты не превышает 87% за 3-5 ч. По-видимому, с нестабильностью комплексов связано предложенный этими же авторами способ окисления спиртов пероксидом водорода с использованием в жидкой фазе массивного катализатора - Pt-черни [US 2006106250, С07С 51/245].
Прототипом предлагаемого способа и катализатора получения бензойной кислоты является процесс [US 4532079, С07С 51/245, С07В 51/245, B01J 31/02, 30.07.1985] получения карбоновых кислот путем окисления пероксидом водорода олефинов, диолов. В качестве катализатора используют комплексное соединение с общей формулой QXW4O24-2n, где Q-«ониевый» катион (R5R6R7R8M)+, М из ряда N, Р, As, Sb; R5, R6, R7, R8 содержат от 25 до 40 углеродных атомов; Х - атомы Р или As; n - 0, 1, 2. Каталитический комплекс синтезируется in situ или предварительно путем смешения вольфрамовой и фосфорной кислот или их солей щелочных металлов (или WO2, W2O5, WO3, WS2, WS3, WCl6, WOCl4 и W(СО)6) с водным раствором H2O2 (аналогично для As-соединений) при температуре 20° и 80°С; кислотность водной фазы доводят до рН 2 с помощью минеральной кислоты, например H2SO4 или HCl. Соль QY, где Y- - Cl, HSO4 -, NO3 - предварительно растворенную в органическом растворителе (ароматическом или хлорсодержащем углеводороде или алкилэфире, например бензоле, дихлорэтане и т.п.) смешивают с водной фазой и перемешивают в течение 15-30 мин. Образовавшийся пероксополиоксокомплекс выделяют фильтрованием или путем отгонки растворителя под вакуумом при 40-50°С. При этом мольные соотношения P:W=4; H2O2:W=2,5-6; W:Q=2. Основное преимущество данного подхода к синтезу каталитического комплекса относительно [R.Noyori, М.Aoki, and К.Sato, Green oxidation with aqueous hydrogen peroxide, Chem. Commun., 2003, pp.1977-1986] является стабилизация пероксокомплекса за счет введения Р или As.
Реакцию окисления органических субстратов проводят в двухфазном растворе: водная фаза, содержащая пероксид водорода до 70%, органическая фаза, содержащая органический растворитель (ароматический или хлорсодержащий углеводород или алкилэфир, например бензол, дихлорэтан и т.п) при температуре 40-90°С, давлении 1-100 атм и количества катализатора берутся из расчета 0,01-1 грамм-атом W на 1 моль субстрата (т.е. [Sub]/[Cat]=4-400). Выход бензойной кислоты при каталитическом окислении бензилового спирта составляет 85% за 3 ч при [Н2O2]/[Sub]=5,5.
Основными, существенными недостатками способа являются: проведение реакции окисления в присутствии органического растворителя, использование высоких концентраций катализатора, низкий выход бензойной кислоты, а также использование для приготовления катализатора экологически опасных As, Sb, WCl6, WOCl4, хлорсодержащих углеводородов или дефицитных и дорогих соединений - катализаторов межфазного переноса содержащих от 25 до 40 атомов углерода.
Изобретение решает задачу увеличения эффективности процесса получения бензойной кислоты.
Задача решается катализатором получения бензойной кислоты окислением бензилового спирта пероксидом водорода в двухфазном растворе в присутствии металлокомплексного катализатора с общей формулой Q3{PO4[W(O)(О2)2]4}, где: Q - четвертичный аммониевый катион - [(R1)3NR2]+, где: R1, R2 содержат от 16 до 24 атомов углерода.
Задача решается способом приготовления катализатора. Для приготовления катализатора в качестве предшественников используют полиоксометаллаты - фосфорно-вольфрамовые гетерополикислоты структуры Кегина или Даусона (H3PW12O40, Н7[Р(W2O7)6 и т.п.) и 5-35% раствор перекиси водорода. Растворение оксометаллата в растворе пероксида водорода проводят при соотношении [Н2O2]/[W]=15-50 с последующим добавлением соли четвертичного аммониевого катиона в виде гидросульфата (QHSO4). Кристаллические соли добавляют в реакционную смесь в сухом виде, жидкие - предварительно растворенные в минимальном количестве низшего алифатического или бензилового спирта. Полученный кристаллический катализатор выделяют из водного раствора фильтрованием, гелеобразный - декантацией.
Задача решается способом получения бензойной кислоты путем каталитического окисления бензилового спирта пероксидом водорода в двухфазном растворе органическая фаза - водная фаза, где роль органической фазы выполняет субстрат (бензиловый спирт) при температуре 50-90°С и общем давлении 1 атм при следующих соотношениях компонентов: [Sub]/[Cat]=500-2000; [H2O2]/[Sub]=2-4 в присутствии описанного выше катализатора.
Предлагаемый способ синтеза бензойной кислоты, как и прототип, основан на применении метода межфазного катализа в растворах с использованием наноструктурированных бифункциональных металлокомплексных катализаторов, выполняющих функции катализаторов окисления и межфазного переноса.
Основными отличиями предлагаемого способа синтеза бензойной кислоты являются:
а) проведение реакции окисления бензилового спирта без применения органических растворителей делает процесс экологически благоприятным и не требует дополнительных стадий для отделения растворителя;
б) осуществление процесса в мягких условиях: 50-90°С и общем давлении 1 атм, делает процесс технологичным;
в) использование катализатора в малых концентрациях, [Sub]/[Cat]=500-2000, положительно влияет на экономические показатели процесса;
г) использование разбавленных растворов пероксида водорода (5-35%), повышает безопасность процесса;
д) проведение реакции окисления при минимальном избытке окислителя по отношению к субстрату [Н2О2]/[Sub]=2-4, которое достигается путем дозировки окислителя тремя порциями, позволяет уменьшить вклад параллельно протекающей реакции разложения Н2О2 во времени, а следовательно, и расход пероксида водорода;
к катализатору:
е) использование для приготовления катализаторов более доступных и дешевых четвертичных аммониевых солей, (R1)3NR2)HSO4, R1, R2 содержат от 8 до 24 атомов углерода и не содержащих галоген-ионов, положительно влияет на экономические и экологические показатели процесса;
ж) выдерживание соотношения [Н2O2]/[W]=15-50 при синтезе катализатора позволяет: синтезировать наиболее активную форму комплекса, содержащую до четырех пероксогрупп, применение которого увеличивает выход целевого продукта в процессе окисления бензилового спирта; не требует дополнительного подвода тепла (нагревания реакционной смеси);
з) использование в качестве предшественников фосфорно-вольфрамовых гетерополикислот структуры Кегина или Даусона и четвертичных аммониевых солей в виде гидросульфатов позволяет не использовать дополнительно минеральные кислоты для подкисления реакционной смеси.
и) проведение синтеза катализатора без использования ароматических или хлорсодержащем углеводородов в качестве растворителей для «ониевых» солей существенно упрощает стадию выделения катализатора.
Сущность изобретения иллюстрируется примерами синтеза каталитических комплексов (примеры А, Б, В, Г, Д) и получения бензойной кислоты (таблицы 1, 2 и чертеж).
Пример А.
К раствору H3PW12O40·15,4H2O (4,0101 г, 1.27 ммоль) в 5 мл воды добавляют 25%-ный раствор Н2O2 (34 мл, 250 ммоль). Смесь перемешивают при комнатной температуре и небольшими порциями в сухом виде при перемешивании добавляют 3.81 ммоль четвертичной аммониевой соли [Bun 4N]HSO4 (1,2932 г). Образовавшийся кристаллический осадок катализатора состава [Bun 4N]3{PO4[W(O)(O2)2]4} выделяют фильтрованием.
В ИК-спектре каталитического комплекса регистрируются следующие полосы поглощения (ПП) иона PO4 3- (1085, 1052, 1038 (пл) см-1), связи W=O (971 см-1), связи O-O (856, 845 см-1) и антисимметричных и симметричных колебаний W-O-O (590, 521 см-1), а также ПП (722, 736, 651, 577, 550 см-1), связанные с поглощением катиона.
Пример Б.
Аналогичен примеру А, отличающийся тем, что добавляют четвертичную аммониевую соль [C5H5N(n-C16H33)]HSO4 (1,5298 г), предварительно растворенную в минимальном количестве воды (2 мл).
В ИК-спектре полученного каталитического комплекса [C5H5N(n-С16Н33)]3{PO4[W(O)(O2)2]4}, регистрируются следующие ПП (см-1): (PO4 3-) 1088, 1061, 1038 (пл), (W=O) 988, 961 см-1, (O-O) 856, 844, (W-O-O)591, 526 и ПП (722, 650, 571 и 548 см-1), связанные с поглощением катиона.
Пример В.
Аналогичен примеру А, отличающийся тем, что добавляют четвертичную аммониевую соль [Me(n-C8H17)3N]HSO4 (1,7741 г), предварительно растворенную в минимальном количестве этанола (3 мл). Гелеобразный катализатор выделяют декантацией.
В ИК-спектре полученного каталитического комплекса [Ме(n-C8H17)3N]3{PO4[W(O)(O2)2]4} регистрируются следующие ПП: (PO4 3-) 1088, 1056, 1033 (пл), (W=O) 973, (O-O) 855, 846, (W-O-O) 591, 523, и ПП (741, 733, 702, 651, и 625 см-1), связанные с поглощением катиона.
Пример Г.
Аналогичен примеру А, отличающийся тем, что берут 5 мл раствора H7[P(W2O7)6·7Н2O (3,8659 г).
В ИК-спектре полученного каталитического комплекса [Bun 4N]3{PO4[W(O)(O2)2]4}, регистрируются следующие ПП (см-1): (PO4 3-) 1085, 1052, 1038 (пл), (W=O) 971, (O-O) 856, 845, (W-O-O) 590, 521 и ПП 722, 736, 651, 577, 550 см-1), связанные с поглощением катиона
Пример Д.
Аналогичен примеру Г, отличающийся тем, что используют 35-ный раствор Н202 (44,4 мл, 457 ммоль) и четвертичную аммониевую соль [Me(n-C8H17)3N]HSO4 (1,7741 г) предварительно растворенную в минимальном количестве бензилового спирта (3 мл). Гелеобразный катализатор [Me(n-C8H17)]3{PO4[W(O)(O2)2]4} выделяют декантацией.
В ИК-спектре каталитического комплекса регистрируются следующие ПП (см-1): (PO4 3-) 1088, 1056, 1033 (пл), (W=O) 973, (O-O) 855, 846, (W-O-O) 591, 523 и ПП 741, 733, 702, 651, 625, 576, 549 см-1, связанные с поглощением катиона
Получение бензойной кислоты осуществляют следующим способом.
Реакцию селективного каталитического окисления бензилового спирта (7) проводят в термостатированном реакторе типа «каталитическая утка», закрепленный на качалке (300-400 двойных качаний) или в термостатированной конической колбе с использованием магнитной мешалки (600-1200 об/мин-1). Реактор снабжен обратным холодильником и имеет устройство для дозировки раствора пероксида водорода.
Последовательность приготовления реакционной смеси. В реактор помешают навеску катализатора, добавляют бензиловый спирт, перемешивают, вводят первую порцию раствора пероксида водорода в соответствии со стехиометрией реакции (7) и включают нагрев. Температуру 50-90°С поддерживают с помощью водяного термостата с точностью ±0,1°С. Последующие две порции раствора пероксида водорода добавляют в реакционную смесь через 15 и 30 мин соответственно после начала реакции.
Для определения выхода продукта количественное извлечение бензойной кислоты осуществляют следующим образом. Реакционную смесь охлаждают до комнатной температуры, добавляют расчетное количество 10%-ного раствора NaHCO3, переносят в делительную воронку, отделяют водный слой и подкисляют его до рН 3. После этого раствор охлаждают до 8-10°С. Выпавший кристаллический осадок бензойной кислоты отфильтровывают, промывают небольшим количеством охлажденной воды и сушат на воздухе. Идентификацию проводят методом ИК-спектрометрии.
Примеры по получения бензойной кислоты приведены в таблицах 1-2 и на чертеже.
| Таблица 1 | ||||
| Выход бензойной кислоты в зависимости от мольного отношения [Sub]/[Cat].Условия: Т опыта = 85°С; Р - атмосферное; [H2О2]/[Sub]=3 | ||||
| № примера | Катализатор | [Sub]/[Cat] | Время реакции, ч | Выход PhCHOOH, % |
| Пример 1 | А | 500 | 1,3 | 99,8 |
| Пример 2 | Б | 500 | 1,0 | 99,8 |
| Пример 3 | В | 1000 | 1,0 | 98,0 |
| Пример 4 | Г | 1500 | 2,0 | 98,9 |
| Пример 5 | Д | 500 | 1,0 | 99,9 |
| Пример 6 | Д | 2000 | 2,0 | 99,9 |
| Пример 7(для сравнения) | В | 3000 | 2,5 | 63,0 |
| Пример 8(для сравнения) | А | 2500 | 1,5 | 45,0 |
| где: Sub - бензиловый спирт; Cat - катализатор; PhCHOOH - бензойная кислота. |
Данные таблицы 1 показывают, что для достижения выхода бензойной кислоты от 98,0 до 99,9% оптимальным является интервал соотношений [Sub]/[Cat]=500-2000. Уменьшение концентрации катализатора (Примеры 7, 8) при [Sub]/[Cat]>2000 приводит к существенному снижению выхода продукта, увеличение концентрации катализатора [Sub]/[Cat]<500 экономически нецелесообразно.
В таблице 2 приведены примеры показывающие, что при температуре реакции ниже 70°С (Примеры 9, 15, 16) за 2 ч реакции выход бензойной кислоты составляет 41-72%. Для достижения более высоких выходов продукта существенно увеличивается время реакции и, как следствие, повышается расход окислителя - пероксида водорода на нецелевую реакцию разложения. Таким образом, оптимальным является интервал 70-85°С.
| Таблица 2 | |||
| Выход бензойной кислоты в зависимости от температурыУсловия: [Sub]/[Cat]=500; Р - атмосферное; [H2O2]/[Sub]=2,5, время реакции 2 ч | |||
| № примера | Катализатор | Температура опыта, °С | Выход PhCHOOH, % |
| Пример 9 (для сравнения) | Д | 50 | 41,0 |
| Пример 10 | Д | 70 | 88,2 |
| Пример 11 | Д | 85 | 99,8 |
| Пример 12 | Г | 75 | 98,9 |
| Пример 13 | А | 85 | 99,9 |
| Пример 14 | В | 85 | 99,9 |
| Пример 15(для сравнения) | В | 60 | 72,0 |
| Пример 16(для сравнения) | А | 60 | 55,0 |
На чертеже приведена зависимость выхода бензойной кислоты от мольного отношения [H2O2]/[Sub] в реакции окисления бензилового спирта. Условия: Катализаторы примеров: В, Г, Б соответственно; [Sub]/[Cat]=500; Топытов=83°С; Время реакции - 2 ч.
Характер зависимости указывает на то, что не требуется большой избыток окислителя, т.е. достаточно, чтобы [Н2O2]/[Sub]≤4. При величине данного отношения [Н2О2]/[Sub]≤1,5 протекает реакция образования бензальдегида. Участок зависимости при 1,5≤[H2O2]/[Sub]≤2,0 является переходным, где наряду с бензойной кислотой образуется бензальдегид. В связи с этим для сведения к минимуму нецелевого расхода пероксида водорода его дозировка в реакционную смесь осуществляется в три приема так, чтобы после добавления первой порции 2,0<[Н2О2]/[Sub]<3,0. При добавлении последующих двух порций это отношение не превышало 4. Таким образом, оптимальные величины [Н2О2]/[Sub] при проведении реакции находятся в интервале 2-4.
1. Катализатор получения бензойной кислоты, представляющий собой наноструктурированный бифункциональный металлокомплексный катализатор, выполняющий функции катализатора окисления и межфазного переноса, отличающийся тем, что он представляет собой комплексное соединение общей формулы Q3{PO4[W(O)(O2)2]4}, где Q - четвертичный аммониевый катион - [(R1)3NR2]+, где R1, R2 содержат от 8 до 24 атомов углерода.
2. Способ приготовления катализатора получения бензойной кислоты растворением соединений, содержащих фосфор и вольфрам, в растворе пероксида водорода с добавлением соединения катализатора межфазного переноса, отличающийся тем, что в качестве соединений, содержащих фосфор и вольфрам используют фосфорно-вольфрамовые гетерополикислоты структуры Кегина или Даусона, растворение проводят при мольном отношении пероксида водорода к вольфраму [H2O2]/[W]=15-50, с последующим добавлением в качестве катализатора межфазного переноса соединения четвертичного аммониевого катиона - [(R1)3NR2]+, где R1, R2 содержат от 8 до 24 атомов углерода.
3. Способ получения бензойной кислоты окислением субстрата-Sub пероксидом водорода в присутствии катализатора, представляющего собой наноструктурированный бифункциональный металлокомплексный катализатор, выполняющий функции катализатора окисления и межфазного переноса, отличающийся тем, что в качестве субстрата используют бензиловый спирт и процесс проводят в присутствии катализатора, представляющего собой комплексное соединение общей формулы: Q3{PO4[W(O)(O2)2]4}, где Q - четвертичный аммониевый катион - [(R1)3N R2]+, где R1, R2 содержат от 8 до 24 атомов углерода.
4. Способ по п.3, отличающийся тем, что процесс проводят при температуре 50-90°С.
5. Способ по п.3, отличающийся тем, что процесс проводят при общем давлении, равном 1 атм.
6. Способ по п.3, отличающийся тем, что используют катализатор в мольном отношении [Sub]/[Cat]=500-2000.
7. Способ по п.3, отличающийся тем, что используют разбавленные растворы пероксида водорода с концентрацией 5-35%.
8. Способ по по.3, отличающийся тем, что раствор пероксида водорода добавляют в реакционную смесь тремя порциями так, чтобы после добавления первой порции мольное отношение [H2O2]/[Sub] было не меньше 2, а при добавлении последующих двух порций это отношение не превышало величину равную 4.