Средства и способы для лечения нарушений свертываемости
Иллюстрации
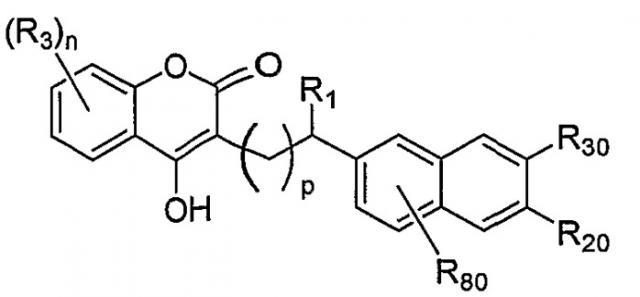
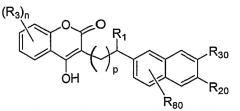
Показать всеДанное изобретение относится к новым соединениям-антикоагулянтам формулы (I):
и их фармацевтически приемлемым солям, где R представляет собой C1-C8алкил, замещенный по меньшей мере одним галогеном. Изобретение также относится к фармацевтическим композициям, содержащим соединения формулы (I) и его соли, а также способам применения соединений, солей и к способу лечения нарушений свертываемости. 10 н. и 11 з.п. ф-лы, 14 ил., 4 табл.
Реферат
Варфарин (кумарин) - это антикоагулянт, действующий путем ингибирования зависящих от витамина К факторов свертывания крови. Соединения на основе варфарина обычно представляют собой производные 4-гидроксикумарина, такие как 3-(α-ацетонилбензил)-4-гидроксикумарин (COUMADIN). COUMADIN и другие кумариновые антикоагулянты ингибируют синтез зависящих от витамина K факторов свертывания крови, включающих Факторы II, VII, IX и X. Задерживающие свертывание крови белки C и S также ингибируются варфариновыми антикоагулянтами. Считается, что варфарин воздействует на синтез факторов свертывания крови ингибированием эпоксидредуктазы витамина К, таким образом ингибируя регенерацию витамина К.
Антикоагуляционный эффект обычно наблюдается через приблизительно 24 часа после введения одной дозы варфарина и длится 2 - 5 дней. Хотя антикоагулянты не оказывают непосредственного влияния на возникший тромб и не восстанавливают поражения ишемической ткани, цель лечения антикоагулянтами состоит в предотвращении роста сформировавшихся сгустков и/или вторичных тромбоэмболических осложнений. Эти осложнения могут приводить к очень серьезным последствиям и даже к летальному исходу.
FDA (Управление по контролю за продуктами и лекарствами (США)) одобрило варфарин для следующих применений: 1) лечение или профилактика тромбоза вен и эмболии легочной артерии; 2) тромбоэмболические осложнения, связанные с мерцательной аритмией и/или замененным сердечным клапаном, и 3) снижение риска смерти, повторяющегося инфаркта миокарда, инсульта или системной эмболии после инфаркта миокарда.
С приемом варфарина связан ряд неблагоприятных воздействий. Среди них - кровотечение со смертельным исходом или без смертельного исхода из ткани или органа или такие геморрагические осложнения, как паралич. Другие отрицательные воздействия включают парестезию, в т.ч. ощущение холода и озноб; головную боль; боль в груди, животе, суставах, мышцах или иные виды боли; головокружение; недостаточность дыхания; затрудненность дыхания или глотания; необъяснимое опухание, слабость, гипотонию или необъяснимый шок. Среди других неблагоприятных реакций, о которых было сообщено, - гиперчувствительность/аллергические реакции, системная холестериновая микроэмболизация, синдром пурпурных пальцев, гепатит, холестатическое поражение печени, желтуха, повышенный уровень печеночных ферментов, васкулит, отек, жар, сыпь, дерматит, в т.ч. буллезная сыпь, крапивница, боль в животе, включая спазмы, метеоризм/вздутие, усталость, летаргия, недомогание, астения, тошнота, рвота, диарея, боль, головная боль, головокружение, искажение вкуса, зуд, алопеция и чрезмерная чувствительность к холоду.
Токсичность лекарственного средства - важный фактор в лечении людей и животных. Токсичные побочные эффекты, вызванные приемом лекарственных средств, включают ряд разнообразных условий от легкого повышения температуры до летального исхода. Лечение лекарственными средствами оправдано только в том случае, если положительный эффект протокола лечения перевешивает потенциальные риски, связанные с ним. Факторы, принимаемые во внимание практикующим врачом, включают качественную и количественную оценку влияния лекарства, которое собираются применять, а также последствий того, если лекарство не будет введено пациенту. Другие учитываемые факторы включают физическое состояние пациента, стадию заболевания и историю его протекания, а также известные нежелательные последствия приема лекарственного средства.
Выведение лекарственного средства из организма является результатом его метаболизма и экскреции из тела. Метаболическое действие может иметь место в кровоснабжении и/или клетках или органах. Печень является важнейшим местом метаболизма лекарственного средства. Обмен веществ можно разделить на первичный и вторичный метаболизм, который также называют метаболизмом фазы 1 и метаболизмом фазы 2. В процессе метаболизма фазы 1 лекарственное средство претерпевает химические изменения путем окисления, восстановления, гидролиза или какого-либо сочетания указанных выше процессов и обычно дает в результате более полярный продукт, чем исходное лекарственное вещество. В метаболизме фазы 2 продукты реакции фазы 1 соединяются с эндогенными субстратами, например, глюкуроновой кислотой, с получением аддитивного продукта или конъюгата, являющегося более гидрофильным, чем продукт фазы 1 и легко выводится с желчью или мочой. В некоторых случаях лекарственное средство претерпевает только метаболизм фазы 2 (конъюгацию), в других случаях - выводится из организма в неизменном виде. Первым этапом в таких реакциях синтеза часто является окислительное конъюгирование, осуществляемое цитохромной системой P450 (CYP450). Образующиеся в результате реакций фазы 2 метаболиты обычно являются продуктами реакции конъюгирования, осуществляемой ферментом трансферазой. Эти реакции включают глюкуронидирование, аминокислотное конъюгирование, ацетилирование, сульфоконъюгирование и метилирование.
Ферменты цитохрома P450 млекопитающих (CYP450), в т.ч. CYP450 человека, являются мембраносвязанными, генсодержащими белками, которые впервые были обнаружены в микросомах печени крысы. Для функционирования ферментам CYP450 требуется источник электронов. Для CYP450 возможны два различных типа цепей переноса электронов. Они зависят от расположения фермента в клетке. Некоторые Р450 обнаружены в митохондриальной внутренней мембране, а некоторые - в эндоплазматической сети (ER). Белок, отдающий электроны CYP450 в ER, называется NADPH-цитохром-P450-редуктазой. Ферредоксин - непосредственный донор электронов для CYP450 в митохондриях (CYP11A1, CYP11B1, CYP11B2, CYP24, CYP27A1, CYP27B1, CYP27C1). NADPH представляет собой источник электронов, которые переходят от ферредоксин-редуктазы к ферредоксину, а затем - к CYP450. Известно также, что некоторые P450 могут получать электроны от цитохрома b5.
Полиморфизм (различия в последовательности ДНК на уровне 1% или выше, обнаруживаемые в совокупности) может обуславливать различия в метаболизме лекарственных средств, поэтому является важной характеристикой генов CYP450 у людей. CYP2C19 обладает полиморфизмом, изменяющим способность фермента метаболизировать мефенитоин (лекарственное средство-маркер). У людей европеоидной расы полиморфизм, относящийся к фенотипу слабого метаболизма, наблюдается только у 3% населения. Однако его можно встретить у 20% жителей Азии. Ввиду наличия таких различий, очень важно учитывать расу человека, выписывая ему лекарства, метаболизм которых характеризуется такими отличиями. Некоторые лекарственные средства имеют узкий диапазон действующей дозы, поскольку становятся токсичными при превышении дозы в случае введения человеку со слабым метаболизмом.
CYP2D6 - вероятно наиболее изученный P450 с полиморфизмом по метаболизму лекарственных веществ. Этот фермент отвечает за окисление более чем 70 различных лекарственных средств. Поскольку иного пути выведения лекарственных средств из организма может не существовать, людям со слабым метаболизмом грозит серьезная опасность негативного воздействия со стороны лекарства. Субстраты CYP2D6 включают средства от аритмии (флекаинид, мексилетин, пропафенон), антидепрессанты (амитриптилин, пароксетин, венлафаксин, флуоксетин, тразадон), нейролептические средства (клорпромазин, галоперидол, торидазин), бета-блокаторы (лабеталол, тимолол, пропанолол, пиндолол, метопролол), анальгетики (кодеин, фентанил, меперидин, оксикодон, пропоксифен) и многие другие лекарственные препараты. CYP2E1 индуцируется у алкоголиков. Существует полиморфизм, связанный с этим геном, который чаще всего наблюдается у китайцев.
Подсемейство CYP3A - одно из важнейших семейств, метаболизирующих лекарственные вещества в организме человека. CYP3A4 - "наиболее сильно экспрессируемый CYP450 в печени человека". (Arch. Biochem. Biophys. 369, 11-23 1999). Известно, что CYP3A4 метаболизирует свыше 120 различных лекарственных веществ, например, ацетаминофен, кодеин, циклоспорин A, диазепам, эритромицин, лидокаин, ловастатин, таксол, цисаприд, терфенадин и варфарин. Этот список далеко не полный.
За последние годы показатель неблагоприятных реакций лекарственных веществ (ADR) значительно вырос в США и в настоящее время представляет собой значительную проблему для национального здравоохранения. Всемирная Организация Здравоохранения (ВОЗ) определяет ADR как "вредную и непреднамеренную реакцию на лекарственное вещество, наблюдаемую при дозах, обычно применяемых у людей для профилактики, диагностики или лечения заболевания или изменения физиологической функции". Для того, чтобы подчеркнуть большое значение ошибки в генезисе ADR и тот факт, что большинство (30-80%) ADR можно предотвратить, этим реакциям недавно дано было следующее определение: "ощутимо вредная или неприятная реакция, вызванная вмешательством в применение медицинского продукта, которая предвещает опасность будущего приема и обуславливает неприменение определенного лечения, изменение режима дозировки или отказ от использования продукта".
Поскольку в нашей системе здравоохранения ADR являются существенной причиной заболеваемости и смертности, снижение частоты случаев ADR стало приоритетной задачей (FDA, Центр изучения и исследования лекарственных средств). Согласно официальной статистике ежегодно в больницах, амбулаториях и домах престарелых наблюдается свыше 2,5 миллионов ADR, которые приводят более чем к 106 000 смертям и стоят экономике США 136 млрд долларов в год в виде расходов, связанных с заболеваемостью и смертностью от лекарств. Сумма этих расходов превышает годовые расходы, связанные с сердечно-сосудистыми заболеваниями и диабетом в США. Кроме того, оценки показателя смертности, связанной с ADR, выводят эти реакции на четвертое место среди основных причин смерти в стране.
Большинство ADR возникают из-за того, что большинство лекарственных средств, разработанных фармацевтическими компаниями, в значительной степени взаимодействуют с компонентами системы CYP, полагаясь на них в процессе метаболизма и/или ингибируя или индуцируя те или иные части CYP. Другими словами, поскольку множество классов лекарственных веществ (в т.ч. гипотензивные средства, антигистаминные препараты, антидепрессанты, иммунодепрессанты, статины) взаимодействуют с системой CYP, она может оказаться "узким местом" в безопасном метаболизме и выведении этих веществ из организма, результатом чего может стать токсическое воздействие. Говоря о метаболизме лекарственных веществ, следует отметить две части системы CYP: CYP3A4 и CYP2D6. Примерно половина всех известных на сегодняшний день лекарств взаимодействуют с CYP3A4. Аналогично, CYP2D6 - часть ферментов, активность которой сильно зависит от генетического фактора (генетического полиморфизма), отвечает за метаболизм трети клинически используемых препаратов. Оба фермента вовлечены в метаболизм сходных с варфарином соединений.
Значительное количество (70-90%) ADR происходит в виде усиления фармакологического действия по сравнению с ожидаемым. Это особенно относится к применению варфарина, поскольку усилением фармакологического действия варфарина является кровотечение. Хотя в развитие ADR могут вносить вклад различные факторы, изменение метаболизма лекарственного вещества, приводящее к повышенным его уровням, вследствие взаимодействия лекарственных веществ на уровне ферментов, генетически обусловленных отличий в активности ферментов и/или нарушения функции органа (печени, почек) играет особо важную роль в возникновении ADR.
Фармакотерапия с применением варфарина оказывается особенно сложной, поскольку метаболизм варфарина очень сложен и подвержен влиянию множества других веществ, в т.ч. препаратов, которые обычно выписывают пациентам, страдающим от мерцательной аритмии, например, амиодарона. Варфарин представляет собой смесь энантиомеров, обладающих различной активностью в отношении фермента эпоксид-редуктазы витамина К (VKER). Эти энантиомеры характеризуются различными способами метаболизма, в которых участвуют разные изоферменты CYP450. Метаболическая система CYP450 легко индуцируется или подавляется множеством таких внешних факторов, как диета и другие принимаемые лекарства. Кроме того, система CYP450 является объектом множества генетических вариаций, обладает низкой функциональной активностью и легко насыщается. По этим причинам метаболизм варфарина может претерпевать непредсказуемые изменения, каждого энантиомера оказывается своя метаболическая "судьба", и он по-разному влияет на фермент VKER.
Кроме того, действие варфарина на фермент VKER приводит к ингибированию факторов свертывания крови II, VII, IX и X, которые сами имеют различную длительность полужизни: от часов (фактор VII) до дней (фактор X). Ввиду столь сложной ситуации фармакологический эффект (увеличение времени свертываемости) варфарина проявляется только через 5-10 дней после введения дозы. Совершенно очевидно, почему очень сложно предвидеть результаты лечения варфарином и почему пациентам грозит серьезная опасность осложнений в виде кровотечений, которые могут даже привести к смерти. При нынешнем состоянии лечения варфарином пациенты должны раз в неделю посещать лабораторию для определения показателей свертываемости с тем, чтобы на ранней стадии обнаружить риск осложнений в виде кровотечения. Но даже при такой строгой системе наблюдения много пациентов, принимающих варфарин, умирают от кровотечений.
В США рост потенциальных клинических проблем и рисков бизнеса, связанных с разработкой лекарственных препаратов, которые должны пройти "по узкому мосту" метаболизма P450, обусловлены следующими двумя факторами: 1) количество рецептов, выдаваемых пациентам в стране, выросло до примерно 3 миллиардов в год или 10 на каждого пациента и 2) среди пациентов, особенно старшего возраста с различными сложными заболеваниями, наблюдается тенденция к одновременному приему нескольких лекарственных препаратов. Последний фактор особенно важен, поскольку частота наступления ADR возрастает экспоненциально при приеме более чем четырех лекарств. Хотя врачи стараются избегать одновременного назначения нескольких лекарственных средств, во многих случаях это оказывается невозможным, поскольку пациенты нуждаются в приеме различных классов лекарственных средств для эффективного лечения сложных состояний.
Общий вид исследования и разработки новых лекарств портят неудачные образцы, применение которых было запрещено FDA ввиду опасности для жизни ADR, связанных с метаболизмом CYP. Во многих случаях эти лекарства были клинически и экономически эффективными. Среди наиболее заметных лекарственных препаратов, применение которых было прекращено из-за связанных с ADR случаев смерти пациентов, обусловленных метаболизмом CYP450, следует отметить терфенадин (февраль 1998 г.), астемизол (июль 1999 г.) и цисаприд (январь 2000 г.). В каждом из этих случаев взаимодействия лекарственных веществ с вовлечением CYP3A4 приводило к повышению концентрации фармацевтического вещества до такой степени, что вызывало значительное ингибирование определенного типа калиевого канала сердца IKr, что, в свою очередь, продлевало интервал QT и вызывало опасную для жизни форму желудочковой тахикардии, называемую трепетанием-мерцанием желудочков.
Поэтому имеется насущная необходимость в аналоге варфарина, который бы характеризовался контролируемым и предсказуемым путем метаболизма, не зависящим от CYP450, такой препарат стал бы важным дополнением в ряду лекарственных веществ для лечения пациентов, страдающих мерцательной аритмией. О некоторых аналогах варфарина уже сообщалось ранее. См., например, WO 02/085882, который включен сюда в качестве ссылки.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Объектом настоящего изобретения являются соединения и фармацевтические композиции, которые могут применяться в качестве антикоагулянтов или в антикоагулянтной терапии.
В широком смысле объектом изобретения являются соединения формулы I
или их фармацевтически приемлемые соли или изомеры, где
R1 представляет собой Н или -(C1-C4 алкил)-CO2R2; где
R2 представляет собой Н или C1-C6 алкил;
R3 в каждом случае независимо представляет собой галоген, OH, C1-C6 алкил, C1-C6 алкокси, C1-C4 галогеналкил или C1-C4 галогеналкокси;
n равно 0, 1, 2, 3 или 4,
p равно 0, 1 или 2; и
Ar представляет собой арильную группу, необязательно замещенную по меньшей мере одной группой, представляющей собой -COR5, -(C1-C6 алкил)-COR5, -(C0-C6 алкил)-O-R6, галоген, OH, амино, моно или диалкиламино, гидроксиалкил, C1-C4 галогеналкил или C1-C4 галогеналкокси, где
R5 представляет собой С1-C8 алкокси, необязательно замещенный 1 или 2 группами, которые независимо означают OH, C1-C4 алкокси, гетероциклоалкил, C3-C7 циклоалкил, -SO2-(C1-C4 алкил), -SO2-(C1-C4 галогеналкил) или -SO2-фенил, OH, амино, моно или диалкиламино или C1-C6 галогеналкокси, необязательно замещенный 1 OH, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино;
и
R6 представляет собой С1-C6 алканоил, арил C1-C6 алканоил, арил C1-C6 алкил, (C1-C6 алкил)-O-арил или арил, где алкильные части алканоильных групп необязательно замещены одним или несколькими галогенами и где арильные группы необязательно замещены в каждой позиции возможного замещения группой, которая представляет собой С1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
Соединения формулы I взаимодействуют с VKER и/или могут применяться в качестве антикоагулянтов и/или в антикоагулянтной терапии. Изобретение также включает фармацевтические композиции, содержащие соединения формулы I, и способы применения таких соединений или композиций при лечении нарушений коагуляции.
Объектом изобретения также является способ лечения пациента с нарушениями коагуляции или пациента, которому угрожает появление такого нарушения свертывания крови и который нуждается в лечении, включающем введение терапевтически эффективного количества соединения формулы (I).
В другом аспекте объектом изобретения являются способы получения интересующих соединений, а также промежуточные соединения, которые могут использоваться в процессе получения интересующих соединений.
Краткое описание чертежей
На Фиг.1 показана ингибирующая VKER активность 3-(4-гидрокси-2-оксо-2H-хромен-3-ил)-3-(4-трифторметокси-фенил)-пропионовой кислоты.
На Фиг.2 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 2,2,3,3,3-пентафтор-пропилового эфира.
На Фиг.3 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 3,3,3-трифтор-пропилового эфира.
На Фиг.4 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 2,2,3,3,3-пентафтор-1-метил-пропилового эфира.
На Фиг.5 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 4-фтор-бензилового эфира.
На Фиг.6 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 2-(4-фтор-фенокси)-этилового эфира.
На Фиг.7 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 2,2,2-трифтор-1-метил-этилового эфира.
На Фиг.8 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 2,2,2-трифтор-1-трифторметил-этилового эфира.
На Фиг.9 показана ингибирующая VKER активность 4-(4-гидрокси-2-оксо-2H-хромен-3-илметил)-бензойной кислоты 2,2,2-трифтор-1-метил-1-трифторметил-этилового эфира.
На Фиг.10 показана ингибирующая VKER активность варфарина.
На Фиг.11 показана ингибирующая VKER активность 4-[(4-гидрокси-2-оксо-2H-хромен-3-ил)метил]бензойной кислоты.
На Фиг.12 показано влияние фторирования на метаболизм с участием цитохрома P450 и эстеразы в собранных в группу микросомах человека. Отношения площадей пиков показаны для инкубации микросом в присутствии (заполненные столбики) или отсутствии (пустые столбики) NADPH. Заполненные столбики соответствуют CYP450 + эстераза, а незаполненные - только эстеразе.
На Фиг.13 показано влияние фторирования на метаболизм с участием цитохрома P450 и эстеразы в собранных в группу микросомах человека. Отношения площадей пиков показаны для инкубации микросом в присутствии (заполненные столбики) или отсутствии (пустые столбики) NADPH. Заполненные столбики соответствуют CYP450 + эстераза, а незаполненные - только эстеразе.
На Фиг.14 показано отсутствие исходного соединения в группе микросом человека, содержащих NADPH, при отсутствии (сплошные столбики) параоксона или в присутствии (незаполненные столбики) параоксона - известного ингибитора эстеразы.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном аспекте объектом изобретения являются соединения формулы I-a, т.е. соединения формулы I, где n равно 0, 1, 2 или 3.
В другом аспекте объектом изобретения являются соединения формулы I-b, т.е. соединения формулы I-a, где R1 представляет собой Н или -(C1-C4 алкил)-CO2R2; где R2 представляет собой Н.
В ином аспекте объектом изобретения являются соединения формулы I-c, т.е. соединения формулы I-b, где n равно 1 и R3 представляет собой галоген.
В другом аспекте объектом изобретения являются соединения формулы I-d, т.е. соединения формулы I-b, где n равно 0.
В ином аспекте объектом изобретения являются соединения формулы I-e, т.е. соединения формулы I-c или I-d, где p равно 1.
Согласно еще одному аспекту объектом изобретения являются соединения и соли формулы II, т.е. соединения формулы I, имеющие формулу:
Формула II
где:
n равно 0, 1 или 2;
R1 представляет собой Н или CH2COOH;
R3 в каждом случае независимо представляет собой галоген, OH, C1-C6 алкил, C1-C6 алкокси, C1-C4 галогеналкил или C1-C4 галогеналкокси; и
R20, R30, и R40 независимо означают H, -(C0-C6 алкил)-COR5, -(C1-C6 алкил)-COR5, -(C0-C6 алкил)-O-R6, галоген, OH, амино, моно или диалкиламино, гидроксиалкил, C1-C4 галогеналкил или C1-C4 галогеналкокси, где
R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 или 2 группами, которые независимо означают OH, C1-C4 алкокси, пиперидинил, пирролидинил, морфолинил, пиперазинил, C3-C7 циклоалкил, -SO2-(C1-C4 алкил), -SO2-(C1-C4 галогеналкил) или -SO2-фенил, OH, амино, моно или диалкиламино или C1-C6 галогеналкокси, необязательно замещенный 1 OH, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино;
и
R6 представляет собой С1-C6 алканоил, фенил C1-C6 алканоил, (C1-C6 алкил)-O-фенил, фенил C1-C6 алкил или фенил, где алкильные части алканоильных групп необязательно замещены одним или несколькими галогенами и где фенильные группы необязательно замещены 1, 2, 3, 4 или 5 группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В другом аспекте объектом изобретения являются соединения формулы II-a, т.е. соединения формулы II, где R1 представляет собой Н.
В ином аспекте объектом изобретения являются соединения формулы II-b, т.е. соединения формулы II-a, где R20 представляет собой -(C0-C6 алкил)-COR5.
В другом аспекте объектом изобретения являются соединения формулы II-c, т.е. соединения формулы II-b, где R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 или 2 группами, которые независимо означают OH, C1-C4 алкокси, пиперидинил, пирролидинил, морфолинил, пиперазинил, C3-C7 циклоалкил, -SO2-(C1-C4 алкил), -SO2-(C1-C4 галогеналкил) или -SO2-фенил, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В ином аспекте объектом изобретения являются соединения формулы II-d, т.е. соединения формулы II-c, где R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 группой, представляющей собой пиперидинил, пирролидинил, морфолинил или пиперазинил, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В ином аспекте объектом изобретения являются соединения формулы II-e, т.е. соединения формулы II-c, где R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 группой, представляющей собой -SO2-(C1-C4 алкил), -SO2-(C1-C4 галогеналкил) или -SO2-фенил, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В другом аспекте объектом изобретения являются соединения формулы II-f, т.е. соединения формулы II-c, где R5 представляет собой С1-C6 алкокси, необязательно замещенный C3-C7 циклоалкилом (предпочтительно C3-C6 циклоалкилом, предпочтительней C3-C5 циклоалкилом, еще более предпочтительно, циклопропилом), где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В ином аспекте объектом изобретения являются соединения формулы II-g, т.е. соединения формулы II-b, где R5 означает OH, амино, моно или диалкиламино или C1-C6 галогеналкокси.
В другом аспекте объектом изобретения являются соединения формулы II-h, т.е. соединения формулы II-g, где R5 означает амино или моно или ди(C1-C6 алкил)амино.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-i, т.е. соединения формулы II-b, где R5 представляет собой С1-C6 галогеналкокси, необязательно замещенный 1 OH.
В другом аспекте объектом изобретения являются соединения формулы II-j, т.е. соединения формулы II-i, где R5 означает -CH2C(галоген)2C(галоген)3, -CH2CH2C(галоген)3, где каждый галоген независимо представляет собой F или Cl.
В ином аспекте объектом изобретения являются соединения формулы II-k, т.е. соединения формулы II-j, где R5 означает -CH2CF2CF3, -CH2CH2CF3.
В другом аспекте объектом изобретения являются соединения формулы II-l, т.е. соединения формулы II-i, где R5 означает -CH(CH3)C(галоген)2C(галоген)3, -CH(CH2галоген)2, -CH(CH3)C(галоген)3, -CH(C(галоген)3)2, -C(CH3)(C(галоген)3)2 или -CH(OH)C(галоген)3, где каждый галоген независимо представляет собой F или Cl.
В другом аспекте объектом изобретения являются соединения формулы II-l1, т.е. соединения формулы II-i, где R5 означает -CH(CH3)CF2CF3, -CH(CH2F)2, -CH(CH3)CF3, -CH(CF3)2, -C(CH3)(CF3)2 или -CH(OH)CF3.
В ином аспекте объектом изобретения являются соединения формулы II-m, т.е. соединения формулы II-l, где R5 означает -C(CH3)(C(галоген)3)2 предпочтительно каждый галоген является F.
В ином аспекте объектом изобретения являются соединения формулы II-n, т.е. соединения формулы II-l, где R5 означает -CH(OH)C(галоген)3. В одном случае стереогенный центр в R5 имеет S-конфигурацию. В другом случае стереогенный центр в R5 имеет R-конфигурацию.
В другом аспекте объектом изобретения являются соединения формулы II-o, т.е. соединения согласно любой из формул II-a, II-b, II-c, II-d, II-e, II-f, II-g, II-h, II-i, II-j, II-k, II-l, II-l1, II-m или II-n, где по меньшей мере один из R30 и R40 представляет собой Н.
В ином аспекте объектом изобретения являются соединения формулы II-p, т.е. соединения формулы II-o, где один из R30 и R40 представляет собой галоген (в одном аспекте F или Cl), OH, амино, моно или ди(C1-C4)алкиламино, гидрокси(C1-C4)алкил, CF3 или OCF3.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q, т.е. соединения формулы II-o, где оба: и R30, и R40 являются H.
В другом аспекте объектом изобретения являются соединения формулы II-q1, т.е. соединения согласно любой из формул II-o, II-p или II-q, где n равно 1.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q2, т.е. соединения формулы II-q1, где R3 представляет собой галоген, OH, C1-C4 алкил, C1-C4 алкокси, C1-C2 галогеналкил или C1-C2 галогеналкокси.
В ином аспекте объектом изобретения являются соединения формулы II-q3, т.е. соединения формулы II-q2, где R3 представляет собой галоген, OH, C1-C4 алкил, C1-C4 алкокси, CF3 или OCF3.
В ином аспекте объектом изобретения являются соединения формулы II-q4, т.е. соединения формулы II-q3, где R3 представляет собой галоген.
В другом аспекте объектом изобретения являются соединения формулы II-q5, т.е. соединения формулы II-q3, где R3 означает ОН, C1-C4 алкил или C1-C4 алкокси.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q6, т.е. соединения формулы II-q3, где R3 представляет собой CF3 или OCF3.
В ином аспекте объектом изобретения являются соединения формулы II-q7, т.е. соединения согласно любой из формул II-o, II-p или II-q, где n равно 0.
В другом аспекте объектом изобретения являются соединения формулы II-q8, т.е. соединение согласно формуле II-a, где R20 обозначает (C0-C6 алкил)-OR6.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q9, т.е. соединения формулы II-q8, где R6 представляет собой С1-C6 алканоил, где алкильная часть алканоильной группы замещена одним или несколькими галогенами (предпочтительно F или Cl, предпочтительней F.) Или R6 может обозначать -(C1-C4 алкил)-фенил, -(C1-C4 алканоил)-фенил или фенил, где фенильные группы необязательно замещены 1, 2, 3, 4 или 5 группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил (такой как CF3), C1-C4 галогеналкокси (такой как OCF3), амино или моно или ди C1-C6 алкиламино.
В ином аспекте объектом изобретения являются соединения формулы II-q10, т.е. соединение согласно формуле II-q9, где R20 представляет собой -(С0-C6 алкил)-O-R6.
В ином аспекте объектом изобретения являются соединения формулы II-q11, т.е. соединение согласно формуле II-q10, где R20 представляет собой -(С0-C4 алкил)-O-R6.
В другом аспекте объектом изобретения являются соединения формулы II-q12, т.е. соединения согласно любой из формул II-q8, II-q9, II-q10 или II-q11, где по меньшей мере один из R30 и R40 представляет собой Н.
В ином аспекте объектом изобретения являются соединения формулы II-q13, т.е. соединения формулы II-q12, где один из R30 и R40 представляет собой галоген (в одном аспекте F или Cl), OH, амино, моно или ди(C1-C4)алкиламино, гидрокси(C1-C4)алкил, CF3 или OCF3.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q14, т.е. соединения формулы II-q12, где оба: и R30, и R40 являются H.
В другом аспекте объектом изобретения являются соединения формулы II-q15, т.е. соединения согласно любой из формул II-q8, II-q9, II-q10, II-q11, II-q12, II-q13 или II-q14, где n равно 1.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q16, т.е. соединения формулы II-q15, где R3 представляет собой галоген, OH, C1-C4 алкил, C1-C4 алкокси, C1-C2 галогеналкил или C1-C2 галогеналкокси.
В ином аспекте объектом изобретения являются соединения формулы II-q17, т.е. соединения формулы II-q16, где R3 представляет собой галоген, OH, C1-C4 алкил, C1-C4 алкокси, CF3 или OCF3.
В ином аспекте объектом изобретения являются соединения формулы II-q18, т.е. соединения формулы II-q17, где R3 представляет собой галоген.
В другом аспекте объектом изобретения являются соединения формулы II-q19, т.е. соединения формулы II-q17, где R3 означает ОН, C1-C4 алкил или C1-C4 алкокси.
Согласно еще одному аспекту объектом изобретения являются соединения формулы II-q20, т.е. соединения формулы II-q17, где R3 представляет собой CF3 или OCF3.
В ином аспекте объектом изобретения являются соединения формулы II-q21, т.е. соединения согласно любой из формул II-q8, II-q9, II-q10, II-q11, II-q12, II-q13 или II-q14, где n равно 0.
В другом аспекте объектом изобретения являются соединения формулы II-r, т.е. соединения формулы II, где R1 представляет собой CH2COOH.
В ином аспекте объектом изобретения являются соединения формулы II-s, т.е. соединения формулы II-r, где R20 представляет собой -(С0-C6 алкил)-COR5.
В другом аспекте объектом изобретения являются соединения формулы II-t, т.е. соединения формулы II-s, где R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 или 2 группами, которые независимо означают OH, C1-C4 алкокси, пиперидинил, пирролидинил, морфолинил, пиперазинил, C3-C7 циклоалкил, -SO2-(C1-C4 алкил), -SO2-(C1-C4 галогеналкил) или -SO2-фенил, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В ином аспекте объектом изобретения являются соединения формулы II-u, т.е. соединения формулы II-t, где R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 группой, представляющей собой пиперидинил, пирролидинил, морфолинил или пиперазинил, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В ином аспекте объектом изобретения являются соединения формулы II-v, т.е. соединения формулы II-t, где R5 представляет собой С1-C6 алкокси, необязательно замещенный 1 группой, представляющей собой -SO2-(C1-C4 алкил), -SO2-(C1-C4 галогеналкил) или -SO2-фенил, где циклические части указанного выше необязательно замещены в позиции возможного замещения группами, которые независимо означают C1-C4 алкил, C1-C4 алкокси, галоген, OH, C1-C4 галогеналкил, C1-C4 галогеналкокси, амино или моно или диалкиламино.
В другом аспекте объектом изобретения являются соединения формулы II-w, т.е. соединения формулы II-t, где R5 представляет