Биоадгезивная жидкая композиция, по существу свободная от воды
Иллюстрации
Показать всеКомпозиция по изобретению предназначена для прилипания к поверхности тела, в частности к поверхности эпидермиса или слизистой оболочки. Композиция содержит частицы способного к набуханию в воде полимера, суспендированные в жидком разбавителе, способном смешиваться с водой. Частицы полимера содержат анионный полимер, представляющий собой альгинат, ксантановую смолу или соль целлюлозы. Жидкий разбавитель свободен от воды или включает количество воды, недостаточное для полного набухания частиц полимера. Композиция не включает дополнительного фармацевтически активного вещества. Композиция по изобретению при смешивании с водой загустевает с образованием прилипшего слоя в области целевой поверхности тела, обеспечивая барьер поверх поврежденной поверхности, предотвращая или облегчая воспаление или повреждение. 3 н. и 8 з.п. ф-лы, 12 ил., 3 табл.
Реферат
Настоящее изобретение относится к органическим композициям. Более точно настоящее изобретение относится к жидким композициям, способным к загустеванию при использовании и/или прилипанию к поверхности; в частности, но не исключительно, к поверхности эпидермиса или слизистой оболочки.
Альгинатные композиции применяются в медицине, например, чтобы облегчать последствия рефлюкс-эзофагита. Однако такие композиции, хотя и полезны, не предназначены для прилипания к поверхности слизистой оболочки пищевода.
В US-B-6391294 описывается фармацевтически приемлемый полимерный материал, сформированный in situ на поверхности тела посредством реакции анионного полимера с катионным полимером в присутствии воды. Эти полимеры могут применяться в виде раздельных композиций или в виде единой композиции в неводном носителе и реагировать друг с другом in situ.
International Journal of Pharmaceutics, 238, 2002, 123-132 описывает применение водных альгинатных растворов в качестве биоадгезивов внутри пищевода.
Было бы выгодно создать композицию, способную загустевать в области целевой поверхности тела и/или прилипать к ней.
В первом аспекте настоящее изобретение включает жидкую композицию для прилипания к поверхности, которая содержит способные к набуханию в воде частицы полимера, суспендированные в жидком разбавителе, способном смешиваться с водой, где жидкий разбавитель по существу свободен от воды или включает количество воды, недостаточное для полного набухания частиц полимера, где частицы полимера не включают ни анионных полимерных частиц, ни катионных полимерных частиц.
Хотя композиция могла бы применяться в области домашнего хозяйства, предпочтительно композиция для прилипания к поверхности тела. Способный смешиваться с водой жидкий разбавитель предпочтительно является фармацевтически приемлемым разбавителем. В предпочтительных вариантах осуществления изобретения композиция является терапевтической композицией.
Далее следует описание композиции по изобретению, предназначенной для терапевтического применения. Нетерапевтические применения будут описаны позже. Ссылки на последующих страницах на природу композиции - например, на природу частицы, тип разбавителя, который может использоваться, подходящие анионные полимеры, которые могут использоваться, и т.д. - применимы также к нетерапевтическим применениям.
Композиция по настоящему изобретению находится, таким образом, в форме суспензии частиц. Данные частицы сохраняются в композиции до ее применения в виде частиц, предпочтительно по существу без набухания. Их размер может колебаться в широких пределах - от видимого невооруженным глазом до микроскопического. Суспензия может находиться в форме гомогенной дисперсии. Композиция может быть смешана с водой ex vivo (например, в стакане), например, непосредственно перед применением. Альтернативно, она может быть смешана с водой in vivo, например, во рту (воду предоставляет слюна). Однако когда вода введена, она вызывает набухание полимерных частиц, позволяя им слипаться, повышает вязкость композиции и приводит к тому, что по меньшей мере часть из них прилипает к поверхности тела. Частицам необязательно проявлять растворение в воде, но в предпочтительных вариантах осуществления они частично или полностью растворяются в воде. Однако во всех вариантах осуществления вода заставляет частицы, до этого находившиеся в безводной среде или среде с низким содержанием воды, набухать.
Предпочтительно, чтобы прилипший слой предотвращал или облегчал воспаление или повреждение. Он может позволить поверхности зажить, обеспечив барьер поверх поврежденной поверхности, чтобы защитить ее от дальнейшего воспаления или повреждения.
Альтернативно или в дополнение прилипшее покрытие является таким, которое способствует абсорбции через поверхность тела активного фармакологического вещества. Активное фармакологическое вещество может вводиться в процессе изготовления композиции или вводиться отдельно. Оно может быть нанесено вниз как часть покрытия или может быть отдельным, но абсорбироваться через покрытие при применении.
Поверхность тела могла бы быть поверхностью эпидермиса. Поверхность эпидермиса может быть любая наружная поверхность кожи. Поврежденной кожей может быть кожа, которая покрыта пузырями, обожжена огнем, воспалена, покрыта пустулами, обожжена солнцем, подверглась укусу или ужалению.
Поверхностью тела может быть поверхность слизистой оболочки. Поверхностью слизистой оболочки может быть любая внутренняя поверхность тела. Примеры включают рот (включая язык), нос, глаза, глотку, пищевод, желудок, влагалище и прямую кишку.
Поверхность тела может быть рваной или разрезанной поверхностью, например обнаженной поверхностью мышцы, обнажившейся вследствие раны или другой травмы.
Композиция по изобретению может служить композицией для гидратации или смягчения кожи, или композицией для обработки волос или удаления волос.
Композиция по изобретению может быть стоматологической композицией, например фиксирующей зубной протез.
Когда композиция по настоящему изобретению смешивается с водой слюны, она предпочтительно предназначается для прилипания к поверхности желудочно-кишечной трубки, предпочтительно к пищеводу, и наиболее предпочтительно к нижнему отделу пищевода. Тем не менее, она может предназначаться для прилипания к другой поверхности, например, поверхности рта или глотки, например, чтобы уменьшить изъязвление рта или воспаление глотки.
Предпочтительно, чтобы интервал между смешиванием с водой и достижением благоприятной степени набухания находился в пределах 1-60 секунд, наиболее предпочтительно 2-30 секунд.
Подходящий полимер предпочтительно представляет собой такой, который способен набухать в воде, нетоксичен и не набухает в разбавителе.
Соответственно, полимер может быть анионным, катионным или неионным. Могут применяться комбинации таких полимеров, за исключением комбинаций анионных и катионных полимеров, из-за возможного взаимодействия между ними. Таким образом, в качестве полимера соответственно могут применяться в любой заданной композиции следующие:
- Только анионный(ые) полимер(ы). Эта композиция особенно предпочтительна. В пределах данного определения могут использоваться смешанные анионные полимеры, но предпочтительно, чтобы использовался только один анионный полимер.
- Только неионный(ые) полимер(ы). Эта композиция предпочтительна. В пределах данного определения могут использоваться смешанные неионные полимеры, но предпочтительно, чтобы использовался только один неионный полимер.
- Только катионн(ые) полимер(ы). Эта композиция предпочтительна. В пределах данного определения могут использоваться смешанные катионные полимеры, но предпочтительно, чтобы использовался только один катионный полимер.
- Анионный(ые) полимер(ы) и неионный(ые) полимер(ы) вместе. В пределах этого определения могут использоваться смешанные анионные полимеры и/или смешанные неионные полимеры, но предпочтительно, чтобы использовался только один анионный полимер и один неионный полимер.
- Катионный(ые) полимер(ы) и неионный(ые) полимер(ы) вместе. В пределах этого определения могут использоваться смешанные катионные полимеры и/или смешанные неионные полимеры, но предпочтительно, чтобы использовался только один катионный полимер и один неионный полимер.
Примеры подходящих анионных полимеров даны, например, в US-В-6391294. Предпочтительные анионные полимеры включают растворимые в воде соли гиалуроновой кислоты, соли альгиновых кислот (например, альгинаты, такие как соли щелочных и щелочно-земельных металлов, например альгинат натрия, альгинат калия, альгинат кальция и альгинат магния), ксантановую смолу, гуммиарабик, пектины, кислые производные полисахаридов, предпочтительно материалы, содержащие уроновую кислоту, например, гиалуроновые кислоты или стеркулию, соли каррагинанов и полимолочные кислоты, и растворимые в воде производные целлюлозы (например, натриевую соль карбоксиметилцеллюлозы).
Более предпочтительными анионными полимерами для использования в настоящем изобретении являются полимеры, способные набухать в воде, предпочтительно растворимые в воде соли альгиновых кислот (т.е. альгинаты) и способные набухать в воде, предпочтительно растворимые в воде соли производных целлюлозы.
Пример подходящих катионных полимеров даны, например, в US-B-6391294. Предпочтительные катионные полимеры включают соли хитозана (например, хитозана хлорид, хитозана ацетат), диэтиламиноэтилдекстран, соли хондроитина, полилизин, дерматан и кератин.
Примеры подходящих неионных полимеров включают производные целлюлозы (например, метилцеллюлозу, гидроксиэтилпропилцеллюлозу, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу) и крахмал, и производные крахмала.
Полимерные частицы в ненабухшем состоянии предпочтительно имеют средний размер частицы от 30 до 500 микрометров, особенно от 50 до 200 микрометров, особенно от 90 до 125 микрометров. Для измерения среднего размера частиц они могут быть разделены на фракции посредством просеивания перед приготовлением композиции по изобретению.
Композиция предпочтительно содержит от 2 до 90 мас.% упомянутых полимерных частиц, основываясь на общей массе композиции, более предпочтительно от 5 до 70 мас.%, еще более предпочтительно от 20 до 60 мас.%, и наиболее предпочтительно от 30 до 50 мас.%.
Под «водой» здесь также подразумеваются водные жидкости, например слюна.
Неводная жидкость сама по себе, разумеется, фармацевтически приемлема. Предпочтительные неводные жидкости включают или состоят из одноатомных спиртов, многоатомных спиртов, сахарных спиртов и сахарных полиолов.
Подходящие одноатомные спирты включают этанол и изопропиловый спирт.
Подходящие многоатомные спирты включают глицерин, гликоли, полиалкиленгликоли или их смеси. Подходящим гликолем, например, является пропиленгликоль. Подходящим полиалкиленгликолем является полиэтиленгликоль, предпочтительно с молекулярной массой по меньшей мере 100, предпочтительно по меньшей мере 200. Предпочтительно, чтобы молекулярная масса составляла до 1000, более предпочтительно - до 700, наиболее предпочтительно - до 400.
Подходящим сахарным полиолом является гидрогенизированный сироп глюкозы (LYCASIN (RTM)).
Фармацевтически приемлемый жидкий разбавитель предпочтительно по существу не содержит воду, например, менее 1 мас.% воды, или предпочтительно менее 0,5 мас.% воды от общей массы композиции. Наиболее предпочтителен безводный разбавитель.
Альтернативно фармацевтически приемлемый жидкий разбавитель содержит немного воды. Это может быть полезным, чтобы создать заказанную способность к набуханию анионных полимерных частиц для оптимальной эффективности в требуемом месте. Например, содержание небольшого количества воды в композиции вызовет набухание частиц до некоторой степени, но слипание по существу будет отсутствовать. Когда композиция, включающая предварительно частично набухшие частицы, проглатывается и смешивается со слюной, частицы слипаются и формируют барьерную пленку быстрее, чем предварительно частично не набухшие. По аналогии они могут расцениваться как «содержащие затравку».
В таких вариантах осуществления композиция должна содержать долю воды, достаточную, чтобы послужить «затравкой» для частиц, но не более; значительно загущать композицию до применения нежелательно. Оптимальная доля воды зависит от других компонентов композиции и особенно от жидкого разбавителя. В целом, жидкий разбавитель может содержать 10-70 мас.% воды по массе на массу разбавителя.
Когда жидкий разбавитель представляет собой глицерин, он может содержать до 20% воды, предпочтительно 10-20 мас.% воды по массе на массу разбавителя (т.е. глицерина).
Если жидкий разбавитель представляет собой простой гликоль, предпочтительно пропиленгликоль, он может содержать до 50 мас.% воды, предпочтительно 10-50 мас.% воды, наиболее предпочтительно 25-50 мас.% воды по массе на массу разбавителя (т.е. гликоля).
Если жидкий разбавитель представляет собой полиалкиленгликоль, например, полиэтиленгликоль, он может содержать до 60% воды, предпочтительно 10-60% воды, наиболее предпочтительно 30-60% воды по массе на массу разбавителя (т.е. полиалкиленгликоля). Хотя верхний предел предпочтительно составляет 60% воды по массе на массу разбавителя, если растворитель представляет собой ПЭГ 400, если он представляет собой ПЭГ 200, верхний предел предпочтительно составляет 40%.
Предпочтительно, чтобы параметр растворимости Гильдебранда разбавителя (включая любую присутствующую воду) составлял по меньшей мере 15, предпочтительно по меньшей мере 20 (Дж·см-3)1/2.
Предпочтительно, чтобы параметр растворимости Гильдебранда разбавителя (включая любую присутствующую воду) не превышал 35, предпочтительно не превышал 31 (Дж·см-3)1/2.
Композиция может содержать также активное вещество, особенно когда активное вещество действует на воспаленную или поврежденную поверхность тела, например, пищевод, воспаленный вследствие желудочного рефлюкса, или когда желательно позволить активному веществу абсорбироваться в кровоток через кожу посредством прилипшей композиции. Подходящие активные вещества включают анальгетики, противовоспалительные вещества и жаропонижающие (например, ацетаминофен, ибупрофен, напроксен, диклофенак, кетопрофен, холина салицилат, бензидамин, бупренорфин, гидрокортизон, бетаметазон); антиконгестанты (например псевдоэфедрин, фенилэфрин, оксиметазолин, ксилометазолин); минеральные соли (например, глюконат цинка, ацетат цинка); противокашлевые средства (например, декстрометорфан, кодеин, фолокодин); отхаркивающие средства (например, гвайфенезин, n-ацетилцистеин, бромгексин), антисептики (например, триклозан, хлороксинол, хлорид цетилпиридиния, хлорид бензалкония, амилметакрезол, гексилрезорцинол, дихлорбензиловый спирт, бензиловый спирт, хлорид деквалиния, сульфадиазин серебра); сердечно-сосудистые средства (например, тринитрат глицерина); местноанестезирующие средства (например, лигнокаин, бензокаин); цитопротекторы (например, карбеноксолон, сукралфат, субсалицилат висмута); противоязвенные средства (например, карбонат кальция, бикарбонат натрия, трисиликат магния, магалдрат, циметидин, ранитидин, низатидин, фамотидин, омепразол, пантопразол); антигистаминные средства (например, лоратидин, терфенадин, дифенилгидрамин, хлорфенирамин, трипролидин, акривастин); средства, подавляющие тошноту (например, прохлорперазин, суматриптан), средства, регулирующие деятельность кишечника (например, дифеноксилат, лоперамид, сеннозиды); противогрибковые средства (например, клотримазол); антибиотики (например, фузафунгин, тиротрицин) и антипсориатические средства (например дитранол, кальципотриол). Могут включаться одно или более веществ.
Композиции по настоящему изобретению могут предназначаться только для прилипания к поверхности тела, чтобы лечить ее состояние. Однако в случае поверхности пищевода она может дополнительно выполнять функцию лечения желудочно-кишечного напряжения, такого как рефлюкс-эзофагит, гастрит, диспепсия или пептическая язва. Поэтому в данном аспекте настоящего изобретения композиция может содержать также бикарбонат и, необязательно, вещество, создающие поперечные сшивки в альгинатах, с тем, чтобы композиция, которая достигла желудка, сформировала «плот», препятствующий рефлюксу. Особенно предпочтительный вариант осуществления для такого применения может включать композицию по настоящему изобретению вместе с карбонатом кальция и бикарбонатом натрия, приготовленную в виде препарата, который можно пить.
В соответствии со вторым аспектом включен способ лечения пациента с применением композиции по изобретению как определено выше, прилипшей к поверхности тела пациента. Это может быть осуществлено, например, чтобы предотвратить или облегчить медицинское состояние поверхности тела. Альтернативно или в дополнение это может быть осуществлено, чтобы доставить активное фармакологическое вещество пациенту чрезкожно.
Сверх того изобретение включает применение полимерных частиц в производстве композиции, как определено здесь, для лечения поверхности тела при потребности в профилактическом или восстановительном лечении, или для чрезкожного введения активного фармакологического вещества.
Композиция по настоящему изобретению может быть приготовлена путем смешивания компонентов до образования гомогенной смеси, в типичном случае - гомогенной дисперсии.
Нетерапевтические применения настоящего изобретения представляют собой применения, которые тоже извлекают выгоду из наличия композиции первоначально низкой вязкости, и которая при разбавлении водой становится жидкостью более высокой вязкости, предпочтительно со склонностью прилипать к целевой поверхности. Композиция по настоящему изобретению может найти применение в качестве бытовой чистящей композиции. Например, композиция может применяться в устройстве, которое периодически выпускает композицию согласно первому изобретению в ее неразбавленной, невязкой форме, в унитаз. Композиция может свободно опускаться по унитазу в воду, где она загустевает и прилипает к санитарному фаянсу ниже уровня воды, где она может оказывать очищающее действие. Если полимер представляет собой альгинат, он может предотвращать появление или удалять известковый налет благодаря сильному секвестрирующему действию альгината.
В другом нетерапевтическом варианте осуществления композиция по изобретению может быть частью композиции, заключенной в капсулу, для применения в моечной машине. Инкапсулирующий материал может быть проницаемым для воды, и полимер внутри капсулы по мере проникновения воды внутрь будет набухать и вызовет разрыв капсулы с высвобождением содержимого в моечную машину. После этого полимер высвобождается и может прилипать к твердым поверхностям внутри моечной машины. Таким образом, он может выполнять функцию по борьбе с налетом на поверхностях моечной машины или предотвращению его образования.
Теперь изобретение будет дополнительно описано посредством иллюстрации со ссылкой на следующие совокупности примеров.
Совокупность примеров 1
В этих примерах целью было оценить влияние
- Разбавления разбавителя искусственной слюной на скорость набухания альгинатных частиц.
- Выбора разбавителя композиции на скорость набухания альгинатных частиц.
| Таблица 1 | |
| Материалы | |
| Наименование | Поставщик |
| Protanal LF120L (альгинат натрия) | FMC BioPolymer AS, Drammen, Норвергия |
| 1,9-диметилметиленовый синий (DMMB) | Sigma-Aldrich Company Ltd, Dorset, Англия, Соединенное Королевство. |
| Глицерин 99,5% | Sigma-Aldrich |
| Пропиленгликоль | Sigma-Aldrich |
| ПЭГ 200 | Fluka Chemika |
| ПЭГ 400 | Sigma-Aldrich |
Оборудование
Оптический микроскоп Nikon Labophot, присоединенный к COHU High Performance CCD Camera, связанной с программным обеспечением по анализу изображения Image Proplus v.4.1 (Media Cybernetics, Мэриленд, USA-Supplier Datacell Ltd, Finchampstead, Беркшир, Великобритания).
Vortex Mixer VM20, Chiltern Scientific, Bucks. Великобритания.
Счетная камера гемоцитометра Thoma, глубиной 0,1 мм, 0,0025 мм2, Hawksley, Англия.
Методология
Приготовление искусственной слюны
Искусственная слюна готовилась по следующей формуле: 5 мМ бикарбонат натрия, 7,36 мМ хлорид натрия, 20 мМ хлорид калия, 6,6 мМ моногидрат дигидрофосфата натрия, 1,5 мМ дигидрат хлорида кальция в воде.
Визуальное наблюдение за набуханием одиночной частицы
Одиночная (90-125 мкм) альгинатная частица помещалась в центр счетной камеры гемоцитометра, накрывалась с использованием покровного стекла и покровного стекла, нагруженного с обеих сторон Blu-Tack® (Bostick Ltd, Leicester, Великобритания). 15 мкл гидратирующей жидкости (искусственная слюна:разбавитель:DMMB) вводились с передней стороны камеры вблизи от покровного стекла. Капиллярные силы между поверхностью камеры и покровным стеклом засасывали жидкость между границами раздела и погружали одиночную частицу в жидкость. По мере того, как альгинатная частица гидратировалась, можно было обрисовать слой геля благодаря изменению цвета от синего к фиолетовому при образовании комплекса между DMMB и растворимым альгинатом. Означающее его изменение цвета было возможно наблюдать визуально в двух измерениях, используя оптическую микроскопию (Nikon Labophot). После заданного периода времени программное обеспечение для анализа изображения (Image Pro Plus v.4.0, Media Cybernetics, США) захватывало изображение, и по программным измерениям набухшей области вычислялась степень радиального набухания частицы.
Основанием для использования счетной камеры гемоцитометра было обеспечение фиксированного объема набухания. Расстояние между покровным стеклом и поверхностью камеры создается с точностью до 100 мкм, поэтому альгинатные частицы из просеянной фракции 90-125 мкм, как правило, оказываются в «ловушке», ограничивающей осевое набухание. В результате набухание будет происходить радиально, и степень набухания можно вычислить по двумерному изображению с использованием анализа изображения.
Приготовление гидратирующей жидкости
Гидратирующая жидкость использовалась, чтобы гидратировать альгинатную частицу внутри камеры гемоцитометра. Чтобы определить влияние выбора разбавителя и разбавления разбавителя искусственной слюной на набухание частицы, был приготовлен ряд растворов разбавителя:искусственной слюны (0-100 мас.%/мас.). Были исследованы следующие растворители:
- Глицерин
- 70:30 мас./мас. глицерина:пропиленгликоля
- 40:60 мас./мас. глицерина:пропиленгликоля
- Пропиленгликоль
- ПЭГ 200
- ПЭГ 400
К гидратирующей жидкости (смеси разбавителя: искусственной слюны) был добавлен 1,9-диметилметиленовый синий (DMMB). DMMB представляет собой катионный краситель, который образует комплексы с солюбилизированным альгинатом натрия, и получающееся в результате изменение цвета от синего к фиолетовому обрисовывает слой геля набухшей частицы. Концентрация разбавителя в гидратирующей жидкости определяет количество добавленного DMMB (350-1490 мкМ). Количество добавленного DMMB было минимальной концентрацией, необходимой для визуального наблюдения.
Результаты и обсуждения
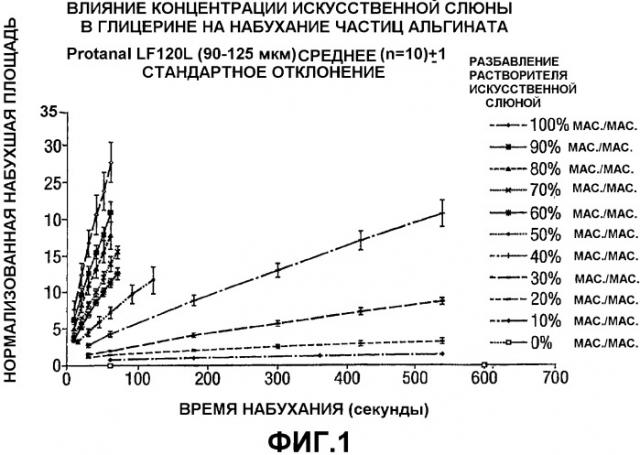
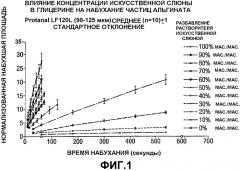
Фиг.1 показывает набухание одиночных альгинатных частиц в глицерине и иллюстрирует, как характер набухания изменяется при разбавлении искусственной слюной. В 100%-ном разбавителе (т.е. при 0 мас.%/мас. разбавлении разбавителя) альгинатные частицы не набухали, поскольку с течением времени никаких изменений в области частицы не было. Однако по мере того, как для гидратации альгинатной частицы использовались возрастающие разбавления глицерина искусственной слюной, скорость набухания, вычисленная по градиенту нормализованной области против времени, увеличивалась (Фиг.1 и 2).
Из результатов, показанных на Фиг.1 и 2, следует, что отношения между скоростью набухания альгинатной частицы и возрастающим разбавлением глицерина искусственной слюной можно рассматривать как имеющие две основные особенности. Во-первых, отношения могут быть характеризованы с точки зрения начальной фазы. Начальная фаза представляет ряд разбавлений разбавителя, во время которых взвешенные альгинатные частицы остаются в ненабухшем состоянии. Во-вторых, при критическом уровне разбавления наблюдается выход за пределы начальной фазы и увеличение скорости набухания при последующем разбавлении (активная фаза).
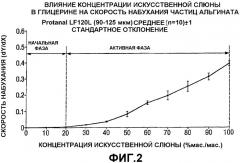
Фиг.3 показывает, что отношения между скоростью набухания и разбавлением разбавителя были индивидуальными для каждого разбавителя.
Различные разбавители проявляли различия как в уровне разбавления, необходимом, чтобы выйти за пределы начальной фазы, т.е. разбавлении разбавителя, необходимом, чтобы началось набухание частиц, так и, после входа в активную фазу, в чувствительности скорости набухания к дальнейшему разбавлению. Было отчетливо видно, что альгинатные частицы начали набухать примерно в 25 мас.%/мас. глицерине:искусственной слюне. Однако чтобы вызвать набухание в ПЭГ 400, было необходимо разбавить разбавитель до 60 мас.%/мас., используя искусственную слюну.
Эти шесть разбавителей предлагают ряд степеней набухания при разбавлении и предоставляют средство управления степенью разбавления разбавителя, необходимой, чтобы активировать набухание.
Энтальпия испарения представляет собой количество энергии, необходимое, чтобы преобразовать чистую жидкость в газ. При преобразовании жидкости в газ необходимо полностью разделить отдельные молекулы жидкости, поэтому энтальпия испарения является непосредственной мерой количества ван-дер-ваальсовых сил, удерживающих молекулы жидкости вместе.
Во время смешивания растворителя и растворенного вещества раствор должен разрушить ван-дер-ваальсовы взаимодействия между молекулами растворителя способом, аналогичным испарению. Следовательно, энтальпия испарения растворителя, которая является мерой силы ван-дер-ваальсова взаимодействия между молекулами растворителя, может предоставить признак характера изменения растворяющей способности. Характер изменения растворяющей способности конкретного разбавителя может быть выражен через параметр растворимости Гильдебранда (δ), который вычисляется как квадратный корень из плотности энергии когезии.
Параметр растворимости Гильдебранда (δ)=(ΔE/V)0,5
(ΔE/V) = Плотность энергии когезии
Таким образом, параметр растворимости Гильдебранда растворителя дает меру ван-дер-ваальсовых сил между молекулами растворителя и может использоваться, чтобы оценить характер изменения растворяющей способности ряда разбавителей.
В контексте данной работы растворители, использовавшиеся для набухания альгинатных частиц, представляли собой 6 разбавителей:
- Глицерин
- Пропиленгликоль
- 70:30 мас./мас. смесь глицерина:пропиленгликоля
- 40:60 мас./мас. смесь глицерина:пропиленгликоля
- ПЭГ 200
- ПЭГ 400
Считается, что параметр растворимости Гильдебранда разбавителя имеет значение для настоящего изобретения. Это можно вычислить с использованием метода вклада групп (ссылки: Sperling, L.H.< Introduction to Physical Polymer Science, 3rd ED 2001, Wiley; Cowie J.M.G, Polymer Chemists and Physics of Modern Materials, 2nd ed 1991, Glasgow:Blackie)
Параметр растворимости Гильдебранда вычислялся для каждого разбавителя как показано в таблице 2.
| Таблица 2 | |
| Разбавитель | Параметр растворимости Гильдебранда (Дж·см-3)1/2 |
| Глицерин | 28,77 |
| 70:30 мас./мас. глицерин:пропиленгликоль | 26,99 |
| 40:60 мас./мас. глицерин:пропиленгликоль | 25,22 |
| Пропиленгликоль | 22,81 |
| ПЭГ 200 | 21,83 |
| ПЭГ 400 | 20,81 |
Параметр растворимости Гильдебранда для каждого разбавителя предоставляет меру сил когезии между отдельными молекулами разбавителя, и представляется возможным использовать параметр растворимости Гильдебранда, чтобы понять отношения между скоростью набухания частиц и степенью разбавления растворителя.
Фиг.4 и 5 связывают параметр растворимости Гильдебранда с моделированной скоростью набухания при 80 мас.%/мас. разбавлении растворителя и степенью растворения, необходимой, чтобы показать набухание частицы.
Совокупность примеров 2
В этих примерах исследовалось влияние выбора разбавителя на набухание взвешенных альгинатных частиц, когда их наносили на слизистую оболочку пищевода.
На основании результатов совокупность примеров 1 было предположено, что когда композиция поступает в верхний отдел желудочно-кишечного тракта, взвешенный альгинат начинает набухать, поскольку разбавитель разбавляется слюной, находящейся на поверхности слизистой оболочки. Контакт между набухающим альгинатом и поверхностью слизистой оболочки, по-видимому, должен привести к формированию набухшей биоадгезивной пленки, покрывающей поверхность ткани. Набухание взвешенных частиц на границе раздела между слизистой оболочкой и композицией может быть решающим для создания биоадгезивного слоя.
Чтобы понять влияние выбора разбавителя на изменение характера набухания альгинатных частиц на границе раздела композиции:слизистой оболочки, было желательно визуально наблюдать микроструктуру биоадгезивной пленки по мере того, как она создается на поверхности слизистой оболочки.
Оборудование
Под «Макроскоп» подразумевается цифровая камера Cool Snap Pro, присоединенная к объективу Nikon AF Micro Nikkor 60 мм f/2.8D, соединенная через PCI интерфейс CoolSnap Pro с персональным компьютером Pentium PIII 1 ГГц. Анализ изображения был выполнен с использованием Image ProPlus v4 (Media Cybernetics, Мэриленд, USA-Supplier Datacell Ltd, Finchampstead, Беркшир, Великобритания).
Счетная камера гемоцитометра Thoma 0,1 мм, 0,0025 мм2, Hawksley, Англия.
Методология
Приготовление ткани слизистой оболочки
Свежий свиной пищевод изымался немедленно после забоя в фосфатно-солевой буфер и перевозился на льду. Мускулатура удалялась путем препарирования в пределах одного часа после забоя, оставляя чистую трубку эпителиальной ткани. Срез ткани 25 мм ×50 мм прикреплялся к предметному стеклу микроскопа с использованием цианоакрилатного клея (Super Glue®, Loctite (Ирландия) Ltd), гидратировался в 40 мл 0,9 мас.%/об. NaCl в течение 1 минуты и промывался искусственной слюной перед тем, как помещался под Макроскоп.
Приготовление композиции
Были приготовлены следующие разбавители, каждый из которых содержал DMMB в концентрации 1,9 ммоль.
- Глицерин
- Пропиленгликоль
- ПЭГ 200
- ПЭГ 400
- 70:30 мас./мас. смесь глицерина:пропиленгликоля
- 40:60 мас./мас. смесь глицерина:пропиленгликоля
Каждый раствор затем использовался для приготовления 40 мас.%/мас. суспензии альгината натрия. Приготовление производилось путем отвешивания соответствующего количества разбавителя и альгината, а затем перемешивания этих двух материалов в стеклянном флаконе лопаточкой.
Нанесение композиции на ткань слизистой оболочки
Суспензия альгината наносилась на поверхность ткани путем заполнения открытой камеры предметного стекла гемоцитометра и опрокидывания ее на поверхность ткани. Стекло гемоцитометра гарантировало, что по поверхности ткани распределялся одинаковый монослой суспензии.
Захват и анализ изображения
Набухание взвешенных альгинатных частиц визуально наблюдалось с использованием Макроскопа. Макроскоп можно описать как макроскопическую линзу, прикрепленную к цифровой камере, соединенной с персональным компьютером, позволяющим захватывать цифровые изображения, делающие видимой микроструктуру биоадгезивной пленки. Поскольку альгинатные частицы гидратировались на поверхности слизистой оболочки и образовывали комплексы с DMMB, набухшая область была очерчена изменением цвета от синего к фиолетовому. Программа анализа изображений захватывала изображение после заданного периода времени и преобразовала ряд изображений в фильм, запечатлевающий степень набухания частицы с течением времени. Затем на все изображение помещалась цифровая сетка, и выполнялся анализ изображения определенных частиц, отобранных в соответствии с их особым соотнесением с сеткой. Измерение степени радиального набухания частиц дало представление о характеристиках формирования набухшей области альгината внутри биоадгезивной пленки.
Макроскоп показал, что когда композиция помещалась на поверхность слизистой оболочки, взвешенные альгинатные частицы начинали гидратироваться и набухать. Наличие в разбавителе DMMB означало, что когда частицы начали набухать, появилось цветовое изменение от синего к фиолетовому из-за образования комплекса альгината:DMMB. Использование программного обеспечения для анализа изображения дало возможность измерить изменение в набухшей области взвешенных альгинатных частиц с течением времени.
Фиг.6 иллюстрирует изменение в набухшей области альгинатных частиц, взвешенных в ряде разбавителей, когда их помещали на слизистую оболочку пищевода.
Результаты на Фиг.6 означают, что скорость, с которой альгинатные частицы набухают, будучи помещенными на слизистую оболочку пищевода, может модулироваться выбором разбавителя. Как проиллюстрировано в таблице 3, выбор разбавителя влиял как на скорость набухания между 0-й и 360-й секундами, так и на степень набухания.
| Таблица 3 | ||
| Разбавитель | Скорость набухания (Изменение в нормализованной набухшей области/время)Среднее (n=30)±1 станд. отклонение | Степень набухания при t=360 секунд (Нормализованная набухшая область) Среднее (n=30)±1 станд. отклонение |
| Глицерин | 1,71×10-3±3,14×10-4 | 0,5049±0,0773 |
| 70:30 мас./мас. Глицерин: пропиленгликоль | 1,07×10-3±2,46×10-4 | 0,3299±0,0776 |
| 40:60 мас./мас. Глицерин: пропиленгликоль | 8,2×10-4±8,2×10-4 | 0,2763±0,0620 |
| Пропиленгликоль | 5,9×10-4±1,16×10-4 | 0,2002±0,0378 |
| ПЭГ 200 | 6,0×10-4±6,5×10-5 | 0,1997±0,0292 |
| ПЭГ 400 | 4,6×10-4±6,57×10-5 | 0,1518±0,0231 |
Скорость и степень набухания на слизистой оболочке пищевода альгината, взвешенного в разбавителе
Композиция - 40 мас.%/мас. альгината (Protanal LF120L 90-125 мкм):разбавитель
Скорость набухания подсчитывалась между 90-360 секундами.
Фиг.6 иллюстрирует, что частицы, взвешенные в разбавителях, содержащих глицерин, набухали наиболее быстро, и что различные разбавители проявляли различия в равновесной набухшей области и скорости набухания перед достижением равновесия. Например, частицы, взвешенные в ПЭГ 400, начинали выходить на плато в нормализованной набухшей области 0,28, однако частицы, взвешенные в глицерине, при подобной набухшей области все еще быстро набухали. Ясно, что выбор разбавителя влияет на набухание частицы.
Совокупность примеров 3
Эти примеры были выполнены, чтобы исследовать отношения между биоадгезией и набуханием.
Оборудование
Agilent UV-Visible System 8453 (Agilent Technologies UK Td, Стокпорт, Англия)
Измеритель распадаемости Erweka ZT44 USP/BP (Copley-Instruments, Ноттингем, Англия).
Методология
Схема
Адгезия композиции измерялась путем выворачивании отрезка свиного пищевода на пластмассовой трубке и прикрепления к измерителю распадаемости USP, машины, создающей вертикальные возвратно-поступательные движения, окунающие слизистую оболочку в суспензию 40 мас.%/мас. разбавителя:Protanal LF120L (90-125 мкм). Затем ткань и прилипшая композиция промывались в искусственнной слюне (как описано выше) посредством вертикального движения измерителя в промывочной емкости. После заданного периода времени, соотносившегося со степенью общей адгезии, емкость заменялась, чтобы получить примерно 5 наборов проб, каждая из которых содержала измеримое количество (0,7 г·л-1) альгината. После того, как композиция выглядела полностью отделенной (визуальное наблюдение), ткань отделялась от измерителя распадаемости и встряхивалась в течение 2 часов в искусственной слюне, чтобы удалить любые остатки прилипшего материала. Чтобы гарантировать, что весь прилипший альгинат был отделен, после встряхивания слизистую оболочку скоблили, и остаток анализировали на концентрацию альгината.
Подготовка поверхности слизистой оболочки
Свежий свиной пищевод изымался немедленно после забоя в фосфатно-солевой буфер и перевозился на льду. Мускулатура удалялась путем препарирования в пределах одного часа после забоя, оставляя чистую трубку эпителиальной ткани. Затем тканевая трубка рассекалась на 8 см отрезки, и эти отрезки выворачивались на прутке измерителя распадаемости.
Затем прикрепленную ткань осторожно споласкивали и оставляли на 1 минуту в 0,9% хлориде натрия, чтобы привести в равновесие.
Проверка адгезии
Ткань прикрепляли к измерителю распадаемости и опускали в 16 г композиции (40 мас.%/мас. суспензия альгината/разбавителя), и оставляли на 5 секунд. После этого измеритель распадаемости включали, и ткань с прилипшим альгинатом окунали в 18 мл искусственной слюны (37°C) со скоростью и на расстояние, предопределенные фармакопеей США. Окунающее движение промывало поверхность композиции-ткани и вызывало отделение