Способ получения производного индолопирролокарбазола
Иллюстрации
Показать всеНастоящее изобретение относится к способу получения производного индолопирролокарбазола формулы (I) или его фармацевтически приемлемой соли, обладающего противоопухолевой активностью. Изобретение относится также к способу получения индольного соединения формулы (XII), в которой R1 - гидроксизащитная группа, или его фармацевтически приемлемой соли, отличающемуся тем, что осуществляют взаимодействие соединения формулы (XIII), в которой R1 определено выше, Ra и Rb независимо представляют собой С1-С7-алкил, или Ra и Rb вместе образуют С3-С6-алкиленовую группу, или его фармацевтически приемлемой соли, с газообразным водородом при 1-5 атм. в присутствии катализатора гидрирования (предложенного также в качестве нового), состоящего из соединения родия, соединения металла и, необязательно, амина, в инертном растворителе при комнатной температуре, причем соединение родия представляет собой 1-10% родий на угле, окиси алюминия, карбонате кальция или сульфате бария, и соединение металла представляет собой соль никеля (II), железа (II), железа (III), кобальта (II) или кобальта (III). Предложен также способ получения бис-индольного соединения формулы (VIII), в которой R1 - гидроксизащитная группа; Y - водород, С1-С7-алкил, фенил, бензилоксиметил или С7-С12-аралкил, или его фармацевтически приемлемой соли, заключающийся во взаимодействии индольного соединения формулы (XII), в которой R1 - гидроксизащитная группа, или его фармацевтически приемлемой соли с этилмагнийхлоридом или бутилмагнийхлоридом, или с соединением магния формулы (X), в которой Rd - бутил, в инертном растворителе, с последующим осуществлением взаимодействия полученного продукта с малеимидным соединением формулы (IX), в которой X - галоген, a Y определен выше, в инертном растворителе. 4 н. и 11 з.п. ф-лы, 12 табл.
Реферат
Настоящее изобретение применимо в медицине. Более конкретно, настоящее изобретение относится к эффективному способу получения в промышленном масштабе соединения, применимого в медицине.
Полученное в соответствии со способом по настоящему изобретению производное индолопирролокарбазола, представленное формулой (I):
обладает противоопухолевой активностью, и соединение было клинически протестировано (Mitsuru Ohkubo et al., Bioorganic & Medicinal Chemistry Letters, vol. 9, pages 3307-3312, 1999).
Способы получения соединения по настоящему изобретению были раскрыты в WO 95/30682 и WO 01/62769.
Кроме того, в Organic Synthesis Collective Volumes, vol. 7, page 34 раскрыт способ получения производного индолопирролокарбазола, представленного формулой (XII):
в которой R1 представляет собой гидроксизащитную группу.
В дополнение, известна (патент США № 5105012) реакция гидрирования с применением соединения родия, в которой для восстановления нитрогруппы производного нитробензола в кислотном растворителе, таком как уксусная кислота, в качестве катализатора применяется большое количество железного порошка.
Кроме того, в WO 95-30682 раскрыт способ получения бис-индольного соединения, представленного формулой (VIII):
в которой R1 представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную или аралкильную группу.
Настоящее изобретение относится к устранению нежелательных аспектов в общепринятых способах получения представленного формулой (I) производного индолопирролокарбазола, применимого в качестве лекарственного средства. Другими словами, настоящее изобретение относится к способу получения, в который не включена стадия с низким выходом продукта и в соответствии с которым не применяется реагент, производство которого связано с высоким риском и который вызывает серьезное загрязнение окружающей среды.
В известном способе получения индольного соединения (Organic synthesis Collective volumes, vol. 7, page 34) стадию восстановления осуществляют с применением гидразина в присутствии катализатора никеля Ренея. Однако этот способ нежелателен для промышленного производства, так как гидразин обладает высокой взрывоопасностью. Кроме того, в связи с тем, что необходимо большое количество катализатора никеля Ренея, наблюдается серьезное загрязнение окружающей среды полученными в процессе производства жидкими отходами, что указывает на нежелательность применения этого способа в крупномасштабном промышленном производстве.
Кроме того, выход в известных способах получения бис-индольного соединения является невысоким, а потому данные процессы являются экономически неэффективными.
С другой стороны, известна (патент США № 5105012) реакция гидрирования с применением соединения родия, в которой для восстановления нитрогруппы производного нитробензола в кислотной среде, такой как уксусная кислота, в качестве катализатора применяется большое количество железного порошка. В этом случае, в связи с тем, что реакцию гидрирования осуществляют в кислотных условиях, этот способ неприменим для нестабильных в кислотных условиях веществ.
Авторы настоящего изобретения провели тщательное изучение способа получения производного индолопирролокарбазола формулы (I) и обнаружили следующее (i-v):
(i) новый способ получения производного индолопирролокарбазола формулы (I), при котором не наблюдается серьезного загрязнения окружающей среды полученными в процессе производства жидкими отходами, который является исключительно экономически выгодным и производство которого может осуществляться безопасно и высокой воспроизводимостью в качестве промышленного способа производства;
(ii) безопасный новый способ получения производного индола формулы (XII);
(iii) новый и экономически более совершенный способ получения производного бис-индола формулы (VIII);
(iv) новый катализатор гидрирования, который безопасен, не вызывает серьезного загрязнения окружающей среды обработанными жидкими отходами и может применяться не только в кислотных, но и в других условиях, и
(v) способ получения соединения (VII), в котором регулирование стадий является легким, а образование цианистого водорода в качестве побочного продукта в реакции замыкания цикла с применением 1,2-дихлор-5,6-дициано-1,4-бензохинона может быть предотвращено.
Авторы настоящего изобретения провели дальнейшие исследования и в результате создали настоящее изобретение.
А именно настоящее изобретение относится к новому способу получения производного индолопирролокарбазола формулы (I), к новому способу получения производного индола, к новому способу получения производного бис-индола и к новому катализатору гидрирования, который включает следующие (1)-(24).
(1) Способ получения производного индолопирролокарбазола представленного формулой (I), который включает следующие стадии:
(i): стадию взаимодействия соединения формулы (XIII)
в которой R1 представляет собой гидроксизащитную группу, а каждый Ra и Rb независимо представляет собой C1-C7-алкильную группу, или Ra и Rb могут быть объединены вместе с образованием C3-C6-алкиленовой группы, или его соли, с газообразным водородом в присутствии соединения родия и соединения металлас получением индольного соединения формулы (XII):
в котором значения R1 определены выше в этом документе, или его соли;
(ii): стадию осуществления взаимодействия полученного индольного соединения формулы (XII) или его соли с магнийхлоридом формулы (XI):
в которой Rc представляет собой C1-C7-алкильную группу, фенильную группу, винильную группу или аллильную группу; или с соединением магния формулы (X):
в которой Rd представляет собой C1-C7-алкильную группу или фенильную группу, или с его солью, или со смесью магнийхлорида (XI) и соединения магния (X), с последующим осуществлением взаимодействия полученного продукта с малеимидным соединением формулы (IX):
в которой X представляет собой атом галогена, и Y представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную группу или C7-C12-аралкильную группу, с получением бис-индольного соединения формулы (VIII):
в которой значения для каждого R1 и Y определены выше, или его соли;
(iii): стадию осуществления реакции замыкания цепи в полученном бис-индольном соединении (VIII) или его соли с получением соединения формулы (VII):
в которой значения для каждого R1 и Y определены выше, или его соли;
(iv): стадию сочетания полученного соединения (VII) или его соли с активированным производным глюкозы формулы (VI):
в которой каждый R2, R3, R4 и R5 представляет собой гидроксизащитную группу, и X1 представляет собой атом галогена, с получением соединения формулы (V):
в которой значения для каждого R1, R2, R3, R4, R5 и Y определены выше, или его соли;
(v): стадию обработки полученного соединения (V) или его соли основанием с получением соединения формулы (IV):
в которой значения для каждого R1, R2, R3, R4 и R5 определены выше, или его соли;
(vi): стадию взаимодействия соединения (IV) или его соли с соединением формулы (III):
в которой каждый R6 и R7 представляет собой гидроксизащитную группу, и Xa представляет собой молекулу кислоты, с получением соединения формулы (II):
в которой значения для каждого R1, R2, R3, R4, R5, R6 и R7 определены выше, или его соли; и
(vii): стадию снятия защитных групп с полученного соединения (II) или его соли с получением производного индолопирролокарбазола формулы (I):
или его соли;
(2) способ в соответствии с приведенным выше пунктом (1), в котором соединение родия представляет собой родий/углерод, родий/оксид алюминия, родий/карбонат кальция или родий/сульфат бария;
(3) способ в соответствии с приведенным выше пунктом (1), в котором соединение металлапредставляет собой соединение никеля(II), соединение железа(II), соединение железа(III), соединение кобальта(II) или соединение кобальта(III);
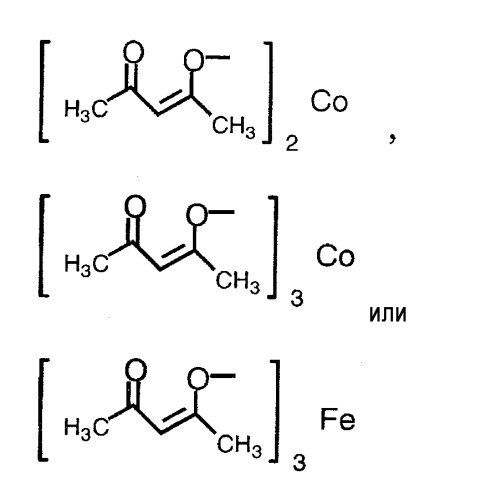
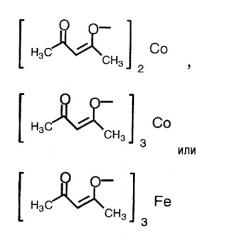
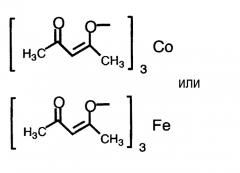
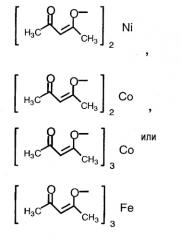
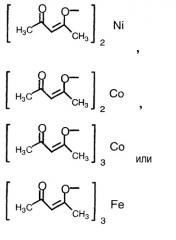
(4) способ в соответствии с приведенным выше пунктом (3), в котором соединение никеля(II), соединение железа(II), соединение железа(III), соединение кобальта(II) или соединение кобальта(III) представляют собой NiBr2, Ni(NO3)2, Ni(OCOCH3)2, FeBr3, FeCl2, FeSO4, FeCl3,FeCl3-SiO2, Fe(OCOCH3)2, фумарат Fe(II), CoBr2, CoCl2,
(5) способ в соответствии с приведенным выше пунктом (1), в котором каждый R1, R2, R3, R4, R5, R6 и R7 представляет собой бензильную группу;
(6) способ в соответствии с приведенным выше пунктом (1), в котором магнийхлорид формулы (XI) представляет собой этилмагнийхлорид, изопропилмагнийхлорид или н-бутилмагнийхлорид;
(7) способ в соответствии с приведенным выше пунктом (1), в котором соединение магния формулы (X) представляет собой ди(н-бутил)магний, ди(втор-бутил)магний, (н-бутил)(втор-бутил)магний, диметилмагний или диэтилмагний;
(8) способ в соответствии с приведенным выше пунктом (1), в котором малеимидное соединение формулы (IX) представляет собой малеимидное соединение, представленное формулой (IX-a):
в которой Y представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную группу или аралкильную группу;
(9) способ в соответствии с приведенным выше пунктом (1), в котором Y представляет собой метильную группу;
(10) способ в соответствии с приведенным выше пунктом (1), в котором Xa представляет собой щавелевую кислоту;
(11) способ в соответствии с приведенным выше пунктом (1), в котором сочетание осуществляют в присутствии катализатора межфазного переноса, такого как Aliquat 336;
(12) способ получения индольного соединения или его соли, который включает получение индольного соединения, представленного формулой (XII):
в которой R1 представляет собой гидроксизащитную группу, или его соли путем осуществления взаимодействия соединения, представленного формулой (XIII):
в которой значение R1 определено выше, и каждый Ra и Rb независимо представляет собой C1-C7-алкильную группу, или Ra и Rb могут быть объединены вместе с образованием C3-C6-алкиленовой группы, с газообразным водородом в присутствии соединения родия и соединения металла;
(13) способ в соответствии с приведенным выше пунктом (12), который включает осуществление взаимодействия соединения, представленного формулой (XIII):
в которой R1 представляет собой гидроксизащитную группу, и каждый Ra и Rb независимо представляет собой C1-C7-алкильную группу, или Ra и Rb могут быть объединены вместе с образованием C3-C6-алкиленовой группы, или его соли, с газообразным водородом в присутствии соединения родия и соединения металла, и обработку полученного неочищенного продукта силикагелем;
(14) способ получения бис-индольного соединения или его соли, который включает осуществление взаимодействия индольного соединения формулы (XII):
в которой R1 представляет собой гидроксизащитную группу, или его соли с магнийхлоридом формулы (XI):
в которой Rc представляет собой C1-C7-алкильную группу, фенильную группу, винильную группу или аллильную группу; или с соединением магния формулы (X):
в которой Rd представляет собой C1-C7-алкильную группу или фенильную группу, или с его солью, или со смесью магнийхлорида формулы (XI) и соединения магния формулы (X), в инертном растворителе, с последующим осуществлением взаимодействия полученного продукта с малеимидным соединением формулы (IX):
в которой X представляет собой атом галогена, и Y представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную группу или C7-C12-аралкильную группу, предпочтительно в инертном растворителе с получением бис-индольного соединения формулы (VIII):
в которой значения для каждого R1 и Y определены выше, или его соли;
(15) способ в соответствии с приведенным выше пунктом (14), в котором малеимидное соединение формулы (IX) представляет собой малеимидное соединение, представленное формулой (IX-a):
в которой Y представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную группу или C7-C12-аралкильную группу;
(16) способ получения соединения, представленного формулой (VII):
в которой R1 представляет собой гидроксизащитную группу, и Y представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную группу или C7-C12-аралкильную группу, или его соли, который включает обработку бис-индольного соединения, представленного формулой (VIII):
в которой значения для каждого R1 и Y определены выше, или его соли, с 2,3-дихлор-5,6-дициано-1,4-бензохиноном в неполярном растворителе в реакции замыкания цепи;
(17) способ в соответствии с приведенным выше пунктом (16), в котором неполярный растворитель представляет собой бензол, толуол, ксилол (орто-, мета- или пара-), этилбензол или 1,2,4-триметилбензол;
(18) применяемый в реакции гидрирования катализатор содержит соединение родия и соединение металла;
(19) катализатор в соответствии с приведенным выше пунктом (18) дополнительно содержит амин;
(20) катализатор в соответствии с приведенным выше пунктом (18) или (19), в котором соединение родия представляет собой родий/углерод, родий/оксид алюминия, родий/карбонат кальция или родий/сульфат бария;
(21) катализатор в соответствии с приведенным выше пунктом (18) или (19), в котором соединение металлапредставляет собой соединение никеля(II), соединение железа(II), соединение железа(III), соединение кобальта(II) или соединение кобальта(III);
(22) катализатор в соответствии с приведенным выше пунктом (19), в котором амин представляет собой вторичный амин или третичный амин;
(23) катализатор в соответствии с приведенным выше пунктом (19), в котором амин представляет собой пирролидин, пиперидин, диметиламин, диэтиламин, диизопропиламин, дибутиламин, триметиламин, триэтиламин или трибутиламин; и
(24) катализатор в соответствии с приведенным выше пунктом (21), в котором соединение никеля(II), соединение железа(II), соединение железа(III), соединение кобальта(II) или соединение кобальта(III) представляют собой NiBr2, Ni(NO3)2, Ni(OCOCH3)2, FeBr3, FeCl2, FeSO4, FeCl3,FeCl3-SiO2, Fe(OCOCH3)2, фумарат Fe(II), CoBr2, CoCl2,
.
Способом в соответствии с изобретением стало возможным получать соединение, которое может безопасно, просто и эффективно применяться в медицине в качестве противоопухолевого средства.
НАИЛУЧШИЙ ВАРИАНТ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Настоящее изобретение будет проиллюстрировано ниже более подробно. Прежде всего, будут разъяснены термины, используемые в описании настоящего изобретения.
Примеры «C1-C7-алкильной группы» включают неразветвленную или разветвленную алкильную группу, такую как метил, этил, пропил, изопропил, бутил, изобутил, трет-бутил, н-пентил, изопентил, неопентил, н-гексил, изогексил и гептил, среди которых предпочтительным является метил, этил, пропил, изопропил или бутил, и более предпочтительным является метил, этил, пропил, бутил или гептил.
Примеры «C3-C6-алкиленовой группы» включают неразветвленную алкиленовую группу, такую как триметилен, тетраметилен, пентаметилен и гексаметилен, среди которых предпочтительным является тетраметилен или пентаметилен.
Примеры «C7-C12-аралкильной группы» включают C7-C12-аралкильную группу, такую как бензил, 1-нафтилметил и 2-нафтилметил, среди которых предпочтительным является бензил.
Примеры «кислотной молекулы» включают протонную кислоту, такую как соляная кислота, серная кислота, азотная кислота, уксусная кислота, метилсульфоновая кислота, пара-толуолсульфоновая кислота, щавелевая кислота, пропионовая кислота, муравьиная кислота и бензойная кислота, среди которых предпочтительной является щавелевая кислота.
Примеры «гидроксизащитных групп» включают группы, защищающие гидроксигруппы, такие как бензильная, толильная, пара-нитробензильная, пара-метоксибензильная и бензилоксиметильная группы, среди которых предпочтительной является бензильная группа.
Термин «соединение родия» относится к содержащему атом родия катализатору, обычно к родиевому катализатору на носителе, и его предпочтительные примеры включают родий/углерод, родий/оксид алюминия, родий/карбонат кальция или родий/сульфат бария.
Примеры «атома галогена» включают хлор, йод и бром.
Термин «соединение металла» не включает соединение родия и относится к катализатору, который вместе с соединением родия способствует реакции восстановления, и его примеры включают соединение никеля(II), соединение железа(II), соединение железа(III), соединение кобальта(II) и соединение кобальта(III), предпочтительно NiBr2, Ni(NO3)2, Ni(OCOCH3)2, FeBr3, FeCl2, FeSO4, FeCl3, FeCl3-SiO2, Fe(OCOCH3)2, фумарат Fe(II), CoBr2, CoCl2,
.
Термин «катализатор межфазного переноса» относится к катализатору, который способствует взаимодействию между гидрофобным (олеофильным) органическим соединением и гидрофильным органическим соединением в двухфазной системе, состоящей из жировой фазы и водной фазы, и его примеры включают соединение формулы (XIV):
в которой каждый Ra независимо представляет собой водород, бензил или C1-C18-углеводород; M представляет собой атом азота или атом фосфора; и A представляет собой гидроксигруппу, атом фтора, атом брома, атом хлора, атом йода, цианогруппу, HSO4, CH3SO3 или PhCH2COO, и трис(2-(2-метоксиэтокси)этил)амин, и его предпочтительные примеры включают трикаприлметиламмонийхлорид, трис(2-(2-метоксиэтокси)этил)амин, бензилтриэтиламмонийхлорид и гидросульфат трибутиламмония. Конкретные примеры соединения формулы (XIV) включают трикаприлметиламмонийхлорид, и тому подобное.
Термин «соль» обычно относится к аддитивной соли кислоты, и предпочтительной является фармацевтически приемлемая соль. Примеры кислоты и аддитивные соли кислоты включают неорганическую кислоту, такую как соляная кислота и серная кислота, и органическую кислоту, такую как уксусная кислота и щавелевая кислота.
Примеры «амина» включают первичный амин, вторичный амин и третичный амин, и более конкретно включают амин, такой как пирролидин, пиперидин, диметиламин, диэтиламин, диизопропиламин, дибутиламин, триметиламин, триэтиламин и трибутиламин, предпочтительно вторичный амин или третичный амин, и более предпочтительно пирролидин.
Термин «обработка силикагелем» относится к процессу фильтрации неочищенного продукта, растворенного в растворителе, через наполненную силикагелем колонку или через фильтр, поверхность которого покрыта силикагелем.
Предпочтительный способ получения по настоящему изобретению будет проиллюстрирован ниже подробно.
Стадия получения индольного соединения формулы (XII):
в которой R1 представляет собой гидроксизащитную группу, путем осуществления взаимодействия соединения (XIII):
в которой значение R1 определено выше, и каждый Ra и Rb независимо представляет собой C1-C7-алкильную группу, или Ra и Rb могут быть объединены вместе с образованием C3-C6-алкиленовой группы, с газообразным водородом в присутствии соединения родия и соединения металла, выполняют так, что соединение (XIII) взаимодействует с газообразным водородом при давлении в 1-5 атм. в присутствии приблизительно от 0,5 мол.% до 30 мол.% соединения родия и приблизительно от 1 мол.% до 100 мол.% соединения металла по отношению к 1 молю соединения (XIII), в инертном растворителе при температуре приблизительно от -20°C до 80°C в течение приблизительно от 1 до 120 часов.
Примеры инертного растворителя, который может применяться на указанной выше стадии, включают тетрагидрофуран, диэтиловый эфир, трет-бутилметиловый эфир, диизопропиловый эфир, дибутиловый эфир, метанол, этанол, изопропанол, пропанол, ацетон, этилацетат, изопропилацетат и циклопентилметиловый эфир, или смесь этих растворителей, среди которых предпочтительным является тетрагидрофуран, циклопентилметиловый эфир или трет-бутилметиловый эфир.
Соединение родия, которое может применяться на указанной выше стадии, может представлять собой любое соединение, содержащее в составе молекулы, по крайней мере, один атом родия, и его примеры предпочтительно включают содержащий 1-10% родия родий/углерод, содержащий 1-10% родия родий/оксид алюминия, содержащий 1-10% родия родий/карбонат кальция или содержащий 1-10% родия родий/сульфат бария, и более предпочтительно представляет собой родий/углерод.
Примеры соединения металла, которое может применяться на указанной выше стадии, включают соединение никеля(II), соединение железа(II), соединение железа(III), соединение кобальта(II) и соединение кобальта(III), предпочтительно NiBr2, Ni(NO3)2, Ni(OCOCH3)2, FeBr3, FeCl2, FeSO4, FeCl3, FeCl3-SiO2, Fe(OCOCH3)2, фумарат Fe(II), CoBr2, CoI2, CoCl2,
Применяемые на этой стадии исходные соединения могут быть получены в соответствии со способом, описанным, например, в Organic Synthesis Collective Volumes, vol. 7, page 34, или в соответствии со сходным с ним способом.
На указанной выше стадии взаимодействие предпочтительно осуществляют в присутствии амина в дополнение к соединению родия и соединению металла. Дополнительное присутствие амина в химической реакции может увеличивать скорость и выход реакции. С применением амина может быть резко увеличена скорость реакции. Амин включает первичный амин, вторичный амин или третичный амин, и более конкретно включает амин, такой как пирролидин, пиперидин, диметиламин, диэтиламин, диизопропиламин, дибутиламин, триметиламин, триэтиламин и трибутиламин, предпочтительно вторичный амин или третичный амин, и более предпочтительно пирролидин.
Амин обычно используют в количестве приблизительно от 0,01 до 10 эквивалентов по отношению к подвергаемому гидрированию материалу (например, соединению (XIII)). Более того, в случае подбора подходящего реагента, генерирующего амин в реакционном растворе при постоянном гидрировании в соответствии с реакцией по настоящему изобретению, дополнительное добавление амина к реакционному раствору не требуется.
К полученному на этой стадии реакционному раствору (суспензии) добавляют водный раствор аммиака и насыщенный солевой раствор, предпочтительно их суспензию, перемешивают смесь приблизительно в течение одного часа и фильтруют для разделения твердого вещества, а затем остаток промывают растворителем, таким как бензол, толуол или ксилол. Фильтрат и промывную жидкость объединяют, затем последовательно промывают водным раствором лимонной кислоты, 5% водным бикарбонатом натрия и насыщенным солевым раствором, а затем упаривают в вакууме досуха. После растворения полученного соединения формулы (XII) или его соли в растворителе, таком как бензол, толуол или ксилол, и тому подобное, раствор наносят на колонку, заполненную силикагелем с тем же самым что и у соединения (XII) весом, или на фильтр, чья поверхность покрыта упомянутым силикагелем, и подвергают воздействию давлением инертного газа, такого как азот. Образующиеся на стадии реакции примеси, такие как окрашенные вещества, могут быть эффективно удалены посредством очистки на силикагеле. Степень чистоты соединения (XII) повышают посредством способа очистки по настоящему изобретению, и поэтому химические реакции и очистка продуктов на последующих стадиях могут проводиться эффективными с точки зрения промышленного производства способами без применения особого способа.
Затем на стадии получения бис-индольного соединения формулы (VIII):
в которой значения для каждого R1 и Y определены выше, или его соли, взаимодействие полученного выше индольного соединения формулы (XII):
в которой значения для R1 определены выше, или его соли, с магнийхлоридом формулы (XI):
в которой Rc представляет собой C1-C7-алкильную группу, фенильную группу, винильную группу или аллильную группу; с соединением магния формулы (X):
в которой Rd представляет собой C1-C7-алкильную группу или фенильную группу, или с его солью, или со смесью магнийхлорида формулы (XI) и соединения магния формулы (X), в вышеупомянутом инертном растворителе, с последующим осуществлением взаимодействия полученного продукта с малеимидным соединением формулы (IX):
в которой X представляет собой атом галогена, и Y представляет собой атом водорода, C1-C7-алкильную группу, фенильную группу, бензилоксиметильную группу или C7-C12-аралкильную группу, в вышеупомянутом инертном растворителе предпочтительно осуществляют в соответствии со следующими способами 1), 2) или 3).
1) При температуре приблизительно от 30°C до 120°C в течение приблизительно от 0,5 до 24 часов в инертном растворителе осуществляют взаимодействие приблизительно от 2 до 4 моль индольного соединения (XII) и приблизительно от 2 до 4 моль магнийхлорида (XI) по отношению к 1 молю малеимидного соединения (IX).
2) При температуре приблизительно от 30°C до 120°C в течение приблизительно от 0,5 до 24 часов в инертном растворителе осуществляют взаимодействие приблизительно от 2 до 4 моль индольного соединения (XII) и приблизительно от 2 до 4 моль соединения магния (X) по отношению к 1 молю малеимидного соединения (IX).
3) При температуре приблизительно от 30°C до 120°C в течение приблизительно от 0,5 до 24 часов в инертном растворителе осуществляют взаимодействие приблизительно от 2 до 4 моль индольного соединения (XII) и приблизительно от 0,8 до 4 моль смеси, содержащей магнийхлорид (XI) и соединение магния (X), по отношению к 1 молю малеимидного соединения (IX).
Предпочтительные примеры применяемого в способах 1), 2) и 3) растворителя включают толуол и смесь толуола и тетрагидрофурана.
Примеры используемого на приведенной выше стадии магнийхлорида формулы (XI) включают алкилмагнийхлориды, такие как метилмагнийхлорид, этилмагнийхлорид, н-пропилмагнийхлорид, изопропилмагнийхлорид, н-бутилмагнийхлорид, втор-бутилмагнийхлорид, изобутилмагнийхлорид, трет-бутилмагнийхлорид, н-пентилмагнийхлорид, н-гексилмагнийхлорид, фенилмагнийхлорид, винилмагнийхлорид и аллилмагнийхлорид, или их смесь.
Примеры применяемого на приведенной выше стадии соединения магния формулы (X) включают диметилмагний, диэтилмагний, ди(н-пропил)магний, диизопропилмагний, ди(н-бутил)магний, ди(втор-бутил)магний, диизобутилмагний, ди(трет-бутил)магний, ди(н-пентил)магний, ди(н-гексил)магний, (н-бутил)(втор-бутил)магний, (метил)(втор-бутил)магний, (этил)(втор-бутил)магний, (метил)(н-бутил)магний, (этил)(н-бутил)магний, (метил)(трет-бутил)магний, (этил)(трет-бутил)магний, (н-пропил)(н-бутил)магний, (н-пропил)(втор-бутил)магний, (н-пропил)(изопропил)магний, (н-бутил)(изопропил)магний, (втор-бутил)(изопропил)магний, (изобутил)(изопропил)магний, (н-пропил)(изобутил)магний и дифенилмагний, или их смесь.
Затем, на стадии получения соединения формулы (VII):
в которой значения для каждого R1 и Y определены выше, или его соли, реакцию замыкания цепи полученного выше бис-индольного соединения, представленного формулой (VIII):
в которой значения для каждого R1 и Y определены выше, или его соли, предпочтительно осуществляют в соответствии со следующими способами 1) и 2).
1) Соединение формулы (VIII) или его соль обрабатывают в инертном растворителе при температуре приблизительно от 20°C до 200°C в течение приблизительно от 1 минуты до 5 суток, например, 2,3-дихлор-5,6-дициано-1,4-бензохиноном (DDQ), палладиевым реагентом, таким как PdCl2 и Pd(OAc)2, или медным реагентом, таким как CuCl2, в количестве приблизительно от 1 до 10 молярных эквивалентов по отношению к 1 моль соединения (VIII) или его соли.
Растворителем, который может применяться на стадии 1), может служить любой общеизвестный инертный растворитель, и его примеры включают полярные растворители, такие как тетрагидрофуран, метанол, этанол, N,N-диметилформамид, диметилсульфоксид, N-метилпирролидон и N,N-диметилацетамид, и неполярный растворитель, такой как бензол, толуол, ксилол (орто-, мета- или пара-), этилбензол и 1,2,4-триметилбензол. В случае применения 2,3-дихлор-5,6-дициано-1,4-бензохинона при использовании полярного растворителя во время химической реакции или при обработке образуется цианистый водород, в то время как при использовании неполярного растворителя образование цианистого водорода подавлено, что благоприятно для ступенчатого контроля.
2) Соединение формулы (VIII) или его соль обрабатывают в инертном растворителе реагентом, состоящим из приблизительно 0,01-1,0 эквивалента нанесенного на углерод, оксид алюминия, карбонат кальция, сульфат бария или силикагель катализатора, содержащего металл переменной валентности (например, палладий, платину и т.д.), по отношению к 1 моль соединения (VIII) при температуре приблизительно от 20°C до 200°C в течение приблизительно от 1 минуты до 5 суток при давлении от 1 до 5 атм. окислителя, выбираемого из группы, состоящей из кислорода, воздуха, этилена и ацетилена.
Примеры инертного растворителя, который может применяться на стадии 2), включают толуол, тетрагидрофуран, метанол, этанол, диметилформамид, диметилсульфоксид, N-метилпирролидон и диметилацетамид.
Затем, на стадии получения соединения формулы (V):
в которой значения для каждого R1 и Y определены выше, и каждый R2, R3, R4 и R5 представляет собой гидроксизащитную группу, или его соли, сочетание полученного выше соединения формулы (VII)
в которой значения для каждого R1 и Y определены выше, или его соли, или его соли, с активированным производным глюкозы формулы (VI):
в которой значения для каждого R2, R3, R4 и R5 определены выше, и X1 представляет собой атом галогена, с предпочтительным использованием системы, содержащей основание в водном растворителе и катализатор межфазного переноса в инертном органическом растворителе, может быть осуществлено следующим образом.
Активированное производное глюкозы (VI):
в котором каждый R2, R3, R4 и R5 представляет собой гидроксизащитную группу, и X1 представляет собой атом галогена, может быть получено путем осуществления взаимодействия производного глюкозы (VIa):
в которой каждый R2, R3, R4 и R5 представляет собой гидроксизащитную группу, например, с галогенангидридом, сульфонилхлоридом или йодтрифенилфосфином при температуре приблизительно от -50°C до 200°C, предпочтительно приблизительно от -10°C до 30°C, предпочтительно в инертном растворителе.
Примеры галогенангидрида, применяемого на вышеупомянутой стадии, включают SOCl2, POCl3, SOBr3, POBr3, PBr3 и оксалилхлорид, среди которых предпочтительным является SOCl2 или оксалилхлорид, а более предпочтительным - SOCl2.
Примеры инертного растворителя, применяемого на вышеупомянутой стадии, включают углеводород, такой как толуол, ксилол, гептан и гексан; нитрил, такой как ацетонитрил; и простой эфир, такой как трет-бутилметиловый эфир и тетрагидрофуран; галогенированный углеводород, такой как метиленхлорид, тетрахлорид углерода, хлороформ, трифтортолуол и дихлорбензол; и кетон, такой как метилизобутиловый кетон и ацетон, среди которых предпочтительным является трет-бутилметиловый простой эфир или тетрагидрофуран, а более предпочтительным - трет-бутилметиловый простой эфир.
Что касается производного глюкозы (VIa), то могут использоваться коммерчески доступные продукты.
Полученное выше активированное производное глюкозы формулы (VI) сочетают с соединением формулы (VII):
в которой значения для каждого R1 и Y определены выше, или с его солью, с использованием системы, содержащей основание в водном растворителе и катализатор межфазного переноса в инертном органическом растворителе, обычно при температуре от -50°C до 200°C, предпочтительно от 0°C до 40°C.
Примером водного растворителя, применяемого на вышеупомянутой стадии, является вода.
Примеры основания, применяемого на вышеупомянутой стадии, включают гидроксиды щелочных металлов, такие как гидроксид лития, гидроксид натрия, гидроксид калия и гидроксид цезия, среди которых предпочтительным является гидроксид натрия или гидроксид калия. Концентрация применяемого основания составляет приблизительно от 5 мас.% до 95 мас.%, предпочтительно приблизительно от 45 мас.% до 50 мас.%.
Примеры инертного растворителя, применяемого на вышеупомянутой стадии, включают углеводород, такой как толуол, ксилол, гептан и гексан; нитрил, такой как ацетонитрил; и простой эфир, такой как трет-бутилметиловый эфир и тетрагидрофуран; галогенированный углеводород, такой как метиленхлорид, тетрахлорид углерода, хлороформ, трифтортолуол и дихлорбензол; кетон, такой как метилизобутиловый кетон и ацетон; и неионный растворитель, такой как N,N-диметилформамид и 1-метил-2-пирролидинон, среди которых предпочтительным является трет-бутилметиловый эфир, метиленхлорид или трифтортолуол.
Примеры катализатора межфазного переноса, применяе