Иммуногенная композиция (варианты) на основе рекомбинантного внутриклеточного патогена
Иллюстрации
Показать всеПредставлены иммуногенные композиции, включающие рекомбинантные аттенюированные внутриклеточные патогены, например бациллу Кальмета-Герена (БЦЖ). Иммуногенная композиция включает, в частности, БЦЖ, содержащую последовательность внехромосомной нуклеиновой кислоты, которая включает ген, кодирующий крупный внеклеточный белок микобактерий размером 23,5, 30 и/или 32 кДа, при этом крупный внеклеточный неслитый белок микобактерий сверхэкспрессируется и секретируется. Вариантом иммуногенной композиции является композиция, содержащая рекомбинантную БЦЖ с регулируемым ростом. При введении иммуногенных композиций в организм млекопитающего указанные белки сверхэкспрессируются и секретируются, вызывая иммунную ответную реакцию организма на введенный антиген. Представленные в изобретении иммуногенные композиции обеспечивают надежный и безопасный защитный иммунитет. 2 н. и 8 з.п. ф-лы, 6 ил., 12 табл.
Реферат
ИНФОРМАЦИЯ, КАСАЮЩАЯСЯ ПРАВИТЕЛЬСТВА
Настоящее изобретение было сделано в рамках гранта № AI31338, финансируемого Правительством и выданного Министерством здравоохранения и социального обеспечения. Правительство имеет определенные права на это изобретение.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение в основном относится к иммуногенным композициям, полученным из рекомбинантных аттенюированных внутриклеточных патогенных бактерий. Более конкретно, настоящее изобретение относится к иммуногенным композициям, содержащим рекомбинантные аттенюированные Mycobacteria, которые сверхэкспрессируют и секретируют основные внеклеточные белки. Кроме того, иммуногенные композиции по настоящему изобретению также содержат рекомбинантные аттенюированные Mycobacteria, включая ауксотрофные штаммы. Иммуногенные композиции по настоящему изобретению могут использоваться для индукции иммунных ответов в организм хозяина.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Давно известно, что паразитирующие микроорганизмы обладают способностью инфицировать животных, вызывая болезни и часто смерть. Патогены являются основной причиной смерти на протяжении всей истории человечества и продолжают причинять огромные страдания. Несмотря на то что за последние сто лет были достигнуты значительные успехи в профилактике и лечении многих инфекционных заболеваний, до сих пор не существует универсального эффективного подхода для лечения из-за сложных взаимоотношений "хозяин-паразит". Трудности в противодействии сложным механизмам инвазии, наблюдаемым у многих патогенных микроорганизмов, подтверждаются возрождением различных заболеваний, таких как туберкулез, а также возникновением большого числа резистентных штаммов бактерий и вирусов.
К числу эпидемиологически важных патогенов относятся внутриклеточные бактерии, которые имеют доказанную устойчивость при лечении или профилактических мероприятиях. Внутриклеточные бактерии, включая род Mycobacterium, весь или часть своего жизненного цикла находятся в клетках инфицированного организма хозяна, а не во внеклеточной среде. Внутриклеточные бактерии вызывают бесчетное множество болезней во всем мире и миллионы смертей ежегодно. Туберкулез является главной причиной смерти от одного возбудителя во всем мире, при этом ежегодно насчитывается 10 миллионов новых случаев и 2,9 миллиона смертельных исходов. Кроме того, внутриклеточные бактерии являются причиной возникновения миллионов случаев лепры. Другие истощающие заболевания, вызываемые внутриклеточными агентами, включают кожный и висцеральный лейшманиоз, американский трипанозомоз (болезнь Шагаса), листериоз, токсоплазмоз, гистоплазмоз, трахому, пситтакоз, лихородку Ку и легионеллез.
В настоящее время считается, что примерно одна треть населения земного шара инфицирована M. tuberculosis, что влечет за собой возникновение миллионов случаев легочной формы туберкулеза ежегодно. Более конкретно, легочная форма туберкулеза человека, вызываемая M. tuberculosis, является основной причиной смерти в развивающихся странах. Способный выживать внутри макрофагов и моноцитов, M. tuberculosis может вызывать хроническую внутриклеточную инфекцию. M. tuberculosis относительно успешно обходит нормальные защитные механизмы организма хозяина, скрываясь внутри клеток, в первую очередь ответственных за обнаружение чужеродных элементов и последующую активацию иммунной системы. Более того, многие химиотерапевтические средства первой линии, используемые для лечения туберкулеза, обладают относительно низкой активностью против внутриклеточных организмов по сравнению с внеклеточными формами. Такие свойства патогенных бактерий до сих пор ограничивали эффективность иммунотерапевтических средств или иммуногенных композиций против туберкулезных инфекций.
В последнее время о резистентности возбудителей туберкулеза к одному или нескольким лекарственным средствам сообщалось в 36 из 50 штатов США. В Нью-Йорке одна треть всех исследованных случаев были резистентны к одному или нескольким основным лекарственным средствам, применяемым для лечения туберкулеза. Несмотря на то что нерезистентный туберкулез может быт излечен после длительного курса антибиотиками, перспективы в отношении штаммов, резистентных к лекарственным препаратам, довольно печальны. У пациентов, которые инфицированны штаммами, резистентными к двум или более основным антибиотикам, уровень смертности составляет около 50%. Соответственно, существует острая необходимость в безопасных и эффективных иммуногенных композициях против разнообразных видов M. tuberculosis.
Первичная инфекция M. tuberculosis почти всегда возникает при вдыхании распыленных в воздухе частиц, поскольку патоген может оставаться жизнеспособным в течение ряда недель или месяцев во влажной или сухой мокроте. Несмотря на то что первичным сайтом инфекции являются легкие, патоген может также вызвать инфекцию почти любого органа, включая, но этим не ограничиваясь, кости, селезенку, почку, оболочки мозга и кожу. В зависимости от вирулентности конкретного штамма и устойчивости организма-хозяина инфекция и соответствующее поражение ткани может быть небольшим или обширным. У большенства людей, подвергающихся воздействию вирулентных штаммов бактерий, первичная инфекция находится под контролем. Развитие приобретенного иммунитета после первичного стимула снижает пролиферацию бактерий, что позволяет излечить патологические нарушения и обеспечивает практически бессимптомное проявление заболевания у субъекта.
Если M. tuberculosis не контролируется инфицированным субъектом, то такая ситуация часто приводит к обширному поражению легочной ткани. У восприимчивых индивидуумов поражение обычно формируется в легких, так как бациллы туберкулеза размножаются в альвеолярных или легочных макрофагах. Поскольку организмы размножаются, они могут распространяться по лимфатической системе до удаленных лимфатических узлов и через кровоток к апикальным частям легкого, костному мозгу, почкам и оболочкам мозга. Первоначально, в результате клеточных реакций гиперчувствительности, образуются характерные грануломатозные поражения или туберкулы, в зависимости от тяжести инфекции. Указанные поражения в основном состоят из эпителиоидных клеток, окруженных моноцитами, лимфоцитами и фибробластами. В большинстве случаев поражение или туберкулы постепенно некротизируются и подвергаются казеозу (преобразованию пораженных тканей в размягченную творожистую субстанцию).
Несмотря на то что M. tuberculosis является важнейшим патогеном, другие виды рода Mycobacterium также вызывают заболевание у животных, включая человека, и они также входят в область настоящего изобретения. Например, M. bovis очень сходен с M. tuberculosis и ответственен за туберкулезные инфекции домашних животных, таких как крупный рогатый скот, свиньи, овцы, лошади, собаки и кошки. Кроме того, M. bovis может инфицировать людей через желудочно-кишечный тракт, обычно при употреблении сырого молока. Локализованная кишечная инфекция постепенно переходит в дыхательные пути и затем приобретает классические симптомы туберкулеза. Другим важным патогенным переносчиком рода Mycobacterium является M. leprae, которая вызывает миллионы случаев древнего заболевания лепры. Другие виды этого рода, которые вызывают заболевание у животных и человека, включают M. kansasii, M. avium intracellulare, M. fortuitum, M. marinum, M. chelonei и M. scrofulaceum. Патогенные виды микобактерий зачастую обладают высокой степенью гомологии последовательностей соответствующих ДНК и соответствующих белков, а некоторые виды, такие как M. tuberculosis и M. bovis, являются очень сходными.
По очевидным практическим и моральным соображениям начальные исследования на людях для определения эффективности экспериментальных композиций в отношении таких поражений недопустимы. Соответственно, на ранних стадиях разработки любого лекарственного препарата или иммуногенной композиции стандартной процедурой является использование соответствующей модели животного, с учетом аспектов безопасности и затрат. Успех внедрения в лабораторную практику моделей животных основан на понимании того, что иммуногенные эпитопы зачастую активны в организмах различных видов. Таким образом, иммуногенная детерминанта одного вида, например грызуна или морской свинки, будет, по существу, иммунореактивной у других видов, например у человека. Только после соответствующего изучения на моделях животных проводятся клинические испытания на людях для дальнейшей проверки безопасности и эффективности иммуногенной композиции для человека.
В отношении альвеолярной или легочной формы инфекций, вызываемых M. tuberculosis, модель на морской свинке во многих отношениях наиболее сходна с патологией данного заболевания у человека. Соответственно, специалистам в данной области будет понятно, что модель данного заболевания на морской свинке подходит для экстраполяции на человека и других млекопитающих. Как и человек, морские свинки восприимчивы к туберкулезной инфекции при низких дозах распыленного патогена M. tuberculosis человека. В отличие от человека, у которого первичная инфекция обычно находится под контролем, у морских свинок при воздействии аэролизованного патогена всегда развивается диссеминированное заболевание, что облегчает последующий анализ. Кроме того, как у морских свинок, так и у человек проявляются кожные реакции гиперчувствительности замедленного типа, характеризующиеся развитием плотного мононуклеарного уплотнения, или ригидной области на месте кожного теста. И наконец, характерные туберкулезные поражения человека и морских свинок имеют близкую морфологию, включая наличие гигантских клеток Лангханса. Поскольку морские свинки более восприимчивы к первичной инфекции и у них быстрее развивается заболевание, чем у человек, любая защита, создаваемая в экспериментах с использованием этой животной модели, является убедительным показателем, что такой же защитный иммунитет может возникать у человека или другого менее восприимчивого млекопитающего. Соответственно, исключительно с целью объяснения, а не для ограничения, настоящее изобретение в основном будет продемонстрировано на примерах с морскими свинками в качестве организма-хозяина млекопитающего. Для специалистов в данной области очевидно, что настоящее изобретение может быть осуществлено и на других организмах-хозяевах млекопитающих, включая человека и домашних животных.
Попытки борьбы с туберкулезом, используя иммуногенные композиции, начались с 1921 года после того, как Кальметт и Герен успешно получили аттенюированный вирулентный штамм M. bovis в Институте Пастера в Лилле, Франция (Institut Pasteur in Lille, France). Аттенюированный M. bovis стал известен как бацилла Кальметта-Герена или сокращенно БЦЖ. Почти восемдесят лет после этого иммуногенные композиции, полученные из БЦЖ, остаются единственным профилактическим средством для борьбы с туберкулезом в настоящее время. Фактически, иммуногенные композиции на основе БЦЖ, доступные сегодня, получают из исходного штамма M. bovis, разработанного Кальметтом и Героном в институте Пастера.
Всемирная Организация Здравоохранения рассматривает иммуногенные композиции на основе БЦЖ как незаменимый фактор снижения заболеваемости туберкулезом в мире, особенно в развивающихся странах. Теоретически, иммуногенная композиция на основе БЦЖ вызывает клеточный иммунитет против аттенюированной бактерии, которая иммунологически близка к M. tuberculosis. Полученный иммунный ответ должен ингибировать развитие первичного туберкулеза. Таким образом, если первичный туберкулез ингибируется, то не могут возникать латентные инфекции и предотвращается реактивация заболевания.
Используемые в настоящее время иммуногенные композиции на основе БЦЖ доступны в виде лиофилизированных культур, которые восстанавливают стерильным разбавителем непосредственно перед введением. В странах, где используется вакцинация БЦЖ, включая развивающиеся и развитые страны, иммуногенную композицию на основе БЦЖ вводят при рождении, на первом году жизни и в раннем детстве. Взрослые люди, посещающие эпидемически неблагополучные районы, где они могут подвергаться воздействию высоких доз микобактерий, в качестве профилактики могут быть вакцинированы БЦЖ, при условии отсутствия реакции на кожный тест. Побочные реакции на иммуногенную композицию редки, и в основном они ограничиваются кожными раздражителями и лимфаденитом вблизи места инъекции. Однако, в отличие от редких побочных реакций на иммунологическую композицию, иммуногенные композиции на основе БЦЖ характеризуются беспрецендентной безопасностью на примере трех миллиардов доз, введенных во всем мире, начиная с 1930 года.
Однако к такой беспрецендентной безопасности традиционных иммуногенных композиций на основе БЦЖ относятся с возрастающей критикой, и она является парадоксом для практической медицины. Оказалось, что той категорией населения, которая наиболее восприимчива к микобактериальной инфекции, являются больные с иммуносупрессией. Лица с ранней или поздней стадией ВИЧ-инфекции особенно восприимчивы к туберкулезной инфекции. К сожалению, большое число людей на ранней стадии ВИЧ-инфекции не знают о своем иммунном статусе. Вполне вероятно, что такие больные могут быть добровольно иммунизированы живой аттенюированной иммуногенной композицией, такой как БЦЖ, без предупреждения о существующем для них риске. Кроме того, другие индивидуумы с незначительной иммуносупрессией также могут быть по незнанию иммунизированы БЦЖ в надежде избежать микобактериального заболевания. В связи с этим желательны более безопасные, более эффективные БЦЖ или БЦЖ-подобные иммуногенные композиции.
В последнее время уделяется большое внимание применению трансформированных штаммов БЦЖ для получения иммуногенных композиций, которые экспрессируют различные клеточные антигены. Например, C.K. Stover et. al. сообщали о получении иммуногенной композиции против болезни Лайма с использованием рекомбинантной БЦЖ (рБЦЖ), которая экспрессирует мембранный липопротеин OspA Borrellia burgdorferi. Аналогично, теми же авторами была получена иммуногенная композиция на основе рБЦЖ, которая экспрессирует пневмококковый поверхностный белок (PsPA) Streptococcus pneumoniae (Stover, C.K., G.P. Bansal, S. Langerman, and M.S. Hanson. 1994. Protective Immunity Elicited by rBCG Immunogenic compositions. In: Brown F. (ed.): Recombinant Vectors in Immunogenic composition Development. Dev Biol Stand. Dasel, Karger, Vol. 82, 163-170).
В патенте США (USPN) 5504005 ("патент '005") и в патенте США USPN 5854055 ("патент '055"), опубликованных B.R. Bloom et al., описываются теоретические векторы рБЦЖ, экспрессирующие широкий спектр клеточных белков слияния различных видов микроорганизмов. Теоретические векторы, описанные в этих патентах, относятся или к клеточным белкам слияния, в противоположность внеклеточным неслитым белковым антигенам, и/или рБЦЖ является предположительно вектором, экспрессирующим белки слияния отдаленных видов. Более того, экспрессируемые в данных моделях белки слияния рекомбинантных клеток кодируются ДНК, которая интегрирована в геном хозяина под контролем промоторов белков теплового шока. Следовательно, экспрессированные антигены являются белками слияния и экспрессия ограничивается уровнями, примерно равными или меньшими, чем векторы нативных белков.
Кроме того, ни в патенте '005, ни в патенте '055 не описывается тестирование безопасности на моделях животных, возникновение иммунного ответа или защитного иммунитета в такой системе животного, которая полностью имитирует заболевание человека. Кроме того, только теоретические векторы рБЦЖ, экспрессирующие белки слияния M. tuberculosis, в патентах '005 и '055 описаны, но не дано описание фактических иммуногенных композиций. Описанные в этих патентах модели иммуногенных композиций в отношении M. tuberculosis относятся к клеткам со слитыми белками теплового шока, а не к внеклеточным неслитым белкам.
В патенте США номер 5830475 ("патент '475") также теоретически описываются микобактериальные иммуногенные композиции, используемые для экспрессии белков слияния. ДНК, кодирующая указанные белки слияния, находится во внехромосомных плазмидах под контролем микобактериальных промоторов белков теплового шока и промоторов стрессовых белков. Описанные иммуногенные композиции предназначены для вызывания иммунных ответов у животных, отличных от человека, для продукции антител и не указывается на то, что они препятствуют развитию заболеваний, вызванных внутриклеточными патогенами, у млекопитающих. Кроме того, в патенте '475 не описаны рекомбинантные иммуногенные композиции, в которых используются белок-специфичные промоторы для экспрессии внеклеточных неслитых белков.
В патенте США номер 6467967, опубликованном теми же изобретателями, заявляются иммуногенные композиции, содержащие рекомбинантную БЦЖ, с внехромосомной последовательностью нуклеиновой кислоты, содержащей ген, кодирующий крупный внеклеточный белок M. tuberculosis размером 30 кДа, где указанный крупный внеклеточный белок M. tuberculosis размером 30 кДа сверхэкспрессируется и секретируется. Кроме того, авторы настоящего изобретения подали частично продолженную заявку (заявка на патент США, серийный номер 10/261981, подана 30 сентября 2002 года), заявляющую дополнительную рекомбинантную БЦЖ, которая сверхэкспрессирует другие крупные внеклеточные белки M. tuberculosis.
Следовательно, до сих пор существует необходимость в рекомбинантных иммуногенных композициях против внутриклеточного патогена, которые экспрессируют крупные внеклеточные неслитые белки внутриклеточных патогенов и которые тесно связаны с иммуногенной композицией. Кроме того, существует необходимость в рекомбинантных иммуногенных композициях против внутриклеточного патогена, которые способны к сверхэкспрессии рекомбинантных внеклеточных неслитых белков благодаря внехромосомной ДНК, содержащей промоторы гена белков, отличных от белков теплового шока, или промоторы гена белков, отличных от стрессовых белков.
Конкретно, все еще есть острая необходимость в создании иммуногенных композиций против внутриклеточного патогена, которые обеспечивают реципиентам защиту от заболеваний и которые дают бóльшую защиту, чем защита у реципиентов при использовании иммуногенной композиции на основе БЦЖ. Кроме того, как в развитых, так и неразвитых странах существует острая необходимость в недорогом иммунотерапевтическом и профилактическом способе лечения туберкулеза и других заболеваний, вызываемых внутриклеточными патогенами.
Кроме того, существует необходимость в иммуногенных композициях против внутриклеточного патогена, которые могли бы безопасно вводиться индивидуумам с иммуносупрессией или с частичной иммуносупрессией.
Следовательно, целью настоящего изобретения является разработка иммуногенных композиций для диагностики, лечения, профилактики, ингибирования или ослабления заболевания, вызванного внутриклеточными патогенами.
Другой целью настоящего изобретения является разработка иммуногенных композиций для диагностики, лечения, профилактики, ингибирования или ослабления заболевания, вызванного внутриклеточными патогенами, используя внутриклеточные патогены, которые трансформированы для экспрессии крупных рекомбинантных иммуногенных антигенов того же внутриклеточного патогена, другого внутриклеточного патогена или их обоих.
Еще одной целью настоящего изобретения является разработка иммуногенных композиций для диагностики, лечения, профилактики, ингибирования или ослабления микобактериальных заболеваний, используя рекомбинантные БЦЖ, которые экспрессируют внеклеточный(ые) белок(и) патогенной микобактерии.
Еще одной целью настоящего изобретения является разработка иммуногенных композиций для диагностики, лечения, профилактики, ингибирования или ослабления туберкулеза, используя рекомбинантные штаммы БЦЖ, которые экспрессируют и секретируют один или более крупных внеклеточных белков Mycobacterium tuberculosis.
Еще одной целью настоящего изобретения является разработка указанных выше иммуногенных композиций в такой форме, которая может безопасно вводиться индивидуумам с иммуносупрессией или с частичной иммуносупрессией.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение достигает указанных выше и других целей за счет нового класса иммуногенных композиций и иммунотерапевтических средств, а также методов диагностики, лечения, профилактики, ингибирования или ослабления заболеваний, вызываемых внутриклеточными патогенами, у млекопитающих. Исторически иммуногенные композиции и иммунотерапевтические средства против внутриклеточного патогена получали из самого внутриклеточного патогена или близкородственных ему видов. Эти старые модели иммуногенных композиций полностью состояли из микроорганизма или его субъединиц. Например, первая и в настоящее время единственная доступная иммуногенная композиция для Mycobacterium tuberculosis представляет собой аттенюированную живую иммуногенную композицию, полученную из близкородственного внутриклеточного патогена M. bovis. Недавно авторами настоящего изобретения было обнаружено, что специфические внеклеточные продукты внутриклеточных патогенов, которые секретируются в среду для роста, могут использоваться как в виде индивидуальных субъединиц, так и в виде сочетаний субъединиц, для стимулирования сильных иммунных ответов у млекопитающих. Однако отсутствовали доказательства того, что указанные субъединичные иммуногенные композиции превосходят по своим свойствам исходную аттенюированную иммуногенную композицию, полученную из M. bovis.
В настоящем изобретении подробно описываются иммуногенные композиции и иммунотерапевтические средства, состоящие из рекомбинантных аттенюированных внутриклеточных патогенов, которые трансформированы и экспрессируют внеклеточный(ые) белок(и) (рекомбинантных иммуногенных антигенов) другого или того же самого внутриклеточного патогена. В одном из вариантов иммуногенные композиции по настоящему изобретению получают с использованием рекомбинантных штаммов бациллы Кальметта-Герена или БЦЖ. В этом варианте рекомбинантная БЦЖ экспрессирует крупные внеклеточные белки патогенных микобактерий, включая, но не ограничиваясь ими, M. tuberculosis, M. leprae и M. bovis, если назвать лишь некоторые из них.
Крупные внеклеточные белки, экспрессируемые рекомбинантной БЦЖ, включают, но не ограничиваются ими, белки размером 12 кДа, 14 кДа, 16 кДа, 23 кДа, 23,5 кДа, 30 кДа, 32А кДа, 32В кДа, 45 кДа, 58 кДа, 71 кДа, 80 кДа и 110 кДа Mycobacterium sp. и соответствующие аналоги, гомологи и их субъединицы, включая рекомбинантные неслитые белки, белки слияния и их производные. Специалистам в данной области очевидно, что величина молекулярной массы, используемая для идентификации крупных внеклеточных белков микобактерий и других внутриклеточных патогенов, является лишь приблизительной. Специалистам в области рекомбинантной технологии и молекулярной биологии понятно, что возможно осуществлять одновременную экспрессию (совместную трансляцию) указанных белков с дополнительными аминокислотами, полипептидами и белками, также возможно экспрессировать эти белки в укороченных формах. Полученные модифицированные белки, рассматриваемые в контексте настоящего изобретения, включают нативные белки, неслитые белки, белки слияния, гибридные белки или химерные белки. Для целей настоящего изобретения белки слияния определяются как включающие, но не ограничиваясь этим, продукты двух или более кодирующих последовательностей из разных генов, которые могут быть клонированы вместе и которые после трансляции образуют одну полипептидную последовательность.
В настоящем изобретении также описываются рекомбинантные аттенюированные иммуногенные композиции на основе внутриклеточного патогена, которые сверхэкспресситуют неслитые белки по меньшей мере из одного другого внутриклеточного патогена. Указанная цель достигается использованием внехромосомных нуклеиновых кислот для экспрессии по меньшей мере одного рекомбинантного гена иммуногенного антигена и при введении указанного(ых) гена(ов) под контроль промоторов гена белка, не относящегося к белкам теплового шока, или промоторов гена белка, не относящегося к стрессовым белкам, предпочтительно под контроль промоторных последовательностей специфичного белка. Следовательно, получают иммуногенные композиции, включающие неслитые рекомбинантные иммуногенные антигены, экспрессированные в бóльших количествах, чем это возможно в том случае, когда гены, кодирующие рекомбинантные иммуногенные композиции, стабильно интегрированы в геномную ДНК иммуногенной композиции. В результате получают иммуногенные композиции на основе внутриклеточного патогена, которые неожиданно обладают повышенной специфичностью и эффективностью, чем существующие субъединичные или аттенюированные иммуногенные композиции на основе внутриклеточного патогена.
Кроме того, в настоящем изобретении описываются способы лечения и профилактики заболеваний у млекопитающих, вызываемых внутриклеточными патогенами, в которых используют иммуногенные композиции по настоящему изобретению. Частичный перечень большого числа внутриклеточных патогенов, которые могут использоваться в качестве аттенюированного организма и/или источника рекомбинантных иммуногенных антигенов, включает, но им не ограничивается, Mycobacterium bovis, M. tuberculosis, M. leprae, M. kansasii, M. avium, Mycobacterium sp., Legionella pneumophila, L. longbeachae, L. bozemanii, Legionella sp., Rickettsia rickettsii, Rickettsia typhi, Rickettsia sp., Ehrlichia chaffeensis, Ehrlichia phagocytophila geno group, Ehrlichia sp., Coxiella burnetii, Leishmania sp., Toxoplasma gondii, Trypanosoma cruzi, Chlamydia pneumoniae, Chlamydia sp., Listeria monocytogenes, Listeria sp. и Histoplasma sp.
Понятно, что иммуногенные композиции по настоящему изобретению могут вводиться любым способом, при котором возникает иммунный ответ и который включает, но ими не ограничивается, внутрикожный, подкожный, внутримышечный, интраназальный, внутрибрюшинный, пероральный путь или ингаляцию. По прошествии соответствующего периода после прививки млекопитающих стимулируют воздействием инфицирующего аэрозоля, содержащего M. tuberculosis. У млекопитающих, получавших иммуногенную композицию по настоящему изобретению, абсолютно не обнаруживали заболевания по сравнению с млекопитающими, получавшими только одну БЦЖ, только один крупный внеклеточный белок или любое их сочетание.
В одном из вариантов осуществления настоящего изобретения иммуногенная композиция, содержащая рекомбинантную БЦЖ с последовательностью внехромосомной нуклеиновой кислоты и ген, кодирующий по меньшей мере один внеклеточный белок микобактерии, где указанный крупный внеклеточный белок микобактерий сверхэкспрессируется и секретируется, индуцируя иммунный ответ у животного.
В другом варианте осуществления настоящего изобретения иммуногенная композиция содержит рекомбинантную БЦЖ с последовательностью внехромосомной нуклеиновой кислоты, которая содержит ген, кодирующий крупный внеклеточный неслитый белок Mycobacterium tuberculosis с массой 23,5 кДа, под контролем промотора, где указанный промотор не является промотором белка теплового шока или промотором стрессового белка и где крупный внеклеточный неслитый белок с массой 23,5 кДа сверхэкспрессируется и секретируется, индуцируя иммунный ответ у животного.
В еще одном из вариантов осуществления настоящего изобретения иммуногенная композиция содержит рекомбинантную БЦЖ с последовательностью внехромосомной нуклеиновой кислоты, которая содержит ген, кодирующий крупный внеклеточный неслитый белок Mycobacteriumtuberculosis 32А кДа под контролем промотора, где указанный промотор не является промотором белка теплового шока или промотором стрессового белка и где крупный внеклеточный неслитый белок 32А кДа сверхэкспрессируется и секретируется, индуцируя иммунный ответ у животного.
В другом варианте осуществления настоящего изобретения иммуногенная композиция содержит рекомбинантную БЦЖ с последовательностью внехромосомной нуклеиновой кислоты, которая содержит генетическую конструкцию с, по меньшей мере, одним геном, кодирующим крупный внеклеточный Mycobacterium tuberculosis (Mtb) размером 30 кДа и крупный внеклеточный неслитый белок Mtb размером 23,5 кДа, где крупный внеклеточный белок Mtb 30 кДа и крупный внеклеточный неслитый белок размером 23,5 кДа сверхэкспрессируются и секретируются, индуцируя иммунный ответ у животного.
В другом иллюстративном варианте осуществления настоящего изобретения иммуногенная композиция включает в себя рекомбинантную БЦЖ с последовательностью внехромосомной нуклеиновой кислоты, которая содержит ген, кодирующий крупный внеклеточный неслитый белок Mycobacterium bovis размером 30 кДа под контролем промотора, где указанный промотор не является промотором белка теплового шока или промотором стрессового белка и где крупный внеклеточный неслитый белок Mycobacterium bovis размером 32 кДа сверхэкспрессируется и секретируется из указанной рекомбинантной БЦЖ, индуцируя гуморальный и клеточный иммунный ответ у животного.
Еще в одном из вариантов осуществления настоящего изобретения иммуногенная композиция включает в себя рекомбинантную БЦЖ с последовательностью внехромосомной нуклеиновой кислоты, которая содержит ген, кодирующий крупный внеклеточный неслитый белок Mycobacterium leprae размером 30 кДа под контролем промотора, где указанный промотор не является промотором белка теплового шока или промотором стрессового белка и где крупный внеклеточный неслитый белок Mycobacterium leprae размером 30 кДа сверхэкспрессируется и секретируется из рекомбинантной БЦЖ, индуцируя гуморальный и клеточный иммунный ответ у животного.
Другие варианты осуществления настоящего изобретения включают в себя иммуногенные композиции, где аттенюированный внутриклеточный патоген (например, рекомбинантная БЦЖ) представляет собой ауксотрофный организм с регулируемым ростом. В контексте настоящего описания термин "регулируемый рост" относится к ауксотрофному организму, который растет при наличии определенного питательного вещества. Такое определенное питательное вещество либо вводят совместно с иммуногенной композицией, либо вводят после введения иммуногенной композиции реципиенту.
В одном из вариантов ауксотрофный организм с регулируемым ростом представляет собой рекомбинантную БЦЖ, которая трансформирована и сверхэкспрессирует и секретирует по меньшей мере один крупный внеклеточный белок M. tuberculosis.
В другом варианте осуществления настоящего изобретения таким определенным питательным веществом, требуемым для регулирования роста ауксотрофного организма с регулируемым ростом, является аминокислота.
Другой вариант осуществления настоящего изобретения включает в себя аттенюированную рекомбинантную БЦЖ (штамм Tice), в которой альфа-субъединицу нитратредуктазы (ген narG) разрушают путем аллельного обмена. Затем эту высокоаттенюированную narG БЦЖ трансформируют, используя по меньшей мере одну гетерологичную нуклеиновую кислоту, кодирующую по меньшей мере один крупный внеклеточный белок Mtb. Полученный высокоаттенюированный narG-мутированный трансформант используют в качестве иммуногенной композиции у млекопитающих с иммуносупрессией.
Другие объекты, особенности и преимущества настоящего изобретения будут очевидны специалистам в данной области при рассмотрении приведенного ниже подробного описания предпочтительных иллюстративных вариантов осуществления изобретения в сочетании с чертежами, которые кратко описываются ниже.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
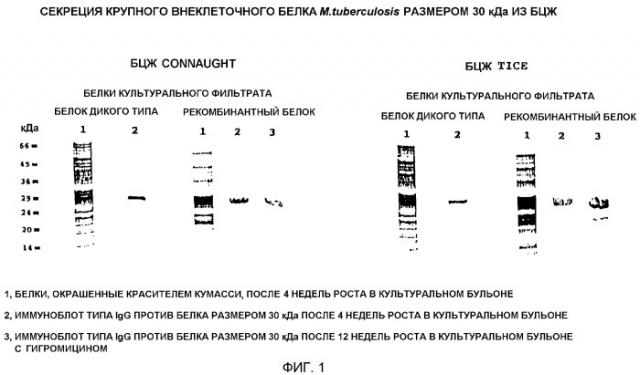
На фиг.1 показаны гели, окрашенные красителем кумасси синим (Coomassie blue), помеченные как 1а и 1b, которые иллюстрируют секрецию рекомбинантного белка Mycobacterium tuberculosis размером 30 кДа трансформированными штаммами БЦЖ из культуральных фильтратов.
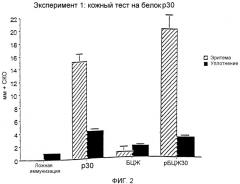
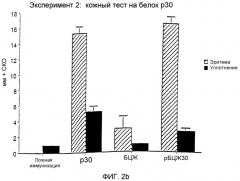
На фиг.2 графически показаны результаты двух экспериментов, помеченных как 2а и 2b, проведенных для сравнения результатов кожных тестов у морских свинок, которым прививали рекомбинантную иммуногенную композицию БЦЖ, экспрессирующую крупный внеклеточный белок M. tuberculosis размером 30 кДа, только БЦЖ, только рекомбинантный белок размером 30 кДа или ложную иммуногенную композицию.
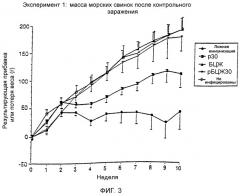
На фиг.3 графически показано изменение массы тела морских свинок, помеченных как 3а и 3b, после стимуляции M. tuberculosis после иммунизации.
На фиг.4а графически показано количество колониеобразующих единиц (КОЕ) инфекционного M. tuberculosis, выделенных из легких морских свинок после стимуляции M. tuberculosis после иммунизации.
На фиг.4b графически показано количество колониеобразующих единиц (КОЕ) инфекционного M. tuberculosis, выделенных из селезенки морских свинок после стимуляции M. tuberculosis после иммунизации.
На фиг.5 графически показана реакция на кожную пробу у морских свинок в ответ на ложную иммунизацию иммуногенной композицией, на введение БЦЖ и БЦЖ в сочетании с рекомбинантным белком M. tuberculosis размером 30 кДа.
На фиг.6 графически показаны титры антител на очищенный рекомбинантный крупный внеклеточный белок M. tuberculosis 30 кДа (р30), крупный внеклеточный белок 32А кДа (р32A) и крупный внеклеточный белок размером 23,5 кДа (р23,5).
КРАТКОЕ ОПРЕДЕЛЕНИЕ ТЕРМИНОВ
Для облегчения понимания приведенного ниже подробного описания примеров и приведенной формулы изобретения может быть полезно дать некоторые определения. Указанные определения по своему характеру являются неограничивающими и приводятся лишь для удобства читателя.
Ауксотроф или ауксотрофный: В контексте настоящего описания термин "ауксотроф" относится к микроорганизму, имеющему спецефические потребности в питании, которые не требуются организму дикого типа. В отсутствие требуемого питательного вещества ауксотроф не растет, тогда как организм дикого типа растет.
Ген: Термин "ген" в контексте настоящего описания относится по меньшей мере к части генетической конструкции, содержащей промотор и/или другие регуляторные последовательности, необходимые для экспрессии или для модификации экспрессии генетической конструкции.
Генетическая конструкция: Термин "генетическая конструкция" в контексте настоящего описания обозначает последовательность нуклеиновой кислоты, кодирующей по меньшей мере один крупный внеклеточный белок по меньшей мере одного внеклеточного патогена. В одном из вариантов осуществления настоящего изобретения генетическая конструкция представляет собой внехромосомную ДНК.
Регулируемый рост: В контексте настоящего описания термин "регулируемый рост" относится к ауксотрофной форме иммуногенных композиций по настоящему изобретению. Рост регулируется введением питательного вещества, необходимого для роста ауксотрофа, в концентрации, достаточной для индукции роста.
Хозяин: В контексте настоящего описания термин "хозяин" относится к реципиенту иммуногенных композиций по настоящему изобретению. Примерами организмов-хозяев являются млекопитающие, включающие, но не ограничиваясь, приматов, грызунов, коров, лошадей, собак, кошек, овец, коз и свиней. В одном из вариантов осуществления настоящего изобретения указанным организмом-хозяином является человек.
Иммуноген: В контексте настоящего описания термин "иммуноген" обозначает любой субстрат, который вызывает иммунный ответ в организме хозяина. Иммуногены по настоящему изобретению включают, но ими не ограничиваясь, крупные внеклеточные белки и их рекомбинантные формы, полученные из внутриклеточных патогенов, таких как, не ограничиваясь ими, представители рода Mycobacterium.
Иммуногенная композиция: В контексте настоящего описания термин "иммуногенная композиция" включает рекомбинантный вектор, вместе или без адъюванта, такой как внутриклеточный патоген, который экспрессирует и/или секретирует иммуноген in vivo, где указанный иммуноген вызывает иммунную реакцию в организме-хозяине. Иммуногенные композиции по настоящему изобретению могут включать или могут не включать в себя ауксотрофный организм в виде трансформанта.