Способ моделирования процесса образования зубного камня
Иллюстрации
Показать всеИзобретение относится к экспериментальной медицине, а именно к методам моделирования патологических процессов, протекающих в полости рта, и может быть использовано для моделирования процесса образования зубного камня. Для этого воздействуют на зуб в течение 7-180 дней искусственно созданной средой следующего состава: CaCl2 - 0.2575 г/л, (NH4)2HPO4 - 0.2376 г/л, К2HPO4 - 1.2107 г/л, NaF - 0.4452 г/л, MgCl2 - 0.1319 г/л, NaHCO3 - 0.6216 г/л, KCl - 3.0843 г/л. Способ обеспечивает возможность обнаружения предрасположенности к образованию зубного камня и последующей выработки профилактических мер его возникновения и роста. 3 табл., 5 ил.
Реферат
Изобретение относится к области медицины, к методам экспериментального моделирования патологических процессов, протекающих в полости рта, в частности, процесса образования зубного налета и роста зубного камня.
Характерным патогенным новообразованием, возникающим на зубах 75-80% людей, являются зубные камни. Зубной камень - отложения на зубах, образующиеся в результате преципитации из слюны фосфатов и карбонатов кальция и магния в органическую матрицу зубного камня, являющуюся ядром образования.
Ряд авторов указывают на важную роль слюны в образовании зубного камня. Процесс камнеобразования в полости рта начинается с изменений в минералообразующих средах. Повышение концентрации Са2+, Mg2+, К+, Cl- и недостаточный синтез защитных белков или нарушение их структуры превращают среду в кинетически нестабильную, что вызывает понижение агрегативной устойчивости ротовой жидкости.
Наиболее близким по технической сущности к заявляемому способу является способ синтеза гидроксилапатитов в среде синтетической биологической жидкости (SBF), в качестве которой выбрана плазма крови человека [A.Tas «Synthesis of biomimetic Cahydrohyapatite powders at 37°С in synthetic body fluids», Biomaterials 21(2000) 1429-1438]. В данном способе синтезировали гидроксилапатит для замещения костной ткани с использованием среды, моделирующей состав плазмы крови человека (по справочным данным), при физиологических значениях рН и температуры. Также устанавливалась стабильность полученных фаз при нагревании до 1600°С.
Данный способ не связывал протекание различных патологических процессов (в том числе и образование зубного камня) с изменением состава биологической жидкости, а также не моделировал биологическую систему при отклонениях состава биологической жидкости от нормы.
Задачей заявляемого изобретения является разработка способа экспериментального моделирования процесса образования зубного камня, выявление условий, способствующих камнеобразованию в полости рта, с целью обнаружения предрасположенности к данному заболеванию и последующей выработки профилактических мер возникновения и роста зубного камня.
Указанный технический результат достигается тем, что в способе моделирования процесса образования зубного камня исследуют ротовую жидкость группы людей, имеющих зубные отложения, и группы людей, не имеющих заболеваний полости рта и пародонта, выделяют диагностически значимые параметры ротовой жидкости для создания модельной среды, полученные данные обрабатывают методами математической статистики (сравнение доверительных интервалов), выявляют достоверные различия в составе слюны первой и второй групп людей, на основе полученных данных создают модельную среду, в которую помещают здоровый зуб, и проводят наблюдение в течение длительного времени. Модельная среда имеет слабощелочную реакцию и завышенное по сравнению с группой здоровых лиц содержание кальция, калия и неорганического фосфора, а также более низкое содержание белка. Создают модельную среду следующего состава: CaCl - 0.2575 г/л, (NH4)2HPO4 - 0.2376 г/л, K2HPO4 - 1.2107 г/л, NaF - 0.4452 г/л, MgCl - 0.1319 г/л, NaHCO3 - 0.6216 г/л, KCl - 3.0843 г/л. При этом через 7-14 дней образуется налет на зубе в виде брушита и аморфного фосфата кальция, а через 60-180 дней на зубе, помещенном в модельную систему, образуется гидроксилапатит, который является основным компонентом зубных камней человека.
Способ поясняется чертежами:
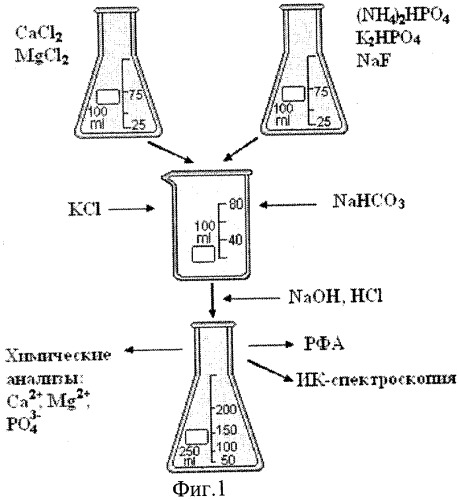
фиг.1 - схема модельного эксперимента;
фиг.2 - модельная система;
фиг.3 - фотография зуба после проведения модельного эксперимента - вокруг проволоки на поверхности зуба виден образовавшийся зубной камень;
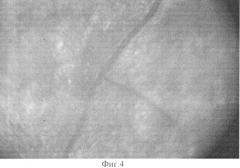
фиг.4 - микрофотография зубного камня на поверхности зуба - на фотографии видны микротрещины поверхности зуба и белый налет - начальная стадия образования зубного камня;
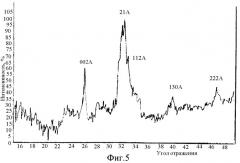
фиг.5 - рентгенограмма образца зубного камня (ось х - угол отражения, ось у - интенсивность рефлекса) - 002, 211, 112, 130 и 222 - основные рефлексы, характерные для гидроксилапатита.
Способ осуществляется следующим образом.
Для определения параметров ротовой жидкости были проведены следующие исследования. Материалом исследования служила слюна 80 пациентов. Забор слюны осуществляли утром, натощак, до чистки зубов в стерильную пробирку с плотно закрывающейся крышкой. Собранную слюну центрифугировали в течение 10 минут при скорости 3000 об/мин в лабораторной медицинской центрифуге ОПЛ-8. Для определения физико-химических параметров ротовой жидкости использовались методики, адаптированные в стоматологии для изучения ротовой жидкости [Питаева А.Н., Коршунов А.П., Дистель В.А. и др. «Физико-химические методы исследования смешанной слюны в клинической и экспериментальной стоматологии» (учебное пособие). - Омск, 2001]. Неорганический фосфор в ротовой жидкости определяли по методу Больца и Льюка [Больц Д.М., Льюк Ч.Г. «Колориметрические методы определения неметаллов», М., 1963], для количественного определения белка использовали биуретовую реакцию [Леус П.А. «Клинико-экспериментальное исследование патогенеза, патогенетической консервативной терапии и профилактики кариеса зубов». Автореферат дис. д-ра мед. наук. - М., 1977].
Осмотр полости рта осуществлялся с помощью стандартного набора стоматологических инструментов (зонда, зеркала и пинцета). У участников исследования проводилось выявление кариозных полостей, пломб и удаленных зубов, оценка состояния тканей пародонта, определение уровня гигиены полости рта, оценка состояния пломб. Интенсивность кариеса описывают индексом КПУ как сумму количеств кариозных (К), пломбированных (П) и удаленных (У) зубов. Индекс КПУП включает в себя сумму всех кариозных полостей, пломбированных кариозных полостей и удаленных зубов. Для оценки гигиенического состояния полости рта визуально с помощью зубоврачебного зонда определяли зубной налет и зубной камень на губных поверхностях 11 и 13, щечных поверхностях 16 и 26 и язычных поверхностях 36 и 46. Оценку зубного налета (ЗН) проводили по четырехбалльной системе: 0 - ЗН не обнаружен, 1 - мягкий ЗН покрывает 1/3 зуба или плотный коричневый налет в любом количестве, 2 - мягкий ЗН покрывает 2/3 поверхности зуба, 3 - мягкий ЗН покрывает более 2/3 поверхности зуба. ИЗН = (сумма показателей шести зубов): 6. Оценку зубного камня (ЗК) также проводили по четырехбалльной системе: 0 - ЗК не обнаружен, 1 - наддесневой ЗК покрывает 1/3 поверхности зуба, 2 - наддесневой ЗК покрывает 2/3 поверхности зуба или имеется поддесневой ЗК в виде отдельных конгломератов, 3 - наддесневой ЗК покрывает более 2/3 зуба или поддесневой ЗК окружает пришеечную часть зуба. ИЗК = (сумма показателей шести зубов): 6. Состояние пародонта оценивали с помощью папиллярно-маргинально-альвеолярного индекса (РМА).
В ходе дальнейшего исследования были выделены две группы людей:
1) группа 1 - люди, имеющие зубные отложения в полости рта. Исследована слюна 40 человек (50%). Результаты клинического обследования состояния полости рта у лиц с наличием зубного камня выявили нарушения состояния твердых тканей зубов кариозного и некариозного происхождения, а также изменение состояния тканей пародонта (табл.1).
| Таблица 1Индексная оценка состояния полости рта у лиц с наличием зубного камня в различных возрастных группах | |||
| Изучаемые показатели | Значения изучаемых показателей | ||
| 30-39 лет | 40-49 лет | 50-59 лет | |
| КПУ | 6,08±2 | 4,69±3 | 4,07±2 |
| КПУП | 6,92±2 | 6,77±3 | 6,21±3 |
| РМА, % | 28,62±7 | 30,69±7 | 29,79±10 |
| ИЗН, баллы | 0,64±0,5 | 0,54±0,2 | 0,45±0,3 |
| ИЗК, баллы | 0,62±0,3 | 0,58±0,2 | 0,61±0,4 |
2) группа 2 - контрольная группа - 40 человек (50%). Взятую в качестве сравнения группу лиц, резистентных к заболеваниям, составили люди с одинаковым соматическим статусом «практически здоровые», а также без заболеваний пародонта и слизистой оболочки полости рта.
У пациентов, не имеющих в полости рта зубных отложений, при анализе состояния полости рта установлено следующее (табл.2):
| Таблица 2Индексная оценка состояния полости рта у лиц с отсутствием зубного камня в различных возрастных группах | |||
| Изучаемые показатели | Значения изучаемых показателей | ||
| 30-39 лет | 40-49 лет | 50-59 лет | |
| КПУ | 3,62±3 | 4,38±4 | 5,21±3 |
| КПУП | 6,23±5 | 6,08±4 | 6,57±3 |
| РМА, % | 8,15±7 | 5,15±4 | 7,93±2 |
| ИЗН, баллы | 0,8±0,5 | 0,74±0,3 | 0,96±0,7 |
Сравнительная оценка состояния полости рта у лиц с наличием и отсутствием зубных отложений (табл.1 и 2) показала, что при наличии зубных камней повышается значение индекса РМА, характеризующего состояние тканей пародонта, т.е. происходит ухудшение состояния тканей пародонта и гигиенического состояния полости рта. Индексы КПУ и КПУП характеризуют распространенность и интенсивность кариеса. В обеих группах наблюдается низкая степень активности кариеса (КПУ<9).
Выявленные нами некоторые особенности индексной характеристики состояния органов и тканей полости рта у лиц с наличием и отсутствием зубных отложений позволили предположить, что их характер может зависеть от ситуации в полости рта, определяемой составом и свойствами ротовой жидкости (табл.3). Статистическая обработка данных проведена методом сравнения доверительных интервалов с помощью пакета программ Statistica 6.0.
| Таблица 3Сравнительная характеристика состава ротовой жидкости лиц с различным состоянием полости рта | ||
| Показатель | Группа №1 n=40*; t=1,96** | Группа №2 n=40; t=1,96 |
| рН | 7,15±0,08 | 6,93±0,05 |
| С (Na), г/л | 0,203±0,013 | 0,239±0,016 |
| С (К), г/л | 0,993±0,057 | 0,656±0,031 |
| Общий кальций, г/л | 0,067±0,003 | 0,045±0,001 |
| Фосфор, г/л | 0,203±0,008 | 0,173±0,006 |
| Вязкость, сП | 0,905±0,014 | 0,822±0,058 |
| Поверхностное натяжение, мН/м | 62,46±0,52 | 64,99±0,30 |
| Белок, мг/мл | 0,931±0,079 | 1,201±0,068 |
| Произведение растворимости гидроксилапатита, *10-7 | 9,31±0,67 | 3,86±0,19 |
| *n - количество человек в группе; **t - коэффициент Стьюдента |
Согласно экспериментальным данным ротовая жидкость лиц с наддесневыми зубными отложениями имеет слабощелочную реакцию среды (7,15±0,08). Различия величины этого показателя для группы №1 с контрольной группой статистически значимы. Колебания общего содержания калия, концентрации кальция и неорганического фосфора также статистически достоверны.
Можно предположить, что изменение именно этих параметров приводит к камнеобразованию в полости рта. Так, у пациентов группы №1 завышено содержание общего кальция и неорганического фосфора в слюне, что благоприятствует образованию нерастворимых фосфатов (брушит и гидроксилапатит). Отмечено также снижение содержания белка, что возможно связано с его переходом в состав комплексов с минеральными компонентами ротовой жидкости и зубных камней (ионы меди, цинка. железа и т.д.). Также в условиях камнеобразования в полости рта происходит сдвиг рН в щелочную сторону. Именно при этих значениях рН создаются оптимальные условия для образования гидроксилапатита - основной минеральной компоненты зубных камней.
Таким образом, установлены факторы, способствующие отклонению параметров ротовой жидкости от нормы и образованию камней в полости рта.
Далее осуществили постановку модельного эксперимента для определения возможности образования зубных камней в гипотетическом растворе, моделирующем состав ротовой жидкости. При проведении эксперимента использовались значения концентраций, полученных нами для группы пациентов с зубными отложениями в полости рта.
В качестве исходных реагентов использовались соли марки ч.д.а. и х.ч. и дистиллированная вода. Выбор исходных реагентов и их соотношение в растворе определялись таким образом, чтобы концентрации ионов и ионная сила раствора были максимально приближены к данным параметрам моделируемой системы, а именно ротовой жидкости.
Для каждой серии экспериментов были подготовлены растворы, содержащие катионы и анионы, при совместном присутствии которых в данных условиях не образуются малорастворимые соединения. После смешения эквивалентных объемов растворов производили корректировку значений рН путем добавления 6 М раствора NaOH или концентрированной HCl. С целью предотвращения уменьшения концентрации в растворе карбонат ионов (за счет гидролиза в кислой среде), необходимое количество NaHCO3 добавляли при рН 5,5-6,0. После корректировки рН моделируемого раствора до необходимого значения добавляли определенную массу кристаллического KCl, рассчитанную таким образом, чтобы ионная сила раствора была максимально приближена к моделируемой системе (см. фиг.1, 2). Готовый раствор состава CaCl - 0.2575 г/л, (NH4)2HPO4 - 0.2376 г/л, К2HPO4 - 1.2107 г/л, NaF - 0.4452 г/л, MgCl2 - 0.1319 г/л, NaHCO3 - 0.6216 г/л, KCl - 3.0843 г/л помещали в стакан, в модельную систему подвешивали зуб и оставляли для кристаллизации в течение определенного времени (7, 14, 21, 28, 60, 90, 120, 150, 180 дней).
Для установления фазового и химического состава полученных твердых фаз были использованы методы рентгенофазового анализа (РФА), ИК - спектроскопии и методы химического анализа. При этом соотношение катионов и анионов в твердой фазе оценивали по разности начальных и конечных концентраций осадкообразующих ионов в модельном растворе по методикам химического анализа.
В результате проведенного исследования была получена серия осадков на поверхности зубов (см. фиг.3, 4). В зависимости от времени кристаллизации в составе осадков были определены следующие фазы: на первом этапе (7-14 дней) в составе зубного налета обнаружен только брушит, при увеличении времени кристаллизации происходит переход брушита в гидроксилапатит как более термодинамически стабильную фазу (60-180 дней). Сравнение фазового состава осадков, полученных в ходе модельного эксперимента, и зубных камней, удаленных у пациентов в ходе медицинского осмотра, показало, что состав практически идентичен (см. фиг.5), т.е. предложенная модельная система позволяет воспроизвести условия ротовой полости человека.
Таким образом, заявляемый способ позволяет выявить параметры, которые при отклонении от нормы вызывают образование зубного камня, и создать модельную систему, с помощью которой можно изучать эффективность воздействия лекарственных препаратов для профилактики возникновения и роста зубного камня.
Способ моделирования процесса образования зубного камня путем воздействия на зуб в течение 7-180 дней искусственно созданной средой следующего состава: CaCl2 0,2575 г/л; (NH4)2HPO4 0,2376 г/л; К2HPO4 1,2107 г/л; NaF 0,4452 г/л; MgCl2 0,1319 г/л; NaHCO3 0,6216 г/л; KCl 3,0843 г/л.