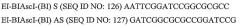Желудочно-кишечный пролиферативный фактор и его применения
Иллюстрации
Показать всеИзобретение относится к биотехнологии. Раскрыто применение полипептида, представляющего собой пролиферативный фактор (GIPF), в качестве активного начала в производстве лекарственного средства для стимуляции пролиферации эпителиальных клеток у млекопитающего субъекта, предусматривающее введение указанному субъекту терапевтически эффективного количества указанного лекарственного средства или для лечения желудочно-кишечного расстройства или повреждения слизистой оболочки ротовой полости у млекопитающего субъекта. Изобретение позволяет расширить ассортимент лекарственных средств для стимуляции пролиферации эпителиальных клеток или для лечения желудочно-кишечного расстройства или повреждения слизистой оболочки ротовой полости у млекопитающего субъекта. 2 и 13 з.п. ф-лы, 80 ил., 16 табл.
Реферат
1. УРОВЕНЬ ТЕХНИКИ
1.1. ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение, в общем, относится к композициям, которые содержат полипептиды и полинуклеотиды фактора пролиферации желудочно-кишечного тракта и способам их применения.
1.2. СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Список последовательностей предоставлен.
1.3. УРОВЕНЬ ТЕХНИКИ
Терапия ионизирующим излучением и цитотоксическая химиотерапия вызывают повреждения слизистой оболочки ротовой полости и желудочно-кишечного тракта, которые остаются существенной проблемой для пациентов, подвергающихся лечению антинеопластическими лекарственными средствами. Мукозит представляет собой воспаление слизистых оболочек и является очень распространенной проблемой в данной популяции пациентов вследствие применения химиотерапии и лучевой терапии, используемых в лечебных или паллиативных целях. Повреждения слизистой оболочки в желудочно-кишечном тракте, наблюдаемые в случае лучевой и химиотерапии (по отношению к указанным областям), включают деструкцию клеток крипт, уменьшение длины ворсинок и изъязвление и некроз эпителия желудочно-кишечного тракта (Berthrong M, World J. Surg. 10: 155-170 (1986)), которые лежат в основе расстройств, включая мукозит желудочно-кишечного тракта и энтероколит. Для пациентов это может означать боль в животе, геморрагическую диарею, мальабсорбцию и в некоторых случаях бактериальную транслокацию (Guzman et al., J. Surg. Res. 46: 104-107(1989)). Кроме того, химиотерапия и ионизирующее излучение могут поражать другие слизистые оболочки, включая слизистые оболочки ротовой части глотки и губ и слизистую оболочку пищевода. Хорошо известно, что терапия комбинированными способами при совместном воздействии облучением и химиотерапией может вызывать сильно выраженные симптомы стоматита у пациентов с раком головы и шеи и эзофагита у пациентов с мелкоклеточным раком легкого.
Химиотерапия и лучевая терапия вызывают повреждение слизистой ротовой полости и желудочно-кишечного тракта вследствие прямой и опосредованной токсичности. Механизм прямого мукозита заключается в неспецифическом убивании быстро делящихся базальных эпителиальных клеток, что приводит к истончению эпителия, воспалению, сниженному восстановлению клеток и в конце концов изъязвлению. Указанные болезненные повреждения также являются причиной повышенного риска локальной и системной инфекции. Опосредованная токсичность по отношению к слизистой оболочке является подобным продуктом индуцированной химиотерапией миелосупрессии, которая создает возможность для бактериальных и вирусных инфекций в месте прямого повреждения слизистой оболочки. Тяжесть указанных эффектов может препятствовать повышению доз, замедлять лечение и предписывать снижение доз, таким образом ограничивая эффективность лечения злокачественных опухолей.
Профилактика и лечение в случае индуцированных химиотерапией и лучевой терапией повреждений (слизистой оболочки) желудочно-кишечного тракта (мукозита) обычно влечет за собой назначение субоптимальных доз химиотерапии или лучевой терапии, модификацию доз по нисходящей при последующих курсах лечения после токсического воздействия или применение специфичных антидотов, таких как лейковорин после умеренных доз или высоких доз метотрексата (Allegra CJ. Antifolates. In: Chabner and Collins, eds. Cancer Chemotherapy: Principles and Practice. Philadelphia, Pa. JP Lippincott Co; 1990:110-153).
Повреждение слизистой оболочки желудочно-кишечного тракта также связано с хроническими воспалительными расстройствами желудочно-кишечного тракта, которые вместе называют воспалительным заболеванием кишечника. Для лечения воспалительного заболевания кишечника доступна основанная на цитокинах терапия (Bouma and Strober Nature Rev 3: 521-533 (2003)). Однако часто показана резекция тонкого кишечника у пациентов с воспалительным заболеванием кишечника, таким как болезнь Крона. Хирургическое удаление тонкого кишечника также может быть необходимо после травматического повреждения, при остром сосудистом расстройстве и злокачественной опухоли. Хирургическое удаление, при котором оставляют менее 200 см жизнеспособного тонкого кишечника, создает для пациента риск развития синдрома короткой кишки (SBS). SBS является расстройством, которое клинически определяют по мальабсорбции, диарее, нарушению баланса жидкости и электролитов и истощению. Ведение пациентов с SBS часто требует долговременного, если не в течение всей жизни, применения парентерального питания (DiBaise et al., Am. J. Gastroenterol. 99: 1823-1832 (2004)).
Таким образом, существует необходимость найти средства, которые можно использовать профилактически или терапевтически, чтобы повысить переносимость лечения антинеопластическими средствами, чтобы усовершенствовать современные способы терапии для лечения воспалительного заболевания кишечника и восстановить процессы пищеварения и всасывания, которые нарушены после хирургической резекции кишечника.
2. СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение отчасти основано на открытии того, что желудочно-кишечный пролиферативный фактор (GIPF) индуцирует пролиферацию эпителиальных клеток желудочно-кишечного тракта. Таким образом, композиции, содержащие GIPF, его фрагменты или аналоги, могут применяться для лечения состояний, при которых требуется эпителизация, например для лечения желудочно-кишечных расстройств, включая индуцированный химиотерапией и лучевой терапией мукозит, мукозит ротовой части глотки, губ и пищевода, воспалительное заболевание кишечника и другие состояния, включая раны, ожоги, глазные расстройства и любое расстройство, при котором требуется стимуляция пролиферации или регенерация эпителиальных клеток.
Соответственно, в одном варианте изобретение относится к композициям, содержащим терапевтически эффективное количество полипептида GIPF и фармацевтически приемлемый носитель.
Композиции согласно настоящему изобретению включают изолированные полинуклеотиды, кодирующие полипептиды GIPF, включая рекомбинантные молекулы ДНК и клонированные гены или их вырожденные варианты, особенно встречающиеся в природе варианты, такие как аллельные варианты. В частности, полинуклеотиды согласно настоящему изобретению основаны на полинуклеотиде GIPF, выделенном из библиотеки кДНК, полученной на основе мРНК кожи плода человека (SEQ ID NO: 2).
Композиции согласно настоящему изобретению также содержат векторы, такие как экспрессирующие векторы, содержащие полинуклеотиды согласно изобретению, клетки, генетически сконструированные так, чтобы они содержали такие полинуклеотиды, и клетки, генетически сконструированные для экспрессии таких полинуклеотидов.
Композиции согласно изобретению содержат изолированные полинуклеотиды, которые включают без ограничения полинуклеотид GIPF, его фрагмент или вариант; полинуклеотид, содержащий кодирующую полноразмерный белок SEQ ID NO: 2 или 3 (например, SEQ ID NO: 4; GIPFwt); полинуклеотид, содержащий последовательность, кодирующую V5-His-меченый белок, SEQ ID NO: 5 (например, SEQ ID NO: 6; GIPFt); полинуклеотид, содержащий нуклеотидную последовательность кодирующей последовательности доминантного зрелого белка SEQ ID NO: 9 (например, SEQ ID NO: 10); полинуклеотид, содержащий нуклеотидную последовательность кодирующей последовательности зрелого белка SEQ ID NO: 11 (например, SEQ ID NO: 12); полинуклеотид, содержащий нуклеотидную последовательность домена тромбомпондина SEQ ID NO: 13 (например, SEQ ID NO: 14), полинуклеотид с последовательностью SEQ ID NO: 15, содержащий нуклеотидную последовательность, которая кодирует последовательность доминантного зрелого белка, в которой отсутствует сайт расщепления фурином (например, SEQ ID NO: 16); полинуклеотид с последовательностью SEQ ID NO: 17, содержащий нуклеотидную последовательность, которая кодирует полипептид GIPF, который содержит мутантный сайт расщепления фурином (SEQ ID NO: 18); и полинуклеотиды, которые кодируют полипептиды GIPF, которые содержат последовательности разной длины полноразмерного GIPF (SEQ ID NO: 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104 и 177). Композиции полинуклеотидов согласно настоящему изобретению также содержат, но не ограничены указанным, полинуклеотид, который гибридизуется в жестких условиях гибридизации с (a) комплементом любой из нуклеотидных последовательностей, указанных в SEQ ID NO: 2, 3, 5, 9, 11, 13, 15, 17, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104 или 177; (b) нуклеотидной последовательностью, кодирующей любую из последовательностей SEQ ID NO: 4, 6, 8, 10, 12, 14, 16, 18, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105 или 178; полинуклеотид, который является вариантом (например, аллельным вариантом) любого полинуклеотида, указанного выше, имеющим по меньшей мере 70% (например, 75%, 80%, 85%, 90%, 92%, 94%, 96%, 98% или 99%) идентичности полинуклеотидной последовательности с полинуклеотидами; полинуклеотид, который кодирует видовой гомолог (например, ортолог) любого из полипептидов, указанных выше; или полинуклеотид, который кодирует полипептид, содержащий конкретный домен или укорочение полипептида с последовательностью SEQ ID NO: 4 или 6.
Данное изобретение, кроме того, относится к клонирующим или экспрессирующим векторам, содержащим по меньшей мере фрагмент полинуклеотидов, указанных выше, и клеткам-хозяевам или организмам, трансформированным указанными экспрессирующими векторами. Применимые векторы включают плазмиды, космиды, производные фага лямбда, фагмиды и тому подобное, которые хорошо известны в данной области. Соответственно, изобретение также относится к вектору, содержащему полинуклеотид согласно изобретению, и клетке-хозяину, содержащей полинуклеотид. В общем, вектор содержит начало репликации, функциональное по меньшей мере в одном организме, подходящие сайты рестрикции эндонуклеазами и селектируемый маркер для клетки-хозяина. Векторы согласно изобретению включают экспрессирующие векторы, векторы для репликации, векторы для создания зондов и векторы для секвенирования. Клеткой-хозяином согласно изобретению может быть прокариотическая или эукариотическая клетка и может быть одноклеточный организм или часть многоклеточного организма.
Фармацевтические композиции согласно настоящему изобретению содержат полипептиды, включающие без ограничения изолированный полипептид, выбранный из группы, состоящей из аминокислотных последовательностей SEQ ID NO: 4, 6, 10, 12, 14, 16, 18, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105 или 178. Полипептиды согласно изобретению также включают полипептиды с биологической активностью, которые кодируются (a) любым из полинуклеотидов, имеющим нуклеотидную последовательность, указанную в SEQ ID NO: 2, 3, 5, 9, 11, 13, 15, 17, 84, 86, 88, 90, 92, 94, 96, 98, 100, 102, 104 177 выше; или (b) полинуклеотидами, которые гибридизуются с комплементом полинуклеотидов по п.(a) в жестких условиях гибридизации. Также рассматриваются биологически или иммунологически активные аналоги любой из последовательностей белка, перечисленных в виде SEQ ID NO: 4, 6, 10, 12, 14, 16, 18, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105 или 178, и по существу их эквиваленты, которые сохраняют биологическую активность. Полипептиды согласно изобретению могут быть полностью или частично синтезированы химическим способом, но предпочтительно получены способами рекомбинации с применением генетически сконструированных клеток (например, клеток-хозяев) согласно изобретению. Изобретение относится к полипептидам, которые по меньшей мере на 85%, 90%, 92%, 94%, 96%, 98% или 99% идентичны любой из последовательностей SEQ ID NO: 4, 6, 10, 12, 14, 16, 18, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105 и 178. Изобретение также относится к полипептидам, которые отличаются по последовательности от любой из SEQ ID NO: 4, 6, 10, 12, 14, 16, 18, 85, 87, 89, 91, 93, 95, 97, 99, 101, 103, 105 и 178 на 20, 15, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 аминокислотным остатком. Изменения аминокислот могут быть консервативными или неконсервативными.
Изобретение также относится к способам получения полипептида GIPF, включающим в себя культивирование клеток-хозяев, содержащих экспрессирующий вектор, который содержит по меньшей мере фрагмент полинуклеотида GIPF, кодирующего полипептид GIPF согласно изобретению, в подходящей культуральной среде в условиях, обеспечивающих экспрессию требуемого полипептида, и очистку белка или пептид из культуры или из клеток-хозяев. Предпочтительные варианты включают варианты, в которых белок, полученный таким способом, является зрелой или доминантной зрелой формой белка.
Полипептиды согласно изобретению можно применять во множестве обычных процедур и способов, которые в настоящее время применяют по отношению к другим белкам. Например, полипептид согласно изобретению можно применять для создания антитела, которое специфично связывает полипептид. Такие антитела, особенно моноклональные антитела, применимы для выявления или количественной оценки полипептида в ткани.
В следующих вариантах настоящее изобретение относится к способу стимулирования пролиферации эпителиальных клеток. Способ заключается в контактировании эпителиальных клеток с композицией, которая содержит терапевтически эффективное количество полипептида GIPF, его фрагмента или аналога и фармацевтически приемлемый носитель. В частности, субъекту, нуждающемуся в стимулировании эпителиальных клеток (включая цитопротекцию, пролиферацию и/или дифференцировку), будет вводиться терапевтически эффективное или профилактически эффективное количество белка GIPF, его фрагментов или аналогов.
Во всех описанных способах эпителиальные клетки могут быть подвергнуты контакту с полипептидами GIPF in vitro или in vivo.
Также предлагается способ профилактики, лечения или облегчения патологического состояния, который включает в себя стадию введения субъекту млекопитающему терапевтически эффективного количества композиции, содержащей пептид согласно настоящему изобретению и фармацевтически приемлемый носитель.
В частности, полипептиды GIPF согласно изобретению можно применять для индукции пролиферации и/или дифференцировки клеток крипт желудочно-кишечного тракта, чтобы восстановить слой эпителия пищеварительного тракта. Таким образом, полипептиды и полинуклеотиды GIPF согласно изобретению можно использовать для лечения индуцированного химиотерапией или лучевой терапией мукозита и энтероколита и воспалительного заболевания кишечника. Их также можно использовать для лечения заболеваний и других состояний, включая раны, ожоги, глазные расстройства и любое расстройство, при котором требуется стимуляция пролиферации или регенерации эпителиальных клеток.
Полинуклеотиды и полипептиды согласно изобретению также можно использовать в качестве маркеров дифференцировки и развития эпителия желудочно-кишечного тракта.
Также предлагаются способы согласно изобретению для лечения расстройств, которые указаны в данном описании, которые заключаются во введении терапевтически эффективного количества композиции, содержащей полинуклеотид или полипептид согласно изобретению и фармацевтически приемлемый носитель, млекопитающему, у которого наблюдаются симптомы или тенденции, связанные с расстройствами, которые указаны в данном описании. Кроме того, изобретение относится к способам лечения заболеваний или расстройств, которые указаны в данном описании, включающим в себя стадию введения композиции, содержащей соединения и другие вещества, которые модулируют общую активность продуктов гена-мишени, и фармацевтически приемлемый носитель. Соединения и другие вещества могут влиять на осуществление такого модулирования либо на уровне экспрессии гена/белка-мишени, либо на уровне активности белка-мишени. В частности, предлагаются способы профилактики, лечения или облегчения патологического состояния, включая мукозит и воспалительное заболевание кишечника, раны, которые заключаются во введении млекопитающему, включая без ограничения человека, терапевтически эффективного количества композиции, содержащей полипептид согласно изобретению, или терапевтически эффективного количества композиции, содержащей связывающий партнер полипептидов GIPF согласно изобретению. Механизмы конкретного состояния или патологии будут определять, будут ли полезными полипептиды согласно изобретению или их связывающие партнеры для индивидуума, нуждающегося в лечении.
Изобретение, кроме того, относится к способам производства лекарственных средств, применимых в описанных выше способах.
Настоящее изобретение, кроме того, относится к способам выявления наличия полинуклеотидов или полипептидов согласно изобретению в образце (например, ткани или образце). Такие способы можно, например, использовать как часть прогностической и диагностической оценки расстройств, которые указаны в данном описании, и для идентификации субъектов, проявляющих предрасположенность к таким состояниям.
Изобретение относится к способу выявления полипептида согласно изобретению в образце, включающему в себя контактирование образца с соединением, которое связывается и образует комплекс с полипептидом в условиях и в течение периода времени, достаточного для образования комплекса, и регистрацию образования комплекса, так что если комплекс образуется, то выявляют полипептид.
Изобретение также относится к наборам, содержащим полинуклеотидные зонды и/или моноклональные антитела и необязательно стандарты количества для осуществления способов согласно изобретению. Кроме того, изобретение относится к способам оценки эффективности лекарственных средств и мониторинга улучшений у пациентов, вовлеченных в клинические испытания в отношении лечения расстройств, которые указаны выше.
Изобретение также относится к способам идентификации соединений, которые модулируют (т.е. увеличивают или уменьшают) экспрессию или активность полинуклеотидов и/или полипептидов согласно изобретению. Такие способы можно использовать, например, для идентификации соединений, которые усиливают терапевтическую активность полипептидов GIPF и ослабляют симптомы расстройств, которые указаны выше. Такие способы могут включать без ограничения анализы для идентификации соединений и других веществ, которые взаимодействуют (например, связываются) с полипептидами согласно изобретению.
Изобретение относится к способу идентификации соединения, которое связывается с полипептидом согласно настоящему изобретению, включающему в себя контактирование соединения с полипептидом в условиях и в течение времени, достаточного для образования комплекса полипептид/соединение, и регистрацию комплекса, так что если регистрируют комплекс полипептид/соединение, то идентифицируют соединение, которое связывается с полипептидом.
Также предлагается способ идентификации соединения, которое связывается с полипептидом, включающий в себя контактирование соединения с полипептидом в клетке в течение времени, достаточного для образования комплекса полипептид/соединение, при этом комплекс запускает экспрессию последовательности репортерного гена в клетке, и регистрацию комплекса посредством выявления экспрессии последовательности репортерного гена, так что если регистрируют комплекс полипептид/соединение, то идентифицируют соединение, которое связывается с полипептидом.
В другом варианте осуществления изобретения предлагается генная терапия посредством доставки полипептидов GIPF для лечения состояний или расстройств, указанных в данном описании.
В связанном варианте изобретение относится к применению вектора, содержащего ген, кодирующий полипептид GIPF, оперативно связанный с последовательностью регуляции экспрессии, которая обеспечивает экспрессию полипептида GIPF, в производстве лекарственного средства для лечения расстройств, которые указаны в данном описании. Более конкретно, изобретение относится к применению аденовирусного вектора согласно изобретению, например, такого как указанный ниже, в производстве лекарственного средства для лечения мукозита или воспалительного заболевания кишечника.
В дополнение к указанным выше способам и применениям изобретение относится к новому вирусному вектору, содержащему ген, кодирующий полипептид GIPF, оперативно связанный с последовательностью регуляции экспрессии. В предпочтительном варианте вирусным вектором является аденовирусный вектор. Вирусные векторы согласно изобретению могут обеспечивать ген, кодирующий любой полипептид GIPF, указанный выше.
Изобретение, кроме того, относится к фармацевтической композиции, содержащей любой из вирусных векторов согласно изобретению и фармацевтически приемлемый носитель.
В еще одном аспекте изобретение относится к трансгенной конструкции, содержащей нуклеиновую кислоту, кодирующую нативный белок GIPF человека, его аналог или фрагмент, под контролем последовательностей регуляции транскрипции, управляющих ее экспрессией в B-клетках. Трансгенная конструкция предпочтительно содержит специфичный для B-клеток промотор, такой как промотор каппа-цепи иммуноглобулина.
В другом аспекте изобретение относится к трансгенному млекопитающему, отличному от человека, которое продуцирует в своих B-клетках регистрируемые уровни нативного белка GIPF человека, его аналога или фрагмента, при этом указанное трансгенное млекопитающее имеет стабильно интегрированную в его геном последовательность нуклеиновой кислоты, кодирующую нативный белок GIPF человека, его аналог или фрагмент, обладающий биологической активностью нативного GIPF человека, оперативно связанную с последовательностями регуляции транскрипции, управляющими ее экспрессией в B-клетках. Последовательности регуляции транскрипции предпочтительно содержат специфичный для B-клеток промотор, такой как промотор каппа-цепи иммуноглобулина. Без ограничения трансгенным млекопитающим, отличным от человека, может быть, например, мышь, крыса, кролик, свинья, овца, коза или крупный рогатый скот.
В другом аспекте изобретение относится к способу скрининга выбранных для исследования лекарственных средств для лечения заболевания или расстройства, указанного в данном описании, включающему в себя (a) введение выбранного для исследования лекарственного средства трансгенной мыши, которая экспрессирует в своих B-клетках полипептид GIPF и у которой развивается растяжение кишечника, связанное с гиперпролиферацией эпителиальных клеток, и (b) оценку влияния выбранного для исследования лекарственного средства на гиперпролиферацию эпителиальных клеток. Выбранные для исследования лекарственные средства могут модулировать (т.е. увеличивать или уменьшать) экспрессию или активность полинуклеотидов и/или полипептидов согласно изобретению.
Изобретение также относится к способу лечения или облегчения патологического состояния, включая мукозит и воспалительное заболевание кишечника и раны, который включает в себя введение млекопитающему, включая, но не ограничивая указанным, человека, терапевтически эффективного количества полипептида GIPF вместе с цитокином.
В другом аспекте изобретение относится к фармацевтическим композициям, содержащим полипептид согласно изобретению, второе терапевтическое средство например цитокин, и фармацевтически приемлемый носитель.
Дополнительные аспекты и преимущества изобретения будут понятны специалистам в данной области при рассмотрении следующего описания, в котором подробно изложено практическое осуществление изобретения.
3. КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На Фигуре 1 изображена последовательность ДНК (SEQ ID NO: 2) (A) и соответствующая аминокислотная последовательность полноразмерного GIPF (SEQ ID NO: 4)(B). SEQ ID NO: 2 содержит 5-штрих- и 3-штрих-нетранслируемые области, связанные с открытой рамкой считывания.
На фигуре 2 изображена экспрессия мРНК GIPF в тканях человека (A) и мыши (B).
Фигура 3 является схематичным представлением полипептидов GIPF, входящих в композиции согласно изобретению. Числа, которые подчеркнуты, соответствуют номерам последовательностей SEQ ID NO полипептидов, а остальные числа являются номерами последовательностей SEQ ID NO кодирующих полинуклеотидных последовательностей.
На фигуре 4A показано выравнивание аминокислотных последовательностей с использованием BLASTP между белком GIPF, кодируемым последовательностью SEQ ID NO: 2 или 3 (например, SEQ ID NO: 4), и фактором роста стволовых клеток человека A1 SEQ ID NO: 23 (SEQ ID NO: 10 в PCT WO01/77169 A2), показано, что две последовательности обладают 63% сходством на протяжении от аминокислотного остатка 10 до 251 последовательности SEQ ID NO: 4 и от 11 до 257 аминокислотного остатка последовательности SEQ ID NO: 23, и 46% идентичностью на протяжении от 10 до 251 аминокислотного остатка последовательности SEQ ID NO: 4 и от 11 до 257 аминокислотного остатка последовательности SEQ ID NO: 23.
На фигуре 4B показано выравнивание аминокислотных последовательностей с использованием BLASTP между белком GIPF, кодируемым последовательностью SEQ ID NO: 2 или 3 (т.е., SEQ ID NO: 4), полипептидом GIPF и специфичной областью тромбоспондина 1 человека (аминокислотные остатки от 501 до 657 белка с номером доступа в SwissProt P07996; SEQ ID NO: 28). На фигуре показано, что две последовательности имеют 36% сходство и 26% идентичность на протяжении от 14 до 166 аминокислотного остатка последовательности SEQ ID NO: 4 и от 501 до 657 аминокислотного остатка последовательности SEQ ID NO: 28, где A=аланин, C=цистеин, D=аспарагиновая кислота, E=глутаминовая кислота, F=фенилаланин, G=глицин, H=гистидин, I=изолейцин, K=лизин, L=лейцин, M=метионин, N=аспарагин, P=пролин, Q=глутамин, R=аргинин, S=серин, T=треонин, V=валин, W=триптофан, Y=тирозин. Пробелы обозначены в виде тире.
На фигурах 5A-5R изображены стадии способа, применяемого для создания вектора для целенаправленного встраивания (knock-in) GIPF (GIPF-KI) согласно изобретению. Также описан предпочтительный способ создания трансгенных мышей, которые экспрессируют GIPF в своих B-клетках.
На фигуре 6 изображено положение зонда, используемого в Саузерн-блот-анализе для отбора клонов ES, возникающих в результате гомологичной рекомбинации, а также размеры фрагментов расщепления EcoRI геномной ДНК мыши, которая была подвергнута гомологичной или негомологичной рекомбинации.
На фигуре 7 показана макроскопическая патология кишечного тракта у мышей GIPF-KI: контроль (A), GIPF-KI (B).
Фигура 8. Окрашивание гематоксилином и эозином поперченных срезов тонкого кишечника мышей GIPF-KI (A) и контрольных химерных мышей (B) соответственно.
На фигуре 9 показано окрашивание гематоксилином и эозином срезов кишечника, показанных на фигуре 8, видимых при более высоком увеличении. Панели A и C соответствуют срезу GIPF-KI, видимому на панели A фигуры 8, а панели B и D соответствуют срезу кишечника, полученному от контрольной химерной мыши, видимому на панели B фигуры 8.
На фигуре 10 показано окрашивание Ki67 поперечных срезов тонкого кишечника от контрольной химерной мыши (A и C) и от мыши GIPF-KI (B и D).
Фигура 11. Поперечные срезы тонкого кишечника, полученные от контрольной мыши (A и C) и от мыши, обработанной 1×1010 вирусных частиц (B и D). Срезы получали через три дня после инъекции пустого аденовируса и GIPF-аденовируса соответственно.
Фигуре 12. Поперечные срезы тонкого кишечника, полученные от контрольной мыши (A и C) и от мыши, обработанной 1×1010 вирусных частиц (VP) (фигуры 12 B и D). Срезы получали через пять дней после инъекции пустого аденовируса или GIPF-аденовируса соответственно.
Фигура 13. Включение BrdU в пролиферирующие клетки крипт тонкого кишечника контрольных мышей (A и C) и мышей, обработанных 1×1010 вирусных частиц (VP) (B и D).
Фигура 14. Окрашивание Ki67 пролиферирующих клеток крипт тонкого кишечника контрольных (A и C) и обработанных GIPF-аденовирусом мышей (B и D).
Фигура 15. Окрашивание гематоксилином и эозином поперечных срезов, полученных из тонкого кишечника контрольных мышей (A и C) и мышей, которые были обработаны GIPF-аденовирусом в количестве 1×109 вирусных частиц (B и D).
Фигура 16. Окрашивание гематоксилином и эозином поперечных срезов, полученных из ободочной кишки контрольных (A и C) и обработанных GIPF-аденовирусом мышей (B и D).
Фигуры 17 (A и B). Необходимые условия растворимости нативного V5-His-меченого белка GIPF, очищенного из клеток CHO.
Фигуры 18 (A и B). Фармакокинетика V5-His-меченого белка GIPF в сыворотке мышей.
Фигура 19. Окрашивание гематоксилином и эозином поперечных срезов, полученных из тонкого кишечника контрольных мышей (A и C) и мышей, которые были обработаны очищенным белком GIPF (B и D).
Фигура 20. Включение BrdU в пролиферирующие клетки крипт тонкого кишечника контрольных мышей (A и C) и мышей, которые были обработаны очищенным белком GIPF (B и D).
Фигура 21. Окрашивание гематоксилином и эозином поперечных срезов, полученных из ободочной кишки контрольных мышей (A) и мышей, которые были обработаны очищенным белком GIPF (B).
Фигура 22. Включение BrdU в пролиферирующие клетки крипт ободочной кишки контрольных мышей (A и C) и мышей, которые были обработаны очищенным белком GIPF (B и D).
Фигура 23. Окрашивание гематоксилином и эозином поперечных срезов, полученных из тонкого кишечника необлученных мышей (A), облученных мышей, обработанных физиологическим раствором (B), KGF (C) или GIPFwt (D).
Фигура 24. Влияние 5-FU на размер опухолей у контрольных мышей и мышей, получающих GIPFwt.
Фигура 25. Влияние GIPF на макроскопическую патологию тонкого кишечника и ободочной кишки нормальных (E и F) и несущих опухоли мышей (A-D).
Фигура 26. Окрашивание гематоксилином и эозином поперечных срезов, полученных из тонкого кишечника и ободочной кишки нормальных и несущих опухоли мышей, которые получили 5-FU и/или GIPF.
Фигура 27. Микроморфометрические измерения высоты ворсинок и глубины крипт показывают влияние GIPF на эпителий кишечника мышей, которые получали 5-FU.
Фигура 28. Окрашивание Ki67 пролиферирующих эпителиальных клеток вентральной поверхности языка контрольных мышей (A и B) и мышей, обработанных KGF или GIPF (C-E) и подвергнутых общему облучению организма.
Фигура 29. Окрашивание Ki67 пролиферирующих эпителиальных клеток дорзальной поверхности языка контрольных мышей (A и B) и мышей, обработанных KGF или GIPF (C и D) и подвергнутых общему облучению организма.
Фигура 30. Пролиферативный индекс эпителия вентральной поверхности языка от мышей, обработанных KGF или GIPF и подвергнутых общему облучению организма.
Фигура 31. Окрашивание гематоксилином и эозином срезов, полученных из языка мышей, обработанных GIPF и подвергнутых общему облучению организма.
Фигура 32. Влияние GIPF на индекс активности воспалительного заболевания кишечника (IBDAI) мышей с DSS-индуцированным колитом.
Фигура 33. Влияние GIPF на количественный показатель массы тела животного у мышей с DSS-индуцированным колитом.
Фигура 34. Влияние GIPF на количественный показатель консистенции кала у мышей с DSS-индуцированным колитом.
Фигура 35. Влияние GIPF на количественный показатель ректального кровотечения у мышей с DSS-индуцированным колитом.
Фигура 36. Влияние GIPF на макроскопическую патологию тонкого кишечника и ободочной кишки контрольных и DSS-обработанных мышей.
Фигура 37. Окрашивание гематоксилином и эозином поперечных срезов, полученных из тонкого кишечника и ободочной кишки мышей, которые получали DSS и/или GIPF.
Фигура 38. Микроморфометрические измерения высоты ворсинок и глубины крипт показывают влияние GIPF на эпителий кишечника мышей с DSS-индуцированным колитом.
Фигура 39. Включение BrdU в пролиферирующие клетки крипт тонкого кишечника и ободочной кишки мышей, которые получали DSS и/или GIPF.
Фигура 40. Влияние GIPF на пролиферацию эпителия тонкого кишечника мышей с DSS-индуцированным колитом.
Фигура 41. Влияние GIPF на стабилизацию β-катенина в эндокринных клетках человека и эпителиальных клетках почки человека. GIPF индуцировал зависимую от дозы (A) и зависимую от времени (B) стабилизацию β-катенина в клетках HEK293. Стабилизирующее влияние GIPF не нарушалось при кипячении (C).
Фигура 42. Влияние GIPF на фосфорилирование GSK3.
Фигура 43. Схематичное представление аналогов полипептида GIPF, сконструированных для определения способности различных областей GIPF стабилизировать β-катенин. Номера фрагментов 1-11 соответствуют последовательностям полипептида SEQ ID NO: 85, 87, 89, 91, 93, 95, 97, 99, 101, 103 и 105 соответственно.
Фигура 44. Стабилизация β-катенина аналогами GIPF, изображенными на фигуре 43.
Фигура 45. Сравнение активности GIPF человека и мыши в отношении макроскопической патологии кишечника мышей.
Фигура 46. Влияние GIPF на глубину кишечных крипт.
Фигура 47. Влияние GIPF на стабилизацию β-катенина в изолированных клетках крипт.
Фигура 48. Влияние GIPF на массу тела животных с TNBS-индуцированным колитом.
Фигура 49. Влияние GIPF на количественный показатель колита у животных с TNBS-индуцированным колитом.
Фигура 50. Влияние GIPF на хронический колит, индуцированный DSS.
Фигура 51. Влияние GIPF на высоту ворсинок и глубину крипт у животных с DSS-индуцированным хроническим колитом.
Фигура 52. Влияние GIPF на пролиферативный индекс крипт животных с DSS-индуцированным хроническим колитом.
Фигура 53. Влияние GIPF на жизнеспособность крипт после облучения.
Фигура 54 A-N. Представление в виде диаграммы конструирования трансгена для управляемой виллином экспрессии GIPF в эпителии трансгенных мышей.
Фигура 55. Эмбриональная экспрессия GIPF в эпителии кишечника и печени трансгенных мышей.
Фигура 56. Стабилизация β-катенина у трансгенных мышей, которые экспрессируют GIPF.
Фигура 57. Окрашивание гематоксилином и эозином срезов тонкого кишечника трансгенных мышей, которые экспрессируют GIPF.
Фигура 58 A-C. Представление в виде диаграммы конструирования трансгена для управляемой виллином экспрессии GIPF и Wnt3a у трансгенных мышей.
Фигура 59. Эмбриональная экспрессия GIPF и Wnt3a в тонком и толстом кишечнике трансгенных мышей.
Фигура 60. Стабилизация β-катенина у трансгенных мышей, которые экспрессируют GIPF и Wnt3a.
Фигура 61. Окрашивание гематоксилином и эозином срезов тонкого кишечника трансгенного эмбриона мыши, который экспрессирует GIPF и Wnt3a.
Фигура 62 A-K. Представление в виде диаграммы конструирования вектора RS-KO.
Фигура 63. Геномная карта клона дикого типа и рекомбинантного клона RS-KO.
Фигура 64A-K. Представление в виде диаграммы конструирования целенаправленно встраивающего вектора pCk m4 KI для экспрессии делеционного мутанта GIPF (SEQ ID NO: 91) у трансгенных мышей.
Фигура 65 A-C. Представление в виде диаграммы конструирования целенаправленно встраивающего вектора pPS m4KI для экспрессии делеционного мутанта GIPF (SEQ ID NO: 91) у трансгенных мышей.
Фигура 66. Геномная карта клона дикого типа и рекомбинантного клона Ck m4 KI.
Фигура 67. Геномная карта клона дикого типа и рекомбинантного клона PS m4 KI.
Фигура 68A-C. Представление в виде диаграммы конструирования целенаправленно встраивающего вектора pCk VRKI для экспрессии варианта GIPF (SEQ ID NO: 177; GenBank, номер доступа AK098225) у трансгенных мышей.
Фигура 69A-C. Представление в виде диаграммы конструирования целенаправленно встраивающего вектора pPS VR KI для экспрессии варианта GIPF (SEQ ID NO: 177; GenBank, номер доступа AK098225) у трансгенных мышей.
Фигура 70. Геномная карта клона дикого типа и рекомбинантного клона Ck VR KI.
Фигура 71. Геномная карта клона дикого типа и рекомбинантного клона PS VR KI.
Фигура 72. Сравнение тонкого и толстого кишечника контрольных и трансгенных мышей, экспрессирующих делеционный мутант GIPF SEQ ID NO: 91.
Фигура 73. Окрашивание гематоксилином и эозином поперечных срезов тонкого кишечника от трансгенных мышей, экспрессирующих делеционный мутант GIPF SEQ ID NO: 91 (малое увеличение).
Фигура 74. Окрашивание гематоксилином и эозином перекрестных срезов тонкого кишечника от трансгенных мышей, экспрессирующих делеционный мутант GIPF SEQ ID NO: 91 (большое увеличение).
Фигура 75. Стабилизация аксина-2 у трансгенных мышей, которые экспрессируют делеционный мутант GIPF SEQ ID NO: 91.
Фигура 76. Сравнение тонкого и толстого кишечника контрольных и трансгенных мышей (PSVR KI), экспрессирующих вариант GIPF (SEQ ID NO: 177; GenBank, номер доступа AK098225), с тонким и толстым кишечником контрольного животного.
Фигура 77. Окрашивание гематоксилином и эозином поперечных срезов тонкого кишечника от контрольной и трансгенной мыши (PSVR KI), экспрессирующей вариант GIPF (SEQ ID NO: 177; GenBank, номер доступа AK098225) (малое увеличение).
Фигура 78. Окрашивание гематоксилином и эозином поперечных срезов тонкого кишечника от контрольной и трансгенной мыши (PSVR KI), экспрессирующей вариант GIPF (SEQ ID NO: 177; GenBank, номер доступа AK098225) (большое увеличение).
Фигура 79. Стабилизация аксина-2 у контрольных и трансгенных мышей, которые экспрессируют вариант GIPF (SEQ ID NO: 177; GenBank, номер доступа AK098225).
Фигура 80. Ок