Способы изготовления имплантов для брахитерапии
Иллюстрации
Показать всеНастоящее изобретение относится к медицине. Изобретение включает способы изготовления имплантов для брахитерапии, способы изготовления сердцевин имплантов для брахитерапии и импланты для брахитерапии, не зависящие от способа изготовления. В одном варианте имплант для брахитерапии содержит герметичный неорганический металлический цилиндр с радиоактивной сердцевиной, помещенной в него. Радиоактивная сердцевина содержит трубку из неорганического аморфного силикатного стекла с внешней поверхностью, продолжающейся аксиально вдоль трубки. Неорганическое кристаллическое керамическое покрытие вмещается на, по меньшей мере, участке внешней поверхности трубки из неорганического аморфного стекла. Покрытие содержит терапевтическую дозу радиоактивного материала. Радиографический маркер помещают внутрь герметичного неорганического металлического цилиндра. Радиотерапию применяют для разрушения злокачественных или нежелательных тканей без чрезмерного поражения соседних здоровых тканей. 3 н. и 40 з.п. ф-лы, 13 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способам изготовления имплантов для брахитерапии, способам изготовления сердцевин имплантов для брахитерапии и к имплантам для брахитерапии, не зависящим от способа изготовления.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Радиационная терапия (радиотерапия) относится к лечению ионизирующим излучением заболеваний, в основном, но без ограничения, к лечению опухолей, например раковых. Радиотерапию применяют для разрушения злокачественных или нежелательных тканей без чрезмерного поражения соседних здоровых тканей.
Ионизирующее излучение можно применять для селективного поражения раковых клеток, содержащихся в здоровых тканях. Злокачественные клетки обычно являются более чувствительными к радиации, чем здоровые клетки. Поэтому подведением излучения в надлежащем количестве в течение идеального периода времени можно разрушать все нежелательные раковые клетки и в то же время не допускать или уменьшать до минимума поражение здоровой ткани. В течение многих десятилетий локализованный рак часто лечили подведением тщательно заданного количества ионизирующего излучения в течение соответствующего периода времени. Разработаны разнообразные способы для облучения раковой ткани, при сведении к минимуму поражения соседней здоровой ткани. Данные способы включают в себя использование пучков высокоэнергетического излучения из линейных ускорителей и других устройств для применения во внешней лучевой терапии.
Другой способ радиотерапии включает в себя брахитерапию. В данном случае непосредственно внутрь/около раковой опухоли имплантируют навсегда или на время вещества в форме зерен, игл, проволоки или катетеров. Применяемые радиоактивные материалы включают в себя радон, радий и иридий-192. В последнее время стали применять радиоактивные изотопы цезий-131, йод-125 и палладий-103. Описания примеров приведены в патентах США №3351049; 4323055 и 4784116, которые включены в настоящее описание в качестве ссылки.
В течение последних 30 лет опубликовано свыше 100 работ (как научных, так и непрофессиональных публикаций) на тему использования йода-125 и палладия-103 при лечении медленно развивающегося рака простаты. Независимо от продемонстрированного благоприятного результата с йодом-125 и палладием-103 существуют некоторые недостатки и ограничения их применения. Хотя суммарную дозу можно регулировать количеством и интервалами размещения зерен, мощность дозы обусловлена периодом полураспада радиоизотопа (60 суток для I-125 и 17 суток для Pd-103). Для применения в быстрее растущих опухолях излучение следует подводить к раковым клеткам с более высокой равномерной мощностью и одновременно сохранять все преимущества применения радиоизотопа, излучающего мягкие рентгеновские лучи. Такие раковые заболевания появляются в мозге, легких, поджелудочной железе, простате и других тканях.
Зерна с I-125 и Pd-103 в качестве источников мягкого рентгеновского излучения успешно применяли при лечении рака. Способы герметизации упомянутых радиоактивных изотопов в виде зерен или капсул для внутритканевой брахитерапии описаны в патентах США №1753287; 3351049; 4323055; 4702228; 4784116; 4891165; 4994013; 5163896; 5405309 и 6099458 и включены в настоящее описание путем отсылки.
Некоторые из вышеупомянутых зерен имеют ряд недостатков и ограничений. К ним относятся: (а) слабая энергия рентгеновского излучения от Pd-103 (20 кэВ (килоэлектрон-вольт)); (b) период полураспада зерна I-125 (60 суток) обычно слишком велик, чтобы его можно было применить в качестве долговременного импланта в каких-либо других опухолях, кроме медленно растущих опухолей; (с) применение маркера из серебряной проволоки, вмонтированного в зерна I-125 (патент США №4323005), сопряжено с формированием серебром в большом количестве ненужного характеристического низкоэнергетического (<10 кэВ) рентгеновского излучения в результате К-захватов и (d) зерна с разными внутренними компонентами с неоптимизированными геометрическими характеристиками, что требует большего количества изотопа для компенсации неравномерной диаграммы распределения дозы вокруг зерна.
Применение герметичных радиоактивных источников распространилось настолько широко, что были приняты производственные стандарты радиационной защиты. Способы проверки на утечку герметичных радиоактивных источников продолжают совершенствоваться (ISO 9978: 1992(E) и ISO 2919: 1999 (Е)). Чтобы выполнять данные стандарты, герметичные зерна должны подвергаться воздействиям окружающей среды и при этом оставаться полностью герметичными. Самым сложным испытанием на соответствие является испытание на ударную нагрузку, в ходе которого требуется помещать металлический корпус зерна на стальную наковальню и обеспечивать падение гири диаметром 2,54 см и массой 50 г на зерно с высоты 1 м. Даже если бы контейнер зерна в типичной титановой оболочке расплющивался после данного воздействия, металлический корпус зерна не должен давать никакой утечки. Для выдерживания описанного строгого испытания изготовители имплантов (например, в форме конструкций известного уровня техники, описанного, например, в патентах США №4702228; 4784116; 4891165; 5405309 и т.д.) вмонтируют толстые торцевые сварные швы, толстые торцевые крышки и/или массивные внутренние компоненты, чтобы сохранять первоначальную цилиндрическую форму. Однако данные характеристики могут иметь следствием неравномерные дозиметрические диаграммы распределения вокруг зерна из-за собственного поглощения излучения. Упомянутая неизотропность дозы повышает вероятность того, что раковые клетки, расположенные в упомянутой затененной зоне слабой дозы, выживут и вызовут позднее возврат рака.
Несколько известных конструкций зерен (патенты США №3351049; 4994013 и 5163896) предполагает применение пластмасс, большое число типов ионообменных смол (нейлона, сложных эфироцеллюлозных или ацетатных связующих веществ или каучука) для захвата и фиксации радиоактивного материала. При повышении концентрации радиоизотопов возможно создание недопустимого давления газа (например, Н2, СО, СО2, СН4 и т.д.) в результате авторадиолиза органических материалов в полости зерна. Существует риск выделения радиоактивного материала из-за образования разрывов в контейнере зерна при повышенном давлении.
Хотя изобретение вызвано стремлением к решению, по меньшей мере, некоторых из вышеупомянутых проблем, оно этим не ограничивается. Настоящее изобретение ограничено только прилагаемой формулой изобретения в дословном изложении без ограничения ссылкой на описание или его трактовку.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение включает способы изготовления имплантов для брахитерапии, способы изготовления сердцевин имплантов для брахитерапии и имплантируемые зерна для брахитерапии, не зависящие от способа изготовления. В одном варианте исполнения имплант для брахитерапии содержит герметичный неорганический металлический цилиндр с радиоактивной сердцевиной, вмещенной в него. Радиоактивная сердцевина содержит трубку из неорганического аморфного силикатного стекла с внешней поверхностью, продолжающейся аксиально вдоль трубки. Неорганическое кристаллическое керамическое покрытие вмещается на, по меньшей мере, участке внешней поверхности трубки из неорганического аморфного стекла. Покрытие содержит терапевтическую дозу радиоактивного материала. Радиографический маркер вмещается внутри герметичного неорганического металлического цилиндра.
В одном варианте осуществления способ изготовления импланта для брахитерапии включает этап, состоящий в том, что используют трубку из неорганического аморфного силикатного стекла с внешней поверхностью, продолжающейся аксиально вдоль трубки. По меньшей мере, участок внешней поверхности трубки покрывают исходными веществами для получения керамики. После покрытия исходные вещества для получения керамики подвергают воздействию температуры, вызывающей формирование сплошного неорганического кристаллического керамического покрытия из исходных веществ на участке внешней поверхности трубки. После воздействия на керамическом покрытии сорбируют терапевтическую дозу радиоактивного материала. Получают, по меньшей мере, участок покрытой керамикой стеклянной трубки с терапевтической дозой радиоактивного материала внутри неорганического металлического цилиндра. Приваривают неорганическую металлическую крышку на торец неорганического металлического цилиндра, содержащего участок покрытой керамикой стеклянной трубки с терапевтической дозой радиоактивного материала в данной трубке.
В одном варианте осуществления способ изготовления сердцевины импланта для брахитерапии содержит этап, состоящий в том, что используют трубку с внешней поверхностью, продолжающейся аксиально вдоль трубки. Используют емкость, которая содержит профилирующий канал, выполненный с таким размером, чтобы допускать вставку трубки с возможностью скольжения через него для формирования покрытия на внешней поверхности трубки. Внутрь емкости помещают смесь исходных веществ для получения керамики. Трубку вдвигают в смесь исходных веществ для получения керамики внутри емкости и через профилирующий канал на выход из емкости, функционально предназначенной для формирования покрытия из исходных веществ, формирования керамики на внешней поверхности трубки. Покрытие из исходных веществ для формирования керамики подвергают воздействию температуры, вызывающей формирование неорганического кристаллического керамического покрытия на участке внешней поверхности трубки. После данного воздействия на керамическом покрытии сорбируют терапевтическую дозу радиоактивного материала.
В одном варианте исполнения способ изготовления сердцевины импланта для брахитерапии содержит этап, состоящий в том, что используют трубку с внешней поверхностью, продолжающейся аксиально вдоль трубки. Берут пресс-форму, которая содержит полость пресс-формы, выполненную с таким размером, чтобы допускать вставку трубки и формирование на ней покрытия. Смесь исходных веществ для получения керамики помещают внутрь полости пресс-формы. Трубку вставляют внутрь полости пресс-формы. Налипшее покрытие из исходных веществ для получения керамики формируется на внешней поверхности трубки внутри полости пресс-формы. После упомянутого формирования пресс-форму расплавляют до разрушения. После расплавления покрытие из исходных веществ для формирования керамики подвергают воздействию температуры, вызывающей формирование неорганического кристаллического керамического покрытия на внешней поверхности трубки. После данного воздействия на керамическом покрытии сорбируют терапевтическую дозу радиоактивного материала.
В одном варианте исполнения способ изготовления импланта для брахитерапии содержит этап, состоящий в том, что используют неорганический металлический цилиндр. Неорганическую металлическую крышку приваривают на торец неорганического металлического цилиндра. Сварка заключается в том, что пока крышку и цилиндр поворачивают, к крышке и цилиндру подводят серию импульсов лазерного излучения, вызывающих формирование последовательности сварных швов внахлест. В одном варианте исполнения соседние сварные швы заходят внахлест один на другой не более чем на 50% из расчета как частное от деления нахлеста по диаметру сварного шва на диаметр сварного шва. В одном варианте исполнения импульсы лазерного излучения подводят к крышке и цилиндру под углом падения к перпендикуляру к внешней поверхности металлического цилиндра. Радиоактивную сердцевину создают внутри неорганического металлического цилиндра. Радиоактивная сердцевина содержит терапевтическую дозу радиоактивного материала.
Предполагается возможность других аспектов и вариантов исполнения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Ниже приведено описание предпочтительных вариантов осуществления настоящего изобретения со ссылками на следующие прилагаемые чертежи.
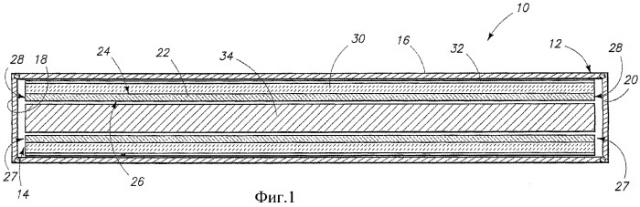
Фиг.1 - схематичное сечение импланта для брахитерапии в соответствии с одним аспектом изобретения.
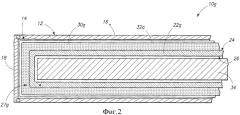
Фиг.2 - увеличенное схематичное сечение торцевого участка другого варианта осуществления импланта для брахитерапии в соответствии с одним аспектом изобретения.
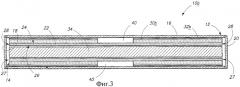
Фиг.3 - схематичное сечение другого варианта осуществления импланта для брахитерапии в соответствии с одним аспектом изобретения.
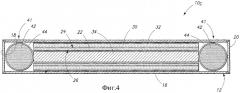
Фиг.4 - увеличенное схематичное сечение торцевого участка еще одного другого варианта осуществления импланта для брахитерапии в соответствии с одним аспектом изобретения.
Фиг.5 - вид в перспективе примера устройства, применимого в соответствии с методическим аспектом изобретения.
Фиг.6 - вид, демонстрирующий применение устройства, изображенного на фиг.5, в соответствии с одним аспектом изобретения.
Фиг.7 - вид в перспективе другого примера устройства, применимого в соответствии с методическим аспектом изобретения.
Фиг.8 - схематичное изображение сварного шва внахлест в соответствии с одним аспектом изобретения.
Фиг.9 - схематичное изображение сварного шва внахлест в соответствии с одним аспектом изобретения.
Фиг.10 - схематичное изображение сварного шва внахлест в соответствии с одним аспектом изобретения.
Фиг.11 - схематичное изображение сварного шва внахлест в соответствии с одним аспектом изобретения.
Фиг.12 - схематичное изображение импланта для брахитерапии при изготовлении в соответствии с одним аспектом изобретения.
Фиг.13 - схематичное изображение импланта для брахитерапии при изготовлении в соответствии с одним аспектом изобретения, на виде сверху по линии 13-13, показанной на фиг.12.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДПОЧТИТЕЛЬНЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
В соответствии с предпочтительными аспектами изобретения предпочтительный вариант осуществления импланта для брахитерапии сначала описан со ссылкой на фиг.1 и обозначен общей позицией 10. В целях настоящего документа под «имплантом для брахитерапии» понимается любой твердый предмет, подлежащий постоянной или временной имплантации для передачи дозы облучения, независимо от внешней формы, например независимо от того, является ли форма игольчатой, капсульной, таблеточной и т.д. Имплант 10 содержит герметичный неорганический металлический цилиндр 12 с радиоактивной сердцевиной 14, вмещенной в упомянутый цилиндр. Примерами предпочтительных материалов для цилиндра 12 являются свободный титан или титановый сплав. Однако предполагается возможность применения любого существующего или разрабатываемого металла или сплава, предпочтительно металлов с низким атомным номером и высокой удельной прочностью.
В одном предпочтительном варианте цилиндр 12 содержит цилиндрическую секцию 16 и пару противоположных торцевых крышек 18 и 20. Компоненты 16, 18 и 20 предпочтительно выполнены из одного и того же материала, при этом крышки 18 и 20 приварены к цилиндрической секции 16. Ниже приведены описания примеров предпочтительных способов изготовления. Примерная предпочтительная длина цилиндрической секции 16 составляет 1,0 - 10,0 мм. Примерная предпочтительная толщина стенки секции 16 составляет 0,05 - 0,1 мм. Примерный предпочтительный наружный диаметр или максимальный поперечный размер цилиндра 12 составляет 0,1 - 2,0 мм. Предпочтительный диапазон изменения толщины крышек 18 и 20 также составляет 0,05 - 0,1 мм, при этом крышки предпочтительно имеют диаметр или максимальный поперечный размер, который немного больше, чем диаметр или максимальный поперечный размер цилиндрической секции 16. Крышки 18 и 20 предпочтительно сцепляют с цилиндрической секцией 16 сваркой, выполненной описанным далее предпочтительным способом. В предпочтительном варианте в конструкции цилиндра 12 применяют компоненты 18, 16 и 20 с одинаковой толщиной стенок.
Изображенный предпочтительный цилиндр 12 выполнен в форме герметически закрытого прямого цилиндра с, по существу, плоскими торцами. Плоские торцы предпочтительны для обеспечения такого преимущества, как возможность стабилизировать зерно после размещения в требуемом положении в опухоли или другой ткани, по сравнению с имплантом со скругленными торцами. Кроме того, как оказалось, скругленные торцы заедают в иглах во время загрузки. Независимо от других условий, конечно, предполагается также возможность применения зерен с другими торцами помимо плоских торцов. Один из примерных предпочтительных вариантов осуществления конструкции цилиндра 12 представляет собой титановая трубка в виде прямого цилиндра длиной 4,3 мм, внутренним диаметром 0,7 мм и внешним диаметром 0,8 мм, с торцевыми крышками, приваренными к цилиндру и имеющими толщину 0,1 мм.
Радиоактивная сердцевина 14 содержит трубку 22 из неорганического аморфного силикатного стекла. Можно считать, что данная трубка содержит продольно противоположные торцы 27, которые, в варианте осуществления, изображенном на фиг.1, являются открытыми. Трубка 22 обладает также внешней поверхностью 24, внутренней поверхностью 26, продолжающейся аксиально вдоль трубки, и торцевыми поверхностями 28. Исключительно для примера, предпочтительными силикатными стеклами являются боросиликатные стекла, фосфоросиликатные стекла, борофосфоросиликатные стекла и кварцевые стекла. Кроме того, также исключительно для примера, любое легирование бором или фосфором упомянутых силикатных стекол осуществляется предпочтительно в пределах от 3 процентов по массе до 12 процентов по массе. Независимо от других условий стекло выполнено предпочтительно из материала, который характеризуется высокой прозрачностью для терапевтического излучения. Примерная предпочтительная длина трубки 22 составляет 1,0 - 10,0 мм. Примерный предпочтительный диапазон изменения внешнего диаметра трубки 22 составляет 0,4 - 2,0 мм, при этом примерный предпочтительный диапазон изменения внутреннего диаметра составляет 0,25 - 1,8 мм. Конкретным примерным вариантом осуществления является стеклянная трубка с внешним диаметром 0,4 мм, внутренним диаметром 0,3 мм и длиной 4 - 4,25 мм.
Неорганическое кристаллическое керамическое покрытие 30 получено на, по меньшей мере, участке внешней поверхности 24 трубки из неорганического аморфного стекла. В примерном варианте осуществления, представленном на фиг.1, покрытие 30 покрывает всю внешнюю поверхность 24 трубки. Неорганическое кристаллическое керамическое покрытие может иметь толщину, которая является такой же, как или больше или меньше, чем толщина трубки из неорганического аморфного силикатного стекла, при этом в примерном варианте осуществления, представленном на фиг.1, толщина покрытия 30 показана больше, чем толщина стеклянной трубки 22. Независимо от других условий примерный предпочтительный диапазон изменения толщины покрытия 30 составляет 0,1 - 0,4 мм, причем конкретная примерная толщина равна 0,15 мм.
Примерные предпочтительные материалы для неорганического кристаллического покрытия 30 включают силикаты металлов, например алюмосиликаты, например натрийалюмосиликат. Дополнительно к упомянутым материалам или вместо них, примерные предпочтительные материалы включают силикаты и оксиды алюминия, натрия, магния, калия, кальция и лития. Кроме того, предпочтительный керамический материал 30 предпочтительно является, по существу, способным к химической адсорбции или абсорбции, по меньшей мере, одного специфического радионуклида или содержит неорганический ионообменный материал, описанный в дальнейшем.
Независимо от других условий покрытие 30 содержит терапевтическую дозу радиоактивного материала. В частности, примерный вариант осуществления, показанный на фиг.1, содержит радиоактивный изотоп 32, который сорбирован на внешней поверхности керамического покрытия 30. Данный материал может проникать до некоторой или значительной степени в керамическое покрытие 30, в зависимости от пористости и гладкости внешней поверхности покрытия 30, но предпочтительно помещен в самые наружные участки керамического покрытия 30. Это обеспечивает прилегание радиохимического вещества к внутренней поверхности металлического цилиндра 12 и предпочтительно уменьшает степень собственного поглощения внутренними компонентами зерна и, тем самым, максимально увеличивает дозу излучения, испускаемую из зерна, а также улучшает равномерную изотропность испускаемого излучения. Примером предпочтительного радиоактивного материала является цезий-131. Однако предусмотрена возможность применения любого радиоизотопа, существующего или намеченного к разработке или выделению. Исключительно в виде примера, типичными материалами являются йод-125, палладий-123, цезий-137, иттрий-90, стронций-90 и другие радиоизотопы палладия, кобальта, серебра, меди, йода, урана, тория, актиния, редкоземельных металлов и актинидов. Кроме того, исключительно в виде примера, типичное предпочтительное характеристическое излучение испускается с энергиями 20 - 100 кэВ, причем конкретным примером является 29 кэВ. Кроме того, исключительно в виде примера, типичные предпочтительные периоды полураспада изготовленных зерен составляют от 8 до 100 суток.
Имплант 10 для брахитерапии дополнительно содержит радиографический маркер, который находится внутри герметичного металлического цилиндра. Исключительно в виде примера, данный маркер может быть выполнен в виде слоя металла, осажденного из паровой фазы, металлической пасты, металлического шарика, металлической проволоки и т.д. В наиболее предпочтительном варианте радиографический маркер находится внутри трубки из неорганического аморфного стекла. В варианте осуществления, показанном на фиг.1, радиографический маркер 34 в форме проволоки, фактически непрозрачной для ионизирующего излучения, находится внутри трубки 22 из неорганического аморфного стекла. Примерным предпочтительным материалом является золото, и, независимо от других условий, примерный диапазон толщин или диаметров проволоки 34 составляет 0,1 - 0,4 мм, при 0,25 мм в конкретном примере. Исключительно в виде примера, типичные дополнительные материалы для маркера, непрозрачного для ионизирующего излучения, включают вольфрам, родий, платину, свинец и олово. Радиографический маркер выполняет функцию рентгеноконтрастного маркера, облегчающего внешнюю визуализацию зерна после имплантации для обеспечения надлежащего размещения зерна относительно опухоли или другой ткани.
На фиг.1 изображен имплант для брахитерапии, содержащий радиоактивную сердцевину, в которой стеклянная трубка 22 содержит продольно противоположные торцы 27, которые являются открытыми. Исключительно в виде примера, на фиг.2 показан имплант 10а для брахитерапии в соответствии с другим примерным вариантом осуществления. В соответствующих случаях использованы позиции, аналогичные позициям в первом варианте осуществления, при этом отличия обозначены индексом «а» или отличающимися позициями. Трубка 22а из неорганического аморфного силикатного стекла содержит продольно противоположные торцы 27а, которые герметизированы неорганическим аморфным силикатным стеклом. Кроме того, в варианте осуществления, показанном на фиг.2, и исключительно в виде примера, материалы 30а и 32а вмещаются также поверх торцов 27а трубки 22а из неорганического аморфного силикатного стекла.
В примерных вариантах осуществления на фиг.1 и 2 неорганическое кристаллическое керамическое покрытие 30/30а показано как покрытие по всей внешней поверхности 24 трубки, и радиоизотоп 30/32а вмещается по всей трубке 22/22а. Исключительно в виде примера, на фиг.3 изображен другой вариант осуществления импланта 10b для брахитерапии. В соответствующих случаях использованы позиции, аналогичные позициям в первом варианте осуществления, при этом отличия обозначены индексом «b» или отличающимися позициями. На фиг.3 показан некоторый центральный или сердцевинный участок 40, который либо не покрыт керамическим материалом, либо эффективно маскирован материалом, который не будет адсорбировать/абсорбировать радиоизотоп. Тем самым, терапевтическая доза радиоактивного материала покрывает меньше, чем всю внешнюю поверхность трубки. Примеры маскирующих материалов включают полиакрилонитрил и воски. В некоторых вариантах осуществления желательными могут быть упомянутые материалы, улучшающие равномерную изотропность. Примерная предпочтительная длина зоны/участка 40 составляет 1,0 - 4,0 мм, при этом с расположением упомянутой зоны/участка по центру длины металлического цилиндра 12.
Исключительно в виде примера, на фиг.4 изображен другой примерный вариант осуществления. В соответствующих случаях использованы позиции, аналогичные позициям в первом варианте осуществления, при этом отличия обозначены индексом «с» или отличающимися позициями. Имплант 10d для брахитерапии содержит пару шариков 41 непосредственно у торцов неорганического металлического цилиндра 12. Данные шарики могут содержать материал радиографического маркера и/или, в более предпочтительном варианте, могут содержать терапевтическую дозу радиографического материала. Исключительно в виде примера, данные шарики могут содержать непрозрачную для ионизирующего излучения или керамическую сердцевину 42, содержащую терапевтическую дозу радиоактивного материала 44, вмещенного вокруг данной сердцевины.
Выше приведены описания примерных предпочтительных вариантов осуществления имплантов для брахитерапии, не зависящих от способа изготовления. Ниже описаны примерные предпочтительные способы изготовления вышеописанных и других имплантов для брахитерапии в соответствии с аспектами настоящего изобретения, включая способы изготовления сердцевины имплантов для брахитерапии в соответствии с аспектами настоящего изобретения.
В одном варианте осуществления способ изготовления сердцевины импланта зерна для брахитерапии описан со ссылкой на фиг.5 и 6. На данных чертежах изображена подходящая емкость 48, содержащая корпус 50 емкости и профилирующий канал 52. Примерный объем корпуса 50 емкости составляет 5 - 50 мл. Примерными размерами профилирующего канала 52 являются длина 20 мм, внешний диаметр 2,5 мм и внутренний диаметр 1 мм. Берут трубку, которая содержит внешнюю поверхность, продолжающуюся аксиально вдоль трубки. Примерный материал трубки включает неорганический аморфный силикатный стеклянный материал, причем предпочтительным примером является трубка 22 из первого описанного варианта осуществления. Независимо от других условий профилирующий канал 52 выполнен с таким размером, чтобы допускать вставку трубки с возможностью скольжения через него для формирования покрытия на внешней поверхности трубки.
Внутри корпуса 50 емкости готовят смесь 51 исходных веществ для получения керамики. Примерные исходные вещества для получения керамики включают любые вещества, способные давать примерные представленные выше керамические покрытия, например смесь силиката натрия, содержащую от приблизительно 10 до 40 процентов по массе оксида алюминия. В одном примерном варианте осуществления смесь исходных веществ для получения керамики содержит неорганический ионообменный материал, обладающий сродством к радиоактивному материалу, подлежащему использованию впоследствии. Примерные предпочтительные неорганические ионообменные материалы включают цеолиты и, например, силикотитанат.
Как показано на фиг.6, трубку (например, трубку 22 в первом описанном варианте осуществления) вдвигают в смесь 51 исходных веществ для получения керамики внутри корпуса 50 емкости и через профилирующий канал 52 на выход из емкости, функциональной предназначенной для формирования покрытия 54 из исходных веществ для получения керамики на внешней поверхности трубки. В примерах, доведенных до практической реализации, применялись трубки из боросиликатного стекла с длинами 100 мм, внешним диаметром 0,4 мм и внутренним диаметром 0,3 мм.
Затем, покрытие из исходных веществ для получения керамики на трубке подвергают воздействию температуры, вызывающей формирование неорганического кристаллического керамического покрытия (например, покрытия 30 в первом описанном варианте осуществления) по внешней поверхности трубки. В примерах, доведенных до практической реализации, трубки с покрытием подвергают воздушной сушке и затем помещают в печь. После этого данную печь нагревают до 170°С в течение около 60 минут для превращения покрытия из исходных веществ в неорганическое кристаллическое керамическое покрытие, которое содержит алюмосиликат натрия. Исключительно в виде примера, типичный температурный диапазон для получения керамического материала составляет 100-500°С. В примерах, доведенных до практической реализации, затем стеклянную трубку с покрытием измеряли для оценки однородности толщины и разрезали на отрезки длиной 4,0 - 4,25 мм. Предпочтительные особенности в других отношениях являются такими же, которые описаны выше в отношении стеклянной трубки 22 с покрытием.
Затем сорбируют терапевтическую дозу радиоактивного материала на керамическом покрытии. Один из предпочтительных способов выполнения данной операции состоит в приведении покрытой керамикой внешней поверхности в контакт с раствором, содержащим ионы радиоизотопа, обладающие сродством к керамическому материалу и/или ионообменному материалу в керамическом материале. Например, и исключительно в виде примера, высокочистую и точно известную дозу радиоактивности из раствора (мКи/мл) можно переносить на покрытые керамикой сердцевины посредством адсорбции и/или абсорбции к внешним поверхностям данных сердцевин при погружении сердцевин по отдельности в 0,1 - 0,4 мл раствора на примерные периоды времени от 1 минуты до 24 часов. И вновь, примером предпочтительного радиоактивного материала является цезий-131. Во время обработки раствор и сердцевину предпочтительно осторожно встряхивают. Конкретный примерный раствор содержал 0,25 мл воды, содержащей 96,4 милликюри цезия-131 на 1 мл, для обработки одной сердцевины, причем время обработки составляло 14,5 часов, и раствор находился в окружающих условиях комнатной температуры и внешнего давления. На сердцевину переносилось более чем 88% радиоактивности. Раствор может быть кислым, основным, водным или неводным, главным образом, в зависимости от изотопа и керамического материала (включая любой ионообменный материал, если таковой присутствует), которые применяются. Затем загруженные радиоактивностью сердцевины извлекают из раствора и высушивают предпочтительно на воздухе в течение одного часа при помощи нагревательной лампы.
Выше приведено описание только одного примерного варианта осуществления способа для изготовления сердцевины импланта для брахитерапии в соответствии с примерными методическими аспектами изобретения. Дополнительный способ изготовления сердцевины импланта для брахитерапии содержит этап, состоящий в том, что берут трубку с внешней поверхностью, продолжающейся аксиально вдоль трубки. И вновь, в предпочтительном варианте, трубка содержит неорганический аморфный силикатный стеклянный материал, например, как трубка 22 из первого описанного варианта осуществления. Используют пресс-форму, которая содержит полость пресс-формы, выполненную с таким размером, чтобы допускать вставку трубки и формирование на ней покрытия. Исключительно в виде примера, на фиг.7 изображена пресс-форма 60 с выполненной в ней полостью 62 пресс-формы. Примерным способом формирования полости 62 было бы сверление. В качестве альтернативы, пресс-форма 60 может быть выполнена из, по меньшей мере, двух компонентов/частей, которые собирают для образования корпуса пресс-формы 60 с полостью 62. Независимо от других условий пресс-форма имеет температуру плавления, которая меньше или равна 500°С. Кроме того, и независимо от других условий, примерные предпочтительные материалы пресс-формы содержат воски (т.е. синтетические и/или природные воски, например животные воски, растительные воски и минеральные воски, например, содержащие нефтяные воски, такие как парафин, микрокристаллический воск и петролатум и другие) и пластики (т.е. полиэтилены, сложные полиэфиры, полипропилены, полиуретаны, поливиниловые полимеры, поликарбонаты, нейлоны, акриловые полимеры, стиролы и другие).
Смесь исходных веществ для получения керамики закладывают в полость пресс-формы и трубку вставляют в полость пресс-формы. В предпочтительном варианте сначала в полости пресс-формы готовят смесь исходных веществ для получения керамики, а затем трубку, хотя предполагается также возможность обратного порядка закладки. На поверхности трубки внутри полости пресс-формы формируется налипшее покрытие из исходных веществ для получения керамики, например, просто посредством предоставления исходным веществам для получения керамики возможности отверждения на внешней поверхности трубки в течение некоторого подходящего периода времени, например от одного часа до двадцати четырех часов.
Затем пресс-форму расплавляют до разрушения предпочтительно расплавлением пресс-формы с трубки, покрытой исходными веществами для получения керамики, и, еще более предпочтительно, расплавлением и испарением материала пресс-формы. Примерный предпочтительный диапазон температур нагревания для расплавления составляет 100-170°С, при этом, по меньшей мере, материал пресс-формы имеет температуру плавления, которая равна или ниже 170°С. Любой остаточный материал пресс-формы может быть растворен в любом подходящем растворителе, например гексане, для воска. После расплавления покрытие из исходных веществ для получения керамики подвергают воздействию температуры, вызывающей формирование неорганического кристаллического покрытия на внешней поверхности трубки, например, керамического покрытия 30 в вышеописанном первом варианте осуществления. Примерный предпочтительный диапазон температур является таким, который описан в вышеприведенном варианте осуществления, с температурой, равной 170°С в конкретном примере, и в котором будет также иметь место тенденция к отжигу любого остаточного воска или другого материала пресс-формы. После воздействия терапевтическую дозу радиоактивного материала сорбируют на керамическом покрытии, например, с помощью любого из вышеописанных или других способов. Следует отметить, что в любом из вышеописанных вариантов осуществления керамическое покрытие может быть сформировано на торцевых поверхностях и/или на внутренних поверхностях трубки. Кроме того, продольно противоположные торцы трубки могут быть открытыми или герметизированными в состоянии вставки в полость пресс-формы. Кроме того, внутри трубки может быть предусмотрен неорганический металлический маркер. Исключительно в виде примера и в соответствии с настоящим аспектом изобретения предпочтительные трубки имеют диаметр от 0,69 - 0,70 мм. Предпочтительная средняя толщина покрытия равна 0,15 мм. По меньшей мере, в случае, когда применяют радиографический маркер в форме проволоки или стержня, и в соответствии с данным конкретным вариантом осуществления предпочтительная длина составляет приблизительно 3,8 мм.
Аспекты изобретения предполагают также способы изготовления импланта для брахитерапии. В одном варианте осуществления данный способ содержит этап, состоящий в том, что берут трубку из неорганического аморфного силикатного стекла с внешней поверхностью, продолжающейся аксиально вдоль трубки. Предпочтительными являются трубки, описанные выше в первом варианте осуществления. По меньшей мере, участок внешней поверхности трубки покрыт исходными веществами для получения керамики. Примерными предпочтительными способами являются вышеописанные способы, включая, например, способы, описанные в связи с фиг.5 и 6, и способы, описанные в связи с фиг.7. Однако предполагается любой способ покрытия, либо существующий, либо разрабатываемый. Исключительно в виде примера, предпочтительные способы покрытия, дополнительные к способам, описанные в связи с фиг.5-7, включают распыление аэрозоля, распыление жидкости, прессование, литье под давлением, неаэрозольное микроструйное распыление жидкости и т.д. Кроме того, исходные вещества для формирования керамики предпочтительно обладают ранее описанными характеристиками.
После операции покрытия исходные вещества для по