Новые кристаллические структуры (полиморфные модификации) полукальциевой соли аторвастатина и способы получения этих и других полиморфных модификаций соли аторвастатина
Иллюстрации
Показать всеИзобретение относится к новым полиморфным модификациям полукальциевой соли аторвастатина, которым присвоены наименования Форма VI, Форма VIII, Форма IX, Форма X, Форма XI и Форма XII, и к способам их получения, а также способам получения полукальциевой соли аторвастатина полиморфных модификаций Форма I, Форма II, Форма IV и Форма V, а также аморфной полукальциевой соли аторвастатина. Использование новых форм в фармацевтических композициях повышает их качество и тем самым улучшает контроль над уровнем липопротеинов низкой плотности. 32 н. и 59 з.п. ф-лы, 26 ил., 5 табл.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА СВЯЗАННЫЕ ЗАЯВКИ
Настоящей заявкой заявляются притязания на приоритетные права, вытекающие из следующих первых заявок США: заявки №60/250.072, поданной 30 ноября 2000 года; заявки №60/267.897, поданной 09 февраля 2001 года; заявки №60/281.872, поданной 05 апреля 2001 года; заявки №60/312.144, поданной 13 августа 2001 года и заявки №60/326.529, поданной 01 октября 2001, которые все включены в настоящую заявку по ссылке.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ПРЕДЛАГАЕМОЕ ИЗОБРЕТЕНИЕ
Предлагаемое изобретение относится к новым кристаллическим полиморфным модификациям полукальциевой соли аторвастатина, к новым способам получения кристаллических полиморфных модификаций полукальциевой соли аторвастатина и к полукальциевой соли аторвастатина с малым разбросом размера частиц.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ПРЕДЛАГАЕМОГО ИЗОБРЕТЕНИЯ
В данной отрасли хорошо известны аторвастатин ([R-(R*,R*)]-2-(4-фторфенил)-β,δ-дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-энантовая кислота), который может быть представлен как циклический сложный эфир, и тригидрат кальциевой соли аторвастатина, структурные молекулярные формулы которых показаны ниже (формула (I) и формула (II) соответственно). Эти соединения описаны, помимо прочих источников, в патентах США №4.681.893 и №5.273.995, а также в одновременно рассматриваемой патентной заявке США №60/166.153, поданной 17 ноября 2000 года, при этом указанные патенты и заявка включены в настоящую заявку по ссылке.
Аторвастатин принадлежит к классу лекарственных веществ, именуемых статинами. Лекарственные вещества класса статинов являются наиболее терапевтически эффективными из известных в настоящее время лекарственных средств для понижения концентрации частиц липопротеинов низкой плотности в крови пациентов с риском сердечно-сосудистых заболеваний. Высокие концентрации липопротеинов низкой плотности в крови связывают с образованием поражений в коронарных сосудах, которые препятствуют кровотоку и могут привести к разрыву или развитию тромбоза (см. работу Goodman and Oilman "The Pharmacologcal Basis of Therapeutics" (Гудмэн и Гильман "Фармакологическая основа терапевтики"), 879. 9-е изд., 1996 год). Было доказано, что при снижении концентрации липопротеинов низкой плотности в плазме уменьшается риск возникновения клинических случаев у пациентов с сердечно-сосудистыми заболеваниями и у пациентов без сердечно-сосудистых заболеваний, но с гиперхолестеринемией (Scandinavian Simvastatin Study Group (Скандинавская группа по изучению симвастатина), 1994; Lipid Research Clinics Program (Клиническая программа исследований липидов), 1984а, 1984b).
В настоящее время выяснены некоторые детали механизма действия лекарственных веществ класса статинов. Они препятствуют синтезу холестерина и других стеринов в печени путем конкурентного ингибирования активности фермента - 3-гидрокси-3-метилглутарил коэнзим А (ГМГ-КоА) редуктазы. ГМГ-КоА редуктаза служит биокатализатором превращения 3-гидрокси-3-метил-глутарила (ГМГ) в мевалонат, что является определяющей стадией в биосинтезе холестерина, и, таким образом, ее подавление приводит к снижению концентрации холестерина в печени. Липопротеин очень низкой плотности служит средством транспортировки холестерина и триглицеридов от печени к периферическим клеткам. В результате катаболизма липопротеина очень низкой плотности в периферических клетках происходит образование жирных кислот, которые могут храниться в адопцитах или подвергаются окислению в мышцах. Липопротеин очень низкой плотности превращается в липопротеин промежуточной плотности, который или удаляется с помощью рецепторов липопротеина низкой плотности, или превращается в липопротеин низкой плотности. Снижение производства холестерина ведет к увеличению количества рецепторов липопротеина низкой плотности и соответственному снижению производства частиц липопротеина низкой плотности при метаболизме липопротеина промежуточной плотности.
Тригидрат полукальциевой соли аторвастатина поставляется на рынок компанией Уорнер-Ламберт Ко. (Warner-Lambert Co.) под товарным знаком LIPITOR. Информация об аторвастатине впервые стала достоянием гласности и предметом изобретения благодаря патенту США №4.681.893. Полукальциевая соль атовастатина (см. формулу (II), приведенную выше) раскрыт в патенте США №5.273.995. В патенте США №5.273.995 говорится, что полукальциевая соль атовастатина может быть получена путем кристаллизации из соляного раствора в результате перегруппировки натриевой соли с хлористым кальцием (CaCl2) с последующей очисткой путем повторной кристаллизации из смеси этилацетата и гексана, взятых в соотношении 5:3.
Настоящим изобретением предлагаются новые полиморфные модификации (кристаллические структуры) полукальциевой соли аторвастатина как в сольватированном, так и в гидратированном состояниях. Свойством некоторых молекул и молекулярных комплексов является способность к образованию разных кристаллических структур (полиморфизм). Из одних и тех же простых молекул, таких как аторвастатин (формула (I)), или солевых молекулярных комплексов, таких как тригидрат кальциевой соли аторвастатина (формула (II)), могут быть образованы различные твердые вещества, четко различающиеся по таким физическим свойствам, как температура плавления, рентгеновская дифракционная картина, картина инфракрасного поглощения и спектр ядерного магнитного резонанса. Различие физических свойств полиморфных модификаций вещества с одной и той же структурной молекулярной формулой обусловлено ориентацией и межмолекулярными взаимодействиями соседних молекул или молекулярных комплексов в массе твердого тела. Следовательно, мы имеем дело с составляющими семейство полиморфных модификаций разными твердыми веществами, имеющими одну и ту же структурную молекулярную формулу, но различающимися желательными или нежелательными для нас физическими свойствами. Одним из важнейших физических свойств полиморфных модификаций веществ, использующихся в качестве фармацевтических препаратов, является их растворимость в водных растворах, в особенности их растворимость в желудочном соке пациента. Так, например, в тех случаях, когда лекарственное вещество всасывается через желудочно-кишечный тракт, часто представляется желательным, чтобы лекарственное вещество, нестабильное в среде желудка или кишечника, растворялось медленно, с тем чтобы не происходило накопления продуктов его разложения, представляющих вред для организма. А в тех случаях, когда эффективность лекарственного вещества коррелирует с пиком концентрации этого лекарственного вещества в крови пациента, а этим свойством обладают лекарственные вещества класса статинов, и когда лекарственное вещество легко всасывается в желудочно-кишечном тракте, желательно, чтобы лекарственное вещество было в легкорастворимой полиморфной модификации, с тем чтобы была обеспечена более высокая эффективность по сравнению с таким же количеством этого вещества в малорастворимой полиморфной модификации.
Предметом патентов США №5.959.156 и №6.121.461, переданных компании Уорнер-Ламберт Ко. (Warner-Lambert Co.), являются полиморфные модификации Форма I, Форма II, Форма III и Форма IV полукальциевой соли аторвастатина, а полиморфная модификация Форма V полукальциевой соли аторвастатина раскрыта в являющейся общим достоянием патентной заявке №PCT/US00/31555. В патенте США №5.959.156 утверждается, что полиморфная модификация Форма I полукальциевой соли аторвастатина обладает более благоприятными, чем известная аморфная форма полукальциевой соли аторвастатина, характеристиками фильтрации и высушивания. Хотя полиморфная модификация Форма I свободна от некоторых недостатков аморфной полукальциевой соли аторвастатина с точки зрения технологичности, все же остается потребность в дальнейшем улучшении как этих, так и других свойств, таких как текучесть, паронепроницаемость и растворимость. Кроме того, открытие новых полиморфных модификаций лекарственного вещества дает занятым в этой отрасли ученым новые возможности для создания лекарственных форм с требуемым профилем высвобождения или другими желаемыми характеристиками.
КРАТКОЕ ОПИСАНИЕ ПРИЛАГАЕМЫХ ЧЕРТЕЖЕЙ
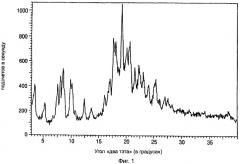
На фиг.1 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма VI, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
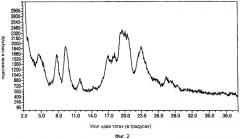
На фиг.2 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма VII, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
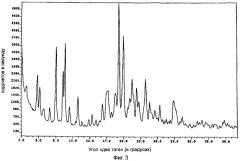
На фиг.3 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма VIII, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
На фиг.4 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма VIII, полученная при использовании синхротронного источника рентгеновского излучения.
На фиг.5 показан спектр ядерно-магнитного резонанса 13С полукальциевой соли аторвастатина полиморфной модификации Форма VIII.
На фиг.6 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма IX, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
На фиг.7 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма IX, полученная при использовании синхротронного источника рентгеновского излучения.
На фиг.8 показан спектр ядерно-магнитного резонанса 13С полукальциевой соли аторвастатина полиморфной модификации Форма IX.
На фиг.9 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма X, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
На фиг.10 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма X, полученная при использовании синхротронного источника рентгеновского излучения.
На фиг.11 показан спектр ядерно-магнитного резонанса 13С полукальциевой соли аторвастатина полиморфной модификации Форма X.
На фиг.12 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма XI, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
На фиг.13 приведена характеристическая диаграмма порошковой рентгеновской дифракции для полукальциевой соли аторвастатина полиморфной модификации Форма XII, полученная при использовании обычного генератора рентгеновского излучения с медным анодом.
На фиг.14 приведена термограмма цифровой сканирующей калориметрии заявляемой Формы IX.
На фиг.15 приведена термограмма цифровой сканирующей калориметрии известной Формы I.
На фиг.16 приведена термограмма цифровой сканирующей калориметрии известной Формы II.
На фиг.17 приведена термограмма цифровой сканирующей калориметрии известной Формы III.
На фиг.18 приведена термограмма цифровой сканирующей калориметрии известной Формы IV.
На фиг.19 приведена термограмма цифровой сканирующей калориметрии известной Формы VI.
На фиг.20 приведена термограмма цифровой сканирующей калориметрии известной Формы VI.
На фиг.21 приведено изображение частиц Формы XI, полученное с помощью оптического микроскопа.
На фиг.22-24 приведены изображения частиц Форм I-IV, полученные с помощью оптического микроскопа.
На фиг.25 приведено изображение частиц заявляемой Формы XII, полученное с помощью оптического микроскопа. Аторвастатин в легком масле.
КРАТКОЕ ОПИСАНИЕ ПРЕДЛАГАЕМОГО ИЗОБРЕТЕНИЯ
Предметом предлагаемого изобретения являются сольваты и гидраты полукальциевой соли аторвастатина.
Предметом предлагаемого изобретения является новая кристаллическая структура (полиморфная модификация) полукальциевой соли аторвастатина, обозначенная как Форма VI, и новые способы ее получения.
Еще одним предметом предлагаемого изобретения является новая кристаллическая структура (полиморфная модификация) полукальциевой соли аторвастатина, обозначенная как Форма VIII, и новые способы ее получения.
Еще одним предметом предлагаемого изобретения является новая кристаллическая структура (полиморфная модификация) полукальциевой соли аторвастатина, обозначенная как Форма IX, и новые способы ее получения.
Еще одним предметом предлагаемого изобретения является новая кристаллическая структура (полиморфная модификация) полукальциевой соли аторвастатина, обозначенная как Форма X, и новые способы ее получения.
Еще одним предметом предлагаемого изобретения является новая кристаллическая структура (полиморфная модификация) полукальциевой соли аторвастатина, обозначенная как Форма XI, и новые способы ее получения.
Еще одним предметом предлагаемого изобретения является новая кристаллическая структура (полиморфная модификация) полукальциевой соли аторвастатина, обозначенная как Форма XII, и новые способы ее получения.
Еще одним предметом предлагаемого изобретения являются новые способы получения полукальциевой соли аторвастатина полиморфной модификации Форма I.
Еще одним предметом предлагаемого изобретения являются новые способы получения полукальциевой соли аторвастатина полиморфной модификации Форма II.
Еще одним предметом предлагаемого изобретения являются новые способы получения полукальциевой соли аторвастатина полиморфной модификации Форма IV.
Еще одним предметом предлагаемого изобретения являются новые способы получения полукальциевой соли аторвастатина полиморфной модификации Форма V.
Еще одним предметом предлагаемого изобретения являются новые способы получения аморфной полукальциевой соли аторвастатина
Еще одним предметом предлагаемого изобретения являются фармацевтические композиции и лекарственные формы, содержащие полукальциевую соль аторвастатина в какой-либо из следующих полиморфных модификаций: Форма VI, Форма VII, Форма VIII, Форма IX, Форма Х, Форма XI, или смеси этих полиморфных модификаций.
ПОДРОБНОЕ ОПИСАНИЕ ПРЕДЛАГАЕМОГО ИЗОБРЕТЕНИЯ
Некоторые кристаллические структуры (полиморфные модификации) полукальциевой соли аторвастатина существуют в сольватированном состоянии и гидратированном состоянии. Гидраты полукальциевой соли аторвастатина исследовались с помощью анализа по методу Карла Фишера и термогравиметрического анализа.
Анализ по методу порошковой рентгеновской дифракции с использованием обычного CuKα-излучения осуществлялся с помощью известных в отрасли способов с использованием порошкового рентгеновского дифрактометра модели X'TRA производства SCINTAG (компании Scintag, inc.), снабженного твердотельным детектором. Использовалось излучение меди с длиной волны λ=1,5418Å. Диапазон измерений составлял от 2 до 40° угла 2θ ("два тэта"). Образец вводился с помощью круглого стандартного алюминиевого держателя, имеющего на дне новую (нулевой категории) круглую кварцевую пластинку. Истолченные в порошок образцы подвергались осторожному перемалыванию, и ими, с уплотнением с помощью стеклянной пластинки, заполнялась имеющая круглую форму полость в держателе образца.
Анализ по методу порошковой рентгеновской дифракции с использованием синхротронного источника рентгеновского излучения осуществлялся на установке "National Synchrotron Light Source" Бруклинской национальной лаборатории (дифрактометрическая станция Х3В1). Образцы были без прессования упакованы в тонкостенные стеклянные капилляры. Длина волны рентгеновского излучения составляла приблизительно 1,15Å. Поскольку длина волны падающего света соответствует длине волны, чаще всего используемой в анализе по методу порошковой рентгеновской дифракции, пиковые значения рентгеновского излучения в диаграмме дифракции, полученной от синхротронного источника, выражаются в терминах d-интервалов, которые при изменении длины волны для получения диаграммы рентгеновской дифракции являются инвариантными. Сканирование осуществлялось в диапазоне от 1 до 20° угла 2θ. Спектральное разрешение находится в диапазоне от 0,01 до 0,03° полной ширины на половине максимума. Положения пиков с хорошим разрешением определены с точностью от 0,003 до 0,01°.
Измерения спектров ядерно-магнитного резонанса 13С с CP/MAS (кросс-поляризация / вращение под магическим углом) проводились при частоте 125,76 МГц с помощью цифрового спектрометра ядерного магнитного резонанса в Фурье-модификации (FT NMR) марки "Bruker DMX-500", снабженного измерительной головкой марки BL-4 с кросс-поляризацией/вращением под магическим углом и предусилителем излучения 1H для твердых веществ: скорость вращения 5,0 кГц, последовательность импульсов SELTICS (сокращение от "Sideband Elimination by Temporary Interruption of Chemical Shift" - "Подавление боковой полосы путем временной приостановки химического сдвига"), держатель образца - циркониевый ротор диаметром 4 мм.
Полукальциевая соль аторвастатина полиморфной модификации Форма VI характеризуется диаграммой порошковой рентгеновской дифракции, показанной на фиг.1, которая имеет пиковые значения при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 3,5, 5,1, 7,7, 8,2, 8,7 10,0, 12,5, 13,8, 16,2, 17,2, 17,9, 18,3, 19,5, 20,4, 20,9, 21,7, 22,4, 23,2, 24,3, 25,5. Наиболее характеристический пик наблюдается при значении угла "два тэта" 19,5±0,2 градуса. Диаграмма порошковой рентгеновской дифракции полукальциевой соли аторвастатина полиморфной модификации Форма VI была получена с помощью дифрактометра марки "Phylips", подобного аппаратуре SCINTAG, которая упоминалась выше.
Полукальциевая соль аторвастатина полиморфной модификации Форма VI может быть получена путем растворения полукальциевой соли аторвастатина любой другой полиморфной модификации, предпочтительно полиморфной модификации Форма I, в ацетоне с последующим осаждением полукальциевой соли аторвастатина полиморфной модификации Форма VI при добавлении антирастворителя, предпочтительно воды.
Полукальциевая соль аторвастатина полиморфной модификации Форма VII характеризуется диаграммой порошковой рентгеновской дифракции, показанной на фиг.2, которая имеет два широких пика: один при значениях угла "два тэта" в диапазоне от 18,5 до 21,8°, другой при значениях угла "два тэта" в диапазоне от 21,8 до 25,0°, и дополнительные широкие пики при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 4,7, 7,8, 9,3, 12,0, 17,1, 18,2. Содержание воды в образцах полукальциевой соли аторвастатина полиморфной модификации Форма VII могут достигать 12%.
Полиморфная модификация Форма VII полукальциевой соли аторвастатина может быть легко отличена от других полиморфных модификаций этого вещества по двум широким пикам при значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса) 7,8 и 9,3. Например, согласно информации, содержащейся в патенте США №5.969.156, полукальциевая соль аторвастатина полиморфной модификации Форма I имеет следующие пиковые значения угла "два тэта" (в градусах): 9,2, 9,5, 10,3, 10,6, 11,0 и 12,2. В этом диапазоне полиморфная модификация Форма II имеет два острых пика при значениях угла "два тэта" (в градусах) 8,5 и 9,0, а полиморфная модификация Форма IV имеет один сильный пик при значениях угла "два тэта" 8,0 градусов. Другие широкие пики в диапазоне углов "два тэта" от 15 до 25° отличают полиморфную модификацию Форма VII от всех других полиморфных модификаций. Полиморфные модификации Форма I, Форма III и Форма IV все имеют в этом диапазоне углов "два тэта" острые пики.
Полукальциевая соль аторвастатина полиморфной модификации Форма VII может быть получена путем обработки полукальциевой соли аторвастатина полиморфной модификации Форма I с помощью этилового спирта, предпочтительно безводного этилового спирта, при температуре от комнатной до температуры дефлегмации в течение периода времени продолжительностью от приблизительно 1 часа до приблизительно 24 часов, предпочтительно от 2,5 до 16 часов. Если процесс осуществляется при дефлегмации этилового спирта, то превращение завершается в течение приблизительно 2,5 часов. Если же процесс осуществляется при комнатной температуре, то для его завершения требуется более длительное время.
Полукальциевая соль аторвастатина полиморфной модификации Форма VIII характеризуется диаграммой порошковой рентгеновской дифракции, показанной на фиг.3, которая получена с использованием обычного CuKα-излучения, при этом излучение имеет пиковые значения при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 4,8, 5,2, 5,9, 7,0, 8,0, 9,3, 9,6, 10,4, 11,9, 16,3, 17,1 (широкий пик), 17,9, 18,6, 19,2, 20,0, 20,8, 21,1, 21,6, 22,4, 22,8, 23,9, 24,7, 25,6, 26,5, 29,0. Наиболее характеристические пики наблюдаются при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 6,9, 9,3, 9,6, 16,3, 17,1, 19,2, 20,0, 21,6, 22,4, 23,9, 24,7, 25,6 и 26,5. С помощью анализа по методу Карла Фишера было установлено, что содержание воды в образцах полукальциевой соли аторвастатина полиморфной модификации Форма VIII достигает 7%. Полиморфная модификация Форма VII полукальциевой соли аторвастатина может быть легко отличена от полиморфных модификаций Форма I - Форма IV по характеристическим острым пикам при значениях угла "два тэта" 9,3 и 9,6°. Согласно информации, содержащейся в патенте США №5.969.156, полукальциевая соль аторвастатина полиморфной модификации Форма I имеет один средний пик при значении угла "два тэта" 6,9° и острые пики при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 9,2, 9,5, 10,3, 10,6, 11,0 и 12,2. Что касается полиморфной модификации Форма IV, то считается установленным, что она имеет два пиковых значения: при значениях угла "два тэта" 8,0 и 9,7°. В отношении полиморфной модификации Форма II считается установленным, что она имеет в этой области два острых пика: при значениях угла "два тэта" 8,5 и 9,0°. А в отношении полиморфной модификации Форма III в соответствии с информацией, содержащейся в патенте США №6.121.461, известно, что она имеет в этой области один сильный пик при значении угла "два тэта" 8,7. Эти характеристики не наблюдаются на диаграмме порошковой рентгеновской дифракции для полиморфной модификации Форма VIII. Кроме того, на диаграмме порошковой рентгеновской дифракции для полиморфной модификации Форма VIII наблюдается один острый пик средней интенсивности при значении угла "два тэта" 7,0°, который четко отличается от других пиков в этой области. Сравнение диаграммы порошковой рентгеновской дифракции для полиморфной модификации Форма VIII с диаграммами порошковой рентгеновской дифракции для полиморфных модификаций Форма I - Форма IV показывает, что эта характеристика полиморфной модификации Форма VIII является отличительной.
Другие пики на диаграмме порошковой рентгеновской дифракции для полиморфной модификации Форма VIII, которые являются уникальными для этой полиморфной модификации, наблюдаются при значениях угла "два тэта" 19,2 и 20,0° (сильные и острые пики). Согласно информации, содержащейся в патенте США №5.969.156, полиморфная модификация Форма I имеет в этой области следующие пиковые значения угла "два тэта" (в градусах): 21,6, 22,7, 23,3 и 23,7. Считается установленным, что в этой области полиморфная модификация Форма IV имеет пики при значениях угла "два тэта" 18,4 и 19,6°, в то время как полиморфная модификация Форма II имеет два главных пика при значениях угла "два тэта" 17,0 и 20,5°, а полиморфная модификация Форма III имеет пики при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 17,7, 18,2, 18,9, 20,0 и 20,3.
Для определения кристаллической системы и размеров элементарной ячейки кристалла полукальциевая соль аторвастатина полиморфной модификации Форма VIII была подвергнута анализу по методу синхротронной порошковой рентгеновской дифракции. В результате анализа было установлено, что полиморфная модификация Форма VIII имеет моноклинальную элементарную ячейку со следующими размерами кристаллической решетки: а=18,55-18,7Å, b=5,52-5,53Å, с=31,0-31,2Å, а угол β между осями "а" и "с" составляет 97,5-99,5°. Указанные параметры элементарной ячейки были определены с помощью метода Ле Бэля (Le Bail).
Дифрактограмма, приведенная на фиг.4, которая получена с помощью синхротронного источника рентгеновских лучей, имеет много острых пиков с высоким разрешением. В помещенной ниже таблице 1 приведены d-интервалы некоторых из более заметных пиков, а также значения угла 2θ ("два тэта"), при которых пики бы имели место в случае использования CuKα-излучения с длиной волны λ=1,5418Å.
| Таблица 1 | |
| d-интервалы (Å) | 2θ (в градусах) |
| 30,81 | 2,87 |
| 18,46 | 4,79 |
| 16,96 | 5,21 |
| 15,39 | 5,74 |
| 14,90 | 5,93 |
| 12,78 | 6,92 |
| 11,05 | 8,00 |
| 9,58 | 9,23 |
| 9,22 | 9,59 |
| 7,42 | 11,93 |
| 6,15 | 14,40 |
| 5,43 | 16,32 |
| 4,62 | 19,21 |
| 4,44 | 20,00 |
| 3,98 | 22,34 |
| Примечание: угол 2θ рассчитан по значениям d-интервалов для CuKα-излучения. |
По причине естественного различия в свойствах независимых образцов и погрешностей измерения пиковые значения могут отклоняться от указанных выше в таблице 1 на 0,5% значения d-интервала. Если материал подвергается измельчению, например микронизации, то возможны более значительные отклонения.
Полукальциевая соль аторвастатина полиморфной модификации Форма VIII дает спектр ядерно-магнитного резонанса 13С в твердой фазе, показанный на фиг.5. Полиморфная модификация Форма VIII характеризуется следующими значениями химических сдвигов при ядерно-магнитном резонансе 13С в твердой фазе (в миллионных долях): 17,8, 20,0, 24,8, 25,2, 26,1, 40,3, 40,8, 41,5, 43,4, 44,1, 46,1, 70,8, 73,3, 114,1, 116,0, 119,5, 120,1, 121,8, 122,8, 126,6, 128,8, 129,2, 134,2, 135,1, 137,0, 138,3, 139,8, 159,8, 166,4, 178,8, 186,5. Полиморфная модификация Форма VIII при исследовании по методу ядерно-магнитного резонанса 13С в твердой фазе характеризуется следующими разностями химических сдвигов между резонансом с самым низким (в миллионных долях) значением химического сдвига и другими резонансами (в миллионных долях): 2,2, 7,0, 7,4, 8,3, 22,5, 23,0, 23,7, 25,6, 26,3, 28,3, 53,0, 55,5, 96,3, 98,2, 101,7, 102,3, 104,0, 105,0, 108,8, 111,0, 111,4, 116,4, 117,3, 119,2, 120,5, 122,0, 142,0, 148,6, 161,0 и 168,7. Указанные выше для полиморфной модификации Форма VIII значения химических сдвигов получены путем усреднения значений, полученных от спектров четырех образцов полукальциевой соли аторвастатина полиморфной модификации Форма VIII. Характеристические части дифракционной диаграммы обнаруживаются при значениях химического сдвига в диапазоне от 24 миллионных долей до 26 миллионных долей (алифатический диапазон), в диапазоне от 119 миллионных долей до 140 миллионных долей (ароматический диапазон) и в других областях. Точность, с которой определены значения химического сдвига, составляет ±0,1 миллионной доли, за исключением карбонилового пика при значении химического сдвига 178,8 миллионной доли, у которого флуктуация составляет ±0,4 миллионной доли.
Полукальциевая соль аторвастатина полиморфной модификации Форма VIII может существовать в виде сольвата с этиловым спиртом, в котором содержание этилового спирта достигает приблизительно 3%.
Для получения полукальциевой соли аторвастатина полиморфной модификации Форма VIII были признаны подходящими способы, описываемые ниже. При этом следует заметить, что эта полиморфная модификация может быть получена также путем эмпирического развития и очевидной модификации этих способов.
Полукальциевая соль аторвастатина полиморфной модификации Форма VIII может быть получена путем суспендирования полукальциевой соли аторвастатина в среде смеси этилового спирта и воды при повышенной температуре, предпочтительно при температуре от 78 до 80°С. Процедура суспендирования может быть включена в последнюю стадию способа получения полукальциевой соли аторвастатина, который обычно состоит в получении полукальциевой соли аторвастатина из свободной аторвастатиновой кислоты или лактона путем обработки ее с помощью источника ионов кальция. При такой комбинированной процедуре получается полукальциевая соль аторвастатина в системе растворителя, состоящей из этилового спирта и воды. При этом удобный способ получения полукальциевой соли аторвастатина полиморфной модификации Форма VIII состоит в осаждении полукальциевой соли аторвастатина путем добавления некоторого дополнительного количества воды с последующим суспендированием этой соли в среде указанной реакционной смеси в течение нескольких часов, предпочтительно от 6 до 16 часов.
Полиморфная модификация Форма VIII может быть получена также из полиморфной модификации Форма V путем обработки полиморфной модификации Форма V с помощью смеси этилового спирта и воды (EtOH:Н2О), взятых предпочтительно в соотношении приблизительно 5:1, при повышенной температуре ниже температуры дефлегмации, предпочтительно при температуре от 78 до 80°С. Одна из особо предпочтительных смесей этилового спирта и воды (EtOH:Н2О) содержит приблизительно 4% (по объему) воды в этиловом спирте. В процессе нагревания постепенно происходит растворение полиморфной модификации Форма V, и при достижении температуры 78-80°С наблюдается помутнение с закипанием или без закипания. По достижении этого состояния суспензию немедленно начинают охлаждать до комнатной температуры.
Кроме того, полиморфная модификация Форма VIII может быть получена путем обработки полукальциевой соли аторвастатина с помощью этилового спирта (EtOH), предпочтительно безводного этилового спирта, при повышенной температуре, предпочтительно при температуре кипения этилового спирта. При этих условиях происходит растворение и повторное осаждение аторвастатина. При дефлегмации может быть добавлен метиловый спирт (МеОН). Добавленный метиловый спирт может оказать неблагоприятное воздействие на выход конечного продукта, но зато может повысить его химическую чистоту. В качестве исходного материала для получения полиморфной модификации Форма VIII по этому способу могут быть взяты другие полиморфные модификации полукальциевой соли аторвастатина, предпочтительно полиморфные модификации Форма I или Форма V, а также их смеси с аморфной полукальциевой солью аторвастатина.
В предпочтительных вариантах осуществления вышеописанных способов получения полукальциевой соли аторвастатина полиморфной модификации Форма VIII этиловый спирт или его смесь с водой используют в количестве от приблизительно 10 мл на грамм до приблизительно 100 мл на грамм, в еще более предпочтительных вариантах от приблизительно 20 мл на грамм до приблизительно 80 мл на грамм.
Авторами предлагаемого изобретения было обнаружено, что полукальциевая соль аторвастатина, содержащая более 0,1% дефторированной формы полукальциевой соли аторвастатина и/или более 1% транс-изомера полукальциевой соли аторвастатина, может быть очищена путем суспендирования в среде раствора, содержащего приблизительно 96% этилового спирта и приблизительно 4% воды, при повышенной температуре, предпочтительно при температуре дефлегмации. Обычно же извлечение полукальциевой соли возможно при загрязнении дефторированной формой полукальциевой соли аторвастатина менее 0,07% и загрязнении транс-изомером полукальциевой соли аторвастатина менее 0,6%.
Кроме того, полиморфная модификация Форма VIII может быть получена путем суспендирования полукальциевой соли аторвастатина в среде определенных смесей первичного бутилового спирта с водой и этилового спирта с водой в течение периода времени, достаточного для превращения полукальциевой соли аторвастатина в полиморфную модификацию Форма VIII. Используемые в этих способах смеси первичного бутилового спирта с водой должны содержать первичный бутиловый спирт в количестве приблизительно 20% по объему, при этом суспендирование осуществляется при повышенной температуре, предпочтительно при температуре дефлегмации.
Полукальциевая соль аторвастатина полиморфной модификации Форма IX характеризуется диаграммой порошковой рентгеновской дифракции, показанной на фиг.5, которая имеет пиковые значения при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 4,7, 5,2, 5,7, 7,0, 7,9, 9,4, 10,2, 12,0, 17,0, 17,4, 18,2, 19,1, 19,9, 21,4, 22,5, 23,5, 24,8 (широкий пик), 26,1, 28,7, 30,0. Наиболее характеристические пики полиморфной модификации Форма IX наблюдаются при следующих значениях угла "два тэта" (в градусах, с допуском ±0,2 градуса): 6,9, 17,0, 17,4, 18,2, 18,6, 19,1, 19,9, 21,4, 22,5 и 23,5. Содержание воды в полукальциевой соли аторвастатина полиморфной модификации Форма IX может достигать 7%. Полиморфная модификация Форма IX может существовать также в форме сольвата с бутиловым спиртом, содержание бутилового спирта в котором достигает приблизительно 5%.
Полиморфная модификация Форма IX полукальциевой соли аторвастатина может быть легко отличена от других полиморфных модификаций этого вещества по характеристическим острым пикам при следующих значениях угла "два тэта" (в градусах): 18,6, 19,1, 19,9, 21,4, 22,5, 23,5. Для сравнения: согласно информации, содержащейся в патенте США №5.969.156, полиморфная модификация Форма I имеет острые пики при следующих значениях угла "два тэта" (в градусах): 21,6, 22,7, 23,3 и 23,7, полиморфная модификация Форма IV в этой области имеет острые пики при значениях угла "два тэта" 18,4° и 19,6°, а полиморфная модификация Форма II имеет два главных пика при значениях угла "два тэта" 17,0 и 20,5°. Полиморфная модификация Форма III имеет в этой области пики при следующих значениях угла "два тэта" (в градусах): 17,7, 18,3, 18,9, 20,0 и 20,3. Следует заметить также, что на диаграмме порошковой рентгеновской дифракции полиморфной модификации Форма IX, как и на диаграмме порошковой рентгеновской дифракции полиморфной модификации Форма VIII, наблюдается острый хорошо различимый пик средней интенсивности при значении угла "два тэта" 7,0°.
Для определения кристаллической системы и размеров элементарной ячейки кристалла полукальциевая соль аторвастатина полиморфной модификации Форма IX была подвергнута анализу по методу синхротронной порошковой рентгеновской дифракции. В результате анализа было установлено, что полиморфная модификация Форма IX имеет моноклинальную элементарную ячейку со следующими размерами кристаллической решетки: а=18,75-18,85Å, b=5,525-5,54Å, с=30,9-31,15Å, а угол β между осями "а" и "с" составляет 96,5-97,5°.
В помещенной ниже таблице 2 приведены d-интервалы некоторых из более заметных пиков дифрактограммы, приведенной на фиг.7, которая получена с помощью синхротронного источника рентгеновских лучей, а также значения угла 2θ ("два тэта"), при которых пики имели бы место в случае использования CuKα-излучения.
| Таблица 2 | |
| d-интервалы (Å) | 2θ (в градусах) |
| 30,86 | 2,86 |
| 18,67 | 4,73 |
| 16,91 | 5,23 |
| 15,17 | 5,83 |
| 12,66 | 6,98 |
| 11,20 | 7,89 |
| 9,50 | 9,31 |
| 9,28 | 9,53 |
| 8,63 | 10,25 |
| 7,69 | 11,51 |
| 7,38 | 11,99 |
| 6,51 | 13,60 |
| 5,45 | 16,26 |
| 5,26 | 16,86 |
| 5,20 | 17,05 |
| 5,12 | 17,32 |
| 4,87 | 18,22 |
| 4,76 | 18,64 |
| 4,63 | 19,17 |
| 4,47 | 19,86 |
| 4,14 | 21,46 |
| 4,08 | 21,78 |
| 3,78 | 23,54 |
| 3,73 | 23,86 |
| 3,62 | 24,59 |
| 3,58 | 24,87 |
| Примечание: угол 2θ рассчитан по значениям d-интервалов для CuKα-излучения. |
По причине естественного различия в свойствах независимых образцов и погрешностей измерения пиковые значения могут отклоняться от указанных выше в таблице 2 на 0,5% значения d-интервала. Если материал подвергается измельчению, например микронизации, то возможны более значительные отклонения.
Полукальциевая соль аторвастатина полиморфной модификации Форма IX дает спектр ядерно-магнитного резонанса 13С в