Способ определения фенола в водных средах
Иллюстрации
Показать всеИзобретение относится к определению и санитарно-эпидемиологическому контролю содержания фенола в питьевых, природных и сточных водах, а также в атмосферных осадках. Способ включает химическую модификацию фенола в 2,4,6-трибромфенол, экстракционное концентрирование 2,4,6-трибромфенола и последующее газохроматографическое детектирование, причем перед химической модификацией из водной пробы удаляют гумусовые кислоты на оксиде алюминия в присутствии сульфата меди в количестве 0,05-0,25% от массы водной пробы. Достигается повышение надежности анализа. 2 табл., 7 ил.
Реферат
Изобретение относится к аналитической химии органических соединений (концентрирование и определение) и может быть использовано для санитарно-эпидемиологического контроля содержания фенола в питьевых, природных, сточных водах, а также в атмосферных осадках.
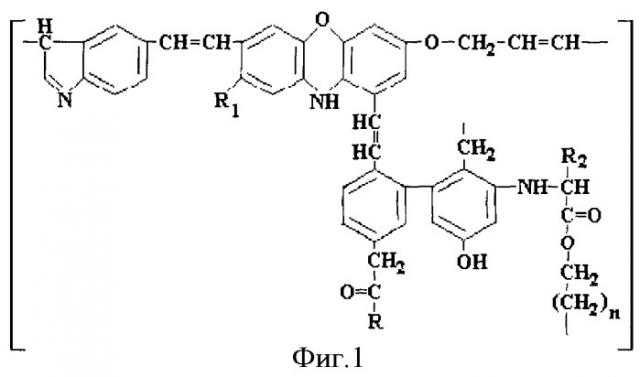
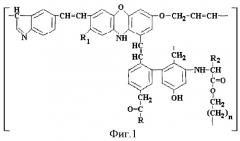
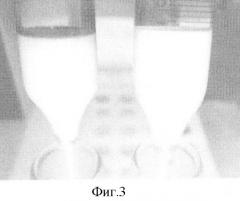
Наиболее близким по технической сущности к заявляемому решению является газохроматографический способ определения фенола в питьевой воде [Коренман Я.И., Груздев И.В., Кондратенок Б.М., Фокин В.Н. Условия бромирования и газохроматографическое определение фенолов в питьевой воде // Журнал аналитической химии. - 1999. - Т.54. - №12. - С.1134-1138]. Недостаток прототипа - получение недостоверных результатов определения фенола в водных средах, содержащих гумусовые кислоты. Согласно современным представлениям [Орлов Д.С. Химия почв. - М.: Изд-во МГУ, 1992. - 400 с.] гумусовые кислоты - это нерегулярные сополимеры ароматических оксиполикарбоновых кислот с включениями азотсодержащих и углеводных фрагментов. На фиг.1 приведена гипотетическая структурная формула фрагмента гумусовой кислоты. Применяемый для химической модификации фенола молекулярный бром вызывает деструкцию гумусовых кислот, одним из продуктов которой является фенол. На фиг.2 представлены процессы, которые протекают в воде, содержащей гумусовые кислоты, в присутствии молекулярного брома: 1 - бромирование нативного фенола, 2 - деструкция гумусовых кислот, 3 - бромирование фенола, образующегося при деструкции. Этот фенол также подвергается химической модификации в 2,4,6-трибромфенол, и результат анализа завышается, поскольку представляет собой сумму концентраций нативного фенола и фенола, образовавшегося при деструкции гумусовых кислот.
Задачей изобретения является устранение мешающего влияния гумусовых кислот при определении фенола в водных средах. В этом состоит технический результат.
Решение поставленной задачи достигается тем, что в способе определения фенола в водных средах, включающем его химическую модификацию в 2,4,6-трибромфенол, экстракционное концентрирование 2,4,6-трибромфенола и последующее газохроматографическое детектирование, новым является то, что перед химической модификацией из водной пробы удаляют гумусовые кислоты на оксиде алюминия в присутствии сульфата меди в количестве 0.05-0.25% от массы водной пробы.
Удаление гумусовых кислот на оксиде алюминия основано на том, что поверхность гидратированного оксида алюминия заряжена положительно, а агрегаты гумусовых кислот несут на себе отрицательный заряд [S.Goldberg, J.A.Davis, J.D.Hem. The surface chemistry of aluminum oxides and hydroxides // The environmental chemistry of aluminum / edited by G.Sposito. - NY: Lewis Publishers, 1996. - P.272-333].
Количественного удаления гумусовых кислот в отсутствие сульфата меди добиться невозможно, так как по мере увеличения объема очищаемой воды слой оксида алюминия преодолевают низкомолекулярные фрагменты гумусовых кислот.
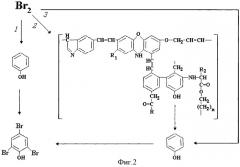
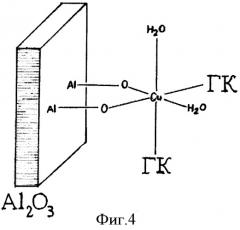
При введении в водный образец сульфата меди образующиеся катионы меди вступают во взаимодействие с оксидом алюминия, формируя узкую хроматографическую зону, которая при пропускании воды постепенно продвигается. На фиг.3 представлена фотография стеклянной хроматографической колонки, заполненной оксидом алюминия: до удаления (справа) и после удаления (слева) гумусовых кислот из водного образца. Кроме этого катионы меди, являясь хорошими комплексообразователями, взаимодействуют и с низкомолекулярными фрагментами гумусовых кислот, связывая и удерживая их в слое хроматографической зоны. На фиг.4 представлена схема образования химических связей катионом меди в слое оксида алюминия (Al2O3 - поверхность оксида алюминия, ГК - низкомолекулярные фрагменты гумусовых кислот). Таким образом, гумусовые кислоты не попадут в элюат до тех пор, пока катионы меди не преодолеют слой оксида алюминия.
В то же время сорбция самого фенола на поверхности оксида алюминия практически отсутствует и составляет 2-3% для 2 граммов Al2О3 и концентрации фенола в воде 0.1-10 мкг/дм3. На фиг.5 приведена зависимость сорбции фенола на оксиде алюминия от массы Al2O3 (объем водного образца - 25 см3, концентрация фенола в воде - 1 мкг/дм3).
Способ определения фенола в водных средах включает четыре этапа.
1) Удаление гумусовых кислот из водной пробы на колонке с оксидом алюминия. Количественное удаление гумусовых кислот необходимо, поскольку их присутствие в воде на стадии химической модификации, даже в следовых количествах, ведет к искажению результатов количественного анализа фенола.
2) Химическая модификация фенола - обработка очищенного от гумусовых кислот водного образца молекулярным бромом. При бромировании атомы брома замещают атомы водорода в ароматическом ядре фенола в положениях 2, 4 и 6. При комнатной температуре (20±5°С) реакция бромирования фенола завершается в течение 40-60 сек с количественным образованием 2,4,6-трибромфенола.
3) Экстракционное концентрирование 2,4,6-трибромфенола методом жидкостной экстракции. Эта стадия предназначена для перевода 2,4,6-трибромфенола в более удобную для последующего газохроматографического анализа органическую фазу, повышения его концентрации в экстракте и отделения мешающих компонентов.
4) Анализ экстракта методом газовой хроматографии. Полученный экстракт 2,4,6-трибромфенола анализируют методом капиллярной газовой хроматографии с детектором электронного захвата (ДЭЗ). Галогенселективный ДЭЗ обеспечивает максимально возможное по чувствительности газохроматографическое определение 2,4,6-трибромфенола.
Определение фенола выполняют по следующей методике. К анализируемой пробе воды объемом 30 см3 приливают 0.3-1.5 см3 раствора сульфата меди (C(CuSO4·5H2O)=0.2 моль/дм3), что составляет 0.05-0.25% от массы пробы, и переливают смесь в предварительно подготовленную стеклянную хроматографическую колонку с 2 г оксида алюминия. Элюат отбирают в стеклянную пробирку вместимостью 25.0 см3, подкисляют серной кислотой до рН 2-3, добавляют 1.0 см3 бромной воды (С(Br2)=0.01 моль/дм3) и бромируют в течение 1 минуты. После завершения реакции бромирования избыток брома удаляют добавлением 1.0 см3 раствора тиосульфата натрия (С(Na2Sa2O3)=0.01 моль/дм3). Далее вводят внутренний стандарт - 0.2 см3 спиртового раствора 2,4,6-трихлорфенола (ρ(2,4,6-трихлорфенол)=0.25 мкг/см3), 1.0 см3 толуола и экстрагируют в течение 5 минут при непрерывном перемешивании. После расслаивания фаз 3 мм3 органического экстракта анализируют на газовом хроматографе с ДЭЗ.
Условия газохроматографического определения: температура детектора 320°С, испарителя 320°С, термостата колонок 200°С; кварцевая капиллярная колонка 30 м×0.25 мм×0.25 мкм со слабополярной неподвижной жидкой фазой (SE-30, SE-52, SE-54), скорость потока газа-носителя (азот, ос.ч.) через колонку 0.8 см3/мин, поддув детектора 20 см3/мин, деление потока 1:50. На фиг.6 приведена хроматограмма стандартного раствора фенола с концентрацией 1 мкг/дм3 (ВС - 2,4,6-трихлорфенол, внутренний стандарт, 2,4,6-ТБФ - 2,4,6-трибромфенол).
Идентификацию 2,4,6-трибромфенола в анализируемой пробе воды проводят по относительному времени удерживания tx*:
tx*=tx/tст,
где tx и tст - исправленные времена удерживания компонентов анализируемой пробы и внутреннего стандарта соответственно.
Относительные времена удерживания компонентов анализируемой пробы сравнивали с относительным временем удерживания 2,4,6-трибромфенола, полученного для стандартного раствора: tх*(2,4,6-трибромфенол)=2.752.
Массовую концентрацию фенола в анализируемой пробе воды рассчитывали по уравнению, полученному на основе градуировочного графика для стандартных водных растворов фенола (таблица 1):
ρ(мкг/дм3)=2.372 S/Sst-0,006(R2=0.9988),
где S/Sst - отношение площади пика 2,4,6-трибромфенола к площади пика внутреннего стандарта (2,4,6-трихлорфенол).
| Таблица 1Результаты газохроматографического анализа стандартных растворов фенола | |
| ρ (фенол), мкг/дм3 | S/Sst |
| 1 | 0.432 |
| 5 | 2.146 |
| 10 | 4.152 |
| 15 | 6.325 |
| 20 | 8.458 |
На фиг.7 приведена градуировочная зависимость массовой концентрации фенола (стандартные растворы) от соотношения площадей хроматографических пиков S/Sst.
Примеры осуществления способа
Пример 1.
Образец природной воды, содержащий гумусовые кислоты, ρ(фенол)=2 мкг/дм3. К анализируемой пробе воды объемом 30 см3 приливают 0,03 см3 раствора сульфата меди (C(CuSO4·5H2O)=0.2 моль/дм3), что составляет 0,005% от массы пробы, и переливают смесь в предварительно подготовленную стеклянную хроматографическую колонку с 2 г оксида алюминия. Элюат отбирают в стеклянную пробирку вместимостью 25.0 см3, подкисляют серной кислотой до рН 2-3, добавляют 1.0 см3 бромной воды (C(Br2)=0.01 моль/дм3) и бромируют в течение 1 минуты. После завершения реакции бромирования избыток брома удаляют добавлением 1.0 см3 раствора тиосульфата натрия (C(Na2S2O3)=0.01 моль/дм3). Далее вводят внутренний стандарт - 0.2 см3 спиртового раствора 2,4,6-трихлорфенола (ρ(2,4,6-трихлорфенол)=0.25 мкг/см3), 1.0 см3 толуола и экстрагируют в течение 5 минут при непрерывном перемешивании. После расслаивания фаз 3 мм3 органического экстракта анализируют на газовом хроматографе с ДЭЗ.
Определяемая концентрация фенола в природной воде равна 5.4 мкг/дм3. Способ неосуществим, так как мешающее влияние гумусовых кислот при содержании сульфата меди в пробе 0.005% не устраняется.
Пример 2.
Содержание сульфата меди в пробе - 0.015%. Анализируют, как указано в примере 1. Определяемая концентрация фенола - 3.3 мкг/дм3. Способ неосуществим, так как мешающее влияние гумусовых кислот не устраняется.
Пример 3.
Содержание сульфата меди в пробе - 0.05%. Анализируют, как указано в примере 1. Определяемая концентрация фенола - 1.9 мкг/дм3. Способ осуществим.
Пример 4.
Содержание сульфата меди в пробе - 0.15%. Анализируют, как указано в примере 1. Определяемая концентрация фенола - 2.1 мкг/дм3. Способ осуществим.
Пример 5.
Содержание сульфата меди в пробе - 0.25%. Анализируют, как указано в примере 1. Определяемая концентрация фенола - 2.1 мкг/дм3. Способ осуществим.
Пример 6.
Содержание сульфата меди в пробе - 0.5%. Анализируют, как указано в примере 1. Определяемая концентрация фенола - 3.7 мкг/дм3. Способ неосуществим, так как мешающее влияние гумусовых кислот не устраняется.
Пример 7.
Содержание сульфата меди в пробе - 1.0%. Анализируют, как указано в примере 1. Определяемая концентрация фенола - 4.5 мкг/дм3. Способ неосуществим, так как мешающее влияние гумусовых кислот не устраняется.
Результаты определения фенола в воде предлагаемым способом приведены в табл.2.
| Таблица 2Примеры осуществления способа | ||||
| № примера | Содержание сульфата меди по отношению к массе пробы, % | Концентрация фенола в воде, мкг/дм3 | Определяемая концентрация фенола в воде, мкг/дм3 | Возможность осуществления заявляемого способа |
| По прототипу | - | 2 | 7.3 | - |
| 1 | 0.005 | 2 | 5.4 | неосуществим |
| 2 | 0.015 | 2 | 3.3 | неосуществим |
| 3 | 0.05 | 2 | 1.9 | осуществим |
| 4 | 0.15 | 2 | 2.1 | осуществим |
| 5 | 0.25 | 2 | 2.1 | осуществим |
| 6 | 0.5 | 2 | 3.7 | неосуществим |
| 7 | 1.0 | 2 | 4.5 | неосуществим |
Из примеров 1-7 и табл.2 следует, что предлагаемый способ определения фенола в водных средах осуществим в диапазоне концентраций сульфата меди 0.05-0.25% по отношению к массе пробы. При меньших концентрациях катионов меди недостаточно для связывания всех низкомолекулярных фрагментов гумусовых кислот, часть из них преодолевает колонку с оксидом алюминия и попадает в элюат. При концентрациях >0.25% катионов меди образуется больше, чем может сорбироваться на оксиде алюминия, и этот избыток попадает в элюат вместе с присоединенными частицами гумусовых кислот.
По сравнению с прототипом предлагаемое техническое решение имеет следующие преимущества.
1) Получение достоверных результатов анализа в независимости от качественного и количественного состава анализируемого водного образца.
2) Полное удаление мешающих компонентов (грубодисперсные, мелкодисперсные и коллоидные частицы).
3) Отсутствие образования устойчивых эмульсий после проведения экстракционного концентрирования, осложняющих последующее газохроматографическое определение.
Способ определения фенола в водных средах, включающий его химическую модификацию в 2,4,6-трибромфенол, экстракционное концентрирование 2,4,6-трибромфенола и последующее газохроматографическое детектирование, отличающийся тем, что перед химической модификацией из водной пробы удаляют гумусовые кислоты на оксиде алюминия в присутствии сульфата меди в количестве 0,05-0,25% от массы водной пробы.