Способ и устройство для уменьшения выделений ртути в отработавших газах
Иллюстрации
Показать всеИзобретение может быть использовано для уменьшения выделения ртути при очистке отходящих газов. Способ уменьшения выделений ртути в отработавшем газе включает образование осажденного соединения ртути на поверхности из значительной части общего количества ртути в отработавшем газе без использования химического катализатора, сублимацию осажденного соединения ртути обратно в отработавший газ в виде дихлорида ртути с поверхности без существенной продукции элементарной ртути и удаление сублимированного дихлорида ртути из отработавшего газа путем очистки. Указанная поверхность является поверхностью модификатора потока отработавшего газа, расположенного внутри этого потока, находящегося в контакте с отработавшими газами и имеющего большую площадь для осаждения на ней значительной части ртути, находящейся в этом потоке. Поверхность выполнена из металлического или керамического материала. Отработавшие газы имеют температуру 150-300°С. Предложено устройство для уменьшения выделений ртути в отработавшем газе, а также вытяжное устройство. Изобретение позволяет повысить эффективность очистки газов от соединений ртути. 5 н.п. и 22 з.п. ф-лы, 3 ил.
Реферат
Предпосылки создания изобретения
Область техники, к которой относится изобретение
Настоящее изобретение относится, в основном, к удалению нежелательных выделений в отработавших газах. Более конкретно настоящее изобретение относится к способу и устройству для уменьшения выделений ртути в отработавшем газе, где дихлорид ртути образуется на поверхности из значительной части ртути в отработавшем газе, где дихлорид ртути сублимируется с поверхности и где сублимированный дихлорид ртути удаляют из потока отработавшего газа.
Описание известного уровня техники
Принятые в 1990 году поправки к Закону о чистом воздухе отразили растущее беспокойство относительно антропогенных выделений ртути в атмосферу и затем в пищевую цепь. В результате в последние годы возросла научная активность относительно этой проблемы, особенно после решения Агентства по охране окружающей среды США регулировать выделения ртути на промышленных предприятиях к концу 2007 года.
В настоящее время не существует какого-либо эффективного способа контролирования этих выделений. Хотя было выдано значительное количество патентов, касающихся этой проблемы, как можно видеть, ни один из них не подтвердил свою достаточную эффективность. Практическое решение еще ищут при все возрастающем ощущении его необходимости.
В данное время природа химии ртути в охлаждающих отработавших газах, которые образуются в результате более высокотемпературных процессов, является плохо изученной. Однако естественные и антропогенные источники ее выделения хорошо известны. На протяжении промышленного века эти искусственные выделения аккумулировались в окружающей среде до такой степени, что они стали, к сожалению, основной частью того, что называют природным фоном.
Антропогенная ртуть выделяется, в основном, в виде пара элементарной ртути, которая является относительно химически инертной в газовой фазе выделений отработавших газов или в атмосфере. Это является, в значительной степени, причиной того, что ее трудно контролировать, так как абсорбенты не очень эффективны для удерживания паров элементарной ртути, которые являются чрезвычайно летучими.
В атмосфере время существования пара элементарной ртути составляет около года. Такова продолжительность времени до того, когда пар элементарной ртути будет окончательно вымыт из атмосферы. Следовательно, ее рассеяние является глобальным, с последующими международными и политическими последствиями.
Перечень основных источников выделения ртути представлен в недавнем отчете по Программе окружающей среды Организации Объединенных Наций (Chem. & Eng. News 81:(6) 20(2003)). Сжигание угля является самым большим источником, причем сжигание городских и медицинских отходов также играет основную роль. Сжигание нефти создает дополнительную часть, равную, примерно, 10 процентам (Wilhelm S.M., Environ. Prog. 18:130(1999), Environ. Sci. Technol. 35:4704 (2001)). Другими значительными источниками являются плавильные печи металла, производители цемента, хлорщелочной процесс, который использует электроды из ртути, и некоторые производства, связанные с добычей золота (Pirrone N. и соав. Atmos. Environ. 30:2981(1996), Pai P. и соав. Fuel Process. Technol. 65:101 (2000)).
Химия ртути является в некотором роде уникальной по сравнению с химией других химических элементов. Ртуть образует несколько прочно связанных молекул. В газообразной фазе большинство химических элементов легко превращаются в устойчивые газообразные оксиды, гидроксиды или галоиды. Ртуть, однако, имеет лишь очень слабо связанные газообразные оксиды, гидроксиды или моногалоиды. В результате в любой высокотемпературной среде ртуть, присутствующая в любом топливе, становится элементарной (атомарной) ртутью в горячих газах. Ее единственно устойчивыми газообразными молекулами из значительного количества при сгорании являются молекулы дихлорида (HgCl2). Является исключительным то, что энергия диссоциации прочности первой связи, D0(HgCl-Cl) составляет около 360 кДж/моль.
Однако дилемма состоит в том, что, хотя термодинамически наиболее благоприятно образование дихлорида ртути, образование его кинетически сдерживается при более низких температурах и, кроме того, он не может образовываться при более высоких температурах в газовой фазе. Не существует каких-либо прямых путей для преобразования атомарной ртути непосредственно в хлорид ртути в газовой фазе (Hranisavljevic J. и соав. J. Phys. Chem. A 101:2323 (1997), Ariya Р.А. и соав., там же 106:7310 (2002)).
В газовой фазе при образовании дихлорида ртути требуется продление процесса путем формирования промежуточных соединений, таких как газообразный оксид, гидроксид или монохлорид. Их нет в наличии, чтобы выполнять эту роль. Когда температуры снижаются в достаточной степени, чтобы эти соединения становились жизнеспособными, энергетические барьеры останавливают любые кинетические реакции в газовой фазе. Однако на практике можно видеть, что небольшая часть ртути, присутствующая в отработавших газах, присутствует, фактически, в виде дихлорида ртути.
После очень интенсивных исследований с моделированием кинетики химических реакций это частичное превращение остается загадкой. Исследователи склоны оценивать свои неудачи указанием на то, что химические подходы должны быть намного более комплексными (Laudel D.L. и соав., Fuel Process. Technol. 65:157 (2000), Niksa S. и соав. J. Air & Waste Manage. Assoc. 52:894 (2002)).
Исследования, выполненные в настоящее время и в прошлые годы, делали акцент на поиски того, какой компонент дымового газа влияет на такое видообразование части ртути между атомарной ртутью и дихлоридом ртути. Важный практический фактор состоит в том, что, в то время как элементарную ртуть очень трудно улавливать, дигалоидное соединение легко растворяется в воде. Его можно легко удалять вместе с газами, такими как двуокись серы, очистителями от водяного тумана в концевых, более холодных секциях отработавших газов.
Что неопровержимо в настоящее время, это то, что появляется летучая зола, играющая некоторую роль в изменении этого соотношения, которая обеспечивает, возможно, присутствие таких газов, как двуокись серы, окись азота, двуокись азота, хлор и хлористый водород (Laudel D.L. и соав., Fuel Process. Technol. 65:157 (2000), Liu К., Energy & Fuels, 15:1173 (2001), Niksa S. и соав., Environ. Sci. Technol. 35:3701 (2001), Fujiwara N. и соав., Fuel, 81:2045 (2002), Norton, G.A., Fuel, 82:107 (2003)). Скорость охлаждения отработавших газов также, по-видимому, является параметром, который оказывает некоторое влияние (Sliger R.N., Fuel Process. Technol. 65:423 (2000), Niksa S. и соав., Environ. Sci. Technol. 35:3701 (2001)). Данные очень противоречивы. Какой-либо определенной корреляции не существует и инженеры остаются в полном неведении относительно того, почему это видообразование изменяется, почему оно является непредсказуемым и как это происходит.
Существует несколько патентов и патентных заявок США, которые имеют отношение к контролированию выделений ртути в отработавших газах. Эти способы базируются, или на адсорбции, или на абсорбции атомарной ртути, или же на создании добавок к топочным газам. Ide и соав. (Патент США №4729882) и Caldwell и соав. (Патент США №6447740) предлагают добавлять хлор с последующей очисткой водной промывкой. Dangtran и соав. (Патент США №6375909) предлагают добавлять в топочную камеру хлорид кальция с последующей мокрой очисткой. Downs и соав. (опубликованная в США патентная заявка №20010043889) предлагают добавлять газ сульфид водорода, Holste (опубликованная в США патентная заявка №20020114750) предлагает добавлять различные формы серы, a Cole (опубликованная в США патентная заявка №20020114749) предлагает добавлять газообразные окисляющие агенты с последующей мокрой очисткой. Во всех других патентах используют различные абсорбирующие материалы для очистки и захвата элементарной (атомарной) ртути.
Никакой из вышеупомянутых способов не доказал свою достаточную эффективность. В попытке преодолеть недостатки известного уровня техники Институт электроэнергетических исследований (EPRI) в Palo Alto, CA проводит в настоящее время испытание способа дополнительной абсорбции. Этот способ использует пластины металла с золотым покрытием, подвешенные в топочных газах, которые предназначаются для абсорбции ртути путем амальгамирования. Указанный способ окажется, возможно, более успешным, чем предыдущие способы, но все же будет дорогим для оборудования, эксплуатации и содержания. Таким образом, все современные методологии и устройства для уменьшения выделений ртути в отработавших газах обладают неотъемлемыми недостатками, которые снижают, в целом, их эффективность и привлекательность.
В сущности, хотя в известном уровне техники признана, до ограниченного предела, необходимость снижения выделений ртути в отработавших газах, предлагаемые решения, на сегодняшний день, являются неэффективными в создании удовлетворительного средства для решения проблемы. Следовательно, желательно создание способа и устройства для уменьшения выделений ртути в отработавших газах, которое является эффективным и которое можно экономно установить, эксплуатировать и содержать.
Краткое описание изобретения
Хотя устройство и способ описаны или будут описаны с функциональными пояснениями, для грамматической плавности изложения следует отчетливо понять, что пункты Формулы изобретения, кроме того, что их специально формулировали согласно 35 USC 112, не должны восприниматься как обязательно ограниченные любым путем толкованием пределов "средств" или "стадий", а что они соответствуют всему объему значения и эквивалентов определения, предусмотренной Формулой изобретения согласно юридической системе эквивалентов, и в любом случае там, где пункты Формулы изобретения специально формулируют согласно 35 USC 112, они должны соответствовать полному объему предусмотренных законом эквивалентов согласно 35 USC 112. Изобретение можно лучше понять, если обратиться теперь к следующим чертежам, где на аналогичные элементы даны ссылки аналогичными номерами.
Настоящее изобретение имеет конкретную направленность, и оно устраняет вышеупомянутые недостатки, связанные с известным уровнем техники. Более конкретно настоящее изобретение включает способ и устройство для уменьшения выделений ртути в отработавшем газе, где образуется дихлорид ртути на поверхности из значительной части ртути в отработавшем газе, где дихлорид ртути сублимируется с поверхности и где сублимированный дихлорид ртути удаляют из потока отработавшего газа. Настоящее изобретение является как эффективным, так и экономичным.
Эти, а также другие преимущества настоящего изобретения будут очевидны из следующего описания и чертежей. Следует понимать, что в пределах объема Формулы изобретения в конкретной конструкции, которая показана и описана, могут быть сделаны изменения без отклонения от сути изобретения.
Краткое описание чертежей
Изобретение и различные варианты его осуществления можно будет теперь лучше понять, если обратиться к следующему подробному описанию предпочтительных вариантов, которые представлены в виде иллюстрированных примеров изобретения, определяемого в Формуле изобретения. Следует отчетливо понять, что изобретение, которое определяется Формулой изобретения, может оказаться более обширным, чем иллюстрируемые варианты, описанные ниже.
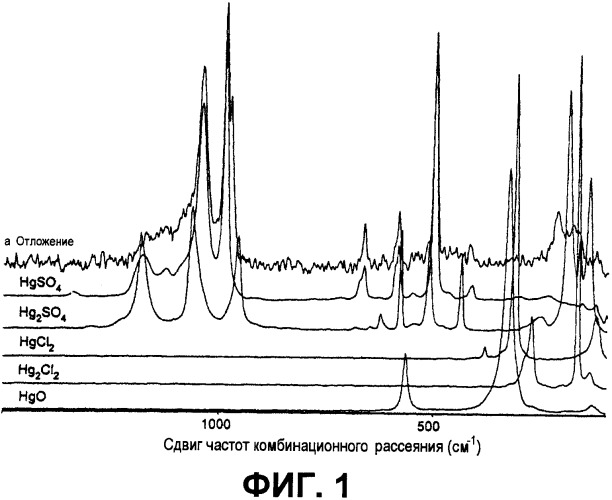
Фиг.1 представляет собой спектр комбинационного рассеяния с Фурье преобразованием покрытия, полученного газоплазменным осаждением, спектр (а), который сравнивают с аналогичными спектрами нескольких приобретенных образцов соединений чистой ртути;
На Фиг.2 иллюстрируют различные спектры типа 2-Theta, снятые на дифрактометре Брукера D8 для рентгеноструктурного анализа порошков; и
Фиг.3 представляет собой полусхематическую диаграмму, на которой показывают спойлер потока и очиститель, установленные внутри дымовой трубы для уменьшения в ней выделений ртути в отработанных газах, согласно настоящему изобретению.
Подробное описание предпочтительных вариантов осуществления изобретения
Специалисты в данной области могут сделать много изменений и модификаций без отклонения от сути и объема данного изобретения. Следовательно, должно быть понятно, что иллюстрируемый вариант осуществления изобретения представлен лишь в виде примера и его не следует рассматривать в качестве ограничения изобретения, которое определяется следующей Формулой изобретения. Например, несмотря на то что элементы пункта Формулы изобретения представлены ниже в определенной комбинации, следует четко понимать, что изобретение включает и другие комбинации из меньшего количества элементов, большего количества элементов или отличающихся элементов, которые раскрываются здесь даже, когда они первоначально не заявлены в такой комбинации.
Слова, используемые в этом подробном изложении для описания изобретения и его различных вариантов осуществления, следует понимать не только в смысле их общепринятых значений, но и как включающие, посредством специального определения в этой структуре изложения, информацию или действия, выходящие за пределы общепринятых значений. Таким образом, если понятие элемент можно рассматривать в контексте этого подробного изложения как включающее большее количество, чем одно значение, тогда его использование в пункте Формулы изобретения следует понимать как использование обобщенного значения для всех возможных значений, которые подкрепляются изложением и самим словом.
Следовательно, определения слов или элементов нижеследующей Формулы изобретения определяют в этом изложении для того, чтобы они включали не только комбинации элементов, которые описаны буквально, но и все эквивалентные структуры, информацию или действия для выполнения, в основном, той же функции, в основном, таким же способом, чтобы получить, в основном, такой же результат. В этом смысле предполагается, следовательно, что эквивалентные замены двух или большего количества элементов можно делать для любого одного из элементов в Формуле изобретения, приводимой ниже, или что единичный элемент можно заменять на два или большее количество элементов в пункте Формулы изобретения. Хотя элементы можно описывать здесь как функционирующие в определенных комбинациях или даже как первоначально заявленные в качестве таковых, следует четко понимать, что один или большее количество элементов из заявленной комбинации можно, в некоторых случаях, исключить из комбинации и что заявленную комбинацию можно переместить в разряд субкомбинации или в разряд вариации субкомбинации.
Несущественные изменения, касающиеся заявленного предмета изобретения, с точки зрения специалиста в данной области, известные в настоящее время или придуманные позже, рассматриваются, категорически, как находящиеся эквивалентно в пределах объема Формулы изобретения.
Следовательно, очевидные замены, известные в настоящее время или позже специалисту в данной области, определяются как находящиеся в пределах объема определенных элементов.
Таким образом, следует понимать, что Формула изобретения включает то, что конкретно иллюстрируют и описывают в ней, то, что является концептуально эквивалентным, то, что можно очевидно заменить, а также то, что, по существу, содержит в себе основную идею изобретения.
Соответственно, подробное описание, представленное ниже вместе с прилагаемыми чертежами, предназначается в качестве описания предпочтительных в настоящее время вариантов осуществления изобретения и не предназначается для представления только форм, в виде которых настоящее изобретение может быть создано или использовано. Описание характеризует функции и последовательность стадий для осуществления и действия изобретения в связи с иллюстрируемыми вариантами. Следует понимать, однако, что те же или эквивалентные функции могут выполняться с помощью различных вариантов, которые также рассматриваются в составе основной идеи изобретения.
Настоящее изобретение включает способ уменьшения выделений ртути в отработавшем газе, включающий устранение ограничений при образовании дихлорида ртути на поверхности из значительной части ртути в отработавшем газе, сублимацию дихлорида ртути с поверхности без существенной продукции элементарной ртути и удаление сублимированного дихлорида ртути из потока отработавшего газа.
Более конкретно способ уменьшения выделений ртути в отработавшем газе включает создание поверхности, которая находится в контакте с отработавшим газом, осаждение значительной части ртути из отработавшего газа на поверхность без химического катализатора, сублимацию осажденной ртути обратно в отработавший газ и очистку отработавшего газа от сублимированной ртути.
Отработавший газ может включать элементарную ртуть, соединения серы и форму хлора, такую как хлористый водород, атомарный или молекулярный хлор.
Поверхность включает предпочтительно спойлер для модификации потока, конфигурированный таким образом, чтобы максимизировать соударения газа с поверхностью. Поверхность включает предпочтительно спойлер для модификации потока, установленный на участке внутри потока отработавших газов, который увеличивает осаждение на ней ртути. Поверхность включает предпочтительно спойлер для модификации потока, установленный на участке внутри потока отработавших газов, где отработавшие газы имеют температуру приблизительно между 150 и 300°С, в зависимости от конкретного применения. Поверхность включает предпочтительно спойлер для модификации потока, установленный на участке внутри потока холодных отработавших газов и там, где поверхность или газы можно нагревать до температур приблизительно между 150°С и 300°С, в зависимости от конкретного применения.
Поверхность включает предпочтительно металл или керамический материал. Однако, как будет понятно специалистам в данной области, поверхность может включать альтернативно любой другой материал, на котором будет происходить образование ртути и/или соединения ртути, такого как дихлорид ртути, и с которой будет происходить в дальнейшем сублимация соединения ртути.
Согласно одному аспекту настоящего изобретения ртуть, которая осаждается на поверхности, образует стабильное соединение - оксид ртути, который в дальнейшем превращается в дихлорид ртути.
Согласно одному аспекту настоящего изобретения ртуть, которая осаждается на поверхности, образует стабильное соединение - сульфат ртути, который в дальнейшем превращается в дихлорид ртути. Дихлорид ртути затем сублимируется.
Необязательно к отработавшему газу добавляют двуокись серы перед тем, как отработавший газ будет контактировать с поверхностью, для того, чтобы увеличить образование сульфата ртути и, следовательно, дихлорида ртути на поверхности.
Необязательно к отработавшему газу добавляют атомарный хлор, молекулярный хлор или хлористый водород перед тем, как отработавший газ будет контактировать с поверхностью, для того, чтобы увеличить образование дихлорида ртути на поверхности.
Очистка включает предпочтительно водяную очистку, так как дихлорид ртути хорошо растворяется в воде. Однако, как будет понятно специалистам в данной области, дихлорид ртути можно удалять из потока отработавшего газа с помощью любого другого подходящего способа, например химической сухой очистки.
Согласно одному аспекту настоящее изобретение включает устройство для уменьшения выделений ртути в отработавшем газе, включающее поверхность, конфигурированную таким образом, чтобы она располагалась внутри потока отработавшего газа с тем, чтобы облегчить образование на ней соединения ртути. Устройство также конфигурируют таким образом, чтобы облегчить сублимацию с нее соединения ртути. Поверхность может иметь любую желаемую конфигурацию. Однако специалистам в данной области будет понятно, что поверхность предпочтительно устанавливает границы искривленного или изогнутого участка, который создает достаточную площадь поверхности для значительной части ртути в потоке отработавшего газа для образования на ней дихлорида ртути.
Поверхность также предпочтительно конфигурируют для облегчения осаждения на ней сульфата ртути. Таким образом, поверхность предпочтительно конфигурируют для облегчения осаждения на ней сульфата ртути и последующего превращения осажденного сульфата ртути в дихлорид ртути.
Поверхность предпочтительно дополнительно конфигурируют для облегчения осаждения на ней оксида ртути. Таким образом, поверхность предпочтительно дополнительно конфигурируют для облегчения осаждения на ней оксида ртути и последующего превращения осажденного оксида ртути в дихлорид ртути.
Границы поверхности устанавливаются предпочтительно, по крайней мере, частично спойлером потока (модификатором потока), сконструированным так, чтобы увеличить частоту соударений газа с поверхностью применительно к атомам ртути в потоке согласно хорошо известным принципам.
Настоящее изобретение необязательно дополнительно включает устройство для вдувания хлора и/или серы, которое конфигурируют таким образом, чтобы вдувать атомарный хлор, молекулярный хлор, хлористый водород или двуокись серы в отработавший газ перед тем, как газ будет контактировать с поверхностью.
Предпочтительно очиститель удаляет сублимированный дихлорид ртути из отработавшего газа. Предпочтительно водяной очиститель удаляет сублимированный дихлорид ртути из отработавшего газа. Однако специалистам в данной области будет понятно, что аналогичным образом пригодны и другие типы очистителей, и другие устройства для удаления сублимированного дихлорида ртути из отработавшего газа.
Согласно одному аспекту настоящее изобретение включает вытяжное устройство для уменьшения содержания ртути в отработавшем газе, где вытяжное устройство включает дымовую трубу и поверхность внутри дымовой трубы, конфигурированную таким образом, чтобы облегчить осаждение на ней дихлорида ртути. Поверхность также конфигурируют таким образом, чтобы облегчить сублимацию на ней дихлорида ртути. Очиститель или другое устройство конфигурируют таким образом, чтобы облегчить очистку отработавшего газа от сублимированной ртути.
Настоящее изобретение имеет конкретную направленность, и оно устраняет вышеупомянутые недостатки, связанные с известным уровнем техники. Настоящее изобретение базируется на химическом процессе, который имеет место в отработавших газах, и включает техническую модификацию технологической линии отработавших газов.
Известно, что в высокотемпературных системах любые следовые примеси ртути улетучиваются в газовую фазу. Это имеет место в случае сгорания угля, торфа, осадка сточных вод, нефти и газа. Это также имеет место в случае сжигания городских и медицинских отходов, при сухой перегонке горючего сланца, в результате функционирования крематориев и также относится к различным промышленным процессам, связанным с плавлением металла, цементным производствам и некоторым технологиям горных работ. В потоках отработавшего газа таких систем, хотя уровни их концентрации являются чрезвычайно низкими (миллиардные доли по объему), когда их сводят воедино в национальном или глобальном масштабе, такие выделения создают тяжелую проблему, связанную с окружающей средой.
Если, как обычно, следы хлора или хлористого водорода также присутствуют, эта газообразная ртуть, которая находится в своем элементарном (атомарном) состоянии, частично превращается в какой-то момент в газ дихлорида ртути. Эти два типа соединений, элементарная ртуть и ее дихлорид, являются в таких системах источником газообразной ртути.
Проблема, которая стоит перед современной технологией заключается в том, что, хотя дихлорид ртути является водорастворимым и его можно легко удалять из отработавших газов, не существует какого-либо удовлетворительного способа для удаления элементарной ртути, которая, в конечном счете, попадает в окружающую среду.
Кроме того, пропорция дихлорида ртути по отношению к элементарной ртути не изменяется логичным образом, что является непонятным и непредсказуемым и не поддается прямой корреляции с чем-либо в системе. Различные многосторонние анализы химии газовой фазы не имели успеха, несмотря на значительные усилия объяснить наблюдаемые данные с помощью моделей (Xu М. и соав. Combust. & Flame 132:208 (2003)). Кинетика газовой фазы подробно изучалась и поэтому эти модели не имели успеха не из-за недостатка данных.
По причине того, что химический процесс, связанный с ртутью, начинается в высокотемпературных газах и заканчивается в газовой фазе, его всегда считали газофазным явлением. Это могло бы показаться справедливым на первый взгляд, но, как установило настоящее открытие, это не является причиной. Все эти исследования являются полезными в том, чтобы показать, что главный процесс не является, фактически, однородным механизмом газовой фазы, но что в этой системе возникает что-то еще.
В недавней работе, проведенной в лаборатории заявителя, было изучено осаждение материала из газов пламени на поверхности. Изучение в деталях химического процесса осаждения сульфата натрия, который является причиной, вызывающей высокотемпературную коррозию в камерах сгорания, привело к значительному пониманию этого процесса (Steinberg и Schofield, Двадцать шестой симпозиум, посвященный проблемам горения (Twenty-Sixth Symposium on Combustion), The Combustion Institute, 1835 (1996), Combust. Flame, 129:453 (2002)).
В настоящее время достаточно хорошо известно, что были рекомендованы добавки, которые могут нарушить химический процесс и предотвратить образование сульфата (Schofield, патент США №632891111/ 2001, Energy & Fuels, 17:191 (2003)). В этом предыдущем процессе было обнаружено, что если в топливе или в воздухе присутствуют натрий и сера, даже при очень низких уровнях концентраций (ppmv, миллионные доли по объему), то сульфат натрия образуется очень эффективно не в самих газах пламени, а на охлажденной поверхности, пересекаемой сгоревшими газами.
Эти же самые технические приемы были применены для решения деталей вопроса, связанного с горением и химией горячего газа следов ртути. Газоплазменные потоки, создаваемые кислородобогащенным пропаном, сжигали в атмосфере, содержащей небольшую добавку водного аэрозоля из нитрата ртути или ацетата ртути, впрыскиваемую ультразвуковым распылителем. Эти добавки создавали концентрации ртути в диапазоне значений 5-30 ppmv в сгоревших газах.
Эксперименты проводили или только с добавкой ртути, или с аналогичными добавками с малым содержанием серы или хлора, или их комбинацией. Поверхности существующих в настоящее время различных металлических зондов для накопления отложений, которые используют при температурах в диапазоне 50-375°С, располагали по линии пересечения на выходе потока сгоревших газов. Отложения сразу же появлялись во всех случаях испытаний, и они никогда не оказывались элементарной ртутью, а были по своей природе молекулярной ртутью. С помощью методов спектроскопии комбинационного рассеяния с Фурье преобразованием, анализа дифракционного рассеяния рентгеновских лучей и ICP анализа спектрального излучения был установлен состав этих отложений и измерена скорость их образования.
Точное определение количества ртути в газах газоплазменного потока и ртути, накопленной на зонде, указывает на то, что газообразная элементарная ртуть осаждается очень эффективно. Фактически, измерения неожиданно показали, что скорости осаждения ртути являются, в основном, такими же, как для солей щелочных металлов в газоплазменном потоке. В исследованных газоплазменных потоках каждое взаимодействие с поверхностью удаляет значительную часть ртути в газовой фазе. Когда в системе присутствует сера, формируется гладкое отложение желтого или белого цвета.
Обратимся теперь к Фиг.1, на которой спектр комбинационного рассеяния с Фурье преобразованием покрытия, полученного газоплазменным осаждением, спектр (а), сравнивают с аналогичными спектрами нескольких приобретенных образцов соединений чистой ртути. Отложение накапливалось в течение 6 миллисекунд на выходе потока сгоревших газов смеси С3Н8/О2/N2 (0,9/5/16), сожженных в пламени на плоской пламенной горелке и содержащих 25 ppmv Hg, 75 ppmv SO2 и 50 ppmv Cl2 в несгоревших потоках газа. Цилиндрический металлический зонд охлаждали изнутри водой и поддерживали при температуре 60°С. Отложение собирали в течение двух часов, что указывает, таким образом, на значительную эффективность улавливания (30%). Отложение было однородным, гладким порошкообразным слоем и было желтого или белого цвета. Отложение является иллюстрацией образования, в основном, чистого сульфата ртути.
Таким образом, когда спектр комбинационного рассеяния с Фурье преобразованием этого отложения сравнивают со спектрами известных приобретенных образцов доступных соединений ртути, видно, что это отложение является чистым отложением сульфата ртути.
Обратимся теперь к Фиг.2, на которой иллюстрируют различные спектры типа 2-Theta, снятые на дифрактометре Брукера D8 для рентгеноструктурного анализа порошков. Спектр (а) является спектром отложения, которое накапливалось в течение около 6 миллисекунд на выходе потока сгоревших газов смеси C3H8/O2/N2 (0,9/5/16), сожженных в пламени и содержащих 25 ppmv Hg и 75 ppmv Cl2 в несгоревших потоках газа. Цилиндрический зонд охлаждали изнутри водой и поддерживали при температуре 60°С. Отложение собирали в течение двух часов, что указывает, таким образом, на значительную высокую эффективность улавливания. Отложение было однородным, гладким порошкообразным слоем и было коричневого цвета.
Спектр (b) является спектром отложения, которое накапливалось аналогичным образом, за исключением того, что в пламя добавляли только ртуть и зонд поддерживали при температуре 55°С. Отложение было аналогично по природе, но более темного коричневого цвета. Количество осажденного материала также было больше. Эти спектры сравнивали с соответствующими спектрами приобретенных образцов оксида ртути и дихлорида ртути. Все образцы подвергали анализу при идентичных условиях. Иллюстрируется образование оксида ртути в обоих случаях. При отсутствии серы образование таких коричневых отложений оксида ртути всегда очевидно.
Спектр (а) указывает также на присутствие небольшого количества дихлорида ртути в образце, что подтверждает образование его на поверхности. Линии платины, присутствующие в спектре, являются результатом рассеяния из платинового субстрата полоски, на которой лежат образцы.
Очевидно, как в случае щелочного отложения, что для образования ртути доступен значительный гетерогенный механизм. Аналогично, как можно видеть в предыдущей программе, элемент металла, в этом случае ртути, никогда не теряет способности продуцировать молекулярное соединение. При достижении поверхности, однако, она имеет предпочтительную упорядоченность для того соединения, которое будет формироваться. Если в газах присутствует сера, она будет формировать сульфат ртути. Если нет, она будет продуцировать оксид ртути. Она не может откладываться и оставаться на поверхности в своем элементарном состоянии.
Важность поверхности является первостепенной. Во-первых, она уменьшает размерность химической системы. Частицы, которые могут даже не соударяться друг с другом в трехмерной газовой фазе, имеют теперь намного более увеличившуюся возможность находить друг друга на двухмерной поверхности. Более важно, как в настоящем случае, что она изменяет химический процесс от газообразной до конденсированной фазы.
Твердофазная химия ртути также более ограничена, чем у большинства химических элементов. Ртуть, однако, обладает двумя валентностями, ртуть одновалентная (1) и ртуть двухвалентная (2), и полностью отличается от газовой фазы. Ниже приведена характеристика твердых фаз.
Hg
Очень летучая жидкость. Температура кипения 357°С. Давление пара 1 Торр (133,322 Па) (125°С), 7.5 Торр (999,915 Па) (175°С), 75 Торр (9999,15 Па) (250°С). 760 Торр (101324,72 Па) соответствуют атмосферному давлению. В отработавших газах, следы ртути (ppbv) означают, что температурные условия всегда будут выше температуры конденсации. Следовательно, конденсация пара ртути на теплую поверхность не может произойти без чрезвычайно быстрого ее химического превращения и связывания в молекулярную форму на поверхности.
HgO
Соединение диссоциирует очень быстро при температуре плавления около 500°С. Современные термогравиметрические измерения показывают, что небольшие количества ее имеют тепловой период полураспада около 15 часов при 375°С, 8 часов при 400°С, 2 часа при 425°С и менее одного часа при 450°С. Эти значения следует рассматривать как приблизительные, так как они не являются в точности зависимостями нулевого порядка, а зависят до некоторой степени от размера и природы образца.
Hg2Cl2
Соединение сублимируется и диссоциирует в Hg+HgCl2 при 382°С. Температура плавления 277°С, температура кипения 304°С. Соединение устойчивое, очень летучее, испаряется не изменившимся, давление пара 10 Торр (1333,22 Па) (180°С), 50 Торр (6666,10 Па) (230°С) (Bernard и соав., J. Phys. III France 7:311 (1997)). Современные измерения показали, что образец испаряется в течение около часа или меньше при температуре 150°С, в течение около 20 минут при температуре 175°С и в течение нескольких минут или меньше при температуре 200°С в относительно спокойной атмосфере.
Hg2SO4
Соединение устойчивое до температуры около 335°С, когда оно распадается до HgSO4.
HgSO4
Соединение устойчивое до температуры около 475°С (период полураспада около 30 часов), когда оно начинает диссоциировать до элементарной ртути. Его тепловая устойчивость в период полураспада составляет около 15 часов при 525°С, 6 часов при 550°С, 2 часа при 575°С и около 30 минут при 600°С.
HgS
Киноварь представляет собой минеральную руду, находимую в естественных условиях. Она имеет температуру плавления 584°С, но не является устойчивой в условиях горячей атмосферы, распадаясь до Hg+SO2.
Hg2СО3
Соединение не устойчивое, диссоциирует при 130°С.
Hg2(NO3)2
Соединение разлагается при 70-100°С (можно приобретать лишь в качестве дигидрата).
Hg(NO3)2
Температура плавления 79°С, соединение разлагается на свету и не считается термически очень устойчивым (можно приобретать лишь в качестве моногидратной соли, является очень гигроскопичной).
Гидрид ртути неизвестен, но ацетат, оксалат и цианид можно приобретать.
Ссылка на любое классическое учебное руководство по неорганической химии показывает, что сульфат ртути и оксид ртути вступают очень легко в реакцию или с хлористым водородом, или с молекулярным хлором, образуя дихлорид ртути (Mellor J.W., А Comprehensive Treatise on Inorganic and Theoretical Chemistry, том 4, John Wiley (1960)). Дихлорид ртути называют коррозионным сублиматом из-за его высокой летучести.
Следовательно, то, что происходит в отработавших газах не является таким сложным, как думали раньше. Когда горячие газы охлаждаются, ртуть в конечном счете становится способной взаимодействовать с серой или кислородом на любой поверхности, с которой она соприкасается. Это может быть даже частица летучей золы или это могут быть только трубы, устанавливающие границы для потока газа. Как можно видеть выше в характеристиках различных молекул ртути, стоит только увеличить температуру и то, что могло бы образоваться, будет немедленно диссоциировать обратно с любой поверхности в движущиеся газы в виде элементарной ртути.
Следовательно, в зависимости от конкретной системы и окружающих условий потока газа, нет оснований ожидать, что до тех пор, пока температура не упадет ниже, чем около 600°С (в системах, содержащих серу), и ниже, чем около 450°С (в системах, не содержащих серу), может возникнуть отложение ртути с некоторым средним временем жизни. В случае сульфатных отложений ртути эксперименты указывают на то, что в отработавших газах хлористый водород, а не молекулярный хлор, энергично вступает в реакцию и превращает отложение в дихлорид ртути на поверхности.
Удачно то, что твердый дихлорид ртути является очень летучим, что он плавится при 277°С и кипит при 304°С. Как показано выше, согласно последним из