Циклоалкильные производные 3-гидрокси-4-пиридинонов
Иллюстрации
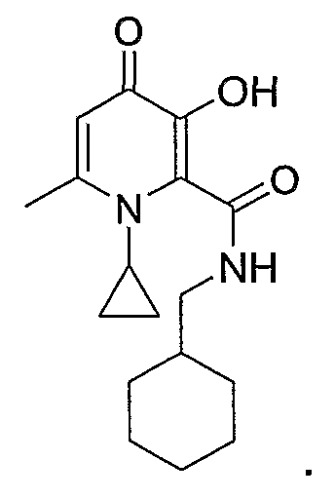
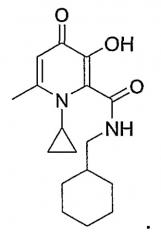
Показать всеНастоящее изобретение относится к циклоалкильному производному 3-гидрокси-4-пиридинона общей формулы
,
где R1 является X при условии, что R2 является Y; или R1 является Т при условии, что R2 является W; или R1 является X при условии, что R2R5N, вместе взятые, образуют гетероциклическое кольцо, выбранное из морфолинила или пиперазинила, где морфолинильная или пиперазинильная группа является либо незамещенной, либо замещенной одной-тремя С1-С6алкильными группами; X является С3-С6циклоалкилом; Y выбирают из группы, состоящей из С3-С6циклоалкила, С1-С6алкила и С1-С6алкила, монозамещенного С3-С6циклоалкилом; Т означает С1-С6 алкил; W означает С3-С6циклоалкил; R3 означает водород; R4 выбирают из группы, состоящей из водорода и С1-С6алкила и; R5 выбирают из группы, состоящей из водорода и С1-С6алкила, и к его способу получения. Также изобретение относится к фармацевтической композиции на основе этих соединений и применению этих соединений в производстве лекарственного препарата. Технический результат: получены новые соединения, которые могут применяться для удаления избытка железа из организма больных с заболеваниями, связанными с перенасыщением железом. 5 н. и 12 з.п. ф-лы, 8 табл., 9 ил.
Реферат
Изобретение относится к новым 3-гидрокси-4-пиридиноновым производным и к их применению в образовании хелатных комплексов с ионами железа (III). Точнее, изобретение относится к циклоалкильным производным 3-гидрокси-4-пиридинона.
3-Гидрокси-4-пиридиноны являются бидентатными лигандами, которые образуют хелатный комплекс с ионом Fe(III) в отношении 3:1, и используются для удаления избытка железа из организма человека. Перенасыщение железом может возникать вследствие избыточного потребления железа с пищей, наследственных генетических состояний, таких как гемохроматоз и регулярное переливание крови. Такие переливания применяют для лечения медицинских состояний, таких как талассемия, серповидно-клеточная анемия, идиопатический гемохроматоз и апластическая анемия. Повышенное всасывание железа при трансфузии приводит к перенасыщению железом. При достижении насыщения в организме ферритином и трансферрином, железо откладывается во многих тканях, таких как миокард, печень и эндокринные органы, приводя к токсическим эффектам.
Исследования в области образования хелатных комплексов железа и применимость хелатообразующих соединений были описаны в обзоре (Current Medicinal Chemistry, 2003, 10, 983-985, Tim F. Tam, et al.). Хелатирующие железо соединения могут быть использованы для предотвращения образования окси-радикалов, лечения опухолей, малярии, пост-ишемической реперфузии и нейродегенеративных заболеваний. Соединения, образующие комплексы с железом, такие как десфералТМ (мезилат десферриоксамина) и феррипроксТМ (деферипрон), используют для удаления избытка железа из организма больного с талассемией, поскольку организм человека не располагает эффективными средствами, способствующими выведению железа, накопленного в процессе переливания крови. Десферриоксамин вводят ежедневно путем подкожной инфузии в течение 8-12 часов. В настоящее время деферипрон (1,2-диметил-3-гидрокси-4-пиридинон) является единственным перорально доступным лекарственным средством. Данное средство подвергается метаболизму в печени, и более 85% введенной дозы обнаруживается в моче в виде нехелатообразующего О-глюкуронида (Drug Metab. Dispo. 1992, 20(2), 256-261, S.Singh, et al.). Относительно высокая пероральная доза 75 мг/кг (3,5-4 г в день) требуется для лечения состояний, связанных с перенасыщением железом. Поэтому существует необходимость в создании нового активного гидроксипиридинона для перорального введения с улучшенными по сравнению с деферипроном фармакологическими характеристиками.
Voest et al. (Annals of Internal Medicine 1994, 120, 490-499) суммировал клинический опыт по испытанию соединений, образующих хелатные комплексы с железом, при состояниях, не связанных с перенасыщением железом. Соединения, образующие хелатные комплексы с железом, использовали для достижения антиоксидантных эффектов, антипролиферативных эффектов, противопротозойных эффектов и для хелатирования алюминия, и могут быть использованы для лечения ряда болезненных состояний, например, для лечения ревматоидного артрита, для защиты от кардиотоксических эффектов, вызываемых антрациклиновыми соединениями, для ограничения повреждения миокарда вследствие ишемии-реперфузии, в качестве протипоопухолевых средств и для лечения малярии. Кроме того, исследователь van Asbeck B.S. et al. (J. Clin. Virol. 2001 Feb; 20(3): 141-7) сообщил о том, что соединения, образующие хелатные комплексы с железом, обладают активностями против ВИЧ-инфекции. Следовательно, применение соединений, образующих хелатные комплексы с железом, не ограничивается только лечением состояний, вызванных перенасыщением железом.
Члены класса 3-гидрокси-4-пиридинонов являются известными из-за их способности образовывать хелатные комплексы с железом. Предыдущий уровень техники включает патенты RE 35948, США 6448273, США 6335353 и США 5480894. В патенте США 6335353 эфирные пролекарственные производные 3-гидрокси-4-пиридинонов использовали для усиления выведения железа из печени, однако ни одно из разработанных соединений не получило оценки для человека.
В других подходах выбранные новые соединения были разработаны с целью блокировки фазы II метаболизма деферипрона, т.е. О-глюкуронидации у кислорода, расположенного у С3-атома остова деферипрона. В патенте США 5688815 описаны 1-алкил-3-гидрокси-4-пиридиноны с С2-метильной группой, замещенной фенильным или гетероильным кольцом и гидроксигруппой, и заместителем у N1, которым является низший алкил. В патенте США 6335353 описан 1-алкил-3-гидрокси-4-пиридинон с С2-алкилкарбомоилом, арилкарбамоилом или аралкилкарбамоильной группой, где N1-заместителем является алифатическая углеводородная группа. Использование С2-метилкарбамоильной функциональности в соединении, таком как СР502 (1,6-диметил-3-гидрокси-4(1Н)пиридинон-2-карбокси-(N-метил)амида хлоргидрат; патент США 6335353), приводит к эффективной блокировке О-глюкуронидирования у С3-кислорода. Другие аналоги, описанные в патенте США 6335353, включают в себя СР506 (1,6-диметил-3-гидрокси-4(1Н)пиридинон-2-карбокси-(N-изопропил)амида хлоргидрат), С2-изопропилкарбомоильный аналог и СР508 (1,6-диметил-3-гидрокси-4(1Н)пиридинон-2-карбокси-(N,N-диметил)амида хлоргидрат), диметилкарбамоильный аналог. СР502, СР506 и СР508 являются соединениями, разработанными в уровне техники, и они не получили оценки для человека.
Сущность изобретения
Первый аспект настоящего изобретения относится к производному 3-гидроксипиридин-4-она формулы I и его фармацевтически приемлемой соли,
где:
R1 является X при условии, что R2 является Y;
или
R1 является T при условии, что R2 является W;
или
R1 является X при условии, что R2R5N, вместе взятые, образуют гетероциклическое кольцо, выбранное из пиперидинила, морфолинила, пирролидинила или пиперазинила, где пиперидинильная, морфолинильная, пирролидинильная или пиперазинильная группа является либо незамещенной, либо замещенной одной-тремя С1-С6 алкильными группами;
Х является С3-С6 циклоалкилом;
Y выбирают из группы, состоящей из С3-С6 циклоалкила, С1-С6 алкила и С1-С6 алкила, монозамещенного С3-С6 циклоалкилом;
Т означает С1-С6 алкил;
W означает С3-С6 циклоалкил;
R3 выбирают из группы, состоящей из водорода и С1-С6 алкила;
R4 выбирают из группы, состоящей из водорода и С1-С6 алкила и
R5 выбирают из группы, состоящей из водорода и С1-С6 алкила.
Второй аспект настоящего изобретения относится к применению соединения формулы I в лечении заболевания, связанного с перенасыщением железом.
Третий аспект изобретения относится к фармацевтической композиции, содержащей соединение формулы I.
Одним предпочтительным классом соединений согласно данному изобретению является соединение формулы I, где R1 является X при условии, что R2 является Y, Х является С3-С6 циклоалкилом; Y является С1-С6 алкилом; R3 является водородом; R4 является С1-С6 алкилом и R5 является водородом.
Еще более предпочтительным соединением в этой подгруппе является соединение формулы I, где R4 является метилом, X означает циклопропил и Y означает метил, причем соединение является метиламидом 1-циклопропил-3-гидрокси-6-метил-4-оксо-1,4-дигидропиридин-2-карбоновой кислоты.
Второй предпочтительный класс соединений согласно данному изобретению представлен соединением формулы I, где R1 является X при условии, что R2 является Y, Х является С3-С6 циклоалкилом, Y является С3-С6 циклоалкилом, R3 является водородом, R4 является С1-С6 алкилом и R5 является водородом.
Предпочтительным соединением в данной подгруппе является соединение, где R4 является метилом, X=Y=циклопропил, причем соединением является циклопропиламид 1-циклопропил-3-гидрокси-6-метил-4-оксо-1,4-дигидропиридин-2-карбоновой кислоты.
Третий предпочтительный класс соединений формулы I представлен соединением, где R1 является T при условии, что R2 является W; T означает С1-С6 алкил; W означает С3-С6 циклоалкил, R3 является водородом, R4 является С1-С6 алкилом и R5 является водородом.
Более предпочтительным соединением в данной подгруппе является соединение, где R4 является метилом, T означает метил и W означает циклопропил, причем соединением является циклопропиламид 3-гидрокси-1,6-диметил-4-оксо-1,4-дигидропиридин-2-карбоновой кислоты.
Четвертый предпочтительный класс соединений согласно настоящему изобретению представлен соединением формулы I, где R1 является X при условии, что R2 является Y, X означает С3-С6 циклоалкил; Y означает С1-С6 алкил; R3 является водородом; R4 означает С1-С6 алкил, R5 является метилом.
Еще более предпочтительным соединением в данной подгруппе является соединение формулы I, где R4 является метилом, X является циклопропилом и Y означает метил, и соединением является 1-циклопропил-3-гидрокси-N,N,6-триметил-4-оксо-1,4-дигидропиридин-2-карбоксамид.
Наиболее предпочтительными соединениями согласно данному изобретению являются соединение IA, соединение формулы I, где R3=H, R4=метил, при условии, что R1=X=циклопропил, R2=Y и Y выбирают из группы С3-С6 циклоалкила; С1-С6 алкила; С1-С6 алкила, монозамещенного С3-С6 циклоалкилом; или R1=X=циклопропил, R2R5N, вместе взятые, образуют гетероциклическое кольцо, выбранное из пиперидинила, морфолинила, пирролидинила или пиперазинила, где пиперидинильная, морфолинильная, пирролидинильная или пиперазинильная группа является либо незамещенной, либо замещенной одной-тремя С1-С6 алкильными группами.
Таким образом, настоящее изобретение относится к циклоалкильному производному 3-гидрокси-4-пиридинона, обладающему улучшенными свойствами по сравнению с соединениями известного уровня техники. Циклоалкильная группа присоединена к N1-атому и/или к атому N С2-амидо группы. До настоящей заявки, соединения с N1-циклоалкильным заместителем или N-циклоалкильным заместителем С2-амидогруппы не были описаны в литературе. Указанные соединения не являются пролекарствами и обладают превосходной избирательностью по отношению к металлу. Они не образуют комплексы с существенными металлами, такими как кальций и магний при рН 7,4 в химических анализах. Величина D7,4 находится в области, установленной для лекарственного средства деферипрона, и соединение является перорально активным в модели крысы с перенасыщением железом. Данные соединения разработаны с подходящими величинами рК фенольной ОН-группы у атома С3 в области от 8,3 до 8,8, величиной pFe3+ выше 20, легко образуют хелатный комплекс с железом при соотношении 1:3, как установлено с помощью графика согласно Job, и имеют величину D7,4>0,1. Исследование монокристаллической структуры хелатного комплекса Fe(III) подтверждает, что соединение формулы I является бидентатным лигандом.
Краткое описание чертежей
На фиг.1 представлен график согласно Job для соединения Аро6622 (циклопропиламид 1-циклопропил-3-гидрокси-6-метил-4-оксо-1,4-дигидропиридин-2-карбоновой кислоты), соединения формулы I.
На фиг.2 представлен график согласно Job для соединения Аро6617 (циклопропиламид 1,6-диметил-3-гидрокси-4-оксо-1,4-дигидропиридин-2-карбоновой кислоты), соединения формулы I.
На фиг.3 представлен график согласно Job для соединения Аро6619 (метиламид 1-циклопропил-3-гидрокси-6-метил-4-оксо-1,4-дигидропиридин-2-карбоновой кислоты), соединения формулы I.
На фиг.4 представлено графическое изображение образования комплекса Fe3+-Аро6619.
На фиг.5 представлено графическое изображение образования комплекса Fe3+-Аро6617.
Фиг.6: Эффективность Аро6619 и Аро6617, способствующих выведению железа с мочой в модели крысы с перенасыщением железом (n=6).
Фиг.7: Монокристаллическая структура хелатного комплекса Fe(Apo6617)3.
Фиг.8: Монокристаллическая структура хелатного комплекса Fe(Apo6619)3.
Фиг.9: Картины циклической вольтамперометрии системы Fe-Apo6619 при рН 7,4.
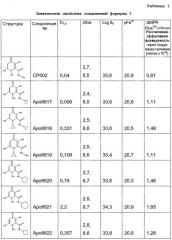
Таблица 1: Химические свойства соединения формулы I.
Таблица 2: Селективность связывания Аро6619 с металлом.
Таблица 3: Эффективность соединений Аро6619 и Аро6617, способствующих выведению железа с фекалиями в модели крысы с перенасыщением железом (n=6). Величины выражены в виде мкг/день/кг.
Таблица 4: Эффективность соединений Аро6619 и Аро6617, способствующих выведению железа с мочой и фекалиями в модели крысы с перенасыщением железом (n=6/группу). Величины выражены в виде мкг/день/кг. Величины выделения с фекалиями даны за 3 дня после введения хелатного соединения и сравнены с базовыми величинами, определенными за 3 дня до введения хелатного соединения. Величины представлены как средние ± 1SD.
Таблица 5: Данные кристаллографии и уточнение структуры Fe(Apo6617)3.
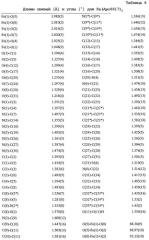
Таблица 6: Длины связей [Å] и углы [°] для Fe(Apo6617)3.
Таблица 7: Данные кристаллографии и уточнение структуры Fe(Apo6619)3.
Таблица 8: Длины связей [Å] и углы [°] для Fe(Apo6617)3.
Подробное описание изобретения
Употребляемые в тексте термины:
Алкил означает разветвленную или неразветвленную насыщенную углеводородную цепь, содержащую, если не указано особо, от одного до шести атомов углерода, включающий, но не ограничивающийся метилом, этилом, пропилом, изопропилом, н-пропилом, бутилом, втор-бутилом, изобутилом, н-пентилом, гексилом.
Термин "циклоалкил", употребляемый в тексте отдельно или как часть другой группы, включает в себя насыщенные циклические углеводородные группы, содержащие 1 кольцо, включающее моноциклический алкил, содержащий от 3 до 6 углеродов, образующих кольцо, который включает в себя циклопропил, циклобутил, циклопентил и циклогексил.
Фармацевтически приемлемые нетоксичные соли относятся к фармацевтически приемлемым солям соединений согласно настоящему изобретению, которые сохраняют биологическую активность родительских соединений и не являются биологически или в других отношениях неподходящими (например, соли являются устойчивыми). Соли двух типов могут быть образованы из соединений согласно настоящему изобретению: (1) соли неорганических и органических оснований соединений формулы I, имеющие фенольную функциональную группу, и (2) аддитивные соли кислоты могут быть образованы у аминной функциональной группы соединений формулы I согласно данному изобретению.
Фармацевтически приемлемые соли неорганических оснований включают натриевые, калиевые, литиевые, аммониевые, кальциевые и магниевые соли. Особенно предпочтительными являются натриевые, кальциевые и магниевые соли. Фармацевтически приемлемые нетоксичные соли органических оснований включают соли первичных, вторичных и третичных аминов, замещенных аминов, включающих природные, замещенные амины, циклические амины и основные ионообменные смолы. Примерами таких солей являются 2-амино-2-гидроксиметилпропан 1,3-диол, изопропиламин, трометамин, глюкозамин, метилглюкамин, пурины, пиперазин, пиперидин, N-этилпиперидин, полиаминные смолы и тому подобное.
Фармацевтически приемлемые аддитивные соли кислоты образуются с неорганическими и органическими кислотами, такими как галоидводородная кислота, серная кислота, азотная кислота, фосфорная кислота, метансульфокислота и этансульфокислота.
Соединениями согласно данному изобретению являются 2-амидопроизводные 4-оксо-1,4-дигидропиридин-2-карбоксамидных производных, имеющих общую структуру:
Большая часть соединений названа как производное 4-оксо-1,4-дигидропиридин-2-карбоксамида, например:
1-циклопропил-N-гексил-3-гидрокси-6-метил-4-оксо-1,4-дигидропиридин-2-карбоксамид:
N-циклогексил-1-циклопропил-3-гидрокси-6-метил-4-оксо-1,4-дигидропиридин-2-карбоксамид:
N-(циклогексилметил)-1-циклопропил-3-гидрокси-6-метил-4-оксо-1,4-дигидроксипиридин-2-карбоксамид:
В некоторых случаях соединения названы с включением в название "пиридин-4(1Н)-он" в качестве основного скелета. Примерами являются:
1-циклопропил-3-гидрокси-6-метил-2-(морфолин-4-илкарбонил)пиридин-4-(1Н)-он:
1-циклопропил-3-гидрокси-6-метил-2-[(4-метилпиперазин-1-ил)карбонил]пиридин-4(1Н)-он:
Термин "животные" относится к человеку, а также к другим видам животных, в частности к млекопитающим (например, собаки, кошки, лошади, крупный рогатый скот, свиньи и т.д.), рептилиям, рыбам, насекомым и глистам.
Соединения согласно данному изобретению разработаны с целью улучшения свойств известных аналогов деферипрона. Одним критерием, применяемым для логического обоснования разработки перорально активных хелатных соединений в серии 3-гидрокси-4-пиридинонов, являются соединения, имеющие величины pFe3+ выше, чем у деферипрона (pFe3+=19,7). Используемое в тексте определение pFe3+ представляет собой концентрацию иона железа в растворе, когда общее количество железа равно 10-6 М, и концентрация лиганда составляет 10-5 М, и рН составляет 7,4. Ее рассчитывают, используя экспериментально определенную величину рКа и константы образования комплекса с металлом с помощью программы Hyperquad (Version 2.1, Peter Gans, University of Leeds). Снижение величины рКа фенольной ОН-группы у атома С3 до менее чем 8,8 свидетельствует о том, что более высокая величина pFe3+ достигается при комбинировании с соединениями с подходящей константой комплексообразования β3. Концепция комплексообразования обсуждается подробно ниже.
Ступенчатыми и общими константами комплексообразования для бидентатного лиганда, такого как 3-гидрокси-4-пиридинон, являются следующие:
| Fe(III) + лиганд → Fe[лиганд]1 | K1 |
| Fe[лиганд]1 + лиганд → Fe[лиганд]2 | K2 |
| Fe[лиганд]2 + лиганд → Fe[лиганд]3 | K3 |
Константа комплексообразования β3 = K1·K2·K3
Хелатирующее железо лекарственное средство деферипрон (1,2-диметил-3-гидрокси-4-пиридинон) образует хелатный комплекс с железом с константами комплексообразования (log β3) 36,3 и pFe3+ 19,7. Величины рК деферипрона составляют 3,56 и 9,64. Большая часть соединений согласно настоящему изобретению имеет подобные константы комплексообразования (log β3) в области от 34 до 36, величину pFe3+>20 и подходящие величины рКа фенола от 8,3 до 8,8. Следовательно, соединения согласно данному изобретению являются превосходными хелатирующими агентами Fe(III). Величина эффективной проницаемости [Рэфф] через тощую кишку человека соединений согласно данному изобретению теоретически рассчитана, исходя из вычислительных расчетов с помощью программы QMPRPlusTM (из Simulationplus Inc.). Большая часть соединений согласно настоящему изобретению имеет рассчитанную величину Рэфф в области 1±0,3 (см/с × 10-4), что позволяет предположить, что соединения имеют хорошую проницаемость через тощую кишку человека. Химические свойства представленных соединений формулы I перечислены в таблице 1.
Соединения формулы I с циклоалкильными группами у R1 и/или R2 являются комплексонами металла с высокими величинами pFe3+. ВеличиныD7,4 соединений формулы I подобны деферипрону, и последующие исследования на модели крыс с перенасыщением железом показали, что соединения формулы I оказывают эффективное действие в удалении железа in vivo. Подробности исследования эффективности соединений у животных описаны в примерах ниже.
Соединения формулы I не связывают существенные металлы, такие как марганец, кальций и магний. Величины рМ и константы комплексообразования типичного примера соединения формулы I представлены в таблице 2 (и обсуждены подробно в примере 11). Соединение преимущественно связывается с Fe3+ по сравнению с другими двухвалентными и трехвалентными металлами, такими как Cu, Zn и Al.
Соединения формулы I являются новыми циклоалкильными производными 3-гидрокси-4-пиридинонов. Они имеют величины pFe3+ выше 20, подходящие величины D7,4, сравнимые с деферипроном, предпочтение относительно образования хелатного комплекса Fe3+ и фрагмента С2-алкилкарбамоила или С2-циклоалкилкарбамоила, который предназначен блокировать фазу II метаболизма 3-ОН-группы.
Кроме вышесказанного, соединения формулы I связывают Fe3+ в отношении 1:3 при физиологических условиях при рН 7,4. Анализ графика согласно Job подтверждает соотношение 1:3 комплексона к железу (фиг.(1-3) и пример 9).
Графики образования Fe-комплекса в отношении различных значений рН могут быть представлены путем использования программы Hyperquad Stimulation and Speciation (HYSS2 © 2000 Protonic Software) с включением экспериментальных величин рКа (пример 10 и 11) и констант комплексообразования K1, K2 и K3 (пример 14). Фигуры 4 и 5 иллюстрируют график образования комплексов металла с соединениями формулы I при различных значениях рН. В обоих исследованиях типичные примеры соединений формулы I исключительно образуют хелаты FeL3 при рН выше 7,0 (где L является бидентатным лигандом), таким образом, подтверждая отсутствие видов FeL2 + или FeL2+ при физиологическом значении рН. Отсутствие указанных видов свидетельствует о том, что не существует незащищенного железа in vivo при физиологическом значении рН 7,4.
Соединения формулы I, где R1 означает X при условии, что R2 означает Y; или R1 означает T при условии, что R2 является W, получают способом, отраженным на схеме 1.
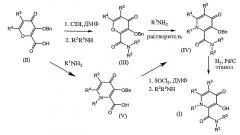
Схема 1
Кислота (II) взаимодействует с 1,1'-карбонилдиимидазолом в инертном растворителе в течение от 2 до 5 часов, предпочтительно 5 часов в инертном растворителе при температурах от 30 до 70°С. После добавления амина R2R5NH, соединение (III) выделяют обычными способами. Раствор соединения (III) и амина R1NH2 в инертном растворителе, таком как спирт, нагревают при температуре от 50 до 80°С, чтобы осуществить введение амина (III) в течение от 3 до 48 часов с получением соединения (IV). Альтернативный способ получения соединения (IV) заключается во взаимодействии соединения формулы (II) с амином R1NH2 в инертном растворителе с получением кислоты формулы (V). Затем соединение (V) подвергают взаимодействию с тионилхлоридом и диметилформамидом с получением соединения формулы (IV). Соединения выделяют традиционными способами, например, колоночной хроматографией и кристаллизацией. Гидрирование соединения (IV) в спирте над катализатором гидрирования приводит к соединению (I), которое выделяют обычными средствами. Предпочтительным катализатором гидрирования является палладий-на-угле или гидроокись палладия-на-угле и Ni Ренея. Получение исходного материала кислоты (II) сообщено в патенте США 6426418. Общая процедура получения кислоты формулы (V) может быть найдена в патенте Канады СА 2379370.
Соединения формулы (I) проверяли на крысах с перенасыщением железом. Данные экскреции железа с фекалиями и экскреции железа с мочой для типичных примеров соединений Аро6617 и Аро6619 приведены в таблицах 3 и 4 и фиг.6 соответственно. Оба соединения проявили значительную экскрецию железа с фекалиями по сравнению с контролем при пероральной дозе 113 и 450 мкмоль/кг. Кроме того, Аро6619 и Аро6617 способствуют экскреции железа с мочой в значительно большей степени, чем деферипрон при дозе 450 мкмоль/кг. Оба соединения рассматривают как более эффективные, чем деферипрон, в мобилизации железа у крыс с перенасыщением железом.
Хелатные комплексы железа и соединений формулы I были синтезированы и выделены (пример 16). Монокристаллические структуры Fe(Apo6617)3 и Fe(Apo6619)3 определенно подтверждают, что указанные бидентатные соединения взаимодействуют с Fe(III) с получением трисбидентатного хелатного комплекса 1:3 (таблицы от 5 до 8, фиг.7-8).
Другой критерий в разработке соединений формулы (I) касается регулирования окислительно-восстановительного потенциала системы Fe-комплексон при рН 7,4 до отрицательной величины ниже -320 мВ (против NHE), чтобы предотвратить какие-либо реакции с формами кислорода. Железо существует во множественных состояниях, включающих Fe2+ и Fe3+. Пара железо(II)/железо(III) может действовать в качестве пары восстановителя и окислителя. Согласно Crumbliss (http://www.medicine.uiowa.edu/FRRB/VirtualSchool/Crumbliss-Fe.pdf) и Pierre (BioMetals, 12, 195-199, 1999) избирательное хелатирование железа путем регулирования окислительно-восстановительного потенциала является способом предотвращения участия железа в каталитическом цикле, в результате которого образуются токсические гидроксильные радикалы и/или реактивные формы кислорода (ROS) (например, посредством реакции Fenton или цикла Haber Weiss). Fe(III)-трисхелатная система с окислительно-восстановительным потенциалом ниже -320 мВ (против NHE или -540 мВ против Ag/AgCl) при рН 7,4 не должна восстанавливаться какими-либо биологическими восстановителями, такими как NADPH/NADH, поэтому она не должна принимать участие в цикле Haber Weiss с образованием ROS (реактивные формы кислорода). В организме млекопитающего железо связано с различными белками, такими как трансферрин в крови человека, таким образом, оно остается в форме, которая не может взаимодействовать с какими-либо молекулами кислорода. Величина Е1/2 Fe-трансферрин составляет -500 мВ (против NHE или -720 мВ против Ag/AgCl).
Окислительно-восстановительный потенциал комплексов железа может быть измерен с помощью циклической вольтамперометрии (CV). Использование CV для измерения окислительно-восстановительных потенциалов хелатных комплексов железа с деферипроном, деферриоксамином и Аро6619 (типичным примером соединения согласно данному изобретению), как с комплексонами, соответственно, иллюстрировано в примере 17 ниже. Хелатные комплексы железа, такие как Fe-десферриоксамин (DFO) и Fe-(деферипрон)3, имеют величины окислительно-восстановительных потенциалов Е1/2 при -698 мВ (против Ag/AgCl) и -834 мВ (против Ag/AgCl) при рН 7,4 соответственно. Хелатные комплексы соединений формулы I, такие как Fe(Apo6619)3, имеют величину Е1/2 -691 мВ (против Ag/AgCl), подобную величине для десферриоксамина. Графическое представление циклической вольтамперометрии Fe-DFO, Fe(деферипрон)3 и Fe(Apo6619)3 можно увидеть на фиг.9. Одно преимущество комплексонов согласно данному изобретению заключается в том, что окислительно-восстановительные потенциалы их хелатных комплексов с железом находятся в крайней отрицательной области при физиологическом рН 7,4, поэтому их хелатные комплексы с железом не будут участвовать в окислительно-восстановительном цикле с образованием активных форм кислорода при физиологическом рН. При сочетании с другими новыми свойствами, как описано в данном изобретении, соединения формулы I представляют собой эффективные средства для удаления железа посредством механизма хелатирования.
Для лечения заболеваний, связанных с перенасыщением железом, таких как талассемия, серповидно-клеточная болезнь, гемохроматоз, и лечения больных с токсической концентрацией железа, соединения согласно изобретению могут быть введены перорально, местно или парентерально в стандартных лекарственных формах, содержащих обычные нетоксичные фармацевтически приемлемые носители, адъюванты и наполнители.
Для лечения состояний, не связанных с перенасыщением железом, таких как ВИЧ-инфекция, защитный эффект от интоксикации сердца антрациклинами, опухоли и малярия, соединения согласно настоящему изобретению могут быть введены перорально, местно или парентерально в стандартных лекарственных формах, содержащих обычные нетоксичные фармацевтически приемлемые носители, адъюванты и наполнители.
Употребляемый в тексте термин парентеральный включает способы подкожной инъекции или инфузии. Помимо лечения теплокровных животных, таких как мыши, крысы, лошади, крупный рогатый скот, овцы, собаки, кошки и т.д., соединения согласно изобретению являются эффективными и в лечении человека.
Для использования в фармацевтических композициях подходящие нетоксичные твердые носители, включающие, например, маннит фармацевтических категорий, лактозу, крахмал, стеарат магния, сахарин натрия, тальк, целлюлозу, глюкозу, сахарозу, карбонат магния и тому подобное, могут быть использованы. Активное соединение, определенное выше, может быть приготовлено в виде жидкости. Фармацевтические вводимые композиции могут быть получены, например, путем растворения, диспергирования и т.д., активного соединения, определенного выше, и возможных фармацевтических адъювантов в носителе, таком как, например, вода, физиологический раствор, водная декстроза, глицерин, этанол и тому подобное, с образованием раствора или суспензии. Если желательно, фармацевтическая композиция, которая должна быть введена, также может содержать небольшое количество нетоксичных вспомогательных субстанций, таких как смачивающие и эмульгирующие средства и тому подобное, например ацетат натрия, сорбитанмонолаурат, триэтаноламина натрий ацетат, триэтаноламина олеат и т.д. Способы получения таких дозированных форм известны или будут очевидны специалистам в данной области: например, смотри Remington's Pharmaceutical Sciences, Mack Publishing Company, Easton, Pa., 15th Edition, 1975, ch. 83, p. 1436-1460, и ch. 89, p. 1576-1607. Композиция препарата, которая должна быть введена, так или иначе, будет содержать эффективное количество активного соединения(й) для ослабления симптомов у субъекта, подвергаемого лечению.
Фармацевтические композиции, содержащие активный ингредиент, могут находиться в форме, пригодной для перорального использования, например, в форме таблеток, пилюль, лепешек, водных или масляных суспензий, дисперсных порошков или гранул, эмульсий, твердых и мягких капсул или сиропов или эликсиров. Композиции, предназначенные для перорального использования, могут быть приготовлены любым способом, известным в данной области для производства фармацевтических композиций, и такие композиции содержат одно или более средств из группы, состоящей из подсластителей, ароматизаторов, красителей и консервантов для получения фармацевтически элегантных и приятных на вкус препаратов. Таблетки содержат активный ингредиент в смеси с нетоксичными фармацевтически приемлемыми наполнителями, которые пригодны для промышленного производства таблеток. Наполнителями могут быть, например, инертные разбавители, такие как фосфат кальция или фосфат натрия; гранулирующие и дезинтегрирующие средства, например кукурузный крахмал или альгиновая кислота; связывающие средства, например крахмал, желатин или гуммиарабик, и смазывающие средства, например стеарат магния, стеариновая кислота или тальк. Таблетки могут быть покрыты оболочками известными способами, чтобы задержать дезинтеграцию и всасывание в желудочно-кишечном тракте и, тем самым, обеспечить замедленное действие в течение длительного периода времени. В качестве смягчающего средства, эмульгатора или увлажнителя может быть использован моностеарат или глицерилдистеарат.
Препараты для перорального использования могут быть представлены в форме твердых желатиновых капсул, где активные ингредиенты смешивают с инертным твердым разбавителем, например фосфатом кальция или каолином, или в форме мягких желатиновых капсул, где активный ингредиент смешивают с водой или масляной средой, например арахисовым маслом, жидким парафином или оливковым маслом.
Водные суспензии могут содержать активные материалы в смеси с наполнителем, подходящим для промышленного производства водных суспензий. Такими наполнителями являются суспендирующие средства, например карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, камедь и аравийская камедь; диспергирующими или смачивающими средствами могут быть природный фосфат, например лецитин, или продукты конденсации простых циклических эфиров с жирными кислотами, например полиоксиэтиленстеарат, или продукты конденсации окиси этилена с длинноцепочечными алифатическими спиртами, например гептадекаэтиленоксицетанол, или продукты конденсации окиси этилена с частичными сложными эфирами жирных кислот и ангидридов гексита, например полиэтиленсорбитанмоноолеат. Водные суспензии также могут содержать один или более консервантов, например этиловый или н-пропиловый эфир п-гидроксибензойной кислоты, один или более красителей, таких как сахароза или сахарин.
Масляные суспензии могут быть приготовлены путем суспендирования активного ингредиента в растительном масле, например, арахисовом масле, оливковом масле, кунжутном масле или кокосовом масле, или в минеральном масле, таком как жидкий парафин. Масляные суспензии могут содержать загуститель, например пчелиный воск, твердый парафин или цетиловый спирт. Подсластители, такие как перечисленные выше, и ароматизаторы могут быть добавлены для получения приятного на вкус перорального препарата. Указанные композиции могут быть защищены путем добавления антиоксиданта, такого как аскорбиновая кислота.
Дисперсные порошки и гранулы, подходящие для приготовления водной суспензии путем добавления воды, способствуют образованию смеси активного ингредиента с диспергирующим или смачивающим средством, суспендирующим средством и одним или более консервантами. Подходящими диспергирующими или смачивающими средствами и суспендирующими средствами являются такие, которые уже были упомянуты выше. Могут быть представлены дополнительные реципиенты, например подсластители, ароматизаторы и красители.
Фармацевтическая композиция согласно изобретению может быть представлена в виде эмульсий масло-в-воде. Масляной фазой может быть растительное масло, например оливковое масло или арахисовое масло, или минеральное масло, например жидкий парафин, или их смеси. Подходящими эмульгирующими средствами могут быть природные фосфаты, сложные эфиры жирных кислот и ангидридов гексита, например сорбитанмоноолеат, и продукты конденсации указанных частичных сложных эфиров с окисью этилена, например полиоксиэтиленсорбитанмоноолеат. Эмульсия также может содержать подсластители и ароматизаторы.
Сиропы и эликсиры могут быть приготовлены с подсластителями, например глицерином, пропиленгликолем, сорбитом или сахарозой. Такие препараты также могут содержать успокоительное средство, консерванты и ароматизаторы и красители. Фармацевтические композиции могут быть приготовлены известными в данной области способами, используя такие подходящие диспергирующие и смачивающие средства и суспендирующие средства, которые были упомянуты выше. Стерильным инъецируемым препаратом также может быть стерильный инъецируемый раствор или суспензия в нетоксичном приемлемом для парентерального введения разбавителе или растворителе, например раствор в 1,3-бутандиоле. Среди приемлемых носителей и разбавителей, которые могут быть использованы, являются вода, растворы Рингера и изотонический раствор хлорида натрия. Кроме того, обычно используют жирные масла, включающие синтетические моно- или диглицериды. Кроме того, жирные кислоты, такие как олеиновая кислота, находят применение в препарате или инъецируемых формах.
Соединения формулы (I), или их соответствующая фармацевтически приемлемая соль и/или фармацевтически приемлемый сольват, также могут быть введены в форме препарата для местного нанесения в комбинации с подходящими для местно