Люминесцентные наночастицы с ядром и оболочкой
Иллюстрации
Показать всеИзобретение может быть использовано в устройствах или материалах для генерации света, печати или маркировки. Люминесцентные наночастицы включают ядро, полученное из люминесцирующей соли металла, выбранной из фосфатов, сульфатов или фторидов, которое окружено оболочкой, полученной из соли или оксида металла, способных предотвращать или уменьшать перенос энергии от ядра после его электронного возбуждения к поверхности наночастицы. Для получения люминесцентных наночастиц согласно изобретению готовят первую смесь, содержащую наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде. Затем полученную смесь подвергают взаимодействию при 50-350°С с источником анионов для формируемой оболочки и второй смесью, содержащей формирующие оболочку ионы металла и органический комплексообразователь. Изобретение позволяет повысить квантовый выход. 4 н. и 18 з.п. ф-лы, 2 ил.
Реферат
Настоящее изобретение относится к люминесцентным, в частности к фотолюминесцентным наночастицам с ядром из люминесцентного вещества, окруженным особой оболочкой, и к их получению.
Уровень техники
Наночастицы, т.е. частицы, размеры которых не превышают 1 микрометра, благодаря своим уникальным свойствам вот уже более десятилетия остаются в центре внимания как исследователей, так и промышленных разработчиков. В исследованиях и разработках в области оптоэлектроники внимание на люминесцентных частицах фокусируется ввиду их возможного применения в светоизлучающих диодах (LED), дисплеях, оптоэлектронных устройствах для нанометрических измерений или как источника излучения в лазерах с низким порогом возбуждения.
Среди люминесцирующих (люминесцентных) веществ часто различают полупроводники и не полупроводники.
Полупроводниковые наночастицы, такие как полупроводники II-VI или III-V, которые могут быть легированными или нелегированными, характеризуются квантовыми ограничениями как для электрона, так и для дырки во всех трех измерениях, что приводит к увеличению эффективной ширины запрещенной (энергетической) зоны вещества с уменьшением размеров кристаллов. Следовательно можно получать сдвиг как оптического поглощения, так и эмиссии полупроводниковых наночастиц в сторону голубой части спектра (более высоких энергий) по мере уменьшения размеров наночастиц. Однако зависимость эмиссии от размеров является нежелательной в ряде применений, поскольку она требует очень строгого контроля на стадиях распределения частиц по размеру или селекции по размеру, прежде чем рассматривать вопрос о промышленном применении.
Водорастворимые полупроводниковые нанокристаллы с ядром/оболочкой описаны, например, в WO 00/17655.
В патенте раскрывается, что особая привлекательность люминесцирующих веществ на основе нанокристаллических не полупроводников, в частности, легированных лантаноидами окислов или солей металлов, состоит в том, что их флуоресцентное излучение относительно узкое и не зависит в большой степени от вещества-хозяина (носителя), а также от размеров наночастиц. Цвет излучения, скорее, зависит лишь от типа лантаноидного металла. Документ PCT/DE 01/03433, переданный авторам, описывает общеприменимый способ получения легированных лантаноидами наночастиц указанного типа. Эти наночастицы можно получать таких размеров (не более 30 нм), при которых более не происходит взаимодействия с длиной волны видимого света, что ведет к образованию прозрачных дисперсных систем, например, в органических или водных растворителях.
Важной характеристикой для легированных лантаноидами наночастиц, определяющей степень их пригодности к применению, является их квантовый выход. Под квантовым выходом авторы понимают отношение числа испускаемых фотонов к числу поглощаемых фотонов.
Как правило, желательно получать нанокристаллические вещества с квантовым выходом такого же порядка, который соответствует люминесцирующему макрокристаллическому веществу. Например, суммарный показатель квантового выхода у коммерчески доступного макрокристаллического зеленого люминесцирующего фосфора (La0,45,Ce0,40)PO4:Tb0,15 составляет порядка 93% (включая УФ-излучение).
Однако за счет значительно большей величины соотношения поверхность/объем у нанокристаллических веществ возрастает вероятность явления гашения поверхностной люминесценции.
K.Riwotzky et al. в J. Phys. Chem. B 2000, 104, 2824-2828, "Liquid phase synthesis doped nanoparticles: colloids of luminescent LaPO4:Eu and CePO4:Tb particles with a narrow particle size distribution" сообщают, например, о квантовом выходе у LaPO4:Eu, составившем менее 10%, при возбуждении при 277 нм и о 16% квантовом выходе у CePO4:Tb, с учетом эмиссии церия, и об 11% выходе при учете эмиссии одного только тербия. Наблюдаемые значения весьма далеки от теоретических значений квантового выхода 89% и 38%, рассчитанных соответственно для нанокристаллических LaPO4:Eu и CePO4:Tb. Авторы названной статьи полагают, что возбужденное состояние основного вещества убывает за счет переноса энергии не только к люминесцирующим центрам, но также и к центрам, в которых имеет место безизлучательная рекомбинация. Вероятно, центрами безизлучательной рекомбинации могут быть те же самые гасящие ионы, к которым осуществляется перенос энергии от люминесцирующих ионов, или же состояния поверхности наночастиц. В этом контексте авторы отмечают, что наращивание оболочки из инертного материала вокруг каждой наночастицы уже применялось с успехом для полупроводниковых наночастиц, посредством чего достигалось увеличение у них квантового выхода люминесценции до значений 30-60% и более (ссылки 37-44 у K. Riwotzki и др.).
Jan W. Stouwdam and Frank C. J. M. van Veggel, Nano Letters, ASAP article, web release May 15, 2002, "Near-infrared emission of redispersible Er3+, Nd3+ and Ho3+ doped LaF3 nanoparticles" раскрывают получение наночастиц, которые могут быть перспективным материалом для основанных на полимерах оптических компонентов, поскольку им свойственна люминесценция и они имеют длину волны в диапазоне 1300-1600 нм, в котором оптические волокна на основе кремния обладают максимальной светопроницаемостью. Эти авторы проводили количественные измерения биэкспоненциального распада при люминесценции этих наночастиц и в этой связи высказывают предположение, что возможным путем усиления люминесценции ионов, локализующихся на поверхности или вблизи от нее, может оказаться наращивание слоя нелегированного LaF3 вокруг частиц.
K. Riwotzki et al., J. Phys. Chem. B 2001, 105, 12709-12713, "Colloidal YVO4:Eu and YO0,95V0,05О4:Eu particles: Luminescence and Energy transfer process" рассматривают вероятность покрытия из YPO4 для ядер из YVO4:Eu как возможного средства по увеличению низкого квантового выхода в 15%, наблюдаемого у нанокристаллического YVO4:Eu.
Получение частиц с ядром и оболочкой наталкивается, однако, на существенные трудности. Во-первых, необходимо предотвращать независимый (самостоятельный) рост исходных веществ, используемых для оболочки, так как он приводит к сосуществованию гомогенных наночастиц различного состава. Одновременно необходимо подавлять процессы обмена между отдельными наночастицами и созревание Оствальда. Созревание Оствальда представляет собой явление, имеющее место в дисперсионных системах малых частиц при повышенных температурах и включающее рост больших частиц за счет более малых частиц. Этот механизм также ведет к рандомизации различных композиций, используемых для ядра и оболочки.
M. Haase et al., Journal of Alloys and Compounds, 303-304 (2000) 191-197, "Synthesis and properties of colloidal lanthanide-doped nanocrystals" сравнивают свойства легированных лантаноидами нанокристаллов, которые были получены гидротермальным способом (в водном растворе) и в высококипящих органических растворителях (трибутилфосфате), соответственно. Авторы сообщают о 15% люминесцентном квантовом выходе при комнатной температуре у наночастиц YVO4:Eu.
Люминесцентные квантовые выходы такого же порядка (15%) приводятся также в G. A. Hebbink et al., Advanced Materials 2002, 14, №16, pages 1147-1150, "Lanthanide (III)-doped nanoparticles that emit in the near-infrared" для LaPO4-частиц, легированных Nd3+ и Er3+.
Таким образом, на сегодняшний день еще не получены не полупроводниковые частицы состава ядро/оболочка.
Соответственно, целью настоящего изобретения является разработка получения особых не полупроводниковых частиц с ядром и оболочкой (ядро/оболочка).
Кроме того, в настоящем изобретении ставится цель увеличения квантового выхода гомогенных люминесцирующих не полупроводниковых частиц.
Сущность настоящего изобретения
Указанные технические задачи решаются следующим образом:
с помощью люминесцентных наночастиц, включающих
(а) ядро, полученное из необязательно легированной люминесцирующей соли металла, выбранной из фосфатов, сульфатов, или фторидов, и окруженное
(b) оболочкой, полученной из соли или окисла металла, способных предотвращать или уменьшать перенос энергии от ядра к поверхности наночастиц после его электронного возбуждения,
а также с помощью способа получения этих наночастиц, где указанный способ включает следующие стадии:
получение первой смеси, содержащей наночастицы легированных люминесцирующих сульфата, фосфата или фторида металлов в органической среде,
взаимодействие указанной первой смеси, источника анионов для оболочки, которую необходимо сформировать, и второй смеси, содержащей формирующие оболочку ионы металлов и органическое комплексообразующее вещество для указанных ионов металлов, при температуре от 50 до 350°С до тех пор, пока вокруг указанных люминесцирующих наночастиц не образуется оболочка.
Фигуры
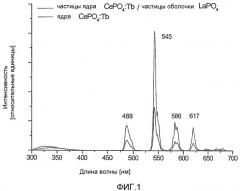
Фиг.1 показывает спектры флуоресценции гомогенных наночастиц CePO4:Tb (сплошная линия) и частиц ядра и оболочки по настоящему изобретению (пунктирная линия), где LaPO4-оболочка выращена вокруг CePO4:Tb-ядра.
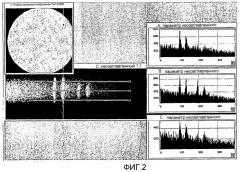
Фиг.2 показывает результаты TEM (просвечивающий электронный микроскоп)-анализа одной частицы ядро/оболочка по настоящему изобретению, а именно, (D) Хельфельдово (Hellfeld) изображение одной наночастицы CePO4:Tb, окруженной LaPO4-оболочкой (диаметром около 7 нм); (E) изображение спектра при 860 эВ-ной потере энергии, а также профили поверхности частицы (A,C) и центра (B).
Детальное описание настоящего изобретения
I. Люминесцирующие наночастицы
Люминесцирующие, в особенности, фотолюминесцирующие наночастицы по настоящему изобретению включают ядро, полученное из необязательно легированной люминесцирующей неорганической соли металла, выбранной из фосфатов, сульфатов или фторидов.
"Люминесценция" характеризует свойство заявленных наночастиц поглощать энергию (например, в виде фотонов, пучков электронов, рентгеновских лучей и т.п.), которая затем выделяется в виде света с меньшей энергией. Следует понимать, что в описании и в формуле изобретения термин "люминесцирующий" включает более конкретное и предпочтительное значение "фотолюминесцирующий".
Под "фотолюминесценцией" авторы понимают способность неорганической соли металла поглощать фотоны конкретной энергии (например, УФ, видимого света) и излучать свет с меньшей энергией (с большей длиной волны, например, УФ, видимый спектр, инфракрасное излучение) в течение определенного периода времени. Период светового излучения может соответствовать продолжительности возбужденного состояния вплоть до 10-7 или 10-8 сек, который обычно называется флуоресценцией, но возможны также и более длительные периоды. Для легированных лантаноидами сульфатов, фосфатов или фторидов обычно длительность возбужденного состояния составляет, по наблюдениям, величины порядка миллисекунд (например, 1-20 мс).
"Легирование" следует понимать в широком смысле. Верхний предел используемой легирующей добавки должен быть достаточно низким для того, чтобы генерируемая люминесценция не уменьшалась за счет явления концентрационного гашения. Соответственно, этот верхний предел зависит от факторов, подобных расстоянию в кристаллической решетке между ионами легирующего металла, которые являются специфическими для каждого материала ядра. Предпочтительно, вещество-хозяин замещается легирующей добавкой в количестве вплоть до 50 мол.%, предпочтительно 0,1-45 мол.%, например, 0,5-40 мол.%, или 1-20 мол.%.
В соответствии с первым вариантом осуществления настоящего изобретения предпочтительно легированное вещество ядра покрывают нелюминесцирующими солями металлов, в частности, фосфатами, сульфатами или фторидами.
Для вещества-хозяина, используемого для ядра, особых ограничений не имеется. Оно может быть выбрано из числа известных сульфатов, фосфатов или фторидов в зависимости от легирующей добавки, которая должна быть внедрена в решетку. Поскольку большинство люминесцирующих легирующих добавок представляют собой ионы двух- или трехвалентных металлов, предпочтительно использовать сульфаты, фосфаты или фториды нелюминесцирующих двух- или трехвалентных металлов, таких как металлы группы 2 (щелочноземельные металлы, такие как Mg, Ca, Sr или Ba) или группы 3 (Sc, Y или La) или группы 13 (например, Al, Ga, In или Tl) или Zn. При выборе подходящего вещества-хозяина для конкретной легирующей добавки следует, кроме того, учитывать, что, как известно в уровне техники, металл-хозяин и металл легирующей добавки предпочтительно должны иметь, одинаковую валентность и сходные (допустимое отклонение, например, ±20%) или идентичные ионные диаметры. Одновременно, это обычно повышает совместимость легирующей добавки и металла-хозяина в случаях, когда они способны к формированию, с определенным анионом, кристаллов с тем же самым или сходным типом решетки, имеющих одинаковые или сходные параметры кристаллических решеток (допустимое отклонение, например, ±20%).
В качестве металла вещества-хозяина для ядра указанным критериям могут отвечать Ba и Sr, поскольку диаметры ионов этих металлов очень близки к диаметрам двухвалентных (+II) лантаноидных легирующих добавок. По этой же причине, соли La и Y являются подходящими веществами-хозяевами для легирующих добавок на основе трехвалентных (+III) лантаноидов.
Не имеется также никаких специальных ограничений в отношении типа вводимого легирующего металла, пока он обладает способностью преобразовывать поглощаемые фотоны в люминесцентное излучение. Так, например, можно использовать такие металлы, как Cr, Ag, Cu, Co или Mn (например, в сочетании с цинком в качестве металла-хозяина). Из их числа предпочтительными в качестве легирующих добавок для атомов металла-хозяина групп 13 и 2 являются соответственно Cr3+ и Mn2+. Однако легирование с помощью металлов-лантаноидов является предпочтительным, поскольку люминесценция лантаноидных металлов особенно не зависит от окружения решетки. Как правило, предпочтительным является использование двух- или трехвалентных легирующих добавок, в особенности, лантаноидных легирующих добавок. Двухвалентные лантаноиды (+II состояния окисления) характеризуются относительно сильным поглощением, но относительно широкими полосами излучения. По этой причине их удобно использовать в качестве сенсибилизаторов, переносящих энергию к другим люминесцирующим металлам (например, Eu2+ к Mn2+). Способность трехвалентных лантаноидов (состояние окисления +III) к световому излучению в форме относительно отчетливых полос также делает их особенно желательными для применения в качестве легирующих добавок в конкретных применениях. Эти легирующие добавки можно использовать в качестве единственного легирующего металла или в комбинации, как раскрывается ниже для некоторых сочетаний трехвалентных лантаноидов.
Легирующие лантаноидные ионы (ион) можно подходящим образом выбирать из Ce (порядковый номер 58), Pr (59), Nd (60), Sm (62), Eu (63), Gd (64), Tb (65), Dy (66), Ho (67), Er (68), Tm (69) или Yb (70). Предпочтительными легирующими добавками являются Ce, Nd, Eu, Tb, Dy, Ho, Er и Yb. Er3+, Nd3+ и Ho3+ представляют особый интерес для области телекоммуникации, поскольку они излучают в диапазоне 1300-1600 нм. Ce используется предпочтительно в сочетании с другим легирующим веществом, таким как Nd, Dy или Tb. Как известно, Ce хорошо поглощает УФ-излучение с длиной волны 250-300 нм и характеризуется довольно широкой полосой люминесценции приблизительно 330 нм в зависимости от окружения решетки (например, в фосфатной решетке). Если использовать Ce в сочетании с другими легирующими добавками, которым можно передать поглощенную энергию, то можно получить очень эффективные люминесцирующие системы. Еще одну интересную комбинацию легирующих металлов представляет Yb и Er, имеющая большое значение для Er3+-легированных оптических усилителей, где Er3+ накачивается косвенно, через Yb3+, имеющий в десять раз большее поперечное сечение поглощения и значительно более широкий пик при 980 нм, чем у Er3+.
Как отмечалось выше, указанные сочетания лантаноидных металлов можно использовать не только как легирующие добавки для ядра. В равной мере выгодно использовать в качестве металла-хозяина ион металла-лантаноида (например, Ce3+, Yb3+), который имеет большее поперечное сечение поглощения, и при замещении его части меньшими количествами другого металла (например, 0,1-40 мол.%, предпочтительно, 0,5-30 мол.%). "Другим" металлом предпочтительно является Nd3+, Dy3+ или Tb3+ для основанных на Ce3+ веществ-хозяев и Er3+ для основанных на Yb3+ веществ-хозяев. По этой причине, в качестве вещества-хозяина для ядра можно использовать также сульфаты, фосфаты или фториды лантаноидов (например, Ce3+, Yb3+). Их можно комбинировать с такими же веществами для оболочки, как это далее детально будет разъяснено, предпочтительно, с сульфатами, фосфатами или фторидами металлов группы 2, в особенности, сульфатами, фосфатами или фторидами La. Особенно предпочтительными вариантами осуществления изобретения являются частицы ядро/оболочка типа CePO4:Tb/LaPO4 и CePO4:Nd/LaPO4.
В соответствии с настоящим изобретением вещество оболочки, а именно, соль или оксид металла, способно предотвращать или уменьшать перенос энергии от ядра, в его электронном возбужденном состоянии, к поверхности частицы ядро/оболочка, где она будет гаситься. Как полагают, эти явления гашения (тушения), наблюдаемые у люминесцирующих ядер наночастиц, не имеющих оболочки, вызваны либо взаимодействием центров люминесценции на поверхности с молекулами из окружающей среды (например, растворителя), контактирующими с поверхностью или связанными с нею, либо состояниями ненасыщенности поверхности. Что касается последнего воздействия, то, как полагают, свободные валентности поверхностных металлических атомов обусловливают низкоэнергетические состояния, которым энергия, поглощенная атомами металла, расположенными ниже поверхности, легко может быть передана.
Задачу предотвращения или уменьшения переноса энергии всегда можно решить с помощью солей или оксидов металла, в которых энергетическое расстояние между основным состоянием электронов и первоначальным возбужденным состоянием электронов больше, чем соответствующее энергетическое расстояние выбранного ядра. При таких обстоятельствах энергия (например, УФ, видимого света, инфракрасного излучения), поглощенная ядром, не может быть передана оболочке, в особенности, атомам металла оболочки. Достигаемая таким образом локализация энергии в ядре предотвращает явления поверхностного гашения и увеличивает квантовый выход. В соответствии с указанным первым вариантом осуществления настоящего изобретения соль или оксид оболочки является нелюминесцирующим и таким образом отсутствуют низкоэнергетические состояния электронов, которым могла бы передаваться энергия от возбужденного ядра.
В соответствии со вторым вариантом осуществления настоящего изобретения ядро состоит из люминесцирующего сульфата, фосфата или фторида лантаноида, а оболочка состоит из соли или окиси лантаноида, отличающихся от вещества ядра и предотвращающих или уменьшающих перенос энергии от ядра после возбуждения его электронов к поверхности наночастицы. Ядро и атом лантаноидного металла можно подходящим образом выбирать из числа Ce (порядковый номер 58), Pr (59), Nd (60), Sm (62), Eu (63), Gd (64), Tb (65), Dy (66), Ho (67), Er (68), Tm (69) или Yb (70) при условии, согласно вышеприведенному объяснению, что относительные энергетические расстояния между основным состоянием электронов и первоначальным возбужденным состоянием не позволят передать энергию возбуждения от ядра к оболочке. Предпочтительно, ядро состоит из сульфата, фосфата или фторида Nd, а оболочка состоит из соли или окиси Gd. Данное сочетание атомов этих металлов особенно желательно, так как Gd-оболочка не только способствует увеличению квантового выхода сульфата, фосфата или фторида Nd, но также обеспечивает прекрасные контрастные свойства ЯМР, что обусловлено, как полагают, местонахождением Gd на поверхности частиц. Способность люминесцировать и давать ЯМР-контрастность вместе делают особенно привлекательным использование данного варианта осуществления в диагностических целях.
Что касается химического состава оболочки, то любой подходящий анион или оксид можно использовать, пока он способен расти на частицах ядра вместе с выбранным атомом металла.
Подходящие анионы для получения оболочки включают, но не ограничиваются ими, фосфаты, галофосфаты, арсенаты, сульфаты, бораты, алюминаты, галлаты, силикаты, германаты, оксиды, ванадаты, ниобаты, танталаты, вольфраматы, молибдаты, алкалгалогенаты, прочие галогениды, нитриды, сульфиды, селениды, сульфоселениды или оксисульфиды. Соли металлов в виде наночастиц такого типа описаны в PCT/DE 01/03433.
В соответствии с настоящим изобретением единственным критерием, определяющим выбор атомов металла для оболочки, является отсутствие способности передавать энергию люминесценции от возбужденного ядра к поверхности после облучения. Предпочтительными ионами металлов, которые можно использовать для этой цели, являются те же ионы металлов, что упомянуты выше для материалов ядра. Они включают, но не ограничиваются ими, металлы группы 2 (щелочноземельные металлы, такие как Mg, Ca, Sr или Ba), металлы группы 3 (как Sc, Y или La), металлы группы 13 (как Al, Ga, In или Tl). Для увеличения способности вещества оболочки расти на поверхности вещества ядра предпочтительно также, но совершенно не обязательно, выбирать в качестве вещества оболочки сульфат, фосфат или фторид того же металла, что составляет вещество-хозяина ядра. Если это условие не выполняется, то предпочтительно, чтобы вещество-хозяин ядра и вещество оболочки принадлежали к одному и тому же типу решетки и имели бы очень схожие (допустимое отклонение, например, ±20%) или идентичные параметры решетки.
Частицы ядро/оболочка по настоящему изобретению образуют предпочтительно кристаллические вещества. Это может быть подтверждено порошковыми рентгенограммами.
Частицы ядро/оболочка по настоящему изобретению могут иметь форму, например, иглоподобную, эллипсоидную или сферическую, последние два варианта являются предпочтительными.
Наночастицы ядро/оболочка по настоящему изобретению предпочтительно имеют средний размер, измеренный по самой длинной оси, 1-100 нм, более предпочтительно 1-50 нм. Еще более желательны средние размеры, составляющие самое большее 30 нм, самое большее 20 нм, самое большее 10 нм, например, 2-8 нм или 4-6 нм. Для каждого случая стандартное отклонение составляет предпочтительно менее 30%, особенно, менее 10%.
Размер частиц и их распределение может быть определено с помощью технологий, описанных также в уже упомянутых статьях K.Riwotzki et al. и M. Haase et al., например, с использованием просвечивающего электромикрографа (TEM).
Средняя толщина оболочки предпочтительно соответствует по меньшей мере одному или двум монослоям. С другой стороны, излишняя толщина оболочки может отрицательно сказаться на суммарных фотолюминесцентных свойствах частицы ядро/оболочка. Предпочтительный верхний предел толщины оболочки равняется таким образом диаметру ядра, более предпочтительно 2/3 диаметра, еще более предпочтительно 1/2 диаметра.
II. Получение наночастиц ядро/оболочка
Указанные наночастицы ядро/оболочка по настоящему изобретению получены по способу, раскрываемому далее в пунктах формулы и включающему по меньшей мере две следующих стадии:
1. Получение так называемой "первой смеси", содержащей наночастицы (ядра) необязательно легированного, люминесцирующего сульфата, фосфата или фторида металла в органической среде.
2. Взаимодействие указанной первой смеси, источника анионов для оболочки, которую необходимо сформировать, в частности, фосфатным, сульфатным или фторидным источником, и "второй смеси", содержащей ионы металла, образующего оболочку, и органическое комплексообразующее вещество для указанных ионов металла при температуре 50-350°С до тех пор, пока вокруг указанных люминесцирующих наночастиц не образуется оболочка.
II.1 Первая стадия способа и получение частиц ядра.
Наночастицы, обеспеченные в качестве материала ядра и присутствующие в так называемой "первой смеси", можно синтезировать (получать) способами, известными в уровне техники. Как правило, жидкостная технология предпочтительней, чем "сухая", поскольку она позволяет лучше контролировать размер частиц. Кроме того, при жидкостных способах получения легче подавлять агрегирование получаемых наночастиц.
Из известных технологий жидкостного получения можно использовать золь-гель процессы, гидротермальный синтез или органический синтез с комплексообразователями, которые регулируют рост кристаллов. Кроме того, конкретно фториды можно получать по методике получения, описанной у J. W. Stouwdam и F. C. J. M. Van Veggel. Так, наночастицы LaF3 и другие фториды могут быть получены нагреванием раствора ди-н-октадецилдитиофосфата аммония и NaF в смеси этанол/вода. Затем водные растворы нитратов соответствующих металлов добавляют по каплям и перемешивают раствор в течение двух часов при 75°С с последующим охлаждением до комнатной температуры. Недостатком этого способа является то, что получаемые частицы все еще отличаются довольно широким распределением частиц по размеру, что требует дополнительных стадий очистки путем центрифугирования.
"Гидротермальный синтез" фосфатов, легированных лантаноидами, описан, например, в "Wet-chemical synthesis of doped colloidal nanomaterials: particles and fibres of LaPO4:Eu, LaPO4:Ce, LaPO4:Ce,Tb" у H. Meyssamy et al., Advanced Materials (1999), Vol. 11, No. 10, pages 840 et seq. В качестве исходных веществ для сульфатных, фосфатных или фторидных наночастиц, предпочтительно использовались хлориды, нитраты или ацетаты металлов. Взаимодействие проводили в воде в качестве реакционной среды в автоклаве, чтобы поддерживать высокое давление, предпочтительно, давление от 10-20 бар во время реакции.
В результате гидротермального синтеза получаются частицы относительно большие по размеру, часто имеющие игольчатую форму. Помимо этого, для получаемого вещества, как правило, характерно относительно широкое распределение частиц по размерам. При указанном способе H. Meyssamy et al. процент наночастиц с диаметром менее 25 нм составляет, например, всего лишь около 20%. Они могут быть выделены на последующих стадиях центрифугирования.
Кроме того, необязательно легированные сульфаты можно получать при давлении окружающей среды в органических средах, выбираемых из полиолов (высокомолекулярных спиртов) и сульфоксидов, которые, как полагают, способны регулировать рост кристаллов за счет способности образовывать металлокомплексы. Далее здесь этот способ будет называться как "полиол- или сульфоксид-способ".
Используемые полиолы предпочтительно содержат две или три гидроксильные группы, в качестве примера можно назвать глицерин, этиленгликоль или полиэтиленгликоль, где предпочтительно использовать полиэтиленгликоль с низкой молекулярной массой (предпочтительное среднее число звеньев этиленгликоля вплоть до 4). В качестве сульфоксида можно использовать диметилсульфоксид (DMSO). Данный способ получения предпочтительно используется при получении сульфатов щелочноземельных металлов, таких как сульфат магния, кальция, стронция или бария как легированного вещества-хозяина.
Предпочтительными источниками атомов металла являются соответствующие хлориды и их гидраты. Как исходное вещество для сульфата предпочтительно использовать сульфаты щелочных металлов, сульфаты аммония или сульфаты, имеющие органические катионы. В равной степени приемлемы соответствующие гидросульфаты.
Органический катион выбирают предпочтительно из основных N-содержащих алифатических, ароматических и алифатических/ароматических веществ, имеющих предпочтительно от 4 до 30 атомов углерода, предпочтительно, от 4 до 20 атомов. Приемлемые катионы включают, например, четвертичный аммоний или четвертичный фосфоний, где 4 замещающие группы могут быть независимо выбраны из алкила, имеющего предпочтительно от 1 до 10 атомов углерода (предпочтительно, 1-5), или бензила, или протонированных ароматических оснований, таких как гидразин, амантадин, пиридин или коллидин.
Соответственно, сульфатные наночастицы можно получать из исходных материалов, таких как тетрабутиламмоний гидросульфат, тетраметиламмоний сульфат, бис-тетрабутиламмоний сульфат или триэтиламмоний гидросульфат. Другими приемлемыми исходными материалами являются аммоний гидросульфат, аммоний сульфат, гидросульфаты щелочных металлов, сульфаты амантадина, этилендиаммоний сульфат и гидразиний сульфат.
Для легирования сульфатного вещества-хозяина можно использовать нитраты или галогениды соответствующей легирующей добавки, особенно хлорида соответствующего металла.
Если в исходном материале содержатся гидросульфаты, то предпочтительно добавлять в реакционную среду органические основания, такие как имидазол, в качестве кислотного акцептора. Реакцию предпочтительно проводят при температуре от 50 до 240°С, при этом для глицерина предпочтительна более низкая температура в интервале 50-100°С, а для других полиол- или сульфоксидных растворителей предпочтительна более высокая температура в интервале 160-240°С, в частности, наиболее приемлема температура от 160 до 180°С. Средний диаметр получаемых частиц составляет порядка 0,2-50 нм, эти частицы легко диспергируют в водной среде.
Ядра наночастиц, получаемые по золь-гелевому способу, гидротермальным синтезом или так называемым "полиол- или сульфоксид-синтезом", являются иногда диспергируемыми в органической среде, используемой на первой стадии способа по изобретению, особенно, когда реакционная среда для ядра и среда в способе по изобретению (при получении оболочки), соответственно, значительно различаются по своей полярности. По этой причине может оказаться необходимым подвергать наночастицы последующей обработке приемлемым полярным органическим соединением для увеличения их диспергируемости. Предпочтительно осуществлять эту последующую обработку с использованием той же органической среды, что будет использоваться при получении оболочки или с помощью органических сред сходной полярности.
Если, например, необходимо осуществлять получение оболочки в N- или P-содержащих средах, то последующая обработка может подходящим образом включать подвергания частиц, полученных золь-гелевым способом, гидротермальным синтезом или так называемым "полиол- или сульфоксид-способом", последующей обработке в N- или P-содержащих средах.
Указанная последующая обработка включает нагревание наночастиц в соответствующем органическом соединении. Результатом этого является замещение водных или других гидрофильных остатков, связанных с поверхностью наночастиц, полярным органическим соединением. По причинам, указанным выше, полярное органическое соединение выбирают предпочтительно из N- или P-содержащих комплексообразователей для ионов металла, что будет описано далее в тексте в связи с "органическим синтезом" и в связи со второй стадией способа. Однако можно использовать также и другие функционализированные полярные органические соединения.
Указанная последующая обработка для сульфатов не требуется, когда они получены по "полиол- или сульфоксид-" способу, если последующие стадии получения выполнялись в полиолах и/или сульфоксидах.
В соответствии с дополнительной и предпочтительной методикой, называемой здесь и далее "органический синтез", способ получения люминесцирующих ядер наночастиц включает следующие стадии:
а) взаимодействие в органической реакционной среде, содержащей по крайней мере один агент, образующий комплекс с металлом, и необязательно по меньшей мере один дополнительный растворитель, растворимый или диспергируемый в реакционной среде источник металла и растворимый или диспергируемый в реакционной среде источник фосфата, сульфата или фторида,
b) необязательно отделение реакционной среды от образовавшихся при этом наночастиц фосфата, сульфата или фторида металла, и
c) необязательно извлечения наночастиц соли.
Под "органической средой" понимаются органические растворители, которые, кроме неизбежных остатков, не содержат воды. Точка кипения этой органической среды предпочтительно выше, чем приводимые ниже температуры реакции. Она составляет, например, от 150 до 400°С, предпочтительно выше 180°С, и особенно выше 210°С (при давлении окружающей среды).
В зависимости от подверженности источника металла к окислению предпочтительно осуществлять реакцию в атмосфере газа, такого как азот или аргон.
Учитывая степень чистоты исходных веществ, можно рекомендовать использовать соли металлов, чистота которых составляет по меньшей мере 99,9%. Все используемые реагирующие вещества и растворители предпочтительно не содержат воды и/или их высушивают до использования. Однако хлориды металлов, часто применяемые в качестве гидроксида, предпочтительно, не следует подвергать слишком длительной процедуре сушки, так как это может способствовать увеличению образования нерастворимых в реакционной среде оксихлоридов.
Реакцию предпочтительно осуществлять при температуре от 50 до 350°С, например, от 120 до 320°С, особенно, от 180 до 290°С. Специалист в данной области техники легко сможет установить приемлемую температуру путем мониторинга реакции реагирующих веществ при постепенно возрастающих температурах, определяя при этом минимальную температуру реакции, при которой реакция протекает с достаточной скоростью. Для этой цели можно, например, осаждать наночастицы из образцов (проб) реакционной среды, что позволит исследовать рост частиц при увеличении продолжительности реакции.
Аналогичным образом можно установить приемлемое время реакции и предпочтительный интервал от 10 мин до 48 час, особенно от 30 мин до 20 час.
После завершения реакции реакционную смесь можно охлаждать до комнатной температуры. Если наночастицы в ходе реакции или после охлаждения осели все еще не полностью, то можно добавить метанол к реакционной среде или наоборот, для того чтобы получить максимальный выход.
Вне связи с теорией, считается, что агент, образующий комплекс с металлом, используемый в "органическом синтезе", координируется с атомами металла на поверхности образованных наночастиц и ограничивает этим их рост после того, как исходные вещества прореагировали. Как полагают, указанный агент, образующий комплекс с металлом, остается на границе с поверхностью частицы и таким образом предотвращает или снижает процессы агломерации и обмена между частицами, подобные созреванию Оствальда. Таким образом, органический синтез приводит к довольно маленьким частицам, со средним диаметром, измеренным по самой большой оси, составляющим, предпочтительно, 1-10 нм, особенно, 2-8 нм, например, 4-6 нм при узких распределениях по размерам (стандартное отклонение <30%, в частности, <10%). Агент, образующий комплекс с металлом, характеризуется наличием полярной группы, способной координироваться с ионом металла и по меньшей мере еще с одним фрагментом молекулы (менее полярным, предпочтительно, гидрофобным), например, с алифатическим, ароматическим/алифатическим, или чисто ароматическим фрагментом молекулы, содержащим предпочтительно 4-20, в частности, 6-14 атомов углерода.
Агент, образующий комплекс с металлом, представляет собой предпочтительно фосфорорганическое соединение или моно- или двузамещенный амин.
Из последних наиболее предпочтительными вариантами являются моно- или диалкиламины, алкильная группа у которых имеет предпочтительно от 4 до 20, в частности, от 6 до 14 атомов углерода, например, додециламин или бис(этилгексил)амин.
Что касается фосфорорганических соединений, то предпочтительно использовать по меньшей мере одно из следующих веществ:
a) эфиры фосфиновой кислоты
b) диэфиры фосфиновой кислоты
c) триэфиры фосфорной кислоты, наиболее предпочтительны такие триалкилфосфаты, как трибутилфосфат или три(этилгексил)фосфат,
d) триалкилфосфины, такие как триоктилфосфин (ТОР),
или
e) окиси триалкилфосфина, такие как окись триоктилфосф