Спермицидная и/или противогрибковая композиция и способы ее применения
Иллюстрации
Показать всеГруппа изобретений относится к медицине, в частности к гинекологии и дерматологии, и касается вариантов спермицидной и/или противогрибковой композиций и способов контрацепции или лечения грибковых заболеваний с использованием таких композиций. Композиции по настоящему изобретению могут содержать эффективные количества гексагидроинденопиридиновых соединений, предотвращающие беременность, или оказывающие фунгицидное воздействие, и подходящий носитель. Изобретения обеспечивают эффективную контрацепцию и фунгицидное воздействие. 5 н. и 39 з.п. ф-лы, 4 ил., 7 табл.
Реферат
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Область техники, к которой относится изобретение
Настоящее изобретение относится к действующим в качестве спермицидных средств и/или противогрибковых средств гексагидроинденопиридиновым соединениям, содержащим их спермицидным или противогрибковым композициям и способам нейтрализации подвижных сперматозоидов или грибков с применением соединений и композиций по настоящему изобретению.
Предпосылки изобретения
В США и большинстве стран Запада высокий и растущий спрос на противозачаточные средства является следствием определенного образа жизни, тогда как во многих развивающихся странах регулирование рождаемости является чрезвычайно важной задачей здравоохранения. Поскольку контрацепция является всеобщей потребностью охраны здоровья, хотя и по различным причинам в разных частях света, общий объем рынка противозачаточных средств для мужчин мог бы быть более значительным, чем представленный только в показателях по США.
На Западе рынок противозачаточных средств подвергся сравнительно небольшим изменениям за последние 50 лет с тех пор, как в 1951 была разработана «противозачаточная таблетка», которая остается единственным средством контрацепции, выбранным населением. Достижения в поисках средств для контрацепции обеспечили всего лишь несколько способов, все для женщин, которые, как исторически сложилось, несут основную ответственность, затраты и риск для здоровья (в особенности, риск развития сердечно-сосудистого заболевания и определенных типов рака, связанных с длительным применением гормональных противозачаточных средств) контрацепции. Презерватив, изобретенный в 16-ом веке, представляет собой единственно значимую форму контрацепции, доступную для мужчин (помимо прерванного полового акта и вазэктомии [иссечения семявыносящего протока]). Единственным действительно инновационным усовершенствованием, произошедшим с презервативом, явилось изобретение вулканизации резины в 19-ом веке. (Из New Scientist, 20 April 1994, Vol 142 No 1923.)
Вследствие разработки фармацевтическими компаниями соединений для лечения половой дисфункции (например, Виагра для лечения эректильной дисфункции) ожидается рост спроса на противозачаточные средства. Продажи презервативов в США за 1999 год выросли на 5,8%, принеся 260 миллионов долларов дохода, отражая тем самым то, что некоторые назвали бы новой американской сексуальной революцией. (Drug Store News, Nov 29, 1999, v.21, i.19, p.29.) Хотя большинство женщин детородного возраста уже применяют контрацептивы, (В мире 58% всех замужних женщин детородного возраста используют какой-либо способ контрацепции The Population Division of the United Nations Department of Economic and Social Affairs 2000), до сих пор половина всех беременностей является нежелательной. (NICHD, Contraception and Reproductive Health Branch: Report to the NACHHD Council September 1999.) Людей, ведущих здоровый образ жизни, и потребителей интересует создание дополнительных альтернативных способов, особенно способов, которые позволяют мужчинам взять на себя большую часть ответственности за контрацепцию. Всеобщий интерес побудил организации, такие как Всемирная организация здравоохранения и Family Health International, инициировать запуск проектов, направленных на поддержку разработки противозачаточных средств для мужчин. По крайней мере, две компании, Schering и Organon, за последние десять лет активно продвигают гормональные противозачаточные средства для мужчин на рынок.
В течение многих лет ведутся поиски безопасных и эффективных пероральных противозачаточных средств для мужчин. Однако было показано, что разработка лекарственного средства, которое может безопасно прерывать сперматогенез, не влияя на половое влечение, и, следовательно, использоваться в качестве противозачаточного средства для мужчин, является непростой задачей.
Идеальным противозачаточным средством для мужчин могло бы являться средство, способное эффективно подавлять продукцию сперматозоидов, блокировать их способность к оплодотворению без нарушения полового влечения или не влияя на вторичные половые признаки и их функции, и/или нейтрализовывать подвижные сперматозоиды. Кроме того, должна существовать большая разница между эффективной и токсичной дозами препарата, а способ контрацепции должен быть обратимым. В настоящее время нет такого совершенного противозачаточного средства для мужчин.
Некоторые неспецифические клеточные токсины, такие как противоопухолевые средства и алкилирующие агенты, влияют на сперматогенез, но, безусловно, неприемлемы в качестве противозачаточных средств. Соединения, препятствующие энергетическим процессам в клетке, такие как тиосахара, также влияют на сперматогенез, но в недостаточной степени селективны. Андрогены, такие как тестостерон и его аналоги, при введении в больших дозах влияют на сперматогенез, по-видимому, посредством механизма вовлечения гипоталамо-гипофизарной системы. Такие стероидные соединения успешно применялись в клинических испытаниях. Однако анаболические свойства этих стероидов могут давать риск возникновения нежелательных побочных эффектов.
В качестве соединений, эффективно блокирующих сперматогенез, активно изучали аналоги гонадотропин-релизинг фактора (GNRH). Однако аналоги GNRH влияют на эндогенную продукцию тестостерона и потому снижают половое влечение в отсутствие введения дополнительных андрогенов.
Один из подходов к созданию противозачаточных средств для мужчин основан на идентификации и использовании биохимических особенностей репродуктивного процесса мужчин. Яичко состоит из трех функциональных отделов. Первый, ответственный за производство сперматозоидов, состоит из семенных канальцев, которые содержат развивающиеся зародышевые клетки. Второй представляет собой расположенные внутри семенных канальцев клетки Сертоли, которые участвуют в организационной и функциональной координации процесса сперматогенеза и, возможно, выполняют паракринную и аутокринную роль. Благодаря комплексному организационному взаимодействию клеток Сертоли и развивающихся зародышевых клеток и наличию плотных контактов между соседними клетками Сертоли образуется гемато-тестикулярный барьер, разделяющий семенной каналец на участки, которые изолированы от прямого контакта с химическими и питательными веществами кровотока. В интерстициальной ткани семенные канальцы окружены клетками Лейдига, которые обладают несколькими эндокринными и паракринными функциями, среди которых наиболее описанной является продукция тестостерона.
Зародышевые клетки делятся и постепенно дифференцируются, продвигаясь по мере созревания от базальной мембраны к просвету семенного канальца. В базальном отделе находятся сперматогонии; избирательно выбранные сперматогонии митотически делятся и либо остаются клетками, продолжающими существовать в виде сперматогониев, либо дифференцируются в сперматоциты первого порядка. Сперматоциты первого порядка мигрируют через контакты между клетками Сертоли и митотически делятся с образованием сперматоцитов второго порядка. Сперматоциты второго порядка делятся с образованием сперматид. Сперматиды затем дифференцируются во взрослые сперматозоиды. Дифференцировку сперматид обычно называют сперматогенезом. Однако в контексте настоящей заявки под определением термина «сперматогенез» понимают весь процесс формирования и созревания (дифференцировки) сперматозоидов, а «антисперматогенным соединением» является соединение, которое нарушает любую часть этого процесса.
Краткий перечень функций клеток Сертоли представляет собой: (a) основа и питание сперматогенного эпителия, (b) высвобождение зрелых сперматид в просвет семенного канальца, (c) образование морфологического и физиологического гемато-тестикулярного барьера, (d) фагоцитоз разрушающихся зародышевых клеток, и (e) регуляция цикла сперматогенного эпителия.
Клетки Лейдига также содействуют сперматогенезу. Лютеинизирующий гормон (LH) гипофиза стимулирует продукцию тестостерона клетками Лейдига. Тестостерон и его метаболит, дигидротестостерон, необходимы для поддержания нормального сперматогенеза. Рецепторы тестостерона присутствуют на различных типах зародышевых клеток. Тестостерон доставляется через гематотестикулярный барьер, по-видимому, посредством транспорта в клетки Сертоли, где он превращается в процессе обмена веществ в эстардиол, дигидротестостерон или остается неизмененным.
Некоторые, если не все, типы зародышевых клеток, взаимодействуют с клетками Лейдига и/или Сертоли. Эти взаимодействия осуществляются посредством химических мессенджеров, которые продуцируются клетками Сертоли, клетками Лейдига и зародышевой клеткой (клетками). Например, пахитенный сперматоцит модулирует секрецию белкового фактора клеток Сертоли, который, в свою очередь, стимулирует биосинтез стероидных гормонов клетками Лейдига. Связывание сперматид происходит только с клетками Сертоли, которые становятся компетентными или функциональными после контакта с FSH. У крыс клетки Сертоли циклически секретируют несколько белков с максимальной продукцией на конкретной стадии развития сперматогенного эпителия, то есть при взаимодействии с конкретной группой зародышевых клеток. Кластерин максимально продуцируется клетками Сертоли, когда сперматогенный эпителий находится на VII или VIII стадии развития, то есть независимо от стимуляции FSH, что наводит на мысль о местной регуляции секреторной функции клеток Сертоли зародышевыми клетками.
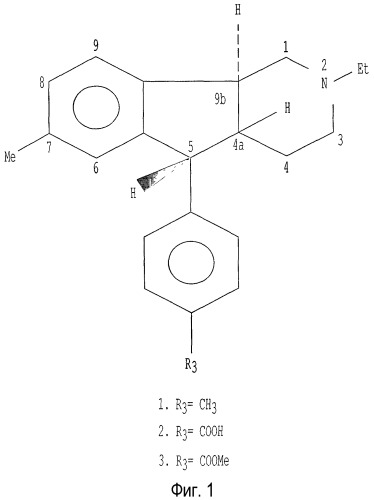
Показано, что гексагидроинденопиридиновое соединение №20-438, разработанное Sandoz, Ltd. (соединение 1 на фиг.1), обратимо ингибирует сперматогенез при пероральном введении животным. См. Arch. Toxicol. Suppl., 1984, 7:171-173; Arch. Toxicol. Suppl., 1978, 1:323-326; и Mutation Research, 1979, 66:113-127.
Синтез различных инденопиридиновых соединений в виде рацемических смесей известен и описан, например, в патентах США №№2470108, 2470109, 2546652, 3627773, 3678057, 3462443, 3408353, 3497517, 3574686, 3678058 и 3991060. Указанные инденопиридиновые соединения имеют различные применения, включая применение в качестве обладающих противовоспалительными и обезболивающими свойствами антагонистов серотонина, ингибиторов агрегации тромбоцитов, седативных препаратов и нейролептиков, а также в качестве противоязвенных, гипотензивных и анорексигенных соединений.
В патентах США №№5319084 и 5952336 описаны обладающие антисперматогенным действием гексагидроинденопиридиновые соединения, в которых в 5-м положении в качестве заместителя содержится фенольное кольцо, содержащее заместитель в пара-положении.
Несмотря на обширные исследования в этой области по-прежнему существует необходимость в эффективных противозачаточных средствах для мужчин, обладающих обратимым действием и ограниченными побочными эффектами. Сохраняющейся проблемой является введение известных соединений в дозах, которые могут вызывать побочные эффекты. Дополнительной проблемой в этой области является отсутствие подходящих контрастных агентов, обладающих специфическими участками связывания в яичках. По-прежнему существует необходимость в соединениях, которые могут применяться в качестве контрастных агентов при изучении функции яичек и для диагностики дисфункции яичек.
В дополнение к пероральным противозачаточным средствам для мужчин необходимы более эффективные композиции для использования в качестве обычно применяемых методик местной/внешней контрацепции.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Соответственно настоящее изобретение относится к пероральному противозачаточному средству для мужчин, которое не влияет на половое влечение, обладает высокой эффективностью и активностью, и обладает минимальными побочными эффектами и токсичностью.
Настоящее изобретение также относится к пероральному противозачаточному средству для мужчин, которое ингибирует сперматогенез, и к способу ингибирования сперматогенеза с применением этого средства.
Кроме того, настоящее изобретение относится к композиции, которая действует в качестве спермицида, нейтрализуя подвижные сперматозоиды, и является, таким образом, эффективной в качестве противозачаточного средства для наружного применения.
Настоящее изобретение дополнительно относится к композиции, которая действует в качестве противогрибковой композиции.
Эти и другие цели настоящего изобретения были достигнуты благодаря созданию гексагидроинденопиридиновых соединений по настоящему изобретению и обнаружения, что эти соединения являются высокоэффективными, нарушают сперматогенез и действуют в качестве спермицида на подвижные сперматозоиды и обладают эффективным противогрибковым действием.
Соединения по настоящему изобретению решают указанные выше задачи. Соединения по настоящему изобретению являются высокоэффективными в дозах, меньших по сравнению с соединением 1, и снижают случаи возникновения побочных эффектов, таких как седативные эффекты, наблюдаемые для соединения 1. Кроме того, соединения по настоящему изобретению взаимодействуют с макромолекулярным участком яичек. Применение соединений по настоящему изобретению, которые содержат метку, такую как радиоактивная метка, решает проблему несовершенных контрастных агентов, предлагая контрастный агент, применимый для изучения функции яичек и при диагностике дисфункции яичек. Также было обнаружено, что соединения по настоящему изобретению действуют в качестве спермицидного средства, чрезвычайно эффективно и действенно нейтрализуя подвижные сперматозоиды, что предполагает применение этих соединений в составе различных спермицидных композиций. Также обнаружено, что соединения по настоящему изобретению обладают противогрибковым действием.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фигуре 1 представлена структура трех гексагидроинденопиридиновых соединений и указана система нумерации атомов в этих соединений.
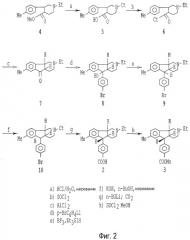
На фигуре 2 представлен процесс получения предшественников соединений по настоящему изобретению.
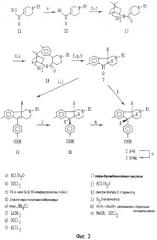
На фигуре 3 представлена схема энантиоселективного синтеза предшественников соединений по настоящему изобретению.
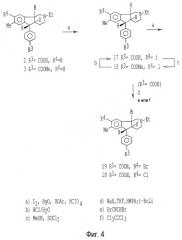
На фигуре 4 представлена схема йодирования предшественников, полученных, как представлено на фиг.2 и 3, и схема преобразования йодированных соединений в дополнительные соединения, подпадающие под объем настоящего изобретения.
ПОДРОБНОЕ ОПИСАНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Было обнаружено, что гексагидроинденопиридиновые соединения, имеющие представленную ниже структуру I(a), и предпочтительно имеющие представленную ниже структуру I(b):
где атомы водорода в положениях 4a, 5 и 9b имеют представленную относительную стереохимию (атомы водорода в положениях 4a и 5 находятся в транс-положении относительно друг друга, и атомы водорода в положениях 4a и 9b находятся в цис-положении относительно друг друга; формула I(b)); или относительная стереохимия в положении 9b может быть обращена таким образом, что атомы водорода в положениях 4a и 5 находятся в транс-положении относительно друг друга, и атомы водорода в положениях 4a и 9b находятся в транс-положении относительно друг друга; или все три атома водорода могут находиться в цис-положении относительно друг друга; или
где пунктирная линия между 4a и 5 показывает, что соединение может также являться 4a,5-дегидросоединением, образуя, таким образом, двойную связь между атомами углерода в положениях 4a и 5, и где R1 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью, предпочтительно C1-3-алкил или C3-C8-циклоалкил; R2 представляет собой атом водорода или С1-6-алкил с неразветвленной или разветвленной цепью, предпочтительно C1-3-алкил, R3 и R5 независимо представляют собой атом водорода, атом галогена, SO3H, С1-6-алкил с неразветвленной или разветвленной цепью, CH2OH, CH2OMe, С1-6-алкоксигруппу с неразветвленной или разветвленной цепью, карбоксил (COOH) или группу, которая в физиологических условиях организма млекопитающих может быть преобразована в карбоксильную группу, эфир карбоновой кислоты (COOR, где R представляет собой С1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметиловый эфир (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атом галогена; и R4 представляет собой атом водорода, атом галогена, R3Si или COR,
являются не только антисперматогенными и при пероральном применении обладают приблизительно в 40 раз большей антисперматогенной активностью, чем описанные ранее в патенте США №5319084 соединения, но также действуют в качестве нейтрализующего подвижные сперматозоиды спермицида, а также действуют в качестве противогрибкового средства.
Представленный в контексте настоящего изобретения термин «антисперматогенный» относится к способности нарушать продукцию сперматозоидов в яичках, в то время как термин «спермицид» или «спермицидный» относится к способности нейтрализовывать подвижные сперматозоиды после их продукции и более предпочтительно после эякуляции.
Соединения по настоящему изобретению имеют относительную стереохимию, представленную на структуре (I). Настоящее изобретение включает обе энантиомерные формы (по существу оптически чистые), а также любые смеси этих форм, например, рацемическую смесь.
Фармацевтически приемлемые соли соединений, имеющих представленную выше структуру (I), также включены в настоящее изобретение. Фармацевтически приемлемые соли включают без ограничения соли взаимодействия основной функциональной группы (такой как без ограничения аминогруппа) с неорганическими кислотами, такие как гидрохлорид, гидройодид, сульфат, фосфат, дифосфат, гидробромид или нитрат, или соли взаимодействия основной функциональной группы с органическими кислотами, такие как ацетат, малат, малеат, фумарат, тартрат, сукцинат, цитрат, лактат, метансульфонат, пара-толуолсульфонат, пальмоат, салицилат и стеарат; или соли взаимодействия кислотной функциональной группы с ионами металлов, таких как без ограничения Na, K, Ca, или соли взаимодействия кислотной функциональной группы с ионом аммония, или соли взаимодействия кислотной функциональной группы с органическими ионами, такими как без ограничения амины и тетразамещенные ионы аммония.
Заместитель R1 предпочтительно представляет собой алкильную группу с неразветвленной цепью (н-алкильную группу), изоалкильную или циклоалкильную группы, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гексил, изогексил, циклопропил, циклопентил, циклогексил. Наиболее предпочтительно R1 представляет собой этил.
Заместитель R2 также предпочтительно представляет собой алкильную группу с неразветвленной цепью или изоалкильную группу, как описано выше для заместителя R1.
Заместитель R3 предпочтительно находится в пара-положении или в 4-м положении кольца и предпочтительно представляет собой группу, выбираемую из гидроксиметила (CH2OH), формила (CHO), карбоксила (COOH), эфира карбоновой кислоты (COOR, где R представляет собой С1-10-алкил, С6-10-арил, С7-10-аралкил), гидроксиметилового эфира (CH2OC(O)R, где значения R определены выше), CONH2, CONHR, CONR2, CH2OCONHR, CN, CH=NHNHCONH2 и атома галогена.
Заместитель R4 предпочтительно представляет собой атом галогена, включая I, Br, Cl и F. Высокая активность этих соединений является неожиданной. Атом галогена может являться радиоактивным изотопом, например 123I, 125I или 131I. В представленных выше соединениях вместо обычных (нерадиоактивных) изотопов могут использоваться другие радиоактивные изотопы, такие как, например, 11C, тритий (3H) или 18F или радиоактивные изотопы брома и хлора.
Соединение 1 представляет собой рацемическую смесь. Структура соединения 1 представлена на фиг.1. Гексагидроинденопиридины имеют три центра асимметрии, которые могут быть определены по известной номенклатуре. Альтернативно относительная стереохимия может быть определена по цис-транс расположению атомов водорода, связанных с углеродной системой в положениях 4a, 5 и 9b трициклической кольцевой системы, что приводит к стереохимическим перераспределениям. По номенклатуре Кана-Ингольда-Прелога стереохимическими характеристиками и наименованием соединения 1 является (4aRS,5SR,9bRS)-2-этил-2,3,4,4a,5,9b-гексагидро-7-метил-5-(4-метилфенил)-1H-индено[1,2-c]пиридин.
В соединении 1 5-фенильная группа содержит гидрофобный метильный заместитель, соответствующий заместителю R3 в представленной выше структуре (I). Антисперматогенная активность соединения 1 присуща по существу исключительно (+)-изомеру (правовращающему, как измерено в условиях, описанных в Cook et al., 1995), который является эффективным антисперматогенным лекарством у мышей. Антисперматогенная активность других соединений этого ряда также присуща по существу исключительно одному оптическому изомеру. Как известно специалисту в области стереохимии, измеренное оптическое вращение может быть или (+) или (-) в зависимости от схемы замещения и условий измерения. С другой стороны, противогрибковые свойства соединений по настоящему изобретению не являются стереоспецифичными и являются и (+) и (-) активными изомерами, хотя их относительная активность может различаться.
Спермицидная активность соединений по настоящему изобретению была обнаружена у изомеров, обладающих антисперматогенной активностью, и предполагается ее наличие и в других изомерах.
Сильнополярная карбоксильная группа или группы, которые могут быть преобразованы в карбоксильную группу в процессе обмена веществ в физиологических условиях организма млекопитающих, могут находиться в любом положении, предпочтительно в пара-положении, 5-фенильного кольца соединений по настоящему изобретению без потери спермицидной и/или противогрибковой активности. Например, соединения, которые в пара-положении замещены гидроксиметильной (CH2OH), формильной (CHO), карбоксильной (COOH) и метоксикарбонильной (C(O)OCH3) группами, сохраняют высокую активность. Указанные соединения являются активными несмотря на присутствие полярного заместителя в пара-положении 5-фенильного кольца.
Под «преобразованием в процессе обмена веществ в физиологических условиях организма млекопитающих» подразумевают преобразование функциональной группы R3 в карбоксильную группу при введении соединения структуры (I) живому млекопитающему, которому требуется антисперматогенное воздействие. Введение может осуществляться при помощи любых традиционных средств и по любому пути, включая без ограничения пероральный, внутрибрюшинный, внутривенный, подкожный, внутримышечный, ингаляционный, трансбуккальный и чрескожный. Указанные пути введения пригодны для спермицидного и/или противогрибкового воздействия, равно как и для местного введения. Преобразование группы R3 в карбоксильную группу легко определяется путем осуществления контроля содержания метаболитов соединения структуры (I) в крови или в моче. Контроль содержания метаболитов может осуществляться с применением традиционных методов анализа, таких как масс-спектрометрия (MS), газовая хроматография (GC), и так далее.
При введении млекопитающему предпочтительно, по крайней мере, 50%, более предпочтительно, по крайней мере, 80% и, еще более предпочтительно 90%, 95% или 100% функциональных групп R3 преобразуются в процессе обмена веществ в карбоксильные группы, хотя это не является необходимым условием приобретения спермицидных и/или противогрибковых свойств. Процентная доля преобразования может быть определена при помощи одного из указанных выше традиционных методов анализа путем количественного определения в образце крови или мочи отношения содержания соединений, не подвергшихся преобразованию и содержащих функциональную группу R3, к содержанию соединений, в которых эта функциональная группа была преобразована в карбоксильную группу.
Антисперматогенная активность соединения 1 наблюдалась после его однократного перорального введения крысам в дозе 30 мг/кг, резко снижая массу яичек в течение 24 ч. Наблюдались дегенеративные изменения в семенных канальцах. Сперматиды становились пикнотичными, изредка образуя многоядерные слияния. Клетки Сертоли цитологически выглядели нормальными. Судя по всему, соединение 1 целенаправленно действует на сперматиды или на связанные с этими сперматидами клетки Сертоли, так как гистологические изменения наблюдались в первую очередь в этих сперматидах.
Соединение 1 вызывает некоторую заторможенность и седативный эффект у мышей при пероральной дозировке 30 мг/кг и очень сильную заторможенность в той же дозе, введенной подкожно. Заторможенность и седативный эффект, безусловно, являются нежелательными побочными эффектами противозачаточных средств. В отличие от наблюдаемой для соединения 1 заторможенности и седативного эффекта соединения по настоящему изобретению вызывают минимальную заторможенность.
Соединения по настоящему изобретению позволяют отделить противозачаточное действие от седативного действия, наблюдаемого для соединения 1. Поэтому соединения по настоящему изобретению являются эффективными противозачаточными лекарственными средствами, для которых нежелательные побочные эффекты в виде седативного эффекта и заторможенности заметно снижены.
Действие соединений по настоящему изобретению на сперматогенез было протестировано на мышах через трое суток после перорального однократного введения по приведенной ниже методике, описанной Cook et al (1995). Было показано, что соединения, проявившие активность в этом тесте, также являются противозачаточными средствами.
Антисперматогенная активность соединений проверялась путем принудительного введения самцам мышей на 1-е сутки выступающего в качестве контроля растворителя, соединения 1 (положительный контроль) или соединения по настоящему изобретению. Через 72 ч после введения животных убивали, оперативно удаляли яички, очищали их от жира и взвешивали. Одно яичко исследовали гистологически и определяли сперматогенный потенциал с применением «сперматогенного индекса» (J.M.Whitsett, P.F.Noden, J.Cherry and A.D.Lawton, J.Reprod. Fertil., 72, 277 (1984)), который представляет собой полуколичественную оценку способности яичек продуцировать сперматозоиды. Индекс основан на гистологическом выявлении сперматогенных клеток в семенных канальцах. Применяется шкала от 1 до 6, при этом нормальное значение составляет 5-6. Вторая оценка основывалась на массе яичек.
В таблицах 1 и 2 представлены соответствующие биологические результаты, отражающие изменение массы яичек (TW) и сперматогенного индекса (SI) относительно контроля, содержащего только вводимый растворитель без инденопиридина. В таблицах 1 и 2 значения заместителей R3 и R4 относятся к структуре Ib, где R3 находится в пара-положении; R1 представляет собой этил; R2 представляет собой метил; и R5 представляет собой атом водорода.
При наличии 8-йод-7-метил-4'-карбокси-заместителя или 4'-карбометокси-заместителя вводимая перорально доза 2 мкмоль/кг (1 мг/кг) рацемата приводила к снижению сперматогенного индекса на 57-67% и была, по крайней мере, также эффективна, как и доза 79 мкмоль/кг (30 мг/кг) соответствующего аналога без 8-йод-заместителя. В случае 8-бром-аналога или 8-хлор-аналога наименьшая протестированная доза (6 или 2 мкмоль/кг; 3 или 1 мг/кг) была, по крайней мере, также эффективна, как и доза 79 мкмоль/кг (30 мг/кг) негалогенированного аналога (см. таблицу 1). Сравнение активного левовращающего энантиомера 8-йод-7-метил-4'-карбометокси-аналога с активным энантиомером 8-H-7-метил-4'-карбометокси-аналога (таблица 2) показало, что первое соединение в дозе 0,6 и 2 мкмоль/кг (0,3 и 1 мг/кг) обладает тем же или большим эффектом, что и последнее соединение в дозе 25 и 75 мкмоль/кг (10 и 30 мг/кг). Таким образом, путем введения атома галогена в 8-е положение достигается приблизительно 40-кратное увеличение молярной эффективности.
| Таблица 1Антисперматогенный эффект рацемической смеси инденопиридиновых соединений на взрослых самцах мышей линии SWISSa | |||||
| Соединение | R3 | R4 | Доза (мг/кг) | Изменение TWb (%) | Изменение SIc (%) |
| 1 | Me | H | 30 | 19%* | -55%* |
| 2 | СО2H | H | 10 | 2% | -24%* |
| 2 | СО2H | H | 30 | -7% | -52%* |
| 18 | СО2Ме | I | 1 | -16% | -57%* |
| 18 | СО2Ме | I | 3 | -27%* | -69%* |
| 18 | СО2Ме | I | 10 | -36%* | -74%* |
| 17 | СО2Н | I | 1 | -18% | -67%* |
| 17 | СО2Н | I | 3 | -9% | -66%* |
| 17 | СО2Н | I | 10 | -32%* | -76%* |
| 19 | СО2Н | Br | 3 | -8% | -69%* |
| 19 | СО2Н | Br | 10 | -28%* | -71%* |
| 19 | СО2Н | Br | 30 | -39%* | -72%* |
| 20 | СО2Н | Cl | 1 | -16% | -55%* |
| 20 | СО2Н | Cl | 3 | -23% | -66%* |
| 20 | СО2Н | Cl | 10 | -22% | -72%* |
| aВеличины рассчитывали исходя из средних значений (n=5) как [100(тестовый контроль)/контроль]. |
Для неактивных соединений представлена только наибольшая доза.
Мышам принудительно вводили инденопиридин или растворитель в дозе 10 мл/кг.
Растворитель содержал 90% воды, 7% Tween 20 и 3% этанола.
Некропсию проводили на 3-и сутки, спустя приблизительно 72 ч после введения дозы.
bМасса яичек [% изменения относительно значения контроля с введением растворителя, равного 217,8±46,0 (S.E.) мг]
cСперматогенный индекс [% изменения относительно значения контроля с введением растворителя, равного 5,8±0,2 (S.E.)]
*Значимое различие относительно значения контроля с введением растворителя; односторонний критерий по Dunnett, p<0,05.
Статистический анализ проводили на необработанных данных перед пересчетом в % изменения.
| Таблица 2Эффект введения атома йода в 8-е положение на сперматогенный эффект хиральных инденопиридиновых соединений на взрослых самцах мышей линии SWISSa (соединение 1 представляет собой рацемическую смесь; соединения 3 и 18 представляют собой левовращающие изомеры) | |||||
| Соединение | R3 | R4 | Доза (мг/кг) | Изменение TWb (%) | Изменение SIc (%) |
| 1 | Me | Н | 30d | -24%* | -61%* |
| 3(l) | CO2Ме | Н | 1 | 8% | 3% |
| 3(l) | CO2Ме | Н | 3 | -12% | -2% |
| 3(l) | CO2Ме | Н | 10е | -13% | -33%* |
| 3(l) | CO2Ме | Н | 30 | -30%* | -64%* |
| 18(l) | СО2Ме | I | 0,3 | -11%* | -34%* |
| 18(l) | CO2Ме | I | 1 | -21%* | -66%* |
| 18(l) | CO2Ме | I | 3 | -27%* | -71%* |
| 18(l) | CO2Ме | I | 10е | -31%* | -72%* |
| aВеличины рассчитывали исходя из средних значений (n=5) как [100(тестовый контроль)/контроль]. |
Мышам принудительно вводили инденопиридин или растворитель в дозе 10 мл/кг.
Некропсию проводили на 3-и сутки, спустя приблизительно 72 ч после введения дозы.
Растворитель представлял собой 1% Tween 20 в воде.
bМасса яичек [% изменения относительно значения контроля с введением растворителя, равного 227,5±8,6 мг]
cСперматогенный индекс [% изменения относительно значения контроля с введением растворителя, равного 5,7±0,2]
dn=6.
en=4.
*Значимое различие относительно значения контроля с введением растворителя; односторонний критерий по Dunnett, p<0,05.
Статистический анализ проводили на необработанных данных перед пересчетом в % изменения.
Спермицидная активность соединений по настоящему изобретению представлена в значительной степени только при однократном добавлении композиции к эякуляту, причем добавление композиции, содержащей лишь 3 мкМ соединения по настоящему изобретению, приводило к значительному подавлению подвижности сперматозоидов, а после добавления композиции, содержащей лишь 100 мкМ соединения по настоящему изобретению, подвижность сперматозоидов снижалась до нуля. Спермицидная композиция по настоящему изобретению может содержать соединение по настоящему изобретению в любой концентрации, достаточной для снижения подвижности сперматозоидов до уровня, не способного вызвать беременность, предпочтительно в концентрации 1-500 мкМ, более предпочтительно 3-300 мкМ, наиболее предпочтительно 10-200 мкМ. Спермицидную активность определяли по способу, описанному ниже.
Способ определения прямого эффекта агента на подвижность сперматозоидов
Прямой эффект агента на подвижность сперматозоидов определяли, используя следующие протоколы. В основном сперматозоиды получали либо из хвоста придатка яичка крыс, либо из эякулята кроликов, собранного при помощи искусственной вагины. Начальную подвижность сперматозоидов определяли вручную или при помощи анализатора спермы Hamilton Thorn IVOS. Затем сперматозоиды выдерживали при постоянной температуре 34°C, разбавляли до концентрации 10×106/мл и добавляли приблизительно к 3 мл буферного раствора или среды. На этом этапе снова определяли подвижность и регистрировали любое изменение. Затем к препарату сперматозоидов добавляли различные концентрации тестируемого агента. Затем образцы сперматозоидов выдерживали при той же температуре в течение часа и определяли подвижность. Результаты записывали как процент содержания подвижных сперматозоидов в образце.
Протокол определения прямого эффекта агента на подвижность сперматозоидов
Общая информация:
В ходе проведения эксперимента сперматозоиды выдерживали при 34°C. Концентрация сперматозоидов приблизительно составляла 10×106/мл (для достижения данной концентрации, возможно, потребует разбавления препарата буферным раствором или средой).
Для исследования на крысах (применяя сперматозоиды из хвоста придатка яичка):
Получали 1 мМ основной раствор инденопиридина в сбалансированном солевом растворе Хенкса (HBSS-буфер), содержащий бычий сывороточный альбумин (BSA; 5 мг в 10 мл=0,5 мкг/мкл; 0,5 мкг/мл=1 мкМ) и добавляли следующим образом:
1 мкМ=1 мкл основного раствора+949 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
3 мкМ=3 мкл основного раствора+947 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
10 мкМ=10 мкл основного раствора+940 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
30 мкМ=30 мкл основного раствора+920 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
100 мкМ=100 мкл основного раствора+850 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
300 мкМ=300 мкл основного раствора+650 мкл HBSS-буфера+BSA+50 мкл разбавленного раствора сперматозоидов
1000 мкМ=1000 мкл основного раствора+50 мкл разбавленного раствора сперматозоидов
Подвижность сперматозоидов определяли через 1 час.
Для исследований на кроликах (применяя эякулят):
Получали 1 мМ основной раствор инденопиридина в среде М-199, содержащий бычий сывороточный альбумин (BSA; 2,5 мг в 5 мл=0,5 мкг/мкл; 0,5 мкг/мл=1 мкМ) и добавляли следующим образом:
1 мкМ=1 мкл основного раствора+949 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
3 мкМ=3 мкл основного раствора+947 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
10 мкМ=10 мкл основного раствора+940 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
30 мкМ=30 мкл основного раствора+920 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
100 мкМ=100 мкл основного раствора+850 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
300 мкМ=300 мкл основного раствора+650 мкл среды M-199 с BSA+50 мкл разбавленного раствора сперматозоидов
1000 мкМ=1000 мкл основного раствора+50 мкл разбавленного раствора сперматозоидов
Подвижность сперматозоидов определяли через 1 час.
Для определения морфологических изменений получали микроскопические препараты и окрашивали эозином для определения клеточной гибели.
Результаты тестов на спермицидность представлены ниже в таблице 3 (сперматозоиды из эякулята кролика) и таблице 4 (сперматозоиды из хвоста придатка яичка крысы).