Регулирование содержания жира
Иллюстрации
Показать всеНастоящая группа изобретений относится к медицине, а именно к эндокринологии, и касается регулирования содержания жира в организме. Для этого осуществляют стабилизацию альфа субъединицы индуцируемого гипоксией факторного белка (HIFα). Для стабилизации HIFα вводят эффективные количества соединения, ингибирующего активность HIF гидроксилазы. Изобретения обеспечивают уменьшение образования и отложения жира за счет регулирования его метаболизма. 9 н. и 14 з.п. ф-лы, 11 ил.
Реферат
В настоящей заявка заявлен приоритет предварительной патентной заявки США с порядковым номером 60/431351, поданной 6 декабря 2002 года; предварительной патентной заявки США с порядковым номером 60/476331, поданной 6 июня 2003 года; и предварительной патентной заявки США с порядковым номером 60/476726, поданной 6 июня 2003 года, каждая из которых приводится здесь в виде ссылки во всей своей полноте.
Область техники, к которой относится изобретение
Настоящее изобретение относится к гомеостазу и метаболизму жира и регулированию веса тела.
Предпосылки создания изобретения
Ожирение, обычно определяемое в виде показателя массы тела (BMI) с величиной, равной 30 или выше, представляет собой основную проблему здоровья, особенно в индустриально развитых странах. Подсчитано, что в настоящее время ожирению подвержено 250 миллионов человек среди взрослого населения, и ожидается, что это количество существенно возрастет, как только подростки с чрезмерным весом достигнут возраста взрослых людей, страдающих ожирением. Как отмечалось выше, ожирение связывают со многими опасными для здоровья явлениями, включающими повышенный риск развития диабета и болезни сердца. Было показано, в частности, что абдоминальное ожирение, распространение избыточной жировой ткани в абдоминальной области, коррелируются с диабетом, заболеванием сердца, например, метаболическим синдромом. Избыточное содержание жира коррелируется с повышенной возможностью сердечного приступа, инсульта или другого типа сердечно-сосудистого заболевания; высоким давлением крови, высоким содержанием холестерина, диабетом; раком, включая постклимактерический рак молочной железы и рак матки, толстой кишки и почки; артритом, желчно-каменными заболеваниями, апноэ во сне и появлением астмы у взрослых людей. Существует, таким образом, необходимость в данной области в эффективном средстве для регулирования метаболизма жира и осуществимых способах для достижения снижения веса тела и сведения к минимуму опасности развития или прогрессирования сопутствующих состояний.
Ввиду многочисленных опасных состояний, связанных с измененным или нарушенным метаболизмом жира и гомеостазом жира, увеличением частоты ожирения и нерегулируемого увеличения веса, существует необходимость в способах регулирования метаболизма жира. Кроме того, в данной области существует необходимость в способах регулирования веса тела путем регулирования продуцирования, утилизации и накопления жира. Кроме того, в данной области существует необходимость в способах и соединениях для лечения ожирения.
Краткое описание изобретения
Настоящее изобретение относится к способам и соединениям для регулирования метаболизма жира в организме человека, достижения гомеостаза жира, регулирования веса тела, снижения жировых накоплений и индуцирования потери веса у субъекта. Представлены также способы и соединения для лечения или профилактики ожирения, включая ожирение, стимулированное диетой, ожирение, связанное с диабетом, и т.д.
В различных вариантах осуществления настоящего изобретения, субъектом является клетка, ткань или орган. В других вариантах настоящего изобретения субъектом является животное, предпочтительно, млекопитающее, более предпочтительно, человек. Когда субъектом является клетка, в изобретении конкретно рассматривают тот факт, что клетка может быть изолированной клеткой, либо прокариотической или эукариотической клеткой. В случае, когда субъектом является ткань, изобретение конкретно рассматривает и эндогенные ткани, и ткани in vitro, например, ткани, выращенные в культуре. В предпочтительных вариантах, субъектом является животное, в частности, животное млекопитающего вида, включая крысу, кролика, корову, овцу, свинью, мышь, лошадь и вид примата. В наиболее предпочтительном варианте, субъектом является человек.
В настоящем изобретении представлены способы регулирования метаболизма жира у субъекта. В одном из аспектов изобретения, способы настоящего изобретения включают регулирование метаболизма жира у субъекта путем стабилизирования HIFα у субъекта, регулируя таким образом метаболизм жира у субъекта. В различных аспектах изобретения, HIFα представляет собой HIF-1α, HIF-2α или HIF-3α. В предпочтительном аспекте настоящего изобретения, стабилизирование субъединицы HIFα включает введение субъекту эффективного количества соединения, которое ингибирует HIF гидроксилазную активность, таким образом стабилизируя HIFα.
Стабилизацию HIFα можно осуществлять любым из способов, доступных специалисту в данной области, и эта стабилизация может включать использование любого агента, который взаимодействует с HIFα, связывает HIFα, или модифицирует HIFα, или может включать использование факторов, которые взаимодействуют с HIFα, включая, например, ферменты, для которых HIFα является субстратом. В конкретных аспектах, в настоящем изобретении представлено создание конститутивно устойчивого варианта HIFα, например, устойчивых HIF мутеинов и т.д., или полинуклеотида, кодирующего такой вариант. В другом аспекте, в настоящем изобретении рассматривают тот факт, что стабилизирование HIFα включает введение агента, который стабилизирует HIFα. Агент может состоять из полинуклеотидов; полипептидов; антител; других белков; углеводов; жиров; липидов и органических и неорганических веществ, например, небольших молекул и т.д. В предпочтительном варианте, в настоящем изобретении представлено стабилизирование HIFα, например, у субъекта путем введения субъекту агента, который стабилизирует HIFα, где агент представляет собой соединение, например, низкомолекулярное соединение и т.д., которое стабилизирует HIFα.
В настоящем изобретении, кроме того, представлены способы регулирования метаболизма жира у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, таким образом, регулируя метаболизм жира у субъекта. В одном из аспектов изобретения, соединение настоящего изобретения представляет собой соединение, которое ингибирует HIF гидроксилазную активность. В предпочтительном аспекте изобретения, соединение настоящего изобретения представляет собой соединение, которое ингибирует HIF пролилгидроксилазную активность. В другом предпочтительном аспекте настоящего изобретения, HIF гидроксилазу выбирают из группы, состоящей из EGLN1, EGLN2 и EGLN3.
В настоящем изобретении, кроме того, представлены способы регулирования процесса метаболизма жира у субъекта путем стабилизирования HIFα у субъекта или путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым регулируя процесс метаболизма жира у субъекта. В различных вариантах настоящего изобретения, процесс метаболизма жира выбирают из группы, состоящей, например, из поглощения жира, транспорта жира, накопления жира, процессинга жира, утилизации жира и синтеза жира.
В конкретных вариантах осуществления настоящего изобретения, представлены способы изменения экспрессии регуляторного фактора жира у субъекта путем стабилизирования HIFα у субъекта или путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым изменяя экспрессию регуляторного фактора жира у субъекта.
В одном из вариантов осуществления настоящего изобретения, представлен способ увеличения экспрессии регуляторного фактора жира у субъекта путем стабилизирования HIFα у субъекта или путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым увеличивая экспрессию регуляторного фактора жира у субъекта. В других вариантах осуществления настоящего изобретения, регуляторный фактор жира выбирают из группы, состоящей из лептина, аполипопротеина A-IV, цитозольной ацил-СоА-тиоэстеразы-1, связующего белка инсулиноподобного фактора роста (IGFBP)-1, карнитин-ацетилтрансферазы и PAI-1. В конкретном аспекте настоящего изобретения, увеличение экспрессии регуляторного фактора жира у субъекта представляет собой непрерывное увеличение.
Представлены, кроме того, способы изменения экспрессии адипогенных факторов. В одном из вариантов осуществления изобретения, настоящее изобретение включает способы увеличения экспрессии DEC1/Stra 13 у субъекта, включающие стабилизирование HIFα у субъекта или введение субъекту эффективного количества соединения настоящего изобретения, тем самым уменьшая экспрессию DEC1/Stra 13 у субъекта. В другом варианте осуществления изобретения, представлены способы снижения экспрессии пролифератором пероксисомы активированного рецептора (PPAR)-γ у субъекта, спосо6, включающий стабилизирование HIFα у субъекта или введение субъекту соединения настоящего изобретения, тем самым уменьшая экспрессию (PPAR)-γ у субъекта.
В настоящем изобретении представлены способы достижения гомеостаза жира у субъекта. В одном из аспектов, способы настоящего изобретения включают достижение гомеостаза жира у субъекта, путем стабилизирования HIFα у субъекта, тем самым достигая гомеостаза жира у субъекта. В другом аспекте, способы настоящего изобретения представляют достижение гомеостаза жира у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым достигая гомеостаза жира у субъекта.
В настоящем изобретении представлены способы регулирования веса тела у субъекта. В одном из аспектов, способы настоящего изобретения включают регулирование веса тела у субъекта путем стабилизирования HIFα у субъекта, тем самым регулируя вес тела у субъекта. В другом аспекте, способы настоящего изобретения включают регулирование веса тела у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым регулируя вес тела у субъекта.
В настоящем изобретении представлены способы снижения содержания жира в организме у субъекта. В одном из аспектов, способы настоящего изобретения включают снижение содержания жира в организме у субъекта путем стабилизирования HIFα у субъекта, тем самым достигая снижения содержания жира в организме у субъекта. В другом аспекте, способы настоящего изобретения включают снижение содержания жира в организме у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым снижая содержание жира в организме у субъекта. В различных аспектах настоящего изобретения, жир в организме у субъекта представляет собой накопленный или отложенный жир, и снижение его содержания представляет собой снижение содержания накопленного жира (т.е. жировых накоплений). В других аспектах настоящего изобретения, применяют способы профилактики накопления или отложения жира, например, профилактики увеличения количества накопленного жира. В других аспектах настоящего изобретения, жир в организме у субъекта представляет собой висцеральный жир или абдоминальный жир.
В настоящем изобретении представлены способы индуцирования потери веса у субъекта. В одном из аспектов, способы настоящего изобретения включают индуцирование потери веса у субъекта путем стабилизирования HIFα у субъекта, тем самым индуцируя потерю веса. В другом аспекте, способы настоящего изобретения содержат индуцирование потери веса у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым индуцируя потерю веса. В предпочтительном аспекте изобретения, соединение настоящего изобретения представляет собой соединение, которое ингибирует HIF гидроксилазную активность. В одном из вариантов осуществления настоящего изобретения, представлены способы индуцирования потери веса у субъекта без сопутствующей потери веса мышц. В конкретных вариантах осуществления настоящего изобретения, потеря веса является зависимой от дозы.
В настоящем изобретении представлены способы лечения или профилактики ожирения у субъекта. В одном из аспектов, способы настоящего изобретения включают лечение или профилактику ожирения у субъекта путем стабилизирования HIFα у субъекта, тем самым осуществляя лечение или профилактику ожирения. В другом аспекте, способы настоящего изобретения включают лечение или профилактику ожирения у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым осуществляя лечение или профилактику ожирения. В конкретных аспектах настоящего изобретения предполагается, что ожирение является ожирением, индуцируемым диетой. В других аспектах настоящего изобретения, ожирение ассоциируют с диабетом, например, ожирение как фактор риска развития диабета, или ожирение, которое развивается вместе с прогрессированием заболевания или является результатом прогрессирования заболевания.
В настоящем изобретении представлены способы снижения потребления кислорода у субъекта. В одном из аспектов, способы настоящего изобретения включают снижение потребления кислорода у субъекта путем стабилизирования HIFα у субъекта, тем самым снижая потребление кислорода у субъекта. В другом аспекте, способы настоящего изобретения включают снижение потребления кислорода у субъекта путем введения субъекту эффективного количества соединения настоящего изобретения, тем самым снижая потребление кислорода у субъекта. В конкретных вариантах осуществления настоящего изобретения, способами изобретения снижают потребность кислорода у субъекта. В различных вариантах осуществления настоящего изобретения, субъект представляет собой клетку, ткань, орган, систему, содержащую множество органов, или целый организм, включая животное, предпочтительно, млекопитающее, наиболее предпочтительно, человека. Кроме того, способы настоящего изобретения можно использовать, например, для снижения потребности в кислороде и увеличения метаболической эффективности у клеток, выращенных в культуре.
В одном из вариантов осуществления изобретения, представлены способы генерирования энергии у субъекта в условиях низкого содержания кислорода. В другом варианте осуществления изобретения, представлены способы, индуцирования метаболического сдвига в потреблении кислорода, например, снижения потребления кислорода. Конкретно представлены способы сведения к минимуму потребления кислорода, которые требуются для достижения и поддержания меняющихся уровней напряжения. Эти способы могут быть, в частности, полезными в случаях их применения при повышенных уровнях напряжения, например, атлетических занятиях, физическом напряжении, например, под водой, на большой высоте, в условиях сильного стресса, например, в условиях на поле сражения и т.д.
В указанных выше способах конкретно представлено использование соединения настоящего изобретения. В определенных аспектах изобретения, соединение настоящего изобретения выбирают из группы, состоящей из соединений А, В, С, D, Е, F, G и Н. В одном из аспектов изобретения, соединение представляет собой миметик 2-оксоглутарат-диоксигеназы. В другом аспекте изобретения, миметик 2-оксоглутарат-диоксигеназы представляет собой замещенный гетероциклический карбоксамид. В настоящем изобретении конкретно представлены варианты, в которых замещенный гетероциклический карбоксамид выбирают из группы, состоящей из хинолинов, изохинолинов, фенантролинов, пиридинов, пиримидинов, β-карболинов и т.д.
В различных вариантах осуществления настоящего изобретения, представлены композиции, или лекарственные препараты, или фармацевтические композиции, включающие соединения настоящего изобретения, и способы производства и использования таких композиций, или лекарственных препаратов, или фармацевтических композиций.
В одном из вариантов осуществления изобретения, представлены способы лечения или профилактики состояния, связанного с ухудшенным гомеостазом жира у субъекта исследования, страдающего таким состоянием, способы, включающие стабилизирование HIFα у субъекта или введение субъекту эффективного количества соединения настоящего изобретения, тем самым осуществляя лечение или профилактику развития указанного состояния у субъекта исследования. В различных вариантах осуществления настоящего изобретения, состояние, связанное с ухудшенным гомеостазом жира, представляет собой ожирение, включающее ожирение, индуцированное диетой; генетически индуцированное ожирение; ожирение, которое является результатом определенных терапевтических лечений или развивается в связи с определенными терапевтическими лечениями, например, терапии на основе инсулина и т.д., гиперлипидемии, гиполипидемии, холестеринемии или атеросклероза.
В одном из вариантов осуществления изобретения, представлены способы лечения или профилактики состояния, связанного с ухудшенным метаболизмом жира у субъекта, страдающего таким состоянием, способы, включающие стабилизирование HIFα у субъекта или введение субъекту эффективного количества соединения настоящего изобретения, тем самым осуществляя лечение или профилактику развития указанного состояния у субъекта. В различных вариантах осуществления настоящего изобретения, состояние, связанное с ухудшенным гомеостазом жира, представляет собой ожирение, включающее ожирение, индуцированное диетой; генетически индуцированное ожирение; ожирение, которое является результатом определенных терапевтических лечений или развивается в связи с определенными терапевтическими лечениями, например, терапии на основе инсулина и т.д., гиперлипидемии, гиполипидемии, холестеринемии, атеросклероза и т.д.
Эти и другие варианты осуществления настоящего изобретения будут легко понятны специалистам в данной области в свете раскрываемого здесь ниже описания изобретения.
Краткое описание чертежей
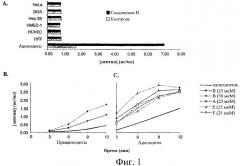
На Фигурах 1А, 1В и 1C показаны уровни лептина в клеточной культурной среде человека после обработки различными соединениями настоящего изобретения. Линии клеток, показанные на чертежах, представляют собой преадипоциты, адипоциты, фибробласты крайней плоти человека (HFF), микрососудистые эндотелиальные клетки человека (НМЕС-1), эндотелиальные клетки пупочной вены человека (HUVEC), клетки гепатоклеточной карционмы человека (Нер 3В), фетальные эпителиальные клетки печени, трансформированные аденовирусом, (293А) и эпителиальные клетки карционмы шейки матки (HeLa).
На Фигурах 2А и 2В показано увеличение экспрессии генов, кодирующих белки, которые принимают участие в метаболизме жира, и распределение генов в печени животных, подвергнутых лечению соединением настоящего изобретения. На Фиг.2А показана экспрессия различных генов, которые принимают участие в метаболизме жира, включая аполипопротеин A-IV, ацил-СоА-тиоэстеразу, карнитин-ацетилтрансферазу и связующий белок инсулиноподобного фактора роста (IGFBP)-1. На Фиг.2В показана экспрессия гена плазминогенного активаторного ингибитора (PAI)-1.
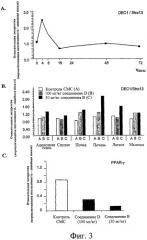
На Фигурах 3А, 3В и 3С показаны изменения экспрессии генов, кодирующих факторы, которые принимают участие в ответной реакции клеток на жирные кислоты и триглицериды. На Фиг.3А показаны изменения экспрессии DEC1/Stra 13 в течение времени после обработки соединением изобретения. На Фиг.3В показано увеличение экспрессии DEC1/Stra 13 в нескольких тканях после обработки. На Фиг.3С показано уменьшение экспрессии пролифератором пероксисомы активированного рецептора (PPAR)-γ после обработки соединениями изобретения.
На Фигурах 4А и 4В показаны изменения веса тела и веса органов у животных, подвергнутых лечению различными дозами соединения настоящего изобретения. На Фиг.4А показано зависимое от дозы замедление увеличения веса тела у животных, подвергнутых лечению соединением изобретения. На фигуре 4В показано, что потеря веса у животных не обусловлена потерей веса мышц и/или жизненных органов, как, например, сердца.
На Фиг.5 показано зависимое от дозы уменьшение содержания висцерального жира у животных, подвергнутых лечению соединением изобретения.
На Фигурах 6А, 6В и 6С показано уменьшение увеличения веса тела и веса абдоминальной жировой ткани у модели животного с ожирением, индуцированным диетой, при лечении соединением изобретения.
На Фигуре 7 показано снижение уровней содержания триглицеридов в сыворотке у модели животного с диабетом при лечении соединением изобретения.
На Фигурах 8А и 8В показана зависимая от дозы стабилизация HIF-1α в клетках, обработанных соединениями изобретения.
На Фигурах 9А и 9В показано индуцирование транспортера-1 глюкозы (GluT-1) и альдолазы в клетках, обработанных соединениями изобретения.
На Фигурах 10А, 10В и 10С показано увеличение экспрессии генов, принимающих участие в регулировании содержания глюкозы в почке, печени и легком, соответственно, у животных, подвергнутых лечению с использованием соединения изобретения.
На Фиг.11 показана ответная реакция на дозу потребления кислорода в клетках аденокарциномы шейки матки (HeLa) и в клетках трансформированной фетальной почки (293А), подвергнутых обработке соединением изобретения.
Описание изобретения
Прежде, чем будут описаны композиции и способы настоящего изобретения, следует понять, что изобретение не ограничивается отдельными методологиями, протоколами, клеточными линиями, анализами и описанными реагентами, так как эти параметры могут изменяться. Следует также понять, что терминология, используемая здесь, предназначается для описания конкретных вариантов применения настоящего изобретения, и никоим образом не предназначается для ограничения объема настоящего изобретения, которое определено в прилагаемой Формуле изобретения.
Следует отметить, что используемые здесь и в прилагаемой Формуле изобретения формы единственного числа включают ссылки на множество, кроме тех случаев, если противоположное в контексте четко не оговорено. Таким образом, например, ссылка на "фрагмент" включает множество таких фрагментов, ссылка на "соединение" представляет собой ссылку на одно или большее количество соединений и его эквиваленты, которые описаны здесь и которые известны специалистам в данной области, и так далее.
Кроме тех случаев, когда противоположное не оговорено, все технические и научные термины, используемые здесь, имеют те же самые значения, которые обычно понимаются специалистом в данной области, к которой изобретение относится. Хотя любые способы и материалы, аналогичные или эквивалентные тем, которые описаны здесь, можно использовать на практике или для тестирования настоящего изобретения, в настоящем случае описываются предпочтительные способы, устройства и материалы. Все приведенные здесь публикации упомянуты здесь в виде ссылки во всей их полноте с целью описания и раскрытия методологий, реагентов и оборудования, представленных в публикациях, которые можно использовать в связи с изобретением. Здесь нет ничего, что могло бы быть истолковано как признание того, что изобретение лишено права предвосхищать такое раскрытие изобретения благодаря предыдущему изобретению.
При практическом применении настоящего изобретения будут использоваться, если не указаны иные, традиционные способы химии, биохимии, молекулярной биологии, клеточной биологии, генетики, иммунологии и фармакологии, в пределах существующих областей наук. Такие технологии описаны подробно в литературе. Смотри, например, Gennaro, A.R., публикация (1990) Remington's Pharmaceutical Sciences, 18-е изд. Mack Publishing Co.; Hardman, J.G., Limbird, L.E. и Gilman, A.G., публикации (2001) The Pharmacological Basis of Therapeutics, 10-е изд., McGraw-Hill Co.; Colowick, S. и соав., публикации. Methods In Enzymology, Academic Press, Inc.; Weir, D.M. и Blackwell, C.C., публикации (1986) Handbook of Experimental Immunology, тома I-IV, Blackwell Scientific Publications; Maniatis, Т. и соав., публикации (1989) Molecular Cloning: A Laboratory Manual (Лабораторный справочник), 2-е издание, тома I-III, Cold Spring Harbor Laboratory Press; Ausubel, F.M. и соав., публикации (1999) Short Protocols in Molecular Biology, 4-e издание, John Wiley & Sons; Ream и соав., публикации (1998) Molecular Biology Techniques: An Intensive Laboratory Course (Интенсивный лабораторный курс), Academic Press; Newton, C.R. и Graham, А., публикации (1997) PCR (Introduction to Biotechniques Serie), 2-е изд. Springer Verlag.
Определения
Термины "регулирование содержания жира" и "регулирование метаболизма жира", как они использованы здесь, относятся к процессам, посредством которых клетка, ткань, орган, система органов или организм в целом достигают и/или поддерживают гомеостаз жира путем изменения, например, усиления или ослабления специфических процессов метаболизма жира. Метаболизм жира охватывают процессы, посредством которых синтезируются, транспортируются, поглощаются, процессируются, утилизируются или накапливаются жиры, такие как триглицериды, жирные кислоты, холестерин, липиды и фосфолипиды. Специфические аспекты метаболизма и регулирования содержания жира включают экспрессию липопротеинов или ферментов, которые облегчают транспорт и перемещение жира в крови и сохранение или секрецию жира клеткой; изменение экспрессии и/или активности ферментов, вовлеченных в утилизацию или образование жира, включающих, например, липолитические и липогененные ферменты, такие как ацилтрансферазы, оксидазы, липоксигеназы и т.д.; и изменение распределения жира в пределах организма, например, в окружающих тканях, жировой ткани и т.д.; или в пределах культуральных жидкостей, включающих, например, внутритканевые (т.е. внеклеточные) и внутриклеточные текучие среды, кровь, мочу и им подобные текучие среды.
Термины "метаболическое состояние" и "метаболическое нарушение" используют взамен друг друга, и они относятся к любому нарушению, связанному с или обострившемуся за счет измененного регулирования содержания жира. Такие нарушения включают, но не ограничиваются ими, атеросклероз, болезнь сердца и ожирение.
Термин "ожирение" относится к избыточному содержанию жира в организме. Ожирение можно оценивать с помощью любого показателя, принятого и используемого специалистами в данной области. Обычно, принятым показателем ожирения является индекс массы тела (BMI), который является показателем веса тела в килограммах по отношению к квадрату высоты в метрах. Обычно для взрослого человека старше 20 лет, величина BMI между около 18,5 и 24,9 считается нормальной, в то время, как величина BMI между около 25,0 и 29,9 рассматривается как избыточный вес, величина BMI, равная или превышающая 30,0, рассматривается как ожирение, а величина BMI, равная или превышающая 40, рассматривается как болезненное ожирение. (Смотри, например, Gallagher и соав. (2000) Am J Clin Nutr 72:694-701.) Эти диапазоны BMI основаны на влиянии веса тела на повышенную опасность заболевания. Некоторые обычные состояния, связанные с избыточным весом и ожирением, включают сердечно-сосудистое заболевание, высокое давление крови, остеоартрит, рак и сахарный диабет. Хотя BMI коррелируется с жиром тела, отношение между ВМ и фактическим жиром тела отличается в зависимости от возраста и пола. Например, женщины с большей вероятностью имеют более высокое процентное содержание телесного жира, чем мужчины при том же самом значении BMI.
Другим показателем ожирения является процентное содержание телесного жира. Приемлемы различные способы для косвенной оценки содержания телесного жира, включая измерение морщинистости кожи, гидроденситометрию, биоэлектрический анализ импеданса (BIA), двухэнергетическую рентгеноспектральную абсорбциометрию, измерение общего содержания калия, и анализ активации нейтронов in vivo. Гидроденситометрия, или гидростатическое взвешивание (HW), определяет общий объем тела путем измерения различий между весом объекта исследования в воде и на воздухе. Аналогично, плетисмография методом вытеснения воздуха (АР) определяет общий объем тела путем измерения уменьшения объема камеры за счет введения объекта исследования в камеру с фиксированным объемом воздуха. Общая плотность тела и состав тела оценивают затем, используя общепринятые уравнения прогноза. С помощью BIA оценивают сопротивление тела, или импеданс, используя падение напряжения, создаваемое слабым электрическим током, проходящим межу электродами. Уровень импеданса, показатель воды и состава электролита тела используют затем для оценки содержания ткани без жира и объема воды в теле, используя усовершенствованные уравнения регрессии. Принимая в расчет гидратационную часть ткани без жира, используют дополнительные уравнения регрессии для оценки массы тела без жира и массы жира. Величина процентного содержания телесного жира у женщин обычно должна составлять около 17-27 процентов, хотя величина вплоть до около 31 процента считается приемлемой. У мужчин величина процентного содержания телесного жира обычно должна составлять около 10-20 процентов, хотя величина вплоть до около 25 процентов считается приемлемой.
Термин "HIFα" относится к альфа субъединице индуцируемого гипоксией факторного белка. HIFα может быть любым белком человека или другого млекопитающего, или его фрагментом, включая человеческие HIF-1α (Genbank, регистрационный № Q16665), HIF-2α (Genbank, регистрационный № AAB41495) и HIF-3α (Genbank, регистрационный № AAD22668); мышиные HIF-1α (Genbank, регистрационный № Q61221), HIF-2α (Genbank, регистрационный № ВАА20130 и ААВ41496) и HIF-3α (Genbank, регистрационный № ААС72734); крысиные HIF-1α (Genbank, регистрационный № САА70701), HIF-2α (Genbank, регистрационный № САВ96612) и HIF-3α (Genbank, регистрационный № САВ96611) и коровьи HIF-1α (Genbank, регистрационный № ВАА78675). HIFα может быть также любым белком немлекопитающего или его фрагментом, включая HIF-1α лягушки (Xenopus laevi) (Genbank, регистрационный № САВ96628), HIF-1α дрозофилы (Drosophila melanogaster) (Genbank, регистрационный № JC4851) и HIF-1α цыпленка (Genbank, регистрационный № ВАА34234). Можно также получать генные последовательности HIFα за счет рутинных технологий клонирования, например, используя всю или часть генной последовательности HIFα, описанной выше, в качестве зонда для обнаружения и определения последовательности гена HIFα в другом виде.
Фрагменты HIFα включают области, устанавливаемые HIF-1α человека от аминокислоты 401 до 603 (Huang и соав., см. выше), от аминокислоты 531 до 575 (Jiang и соав. (1997) J Biol Chem 272:19253-19260), от аминокислоты 556 до 575 (Tanimoto и соав., см. выше), от аминокислоты 557 до 571 (Srinivas и соав. (1999) Biochem Biophys Res Coinmun 260:557-561) и от аминокислоты 556 до 575 (Ivan и соав. (2001) Science 292:464-468). Кроме того, фрагмент HIFα включает любой фрагмент, содержащий, по меньшей мере, один случай присутствия мотива LXXLAP, например, как это имеет место в нативной последовательности HIFα на участке L397TLLAP и L559EMLAP. Кроме того, фрагмент HIFα включает любой фрагмент, сохраняющий, по меньшей мере, одну функциональную или структуральную характеристику HIFα. Например, пептид HIF, используемый в опыте по скрининговому анализу, описанному в Примере 9, может включать последовательность DLDLEMLAPYIPMDDDFQL (SEQ ID N0:1).
Термин "гидроксилаза HIF" относится к любому ферменту, который способен гидроксилировать остаток аминокислоты в белке HIF, конкретно в субъединице HIFα. Предпочтительно, остаток аминокислоты представляет собой остаток пролина и/или остаток аспарагина.
Термин "аспарагинилгидроксилаза HIF" относится к любому ферменту, который способен гидроксилировать остаток аспарагина в белке HIF. Предпочтительно, остаток аспарагина, гидроксилированный аспарагинилгидроксилазой HIF, включает, например, N803 остаток HIF-1α или гомологичный остаток аспарагина в другой изоформе HIFα. Аспарагинилгидроксилаза HIF включает фактор, ингибирующий HIF (FIH), аспарагинилгидроксилазу, ответственную за регулирование трансактивации HIFα (Genbank, регистрационный № AAL27308; Mahon и соав. (2001) Genes Dev 15:2675-2686; Lando и соав. (2002) Science 295:858-861 и Lando и соав. (2002) Genes Dev 16:1466-1471. Также смотри Elkins и соав. (2002) J Biol Chem C200644200).
Термины "пролилгидроксилаза HIF" и "HIF PH" относятся к любому ферменту, который способен гидроксилировать остаток пролина в белке HIF. Предпочтительно, остаток пролина, гидроксилированный пролилгидроксилазой HIF, включает пролин, находящийся в пределах мотива LXXLAP, например, как это имеет место в нативной последовательности HIF-1α человека, соответствующей L397 TLLAP и L559EMLAP. HIF PH включает элементы семейства гена Egl-Nine (EGLN), описанного Taylor (2001, Gene 275:125-132) и охарактеризованного Aravind и Koonin (2001, Genome Biol 2:RESEARCH0007), Epstein и соав. (2001, Cell 107:43-54) и Bruick и McKnight (2001, Science 294:1337-1340). Примеры ферментов пролилгидроксилазы HIF включают человеческий SM-20 (EGLN1) (Genbank, регистрационный № AAG33965; Dupuy и соав. (2000) Genomics 69:348-54), изоформу 1 EGLN2 (Genbank, регистрационный № CAC42510; Taylor, см. выше), изоформу 2 EGLN2 (Genbank, регистрационный № NP_060025) и EGLN3 (Genbank, регистрационный № САС42511; Taylor, см. выше); мышиные EGLN1 (Genbank, регистрационный № САС42515), EGLN2 (Genbank, регистрационный № САС42511) и EGLN3 (SM-20) (Genbank, регистрационный № САС42517) и крысиный SM-20 (Genbank, регистрационный № ААА19321). Кроме того, пролилгидроксилаза HIF может включать генный продукт EGL-9 вида Caenorhabditis elegans (Genbank, регистрационный № AAD56365) и CG1114 вида Drosophila melanogaster (Genbank, регистрационный № AAF52050). Пролилгидроксилаза HIF включает также любой активный фрагмент вышеуказанных полноразмерных белков.
Термин "образец" может относиться к любому материалу, полученному либо прямо, либо косвенно из субъекта. Образцы можно получить или извлечь, например, из жидкостей, секреций, тканей, клеток тела, или из клеток культуры, включающих, но не ограничивающихся ими, слюну, кровь, мочу, сыворотку, плазму, стекловидное тело, синовиальную жидкость, спинномозговую жидкость, околоплодные воды и ткань органов (например, биопсируемую ткань); из хромосом, органелл, или других мембран, выделенных из клетки; из геномных ДНК, кДНК, РНК, мРНК и пр.; и из просветленных клеток или тканей, или блотов, или отпечатков таких клеток, или тканей. Образцы можно извлечь из любого источника, такого как, например, объекта исследования в виде человека, или млекопитающего, не являющегося человеком, и т.д. Подвергаются также изучению образцы, извлеченные из любой модели животного, подверженного заболеванию. Образцы могут находиться в растворе или же могут, например, фиксироваться или связываться с субстратом. Образец может относиться к любому материалу, пригодному для испытания с целью выявления присутствия транскриптов или белков, связанных с регулированием метаболизма; или для измерения уровней содержания жира и глюкозы. Способы для получения таких образцов общеизвестны в данной области.
Термин "субъект" может относиться к выделенным клеткам, либо прокариотическим, либо эукариотическим, или ткани, выращенной в культуре; или, предпочтительно, субъект относится к животным, конкретно, к видам млекопитающего, включая крысу, кролика, корову, овцу, свинью, мышь, лошадь., и примата, конкретно человека.
Изобретение
Настоящее изобретение представляет способы и соединения для регулирования метаболизма жира и достижения гомеостаза жира, а также для лечения и профилактики, а также сведения к минимуму риска развития состояний, связанных с измененным или ухудшенным гомеостазом и метаболизмом жира. Такие состояния включают, но не ограничиваются ими, ожирение и т.д. Представлены также способы и соединения для регулирования уровней содержания накопленного жира; для поддержания или уменьшения веса тела и для регулирования процессинга, поглощения, транспорта, накопления, синтеза, утилизации и распределения жира. В изобретении конкретно представлены способы лечения или профилактики ожирения, например, профилактики или уменьшения увеличения веса и/или индуцирования потери в содержании жира. В одном из аспектов изобретения, это осуществляют путем фармакологического индуцирования метаболического сдвига в направлении использования жира и/или жирных кислот в качестве основного источника энергии для клеток.
Изобретение связано с открытием того, что стабилизация альфа субъединицы индуцируемого гипоксией фактора (HIFα) ведет к снижению отложения жира и что стабилизация HIFα регулирует метаболизм жира. Кроме того, в изобретении представлены способы и соединения, которые снижают образование жировой ткани и отложение жира и эффективно регулируют процессы метаболизма жира, например, транспорт, поглощение, процессинг, утилизацию, накопление жира и т.д.
Индуцируемый гипоксией фактор (HIF) принимает участие в ответной реакции клеток, тканей и органов на снижение содержания кислорода, т.е. на гипоксию. Как известно, воздействие гипоксии, например, на большой высоте, вызывает потерю аппетита и потерю веса (Смотри, например, Fushiki и соав. (1992) Can J Physiol Pha