Вещества и способы для профилактики и лечения опосредованных микроорганизмами эпителиальных нарушений
Иллюстрации
Показать всеГруппа изобретений относится к медицине и может быть использована при лечении или профилактике опосредованных микроорганизмами эпителиальных нарушений, таких как энтерогенный сепсис, ожоги, некротизирующий энтероколит новорожденных и многих других патологических состояний. Для этого в качестве активного агента в способах и фармацевтических композициях, а также при производстве лекарственных препаратов предлагается использовать полиэтиленгликоль со средней молекулярной массой 8000-20000 дальтон. Полиэтиленгликоль именно такой молекулярной массы обеспечивает полное ингибирование проявлений вирулентности микроорганизмов, в том числе Pseudomonas aeruginosa, без их уничтожения с сохранением природной микрофлоры индивидуума. 21 н. и 15 з.п. ф-лы, 8 ил., 1 табл.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к веществам и способам для профилактики или лечения опосредованных микроорганизмами эпителиальных нарушений, таких как энтерогенный сепсис.
ПРЕДПОСЫЛКИ
Опосредованные микроорганизмами эпителиальные нарушения или патологические состояния представляют собой значительную опасность для здоровья человека и животных, налагая нагрузку на системы здравоохранения во всем мире. Один из примеров таких нарушений, энтерогенный сепсис, представляет собой основную причину смертности среди таких организмов, как люди, страдающие любым из множества заболеваний, нарушений или физических недостатков, таких как ожоговые поражения, энтероколиты новорожденных, тяжелая нейтропения, воспалительное заболевание кишечника и отторжение органов после трансплантации. Давно признано, что пространство кишечного тракта является потенциально летальным очагом опосредованного бактериями сепсиса, например, у тяжело больных, госпитализированных пациентов. Способность болезнетворных микроорганизмов, таких как псевдомонады (например, Pseudomonas aeruginosa), нарушать регуляторную функцию кишечного эпителиального барьера может являться определяющей характеристикой условно-патогенных микроорганизмов, способных вызывать энтерогенный сепсис. Во многих случаях данных инфекций в качестве патогенного микроорганизма идентифицировали Pseudomonas aeruginosa. Существенно то, что показано, что кишечный тракт является первичным очагом колонизации условно-патогенными микроорганизмами, такими как P.aeruginosa.
Традиционные терапевтические подходы для профилактики или лечения опосредованных микроорганизмами эпителиальных нарушений, таких как энтерогенный сепсис, не достигают полного успеха. Основанные на антибиотиках способы опасны из-за сложности подбора для кишечных патогенных микроорганизмов антибиотиков в том смысле, чтобы не воздействовать на оставшуюся флору. Кроме того, часто многие кишечные патогенные микроорганизмы, типичным представителем которых является P.aeruginosa, приобретают устойчивость к воздействиям антибиотиков, что приводит к дорогостоящему, длительному и не полностью успешному способу профилактики или лечения. Также затруднения вызывают иммунотерапевтические способы. В частности, многие кишечные микроорганизмы, такие как P.aeruginosa, уклоняются от иммунной системы, делая такие способы минимально эффективными.
Другой способ профилактики или лечения заболеваний, таких как энтерогенный сепсис, представляет собой промывание кишечника. В последние несколько лет предпринимались попытки промывания кишечника с применением растворов полиэтиленгликоля (PEG) при том, что имеется несколько отдельных сообщений, позволяющих предположить, что PEG может в перспективе использоваться для лечения энтерогенного сепсиса при множестве клинических и экспериментальных обстоятельств. Средняя молекулярная масса PEG в данных растворах составляет 3500 дальтон, а растворы доступны коммерчески (например, Golytely). Механизмы, посредством которых данные растворы с относительно низкой молекулярной массой (LMW) PEG оказывают терапевтическое действие при лечении или профилактике энтерогенного сепсиса, не известны. Обычно данные растворы применяют для отмывания или промывания кишечного тракта организмов с риском развития энтерогенного сепсиса или страдающих от него. В результате введения данных растворов PEG LMW в кишечный тракт, в зависимости от способа концентрирования и молекулярной массы применяемых соединений в составе флоры обрабатываемого кишечника происходят непостоянные изменения. Например, растворы с концентрацией PEG более чем приблизительно 20% могут вызывать микробицидное действие, приводя к удалению потенциально защитных микроорганизмов в кишечном тракте подвергнутого стрессу хозяина. Также растворы PEG низкой молекулярной массы, несмотря на их консервацию, могут терять эффективность в ослаблении вирулентной способности определенных микроорганизмов. Следовательно, в данной области существует потребность в растворе, ингибирующем проявление вирулентности микроорганизмами (вредные свойства микроорганизма) без уничтожения микроорганизма или находящихся рядом микроорганизмов, таким образом, обеспечивая эффект сохранения природной экосистемы микрофлоры кишечника. Например, сохранение природного состава флоры могло бы обеспечить конкуренцию с условно-патогенными микроорганизмами, которые в ином случае могут колонизировать кишечник.
Изменение состава флоры сопровождается изменением физиологии организма. Физиологические изменения можно контролировать посредством анализа любого числа характерных видов ферментативной активности, такие как уровни лактатдегидрогеназы. Следовательно, лечение кишечника PEG LMW приводит к значительным изменениям физиологии подвергаемых лечению организмов с непредсказуемыми и, таким образом, потенциально опасными, длительными последствиями для здоровья и хорошего самочувствия подвергаемого лечению организма. Кроме того, такие воздействия провоцируют физически сложные реакции в форме сильного опорожнения кишечника у организмов в критическом состоянии, таких как госпитализированные пациенты.
Таким образом, в данной области остается потребность в композиции, эффективной для профилактики или лечения опосредованного микроорганизмами нарушения (например, энтерогенного сепсиса) и/или симптомов, ассоциированных с таким нарушением, наряду со способами для достижения таких эффектов, без создания возможности для дополнительных осложнений вследствие значительного изменения физиологии подвергаемого лечению организма.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение отвечает указанной выше потребности в данной области посредством предоставления композиции полиэтиленгликоля высокой молекулярной массы (HMW), обеспечивающего эффективную защиту против патологического состояния, характеризующегося эпителиальной поверхностью с риском развития опосредованного микроорганизмами нарушения. Типичные патологические состояния включают в себя энтерогенный сепсис и другие, ассоциированные с кишечной флорой кишечные нарушения/заболевания, обусловленные кишечными патогенными микроорганизмами, включающими в себя в качестве неограничивающих примеров P.aeruginosa. PEG HMW ингибирует или предотвращает контакт таких патогенных микроорганизмов как P.aeruginosa с эпителиальной поверхностью кишечника. Кроме того, PEG высокой молекулярной массы ингибирует проявление вирулентности у данных патогенных микроорганизмов (например, P.aeruginosa), чувствительных к множеству сигналов, которое может включать в себя сети передачи сигнала распознавания кворума. Способность PEG HMW препятствовать инфекционному взаимодействию между кишечным патогенным микроорганизмом и кишечным эпителием обеспечивает альтернативный подход для профилактики или лечения энтерогенного сепсиса, например, после катаболического стресса. Существенно, что лечение PEG HMW могло бы являться рентабельным и относительно простым для осуществления у людей, а также у множества других организмов, таких как значимый с точки зрения сельского хозяйства скот (например, крупный рогатый скот, свиньи, овцы, козы, лошади, куры, индюки, утки, гуси и т.п.), домашние животные и животные в зоопарке.
В одном аспекте данное изобретение относится к способу уменьшения вероятности смертности животного с аномальным состоянием, включающим в себя патологическое состояние, включающее в себя эпителиальную поверхность с риском развития опосредованного микроорганизмами нарушения, выбранного из группы, состоящей из энтерогенного сепсиса, ожогового повреждения, некротизирующего энтероколита новорожденных, тяжелой нейтропении, токсического колита, воспалительного заболевания кишечника, энтеропатии, отторжения трансплантата, резервуарного илеита и вздутого живота, предусматривающий введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Соответствующие животные включают в себя в качестве неограничивающих примеров собаку, кошку, овцу, козу, корову, свинью и человека. В указанном выше способе средняя молекулярная масса PEG предпочтительно составляет, по меньшей мере, 15000 дальтон, и предпочтительно представляет собой от 5000 до 20000 дальтон или от 15000 до 20000 дальтон. Также предпочтительным является PEG со средней молекулярной массой 6000, 7000, 8000, 9000, 10000, 11000, 12000 13000, 14000 и 25000 дальтон. Кроме того, PEG может находиться в водном растворе, содержащем 5-20% PEG, а предпочтительно - 10-20% PEG (например, 10% PEG). В одном осуществлении способа состояние связано с присутствием в кишечнике микроорганизма Pseudomonas aeruginosa и целостность клеточной мембраны такой P.aeruginosa заметно не изменена. В другом осуществлении способа заметно не изменен характер роста.
В другом аспекте настоящее изобретение представляет собой способ ингибирования энтерогенного сепсиса, включающий в себя контакт эпителия млекопитающего, такого как кишечник, с полиэтиленгликолем (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, а предпочтительно, по меньшей мере, 15000 дальтон. В одном осуществлении данного способа кишечник млекопитающего контактирует с PEG в течение, по меньшей мере, 30 минут.
Дополнительные аспекты изобретения включают в себя способ ингибирования экспрессии лектина/адгезина PA-I у патогенного микроорганизма эпителия, например кишечного патогенного микроорганизма, где способ включает в себя введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля; способ ингибирования индуцируемой эпителием (например, индуцируемой кишечным эпителием) активации лектина/адгезина PA-I, включающий в себя введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля; способ ингибирования индуцированного C4-HSL морфологического изменения патогенного микроорганизма эпителия (например, кишечного патогенного микроорганизма), включающий в себя введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля; способ уменьшения проявления вирулентности у патогенного микроорганизма эпителия (например, кишечного патогенного микроорганизма), включающий в себя введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля; способ уменьшения или предотвращения взаимодействия эпителиальной поверхности с фактором вирулентности микроорганизма, включающий в себя введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля; способ улучшения патогенетического процесса в эпителии (например, кишечном), посредством предотвращения активации патогенного распознавания кворума, включающий в себя введение нуждающемуся в этом животному эффективной дозы полиэтиленгликоля; и способ ингибирования взаимодействия между эпителием (например, кишечным эпителием) позвоночного и бактерией, такой как псевдомонада (например, Pseudomonas aeruginosa), включающий в себя контакт эпителия с полиэтиленгликолем. Во всех данных аспектах изобретения средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, а предпочтительно, по меньшей мере, 15000 дальтон.
Еще один дополнительный аспект изобретения представляет собой способ препятствия индуцированному Pseudomonas aeruginosa снижению трансэпителиального электрического сопротивления эпителиального слоя млекопитающих, такого как кишечный эпителиальный слой, где способ включает в себя контакт (кишечного) эпителиального слоя с полиэтиленгликолем, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, а предпочтительно, по меньшей мере, 15000 дальтон. Предпочтительно средняя молекулярная масса PEG составляет от 15000 до 20000 дальтон. В предпочтительном осуществлении целостность мембраны микроорганизма (например, P.aeruginosa) заметно не изменена.
Еще один аспект изобретения представляет собой способ ингибирования прикрепления бактериальной клетки к эпителию млекопитающего, такому как кишечник млекопитающего, где способ включает в себя контакт кишечника с полиэтиленгликолем, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, а предпочтительно, по меньшей мере, 15000 дальтон. В данном способе также предпочтительно, чтобы средняя молекулярная масса PEG составляла от 15000 до 20000 дальтон. PEG может находиться в водном растворе, содержащем 5-20% PEG, а предпочтительно - 5-10% PEG. Типичная бактериальная клетка, прикрепление которой рассматривают, как подлежащее ингибированию данным способом, представляет собой псевдомонаду, такую как P.aeruginosa.
Другой аспект изобретения представляет собой способ уменьшения экспрессии на бактериальной клетке лектина/адгезина PA-I, включающий в себя контакт бактериальной клетки с полиэтиленгликолем, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, а предпочтительно - 15000 дальтон, и предпочтительно составляет от 15000 до 20000 дальтон. Кроме того, PEG может находиться в водном растворе, содержащем 5-20% PEG, а предпочтительно - 5-10% PEG.
В другом аспекте изобретение относится к способу уменьшения вероятности смертности животного с опосредованным микроорганизмами эпителиальным нарушением, выбранным из группы, состоящей из энтерогенного сепсиса, ожогового повреждения, некротизирующего энтероколита новорожденных (NEC), тяжелой нейтропении, токсического колита, воспалительного заболевания кишечника, энтеропатии (например, у тяжелобольных), отторжения трансплантата, резервуарного илеита и вздутого живота, где способ включает в себя введение эффективного количества соединения (например, PEG), прилипающего к клетке, выбранной из группы, состоящей из эпителиальной клетки кишечника млекопитающего и бактериальной клетки кишечника, где соединение прилипает к клетке топографически ассиметричным образом, таким образом, ингибируя взаимодействие эпителиальной клетки кишечника млекопитающего и бактериальной клетки. Предпочтительное соединение представляет собой поверхностно-активное вещество. В одном осуществлении данного способа соединение представляет собой PEG, с молекулярной массой, по меньшей мере, 15000 дальтон. В другом осуществлении данного способа ингибирование определяют посредством атомно-силовой микроскопии. В еще одном осуществлении данного способа бактериальная клетка представляет собой кишечный патогенный микроорганизм, и нет детектируемого изменения характеристик его роста. В связанных аспектах данный способ дополнительно включает в себя введение в кишечник животного эффективного количества декстрана и/или введение в кишечник животного эффективного количества L-глутамина, покрытого декстраном L-глутамина, покрытого декстраном инулина, покрытой декстраном масляной кислоты, одного или несколько фруктоолигосахаридов, N-ацетил-D-галактозамина, покрытой декстраном маннозы и галактозы, лактулозы и уравновешивающих буферов и стабилизирующих средств, известных в данной области. Когда введение проводят совместно в виде одной композиции, данное многокомпонентное введение в одном растворе очищает кишечный тракт и подготавливает к противостоянию нарушению кишечной флоры и барьерной функции кишечника, так как происходит после тяжелых стрессов катаболического, хирургического и травматического характера.
Другой аспект изобретения представляет собой способ улучшения симптомов, связанных с любым заболеванием или состоянием, возникающим вследствие аномального состояния эпителия или характеризующихся им, таким как энтерогенный сепсис, где способ включает в себя введение в кишечник полиэтиленгликоля, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, предпочтительно - по меньшей мере, 15000 дальтон, и предпочтительно составляет от 15000 до 20000 дальтон. PEG может находиться в водном растворе, содержащем 5-20% PEG, а предпочтительно - 5-10% PEG. Изобретение относится к улучшению симптомов, связанных с любым описанным здесь заболеванием или состоянием.
Еще один аспект изобретения представляет собой способ профилактики потери способности к лактации у животного с патологическим состоянием в форме риска развития на эпителиальной поверхности молочной железы опосредованного микроорганизмами нарушения, влияющего на продукцию молока, где способ включает в себя нанесение, например, топически, эффективной дозы полиэтиленгликоля массой, по меньшей мере, 5000 дальтон, а предпочтительно - по меньшей мере, 15000 дальтон, на эпителиальную поверхность молочной железы. Типичные животные включают в себя млекопитающих, таких как овцы, козы, коровы, свиньи, лошади и люди. В связанном аспекте изобретение относится к способу лечения потери способности к лактации у животного, характеризующегося опосредованным микроорганизмами нарушением эпителиальной поверхности молочной железы, влияющим на продукцию молока, где способ включает в себя нанесение, например, топически, эффективной дозы полиэтиленгликоля массой, по меньшей мере, 5000 дальтон, а предпочтительно, по меньшей мере, 15000 дальтон, на молочную железу. В другом связанном аспекте изобретение относится к способу профилактики развития опосредованного микроорганизмами эпителиального нарушения у животного в грудном возрасте, где способ включает в себя введение животному эффективной дозы полиэтиленгликоля массой, по меньшей мере, 5000 дальтон, а предпочтительно, по меньшей мере, 15000 дальтон. Подходящие животные включают в себя млекопитающих, таких как люди, сельскохозяйственный скот, домашние животные и животные в зоопарке. В одном из осуществлений PEG смешивают с любой смесью для питания младенцев, известной в данной области.
Связанный аспект изобретения представляет собой композицию, содержащую смесь для питания младенцев и полиэтиленгликоль (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Кроме того, можно применять любую смесь для питания младенцев, известную в данной области, включая сюда смеси, основанные на молоке животных, таком как коровье молоко, козье молоко и т.п., а также смеси, основанные на соевом молоке. Смесь также можно обогащать любым витамином и/или элементом, включая сюда добавление железа. Средняя молекулярная масса PEG составляет, по меньшей мере, 15000 дальтон, и он предпочтительно находится в диапазоне 5-20% после восстановления влагосодержания или гидратации смеси для питания младенцев или детей младшего возраста. Кроме того, изобретение относится к способу предоставления питания для животного, предпочтительно в грудном возрасте, где способ включает в себя введение животному эффективной дозы композиции, состоящей из смеси для питания младенцев и PEG.
Еще один аспект изобретения представляет собой фармацевтическую композицию, содержащую полиэтиленгликоль со средней молекулярной массой, по меньшей мере, 5000 дальтон, а предпочтительно - 15000 дальтон, и пригодный адъювант, носитель или разбавитель. В связанном аспекте композиция дополнительно включает в себя соединение, выбранное из группы, состоящей из покрытого декстраном L-глютамина, покрытого декстраном инулина, покрытой декстраном масляной кислоты, одного или нескольких фруктоолигосахаридов, N-ацетил-D-галактозамина, покрытой декстраном маннозы и галактозы, лактулозы и уравновешивающих буферов и стабилизирующих средств, известных в данной области.
Дополнительный аспект изобретения представляет собой набор для терапевтического лечения или профилактики патологического состояния, характеризующегося эпителиальной поверхностью с риском развития опосредованного микроорганизмами нарушения, такого как энтерогенный сепсис, где набор содержит одну из описанных выше фармацевтических композиций и протокол, описывающий применение композиции для терапевтического лечения или профилактики патологического состояния. Пригодные для включения в набор протоколы описывают любой один из описанных здесь терапевтических или профилактических способов.
Другие аспекты изобретения относятся к способам профилактики патологического состояния, характеризующегося эпителиальной поверхностью с риском развития опосредованного микроорганизмами нарушения, включая сюда заболевания. Например, изобретение относится к способу профилактики заболевания или патологического состояния, где способ включает в себя введение животному композиции, содержащей эффективную дозу полиэтиленгликоля (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Подходящее заболевание или патологическое состояние, подлежащее воздействию профилактическими способами по изобретению, выбрано из группы, состоящей из "уха пловца", острого отита среднего уха, хронического отита среднего уха, ассоциированной с вентиляторами пневмонии, энтерогенного сепсиса, некротизирующего энтероколита, индуцированной антибиотиками диареи, псевдомембранозного колита, воспалительного заболевания кишечника, синдрома раздраженной кишки, нейтропенического энтероколита, панкреатита, синдрома хронической усталости, синдрома дисбиоза, микроскопического колита, хронической инфекции мочевыводящих путей, передающегося половым путем заболевания и инфекции. Животное, подходящее в качестве субъекта для таких профилактических способов, выбрано из группы, состоящей из собаки, кошки, овцы, козы, коровы, свиньи, курицы, лошади и человека. Предпочтительно средняя молекулярная масса PEG составляет, по меньшей мере, 15000 дальтон; также предпочтителен PEG со средней молекулярной массой от 15000 до 20000 дальтон. Кроме того, PEG может находиться в водном растворе, содержащем 10-20% PEG, а предпочтительно - 10% PEG. Композиция для введения также может дополнительно содержать носитель, выбранный из группы, состоящей из жидкого раствора, топического геля и раствора, пригодного для распыления. Кроме того, композиция может дополнительно содержать вещество, выбранное из группы, состоящей из покрытого декстраном L-глутамина, покрытого декстраном инулина, покрытой декстраном масляной кислоты, фруктоолигосахарида, N-ацетил-D-галактозамина, покрытой декстраном маннозы, галактозы и лактулозы. В одном из осуществлений композиция содержит PEG, покрытый декстраном L-глутамин, покрытый декстраном инулин, покрытую декстраном масляную кислоту, фруктоолигосахарид, N-ацетил-D-галактозамин, покрытую декстраном маннозу, галактозу и лактулозу.
Еще один аспект изобретения представляет собой способ профилактики кожной инфекции, включающий в себя стадию применения для животного композиции, содержащей эффективное количество полиэтиленгликоля (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Композиция дополнительно может содержать носитель, выбранный из группы, состоящей из мази, крема, геля или лосьона. В изобретении полагают, что возбудитель, вызывающий инфекцию, выбран из группы, состоящей из Bacillus anthracis, вируса оспы, энтеропатогенной E.coli (EPEC), энтерогеморрагической E.coli (EHEC), энтероагрегативной E.coli, (EAEC), Clostridium difficile, ротавируса, Pseudomonas aeruginosa, Serratia marcescens, Klebsiella oxytocia, Enterobacteria cloacae, Candida albicans и Candida globrata.
Другой аспект изобретения представляет собой способ профилактики респираторной инфекции, включающий в себя стадию введения животному эффективного количества полиэтиленгликоля (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Респираторная инфекция, подлежащая воздействию профилактическими способами по изобретению, может возникать вследствие контакта с возбудителем инфекции посредством известного в данной области маршрута, включая сюда пневмонии, ассоциированные с вентиляторами (например, ассоциированная с вентиляторами пневмония), переносимые по воздуху возбудители инфекции, возбудители инфекции рассеянные в распыленной жидкости, такой как чихание и т.п. В некоторых осуществлениях способ позволяет предотвращать респираторную инфекцию, вызванную возбудителями, выбранными из группы, состоящей из Bacillus anthracis и вируса оспы.
Еще один аспект изобретения представляет собой способ орошения, по меньшей мере, части мочевыводящих путей для профилактики хронической инфекции мочевыводящих путей, где способ включает в себя стадию введения в мочеиспускательный канал эффективного количества композиции, содержащей PEG, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. В одном из осуществлений композицию вводят в часть мочеиспускательных путей, включающую, по меньшей мере, мочевой пузырь.
Другой аспект изобретения представляет собой способ профилактики передающегося половым путем заболевания, где способ включает в себя стадию нанесения полиэтиленгликоля на презерватив, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Связанный аспект изобретения представляет собой презерватив, содержащий, по меньшей мере, частичное покрытие PEG со средней молекулярной массой, по меньшей мере, 5000 дальтон. Еще один связанный аспект изобретения представляет собой набор, содержащий презерватив и полиэтиленгликоль (PEG) со средней молекулярной массой, по меньшей мере, 5000 дальтон.
Изобретение также относится к способу профилактики нарушения желудочно-кишечного тракта, где способ включает в себя введение нуждающемуся в этом животному эффективной дозы композиции, содержащей полиэтиленгликоль (PEG), где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон. Типичные нарушения желудочно-кишечного тракта, подлежащие воздействию профилактическими способами по изобретению, можно выбрать из группы, состоящей из некротизирующего энтероколита новорожденных, индуцированной антибиотиками диареи, псевдомембранозного колита, воспалительного заболевания кишечника, синдрома раздраженной кишки, нейтропенического энтероколита, панкреатита, синдрома дисбиоза и микроскопического колита.
Другой аспект изобретения представляет собой способ мониторинга введения полиэтиленгликоля (PEG) нуждающемуся в этом животному, где способ включает в себя введение нуждающемуся в этом животному эффективного количества композиции, содержащей меченый PEG, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, и детекцию меченого PEG, посредством чего количество и/или локализация меченого PEG (например, связанного с микроорганизмом) предоставляет информацию, пригодную для оценки эффективности введения. В одном осуществлении способа мониторинга метка представляет собой флуорофор (например, флуоресцеин, родамин, Cy3, Cy5). В другом осуществлении способа детекция меченого PEG включает в себя эндоскопическое обследование. В способе мониторинга также предусмотрено, что меченый PEG определяют в образце стула (т.е. комплексы меченого PEG с таким компонентом, как микроорганизм, источником которого является образец стула). Кроме того, способ мониторинга может дополнительно включать в себя введение второй метки, специфичной для микроорганизма и второй вторичной метки. Как применяют в данном контексте, "специфичная" означает, что метка заметно ассоциирует, по меньшей мере, с одним микроорганизмом.
Другой аспект изобретения представляет собой способ для мониторинга введения полиэтиленгликоля (PEG) нуждающемуся в этом животному, где способ включает в себя получения образца у животного, получавшего полиэтиленгликоль, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, приведение образца в контакт с эпителиальной клеткой и измерение прикрепления микроорганизма в образце к эпителиальной клетки, посредством чего количество и/или локализация PEG предоставляет информацию, пригодную для оценки эффективности введения. Измерение можно сопровождать микроскопическим исследованием.
Другой способ мониторинга по изобретению представляет собой способ для мониторинга введения полиэтиленгликоля (PEG) нуждающемуся в этом животному, где способ включает в себя получения образца у животного, получавшего полиэтиленгликоль, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, приведение слоя эпителиальных клеток в контакт с образцом и измерение трансэпителиального электрического сопротивления эпителиального слоя, посредством чего по уменьшенному снижению трансэпителиального электрического сопротивления по сравнению с контрольной величиной измеряют эффективность введения. Контрольная величина может являться внутренней (т.е. измерение TEER перед введением PEG) или внешней (т.е. полученная в других исследованиях величина, которую надежно применять для сравнения).
Еще один способ мониторинга по изобретению представляет собой способ мониторинга введения полиэтиленгликоля (PEG) нуждающемуся в этом животному, где способ включает в себя получение образца у животного, получавшего полиэтиленгликоль, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, выделение из образца микроорганизма и измерения гидрофобности клеточной поверхности микроорганизма, посредством чего гидрофобность микроорганизма в образце предоставляет информацию, пригодную для оценки эффективности введения. Как применяют в данном контексте, "выделение" означает отделение от других компонентов образца (например, от твердого вещества) в степени, достаточной для обеспечения возможности измерения гидрофобности, как понимают в данной области.
Связанный аспект изобретения представляет собой набор для мониторинга введения полиэтиленгликоля, содержащий меченый PEG и протокол, описывающий применение меченого PEG для мониторинга его введения. Пригодные протоколы включают в себя любой из способов, описанных здесь или известных в области, относящейся к введению, доставке или нанесению PEG. В некоторых осуществлениях данного аспекта изобретения набор дополнительно содержит свободную метку.
Еще один способ мониторинга по изобретению представляет собой способ мониторинга введения полиэтиленгликоля (PEG) нуждающемуся в этом животному, где способ включает в себя получение образца у животного, получавшего полиэтиленгликоль, где средняя молекулярная масса PEG составляет, по меньшей мере, 5000 дальтон, и детекцию активности лектина/адгезина PA-I в образце, посредством чего активность лектина/адгезина PA-I предоставляет информацию, пригодную для оценки эффективности введения. В одном осуществлении данного способа лектин/адгезин PA-I детектируют посредством связывания с лектином/адгезином PA-I партнера по связыванию, такого, как любое из известных специфичных антител против лектина/адгезина PA-I или углевод, с которым лектин/адгезин специфически связывается. Связанный аспект изобретения представляет собой набор для мониторинга введения полиэтиленгликоля (PEG), содержащий партнер по связыванию с лектином/адгезином PA-I и протокол, описывающий применение партнера по связыванию для детекции лектина/адгезина PA-I в образце. Пригодные протоколы включают в себя любой из способов, описанных здесь или известных в области, относящейся к применению PEG.
Другие возможности и преимущества настоящего изобретения будут лучше понятны, исходя из следующего далее подробного описания, включающего в себя рисунки и примеры.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
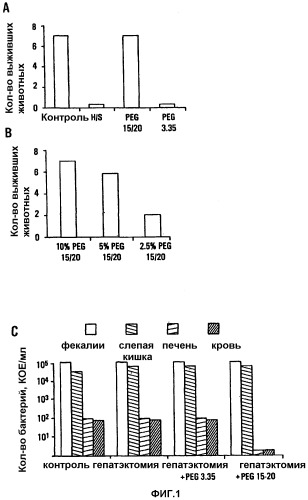
На фигуре 1 представлены коэффициенты смертности у мышей за 48 часов, подвергнутых или ложной лапаротомии, или хирургической резекции 30% печени с последующей прямой инъекцией PA27853 P.aeruginosa в слепую кишку. Мышей сразу подвергали 30% бескровной гепатэктомии левой доли с последующей прямой инъекцией в слепую кишку 1×107 КОЕ/мл PA27853. Каждая группа включала в себя 7 мышей. Контрольных мышей подвергали ложной лапаротомии с последующей инъекцией равных количеств PA27853 в слепую кишку. Для мышей в группе с введением PEG до инъекции в слепую кишку 1×107 КОЕ/мл PA27853 суспендировали или в PEG 3,35 (PEG LMW 3350) или в PEG 15-20 (PEG HMW от 15000 до 20000 дальтон). Кривые "доза-ответ" для PEG 15-20 представлены в части b. a. Статистически значимый защитный эффект PEG 15-20 определяли посредством точного критерия Фишера (p<0,001). b. Определили, что минимальная защитная концентрация PEG 15-20 составляла 5% (p<0,05). c. Количественные бактериальные культуры содержимого слепой кишки (фекалии), отмытой слизистой слепой кишки, печени и крови через 24 часа после хирургической резекции 30% печени и прямой инъекции в слепую кишку 1×107 КОЕ/мл PA27853. Односторонний ANOVA показал статистически значимое увеличение числа бактерий в содержимом слепой кишки, слизистой, печени и крови у мышей после гепатэктомии (p<0,001). Для PEG 3350 наблюдали значимое уменьшение (p<0,05) количества бактерий в печени и крови, тогда как PEG 15-20 полностью предотвращал распространение PA27853 в печени и крови мышей.
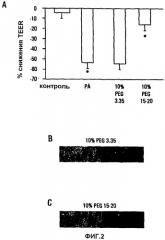
На фигуре 2 представлен защитный эффект PEG 15-20 против индуцированной PA27853 дисфункции эпителиального барьера, как оценивалось посредством измерения трансэпителиального электрического сопротивления (TEER). a. Данные, представляющие средний ± SEM из культур, взятых в трех экземплярах (n=7), процент максимального падения TEER от исходного уровня, наблюдаемый в течение 8 часов воздействия 1×107 КОЕ/мл PA27853 на апикальные поверхности. В клетках Caco-2, подвергнутых воздействию PA27853, показано статистически значимое уменьшение TEER (односторонний ANOVA (p<0,001)). Для PEG 15-20 показан статистически значимый защитный эффект в отношении падения TEER, индуцированного PA27853 (p<0,001). b. Изображение клеток Caco-2 в присутствии PEG 3,35 и воздействия PA27853 на апикальные поверхности. Изображения, полученные после 4 часов совместного культивирования, демонстрировали потерю целостности монослоя с клетками, плавающими на 30-40 микрон выше клеточных контуров, отображая прикрепление PA27853 к клеточным мембранам. c. У клеток Caco-2, подвергнутых воздействию на апикальные поверхности PA27853, после 4 часов в присутствии PEG 15-20 не выявили доказательств плавающих клеток в любой из исследуемых плоскостей.
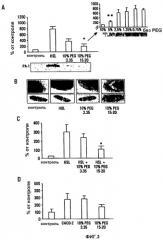
На фигуре 3 представлено ингибирующее действие PEG на экспрессию PA-I в PA27853. a. Анализ "вестерн"-блот. Воздействие на PA27853 1 мМ сигнальной молекулы распознавания кворума C4-HSL приводило к статистически значимому увеличению (p<0,001, односторонний ANOVA) экспрессии белка PA-I, которое частично ингибировалось в присутствии 10% PEG 3,35 и намного более ингибировалось в присутствии 10% PEG 15-20. a'. Минимальная ингибирующая концентрация PEG 15-20 для индуцированной C4-HSL экспрессии PA-I составляла 5% (p<0,01). b. Электронная микроскопия отдельных бактериальных клеток, подвергнутых воздействию C4-HSL в присутствии и отсутствие PEG, показала, что C4-HSL вызывала морфологическое изменение в форме и экспрессии пилей у P.aeruginosa. Индуцированный C4-HSL морфологический эффект полностью устранялся в присутствии PEG 15-20, но не PEG 3,35. Вокруг PA27853, подвергнутых воздействию PEG 15-20, можно наблюдать ореолоподобный эффект. c. "Нозерн"-гибридизация. Воздействие на PA27853 0,1 мМ C4-HSL приводило к статистически значимому увеличению (p<0,001, односторонний ANOVA) экспрессии мРНК PA-I, сильно ингибируемому в присутствии 10% PEG 15-20. d. Увеличение мРНК PA-1, индуцированное посредством 4 часов контакта с клетками Caco-2, ингибировалось в присутствие PEG 15-20, но не PEG 3,35 (p<0,001, односторонний ANOVA).
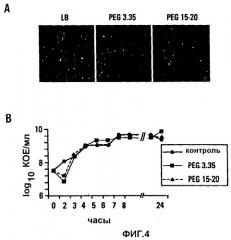
На фигуре 4 показано действие растворов PEG на целостность бактериальной мембраны и характер роста PA27853. a. Действие двух растворов PEG на целостность бактериальной мембраны оценивали посредством способа, состоящего из SYTO 9 и иодида пропидия. Никакой из двух растворов PEG не оказывал какого-либо действия на проницаемость бактериальной мембраны. b. Профили роста PA27853 в двух растворах PEG по сравнению со средой TSB (контроль) без PEG выглядят одинаково.
На фигуре 5 представлены изображения атомно-силовой микроскопии (AFM) клеток Caco-2 и бактериальных клеток, подвергаемых действию PEG. a-c. Изображения AFM клеток Caco-2 в присутствии только среды (a), среды с PEG 3,35 (b) и среды с PEG 15-20. Видно, что PEG 3,35 на клетках Caco-2 формировал ровный ковер (b), тогда как PEG 15-20 формировал более топографически определенное покрытие (c). d-f. Изображения AFM PA27853 в PEG 3,35 и PEG 15-20. PEG 3,35 вокруг отдельной бактериальной клетки формировал гладкую оболочку (e), тогда как PEG 15-20 не только плотно охватывал отдельные клетки (f), но также увеличивал диаметр полимер/бактерия (g, h), таким образом отдаляя отдельные бактерии друг от друга.
На фигуре 6 показано действие раствора PEG на характер рассеивания/агрегации PA27853. Характер рассеивания бактериальных клеток в чашках с dTC3 наблюдали непосредственно с применением флуоресцентного и