Способ получения растворов нитратов платины и платиновых катализаторов на их основе
Иллюстрации
Показать всеИзобретение относится к получению концентрированных водных растворов соединений Pt(IV), не содержащих галогенид-ионов, соединений серы, а также катионов щелочных металлов и органических оснований. Подобные растворы могут быть использованы в качестве предшественников для приготовления высокодисперсных платиновых катализаторов, предназначенных, например, для процессов риформинга и различных процессов полного окисления, актуальных, прежде всего, для очистки отходящих газов промышленных стационарных источников и автомобильных двигателей. Согласно предложенному способу стабильные концентрированные растворы нитратов платины (IV) готовят растворением гексагидроксоплатиновой кислоты при температуре 50-80°С под действием диоксида азота в воде или под действием диоксида азота в водном растворе азотной кислоты. Описано применение полученных растворов в качестве предшественников для приготовления высокодисперсных и ультрадисперсных платиновых катализаторов. Технический эффект - получение стабильных растворов нитратов платины (1V). 2 н. и 1 з.п. ф-лы, 1 табл., 9 ил.
Реферат
Изобретение относится к получению концентрированных водных растворов соединений Pt(IV), не содержащих галогенид-ионов, соединений серы, а также катионов щелочных металлов и органических оснований. Подобные растворы могут быть использованы в качестве предшественников для приготовления высокодисперсных платиновых катализаторов, предназначенных, например, для процессов риформинга и различных процессов полного окисления, актуальных, прежде всего, для очистки отходящих газов промышленных стационарных источников и автомобильных двигателей.
Наряду с другими предшественниками платиновых катализаторов, растворы нитрата платины привлекают особое внимание и широко используются в производстве катализаторов для нейтрализации газовых выбросов промышленных стационарных источников и транспортных средств. В пат. JP 62197148 А2, B01J 23/63, B01D 53/94, 15.12.87 описано приготовление катализатора для одновременного удаления углеводородов, СО и оксидов азота из выхлопных газов бензиновых двигателей путем пропитки каталитического слоя блока нейтрализатора, содержащего оксиды алюминия, церия и лантана, раствором нитрата платины. Кроме того, опубликованы результаты испытаний катализаторов дожигания выхлопных газов дизельных двигателей, приготовленных с использованием раствора нитрата платины в качестве предшественника, где авторы сравнивают дисперсность платины и эффективность приготовленного катализатора с катализаторами на основе альтернативных предшественников, таких как H2PtCl6 и [Pt(NH3)4](ОН)2 [J.A.A. van den Tillaart, J. Leyrer, S. Eckhoff, E.S. Lox, Appl. Catal. В 10 (1-3) (1996) 53-68].
Впервые получение кристаллического нитрата платины путем растворения Н2[Pt(ОН)6] в большом избытке концентрированной азотной кислоты на водяной бане с последующим упариванием растворителя было описано еще в 19 веке [Nilson L.F., Ber., 11 (1878) 882; J. Prakt. Chem., v. 21{2} (1880) 185]. Получившемуся продукту, содержавшему 69.4% Pt и 2.5% N, была приписана формула Pt(OH)2(NO3)2·3PtO2·5H2O.
В патентной литературе первый путь синтеза растворов нитрата платины путем растворения предварительно выделенного и очищенного сухого Pt(NO3)2 (содержание 61.0 мас.% Pt) в воде или органических растворителях типа ацетона и приготовление катализаторов из этого предшественника было описано Kral и Peter [DE 2233677, B01J 23/42, C01G 55/00, 24.01.74]. Твердый нитрат платины, в свою очередь, получали растворением Н2Pt(ОН)6 в концентрированной азотной кислоте, насыщенной оксидами азота, с последующим упариванием избытка азотной кислоты на водяной бане при 80°С, дальнейшей сушкой в вакууме на ротационном испарителе при температуре не выше 40°С до постоянного веса и очисткой перекристаллизацией из органических растворителей. Ни концентрация азотной кислоты, необходимая для растворения Н2Pt(ОН)6, ни максимально возможная концентрация платины в приготовленных таким путем растворах, ни их стабильность в патенте не уточняется. К тому же авторы не обсуждают известную проблему старения твердого нитрата платины, который со временем перестает растворяться в любых растворителях.
Наиболее близким, выбранным в качестве прототипа, является прямой способ получения стабильных растворов нитрата Pt(IV) путем растворения Н2Pt(ОН)6 при небольшом нагревании в концентрированной (300 г/л) азотной кислоте в отсутствие оксидов азота при минимальном соотношении HNO3:Pt=8:1, обеспечивающем стабильность раствора при хранении [JP 11092150 А2, B01J 23/42, C01G 55/00, 06.04.1999]. По указанной концентрации кислоты нетрудно подсчитать, что используемые растворы имеют плотность 1.155 г/мл и содержат 4.81 М HNO3, т.е. для достижения 8-кратного избытка относительно стехиометрического соотношения на 1 г платины (0.0051 моль), содержащийся в 1.54 г Н2Pt(ОН)6, необходимо добавить 8·0.0051=0.041 моль HNO3, содержащейся в 8.52 мл искомого 4.81 М раствора. Таким образом, конечная концентрация приготовленного таким путем раствора нитрата платины всего 8.8 мас.% Pt, что приводит к необходимости хранения больших объемов раствора предшественника.
Известно, что протонирование четырех оставшихся ОН-лигандов в Н2Pt(ОН)6 с ее последующим растворением возможно, однако это требует достижения отрицательного рН [Б.И.Набиванец, Л.В.Калабина, Л.Н.Кудрицкая. Растворимость гидроокисей и ионное состояние палладия (II) и платины (IV) в перхлоратных, хлоридных и сульфатных растворах. ЖНХ, 1971, т.16, вып.12, с.3281-3284]. При растворении Н2Pt(ОН)6 в концентрированной азотной кислоте раствор немедленно приобретает темно-красный цвет, что свидетельствует об изменениях в координационной сфере платины, а именно об образовании олигомерных комплексов, связанных мостиковыми гидроксолигандами [Danan Dou; Di-Jia Liu, W. Burton Williamson, Karl C. Kharas, Heinz J. Robota. Structure and chemical properties of Pt nitrate and application in three-way automotive emission catalysts. Applied Catalysis B: Environmental, 30 (2001) 11-24]. Размер этих олигомеров, однако, зависит от концентрации растворов, рН и других неопределенных факторов. Коммерческие водные растворы нитрата платины темно-красного цвета обычно содержат 14-35 мас.% Pt и большой избыток азотной кислоты. Проявление эффекта Тиндаля свидетельствует о коллоидной природе этих растворов.
Разбавленные растворы коммерческого нитрата платины Pt с концентрациями платины, соответствующими типичным пропиточным растворам, подвержены гидролизу с образованием оранжевого гелеобразного осадка PtO2·xH2O [Danan Dou; Di-Jia Liu, W. Burton Williamson, Karl С.Kharas, Heinz J. Robota. Structure and chemical properties of Pt nitrate and application in three-way automotive emission catalysts. Applied Catalysis B: Environmental, 30 (2001) 11-24]. В зависимости от деталей процедуры приготовления, которые производители тщательно скрывают, видимое глазом расслоение с последующим осаждением начинается через период от одного часа до суток. Образование осадка PtO2·xH2O, по-видимому, происходит из-за дальнейшей олигомеризации или агломерации растворов нитрата платины, вызванной снижением кислотности растворов после разбавления. Разбавленные растворы нитрата платины становятся еще более нестабильными, когда кислотность снижается еще сильнее после контакта с основным оксидом алюминия, являющимся базовым носителем при приготовлении нанесенного каталитического слоя для различных дожигателей отходящих газов. Кроме того, происходит подрастворение носителя избытком азотной кислоты. Добавление в пропиточную суспензию традиционных промоторов - солей Ва2+, La3+, Се3+ - еще более ускоряет процесс осаждения. Такая нестабильность разбавленных растворов нитрата платины ставит под вопрос пригодность нитрата платины в качестве предшественника, поскольку она отражается на дисперсности и эффективности приготовленных катализаторов и вносит элемент невоспроизводимости в производство [Danan Dou; Di-Jia Liu, W. Burton Williamson, Karl С.Kharas, Heinz J. Robota. Structure and chemical properties of Pt nitrate and application in three-way automotive emission catalysts. Applied Catalysis B: Environmental 30 (2001) 11-24].
Таким образом, недостатками известного способа приготовления раствора нитрата платины [JP 11092150] являются:
1) недостаточно высокая концентрация раствора (∼9% Pt), что делает нерентабельным его транспортировку и хранение;
2) нестабильность этих растворов при разбавлении до концентраций 10-2-10-3 М, используемых при приготовлении катализаторов, связанная с динамическим укрупнением коллоидных частиц платинового предшественника, усиливающаяся при контакте с носителем, что делает их непригодными для приготовления высокодисперсных катализаторов.
Изобретение решает задачу получения стабильных концентрированных растворов нитратов платины (IV).
Задача решается способом получения концентрированных растворов нитратов платины (IV) растворением гексагидроксоплатиновой кислоты при температуре 50-80°С под действием диоксида азота в воде или под действием диоксида азота в водном растворе азотной кислоты.
Растворение гексагидроксоплатиновой кислоты проводят в водном растворе, не содержащем или содержащем не более 3 моль HNO3 на моль платины, при этом полученные растворы стабильны не только в концентрированном, но и в разбавленном состоянии, причем при разбавлении происходит уменьшение размеров коллоидных частиц.
Полученные растворы применяют в качестве предшественников для приготовления высоко дисперсных и ультрадисперсных платиновых катализаторов.
В качестве исходного материала для получения растворов нитрата платины можно использовать гексагидроксоплатиновую кислоту, получаемую через промежуточный раствор гексагидроксоплатеата щелочного металла кипячением Н2PtCl6·6Н2O с избытком щелочи в течение 5-6 ч, последующим осаждением продукта уксусной кислотой при рН 5 в виде белого осадка [Б.И.Набиванец, Л.В.Калабина, Л.Н.Кудрицкая. Растворимость гидроокисей и ионное состояние палладия (II) и платины (IV) в перхлоратных, хлоридных и сульфатных растворах. ЖНХ, 1971, т.16, вып.12, с.3281-3284]. Свежеосажденную Н2Pt(ОН)6 отделяют центрифугированием, тщательно промывают от ионов хлора и катионов щелочного металла и сушат до воздушно-сухого состояния на воздухе, а затем в вакууме при температуре не выше 50°С.
Через водную суспензию гексагидроксоплатиновой кислоты при постоянном перемешивании пропускают небольшой ток диоксида азота при температуре 50-80°С и атмосферном давлении до полного растворения кислоты. Продувка прекращается только после перехода исходной красноватой окраски раствора в темно-зеленую. Для некоторого укрупнения олигомерных комплексов платины в целевом растворе к исходной водной суспензии Н2Pt(ОН)6 может быть добавлена азотная кислота концентрацией 850 г/л в количестве, не превышающем 3 моль на 1 моль платины (количество воды может быть соответственно уменьшено). Полное растворение кислоты происходит, как правило, в течение получаса или даже быстрее. После охлаждения раствор следует выдержать 1-2 дня до приобретения им окончательной окраски от желтой до оранжевой в зависимости от используемого соотношения
Pt:HNO3. После этого состояние целевого раствора нитрата платины не изменяется даже после хранения в течение 1 года, а разбавленные растворы с концентрациями около
10-2-10-3 М, пригодные для пропитки носителя в процессе приготовления нанесенных катализаторов, стабильны в течение месяца.
Существенное преимущество нового платиносодержащего предшественника заключается в уменьшении размеров коллоидных частиц в растворе при его разбавлении, что дает возможность воспроизводимо готовить высокодисперсные и ультрадисперсные платиновые катализаторы на традиционных оксидных носителях, например на оксиде алюминия, причем достигается унимодальное распределение частиц платины по размерам с равномерным и однородным распределением по поверхности носителя.
Примеры приготовления растворов (примеры 1-3) и катализаторов на их основе (примеры 6-8) приведены ниже. Для сравнения приготовлены растворы предшественников по упрощенным методикам [DE 2233677 и JP 11092150], аналогичные по свойствам продажным, и катализаторы на их основе. Средний размер коллоидных частиц в разбавленных растворах предшественников (0.01 М) через 15 мин после разбавления, динамика разбавленных растворов (данные малоуглового рентгеновского рассеяния) и средний размер частиц платины на поверхности оксида алюминия в приготовленных из этих растворов катализаторах (данные просвечивающей электронной микроскопии) приведены в Таблице.
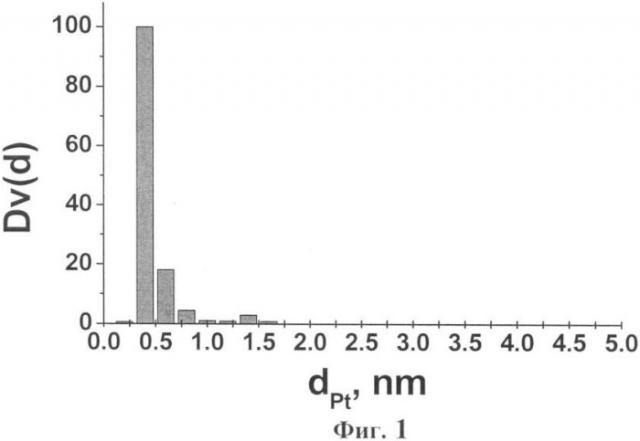
Фиг.1-9 иллюстрируют Таблицу.
На Фиг.1, 2 и 3 показано унимодальное распределение по размерам с максимумом при ~1 нм коллоидных частиц растворов нитрата платины, приготовленных по примерам 1, 2 и 3 соответственно, в результате разбавления водой до концентрации
10-2 М, рассчитанное из обработки данных МУР.
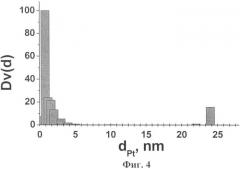
Фиг.4 и 5 иллюстрируют противоположное поведение растворов нитрата платины, приготовленных по примерам 4 и 5 соответственно, в результате разбавления водой до аналогичной концентрации, с появлением наряду с мелкими крупных частиц размером около 24 нм, доля которых возрастает со временем. Микрофотографии высокодисперсных катализаторов 1 мас.% Pt/γ-Al2O3, приготовленных по примерам 6 и 8, с однородным распределением микрокристаллитов платины со средним размером частиц 0.6 и 1.7 нм представлены на Фиг.6 и 7 соответственно. Неоднородное распределение частиц платины по поверхности носителя - микрометровых агрегатов наряду с очень мелкими частицами, характерное для образцов катализаторов 1 мас.% Pt/γ-Al2O3, приготовленных по примерам 9 и 10 из растворов предшественников с высоким содержанием HNO3, показано на Фиг.8 и 9 соответственно.
Пример 1.
Через бледно-желтую суспензию 1.37 г Н2[Pt(ОН)6] (0.046 моль) в 2.5-3.0 мл воды при 50-70°С пропускают слабый ток диоксида азота при постоянном перемешивании, при этом происходит полное его поглощение, а из раствора выделяется немного бесцветного моноксида азота. После полного растворения осадка раствор окрашивается в красноватый цвет, но получившийся раствор недостаточно стабилен, поэтому ток газа не прекращают до тех пор, пока окраска раствора не перейдет в зеленоватую. Время синтеза составляет около 30 мин. В течение суток происходит изменение окраски раствора до желто-оранжевой за счет окисления нитрозильных лигандов в комплексе платины; дальнейших изменений раствора не происходит. Полученный желто-оранжевый раствор содержит 18-20 мас.% Pt (~1.3 М), он стабилен и как минимум в течение года может быть использован для приготовления катализаторов. Разбавленные растворы с содержанием платины 10-2-10-3 М бледно-желтого цвета стабильны в течение месяца.
Пример 2.
В суспензию 1.37 г Н2[Pt(ОН)6] (0.046 моль) в 2.0-2.5 мл воды при помешивании добавляют по каплям 0.46 мл (0.38 г) концентрированной азотной кислоты (d 1.37 г/мл, соотношение HNO3:Pt=1:1). Через полученную желто-оранжевую суспензию при 50-70°С пропускают слабый ток диоксида азота при постоянном перемешивании, при этом происходит полное его поглощение, а из раствора выделяется немного бесцветного моноксида азота. После полного растворения осадка раствор окрашивается в красноватый цвет, но ток газа не прекращают до тех пор, пока окраска раствора не перейдет в зеленовато-бурую. Время синтеза составляет около 20 мин. В течение суток происходит изменение окраски раствора до оранжевой. Полученный оранжевый раствор содержит 18-20 мас.% Pt, он стабилен и в течение года, как минимум, может быть использован для приготовления катализаторов. Разбавленные растворы с содержанием платины 10-2-10-3 М бледно-оранжевого цвета стабильны в течение месяца.
Пример 3.
В суспензию 1.37 г Н2[Pt(ОН)6] (0.046 моль) в 1.12-1.72 мл воды при помешивании добавляют по каплям 1.38 мл (1.15 г) концентрированной азотной кислоты (d 1.37 г/мл, соотношение HNO3:Pt=3:1). Через полученную оранжевую суспензию при 50-70°С пропускают слабый ток диоксида азота при постоянном перемешивании, при этом происходит полное его поглощение, а из раствора выделяется немного бесцветного моноксида азота. После полного растворения осадка раствор окрашивается в красный цвет, но ток газа не прекращают до тех пор, пока окраска раствора не перейдет в бурую. Время синтеза составляет около 10 мин. В течение суток происходит изменение окраски раствора до оранжево-красной. Полученный оранжево-красный раствор содержит 18-20 мас.% Pt, он стабилен и в течение года, как минимум, может быть использован для приготовления катализаторов. Разбавленные растворы с содержанием платины 10-2-10-3 М ярко-оранжевого цвета стабильны в течение месяца.
Пример 4 (для сравнения).
Через красную суспензию 1.37 г Н2[Pt(ОН)6] (0.046 моль) в 2.5-3.0 мл концентрированной азотной кислоты (d 1.37 г/мл, соотношение HNO3:Pt=5-6:1) при 50-70°С пропускают слабый ток диоксида азота при постоянном перемешивании. После полного растворения осадка ток газа не прекращают еще несколько минут. Время синтеза составляет около 10 мин. В течение суток происходит некоторое изменение окраски раствора. Полученный темно-красный раствор содержит 18-20 мас.% Pt, он стабилен и в течение года, как минимум, может быть использован для приготовления катализаторов, однако разбавленные растворы с содержанием платины 10-2-10-3 М ярко-красного цвета стабильны только несколько дней, после чего происходит выпадение оранжевого гидратированного оксида платины.
Пример 5 (для сравнения).
Красную суспензию 1.37 г Н2[Pt(ОН)6] (0.046 моль) в 3.6 мл концентрированной азотной кислоты (d 1.37 г/мл, соотношение HNO3:Pt=8:1, как в прототипе JP 11092150) перемешивают при 70°С в отсутствие оксидов азота. Полное растворение осадка требует нескольких часов; длительность синтеза зависит от предыстории предшественника Н2[Pt(ОН)6]. В течение суток происходит некоторое изменение окраски раствора. Полученный темно-красный раствор содержит ~20 мас.% Pt, он стабилен в концентрированном состоянии и может быть использован для приготовления катализаторов, однако разбавленные растворы с содержанием платины 10-2-10-3 М темно-красного цвета нестабильны - они мутнеют уже через несколько минут, а в течение часа начинается выпадение оранжевого гидратированного оксида платины.
Пример 6. Приготовление нанесенного катализатора 1% Pt/γ-Al2O3 из раствора предшественника, приготовленного по примеру 1.
Носитель γ-Al2О3 (Sosol TKA-432, Германия) предварительно измельчают, рассеивают по фракциям и прокаливают при Т 500°С в течение 2 ч. Для получения катализаторов используют фракцию 0.25 - 0.50 мм (Sуд.~118 м2/г по BET). Носитель (4.5 г), обезвоженный непосредственно перед синтезом при 120°С в течение 4 ч, пропитывают по влагоемкости раствором «нитронитрата платины» №1 (173 мкл раствора (0.247 г) в 5.6 мл дистиллированной воды); сушат до воздушно-сухого состояния не менее 24 ч, затем при 120°С в течение 4 ч и прокаливают на воздухе при 400°С в течение 4 ч.
Пример 7. Приготовление нанесенного катализатора 1% Pt/γ-Al2O3 из раствора предшественника, приготовленного по примеру 2, по методике, как в примере 6.
Пример 8. Приготовление нанесенного катализатора 1% Pt/γ-Al2О3 из раствора предшественника, приготовленного по примеру 3, по методике, как в примере 6.
Пример 9. Катализатор сравнения.
Приготовление нанесенного катализатора 1% Pt/γ-Al2О3 из раствора предшественника, приготовленного по примеру 4, по методике, как в примере 6.
Пример 10. Катализатор сравнения.
Приготовление нанесенного катализатора 1% Pt/γ-Al2O3 из раствора предшественника, приготовленного по примеру 5, по методике, как в примере 6.
| Таблица | |||||
| Раствор нитрата платины (пример №) | Динамика изменения размеров коллоидных частиц в растворе после разбавления | Средний диаметр коллоидных частиц в 0.01 М разбавленном растворе, нм | Катализатор, приготовленный из этого раствора предшественика, разбавленного до 10-2-10-3 М (пример №) | Содержа-ние платины, мас.% | Средний размер частиц Pt на поверхности оксида алюминия, нм1 |
| 1 | Уменьшение | 0.5 | 6 | 0.95 | 0.6 |
| 2 | Уменьшение | 0.8 | 7 | 0.89 | 1.3 |
| 3 | Уменьшении | 1.2 | 8 | 0.93 | 1.7 |
| 4 | Укрупнение | 4.22 | 9 | 0.90 | Неоднор.3 |
| 5 | укрупнение | 5.04 | 10 | 0.87 | Неоднор.5 |
| 1 - Для мелких частиц - по данным ПЭМ, для крупных - по данным ХРД 2 - Бимодальное распределение частиц по размерам, максимумы распределения 1.0 и 24 нм (данные МУР) 3 - Бимодальное распределение частиц, мелкие 1.1 нм и крупные неоднородные рентгеноаморфные агрегаты размером до 200 нм (данные ПЭМ, РФА) 4 - Бимодальное распределение частиц по размерам, максимумы распределения 1 и 24 нм (данные МУР) 5 - Бимодальное распределение частиц, мелкие 1-1.5 нм и крупные неоднородные рентгеноаморфные агрегаты размером до 1 микрона (данные ПЭМ, РФА) |
1. Способ получения стабильных концентрированных растворов нитратов платины (IV) растворением гексагидроксоплатиновой кислоты при температуре 50-80°С, отличающийся тем, что растворение проводят под действием диоксида азота в воде или под действием диоксида азота в водном растворе азотной кислоты.
2. Способ по п.1, отличающийся тем, что растворение гексагидроксоплатиновой кислоты проводят в водном растворе, не содержащем или содержащем не более 3 молей HNO3 на моль платины, при этом получают растворы стабильные не только в концентрированном, но и в разбавленном состоянии, причем при разбавлении происходит уменьшение размеров коллоидных частиц.
3. Применение растворов, полученных согласно п.1 или 2, в качестве предшественников для приготовления высокодисперсных и ультрадисперсных платиновых катализаторов.