Устройство для лечения раковых тканей
Иллюстрации
Показать всеИзобретение относится к области медицинской техники и может быть использовано для лечения раковых тканей различных органов биологических объектов. Устройство содержит полупроводниковый лазерный диод, тактовый генератор, полупрозрачное зеркало, сравнивающее устройство, первый, второй и третий усилители постоянного тока, дифференцирующий усилитель, усилитель-дискриминатор, первый и второй фотоприемники, линию задержки, аналого-цифровой преобразователь, программируемое постоянное запоминающее устройство, первое и второе устройства сравнения двоичных кодов, первую и вторую схемы управления вторичными источниками питания, первый и второй вторичные источники питания и табло/индикатор, при этом биообъект располагается на одной линии между полупроводниковым лазером, полупрозрачным зеркалом и вторым фотоприемником. Использование изобретения позволяет расширить арсенал технических средств лазерной онкотерапии. 4 ил.
Реферат
Изобретение относится к области медицины и может быть использовано для лечения раковых тканей различных биосистем.
Современная медицина при лечении раковых заболеваний стремится уничтожить раковые клетки/ткани. Для уничтожения раковых клеток используют хирургию, лучевую терапию, химиотерапию, а также терапию избирательного действия (лазеры, бетатроны, различные ускорители элементарных частиц и т.п.).
Известные устройства, реализующие известные способы терапии раковых тканей избирательного действия, отличаются лишь конкретными типами лазеров и техническим исполнением систем фокусирующих линз, сохраняя при этом одинаковую структурную схему устройства в целом. Поэтому в качестве прототипа рассмотрим следующее устройство [Эмануэль Н.М., Кавецкий Р.Е., Тарусов Б.Н., Сидорик Е.П. Биофизика рака. - Киев: Наук. думка, 1976. - 296 с.].
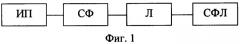
Устройство для осуществления известного способа лечения раковых тканей (см. фиг.1) состоит из источника питания (ИП), схемы формирования и выбора режимов работы лазера (СФ), непосредственного активного излучателя - лазера (Л) и системы фокусирующих линз (СФЛ), которые соединены последовательно.
Работает устройство следующим образом. При включении источника питания оператор с помощью СФ выбирает требуемый режим работы лазера, длина волны которого определена его активной структурой, например, импульсный, с регулируемыми характеристиками (длительностью импульса, крутизной его переднего и заднего фронта и т.п.), или непрерывный режимы излучения оптического сигнала активной структурой, т.е. лазером. Выходной оптический поток оператор может также изменять за счет управления СФЛ. Например, фокусируя оптический поток на малой площади, можно увеличивать его плотность/мощность облучения, и наоборот, расфокусируя - уменьшать его плотность/мощность облучения. В практических схемах источником светового потока служат лазеры на основе рубина (λ=694,3 нм) и неодима (λ=1060 нм), а также возможно использование полупроводниковых лазерных диодов.
Недостатком известного устройства является невозможность его прямого использования для реализации заявляемого способа лечения раковых тканей. Оператор не может обеспечить режим противофазной генерации длин волн лазера по отношению к собственным колебаниям раковой клетки. Начальная фаза колебаний лазера всегда случайна. Плотность /мощность потока облучения также выбирается оператором и, как правило, намного превосходит требуемую мощность для работы. Оператор, добиваясь положительного результата, сознательно завышает мощность потока облучения, чтобы компенсировать различные случайности в процессе лечения.
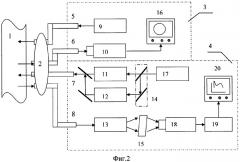
Наиболее близким к заявляемому устройству является другое известное устройство [US 5634922 (Hamamatsu Photonics K.K.) Jun. 3, 1997]. На фиг.2 приведена схема эндоскопической системы, реализующей контроль, диагностику и лечение злокачественных биотканей. Эндоскопическая система с помощью эндоскопа 2 позволяет визуально за счет оптики находить во внутренних органах участки предполагаемых злокачественных тканей 1 путем подсветки их от источника белого света 9 посредством световода 5. Качественный визуальный контроль злокачественного участка биоткани 1 через отраженный от поверхности сигнал посредством световода 6 с помощью цветной видеокамеры 10 регистрируется на телевизионном мониторе 16. Совокупность данных элементов составляет контролирующую схему 3 общей эндоскопической системы.
Оптическая диагностика и лечение обеспечиваются схемой 4 общей эндоскопической системы. Она включает специальный лазерный генератор 17, который позволяет с помощью составляющих 11 и 12 генерировать соответственно две рабочие длины волны: для диагностики - 405 нм и для лечения - 630 нм. В зависимости от вида работы переключатель 14 сигнал от генератора 17 направляет по каналу диагностики 11 или по каналу лечения 12. На выходе генерирующей схемы оптический сигнал лазера поступает посредством световода 7 в рабочую зону участка биоткани 1.
Для реализации диагностики биообъекта предварительно осуществляется внутривенная инъекция специальным контрастным веществом, например, веществом HpD (условное обозначение контрастного вещества по материалам описания патента прототипа). При наклоне лазерного луча 405 нм к диагностируемой ткани возникает флуоресценция с двумя пиками 630 и 690 нм. Данный сигнал посредством световода 8 поступает на спектроскоп 13, на выходе которого реализуется спектр 15. Данный спектральный сигнал 15 посредством высокочувствительной камеры 18 преобразуется в видеосигнал и далее подвергается обработке анализатором 19 для получения графического изображения флуоресценции на телевизионном мониторе 20 (фактически телевизионные мониторы 16 и 20 выполняют функции табло-индикаторов).
Наличие флуоресцентной картины с двумя пиками является классификационным признаком злокачественных тканей и основанием для переключения прибора с режима диагностики на режим лечения. Переключатель 14 по световоду 7 в зону ракового очага, которая строго определенна и зафиксирована на предварительном этапе диагностики, направляет лазерный луч 630 нм и физически разрушает этот очаг. Изменение состава контрастного вещества накладывает ограничения на длину волны по каналу 12. Это требует создания лазерного генератора 17 со специальными возможностями по перестройке рабочей длины волны.
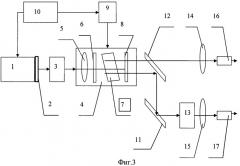
Как следует из описания устройства для диагностики и лечения раковых тканей центральным узлом эндоскопической системы является конструкция лазерного генератора 17, обладающего возможностью перестраивать рабочую длину волны. На фиг.3 представлена схема устройства лазерного генератора 17.
Основу устройства лазерного генератора составляет твердотельный лазерный генератор 1 (полупроводниковый лазер), на выходе которого имеется селективный элемент 2, например подвижная оптическая призма. Она позволяет лазерный луч с нужной длиной волны в пределах широкого диапазона длин волн селективно направлять на гармонический генератор 3, сигнал с которого поступает на оптический параметрический генератор 4. Он состоит из коллиматорной линзы 5, двух зеркал 6 и 8, между которыми находится нелинейный оптический кристалл 7 типа ВВО или LBO (см. описание прототипа). Управление нелинейным оптическим кристаллом осуществляется блоком управления 10 посредством специального вращающегося элемента 9, с помощью которого достигается заданный угол падения лазерного луча на нелинейный элемент 7. Величина угла определяется составом контрастного вещества и связана с длиной волны лазера. Поэтому блок управления 10 осуществляет синхронное управление и непосредственно лазером 1. В итоге на выходе параметрического генератора 4 формируются сигналы двух требуемых длин волн. Для разделения сигналов на два оптических канала используется дихроичный фильтр 12. Прямой лазерный луч через собирательную линзу 14 поступает на вход оптического волокна 16 и используется как лечебный. Другой лазерный луч отражается от дефлектора и поступает на второй гармонический генератор 13, где формируется диагностический лазерный луч. Он также через собирательную линзу 15 поступает на вход оптического волокна 17 и используется как диагностический.
Недостатком известного устройства является зависимость на этапе диагностики от типа контрастного вещества, которое вводится путем внутривенной инъекции. При этом эффект лечения зависит от уровня дозы облучения лазерным лучом и точности наведения на раковый очаг. Следует иметь ввиду тот факт, что форма очага может быть разнообразной, а наличие метастаз требует специального алгоритма последовательности их уничтожения.
Предлагаемое устройство для лечения раковых тканей биосистемы представляет собой совокупность приспособлений и устройств, причем в основу положен полупроводниковый лазерный диод, помимо которого оно содержит также полупрозрачное зеркало, два фотоприемника, сравнивающее устройство, тактовый генератор, три усилителя постоянного тока, дифференцирующий усилитель, усилитель-дискриминатор, линию задержки, аналого-цифровой преобразователь с табло-индикатором, программируемое постоянное запоминающее устройство, два устройства сравнения двоичных кодов, две схемы управления вторичными источниками питания и два вторичных источника питания.
Общим для выбранного заявителем прототипа и предлагаемого устройства является наличие в них:
- полупроводникового лазерного диода;
- полупрозрачного зеркала;
- табло-индикатора.
Отличительные от прототипа признаки следующие:
- тактовый генератор;
- сравнивающее устройство;
- три усилителя постоянного тока;
- дифференцирующий усилитель;
- усилитель-дискриминатор;
- два фотоприемника;
- линия задержки;
- аналого-цифровой преобразователь;
- программируемое постоянное запоминающее устройство;
- два устройства сравнения двоичных кодов;
- две схемы управления вторичными источниками питания;
- два вторичных источника питания, а также связи между указанными устройствами, приведенные в формуле изобретения. В частности, существенное значение имеет расположение диагностируемого объекта по пути рабочего светового потока между полупроводниковым лазерным диодом, полупрозрачным зеркалом и вторым фотоприемником. Это обеспечивает получение информации о соотношении начальных фаз колебаний источника облучения и собственно раковой клетки. Цепочка, образованная первым фотоприемником и вторым усилителем постоянного тока, сравнивающим устройством и первым усилителем постоянного тока, создает канал отрицательной обратной связи, обеспечивающий стабилизацию режима генерации когерентного светового потока по мощности. Тактовый генератор обеспечивает синхронизацию по времени начальной фазы когерентного светового потока с начальной фазой собственных колебаний раковой клетки. Для этой цели служит канал автоматического управления начальной фазой источника облучения, который состоит из второго фотоприемника, третьего усилителя постоянного тока, дифференцирующего усилителя, линии задержки и усилителя-дискриминатора. Для контроля и управления рабочей длиной волны лазерной установки создана схема на основе аналого-цифрового преобразователя с табло-индикатором, программируемого постоянного запоминающего устройства, двух устройств сравнения двоичных кодов, двух схем управления вторичными источниками питания и двух вторичных источников питания. Следует отметить, что первое устройство сравнения двоичных кодов обрабатывает сигналы старших разрядов программируемого постоянного запоминающего устройства, а второе - соответственно сигналы младших разрядов. Это позволяет осуществлять более точное управление рабочей длиной волны лазерной установки.
Технический результат предлагаемого изобретения состоит в расширении арсенала технических средств при реализации лазерной онкотерапии.
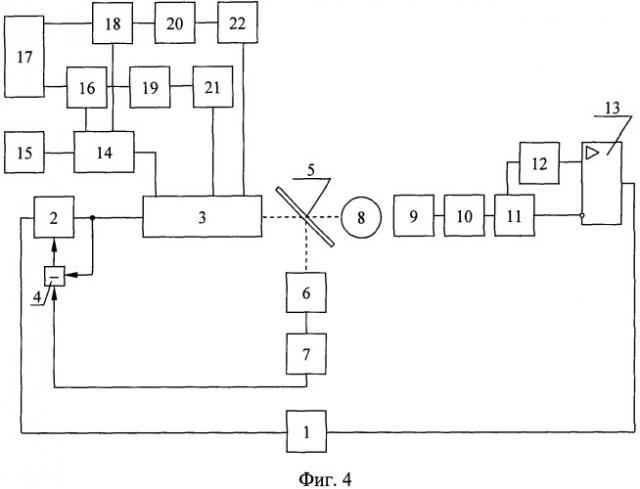
Предлагаемое устройство для лечения раковых тканей показано на Фиг.4.
Оно содержит тактовый генератор (ТГ) 1, выход которого соединен с первым входом первого усилителя постоянного тока (УТ) 2. Выход УТ 2 связан с первым входом полупроводникового лазерного диода (ПЛД) 3 и первым входом сравнивающего устройства (СУ) 4. Выход СУ 4 соединен со вторым входом УТ 2. Выходной оптический поток с ПЛД частично отражается от полупрозрачного зеркала 5 и поступает на первый фотоприемник (ФП) 6, который соединен с вторым УТ 7. Выход УТ 7 подключен ко второму входу СУ 4. Вторая часть оптического выходного потока, пройдя через полупрозрачное зеркало 5, облучает биообъект 8 и поступает на второй ФП 9, выход которого соединен со входом третьего УТ 10. Выход с УТ 10 подключен к входу дифференцирующего усилителя (ДУ) 11. К первому выходу ДУ 11 подключена линия задержки 12, а ко второму выходу - инверсный вход усилителя-дискриминатора (УД) 13. Выход линии задержки 12 соединен соответственно с нормальным входом УД 13. Выход УД 13 подключен к входу ТГ 1. Следует отметить, что ПЛД 3, полупрозрачное зеркало 5, биообъект 8 и ФП 9 расположены на одной линии по пути рабочего светового потока между излучателем полупроводникового лазерного диода и вторым фотоприемником. Выход ПЛД 3 соединен с аналого-цифровым преобразователем (АЦП) 14, первый выход которого соединен с табло-индикатором 15. Выход старшего разряда АЦП 14 соединен с первым входом первого устройства сравнения двоичных кодов (УС) 16. Ко второму входу УС 16 подключен выход старшего разряда программируемого постоянного запоминающего устройства (ППЗУ) 17. Соответственно выход младшего разряда АЦП 14 соединен с первым входом второго УС 18. Ко второму входу УС 18 подключен выход младшего разряда ППЗУ 17. Выход первого УС 16 соединен со входом первой схемы управления первого вторичного источника питания (СУ) 19, а выход второго УС 18 соединен со входом второй СУ 20. В итоге выход первого СУ 19 подключен к входу первого вторичного источника питания (ВИП) 21, выход которого соединен со вторым входом ПЛД 3, а выход второго СУ 20 подключен к входу второго ВИП 22, выход которого соединен с третьим входом ПЛД 3.
Устройство работает следующим образом.
При включении устройства в работу ТГ 1 вырабатывает прямоугольный импульс, который усиливается до уровня требуемой мощности первым УТ 2 и поступает в цепь питания ПЛД 3. Создаваемый ПЛД 3 когерентный световой поток с произвольной начальной фазой колебаний с помощью полупрозрачного зеркала 5 разделяется на рабочий, который служит для облучения биообъекта, и на поток канала стабилизации мощности излучения. Канал стабилизации образован первым ФП 6 и вторым УТ 7, где происходит преобразование оптического сигнала в электрический, его усиление и далее сравнение в устройстве 4 с уровнем прямого сигнала с выхода первого УТ 2. Сигнал ошибки управляет коэффициентом усиления первого УТ 2 и стабилизирует мощность потока излучения ПЛД 3.
Рабочий световой поток подвергает воздействию биообъект 8, расположенный на одной линии между ПЛД 3 и вторым ФП 9 в течение времени, равного длительности рабочего импульса с ТГ 1. В момент времени, равный длительности фронта рабочего импульса, следует отклик биообъекта на воздействие, которое выражается в некотором переходном процессе, так как облучение ведется на резонансной частоте раковой клетки/ткани биообъекта. Разность начальных фаз φи и φ0, как известно, находит отражение в переходной характеристике связанной системы, которая фиксируется вторым ФП 9 и третьим УТ 10. Момент противофазности сигнала облучения и собственных излучений раковой клетки можно установить по минимуму обратного импульса переходной характеристики системы устройство - биообъект. Для этого сигнал с выхода третьего УТ 10 подвергается дифференцированию с помощью ДУ 11, первый выход которого соединен с инверсным входом УД 13, а второй выход через линию задержки 12 с нормальным входом УД 13. Фактически совокупность этих устройств реализует автокорреляционный метод приема импульсных сигналов по схеме селекции импульсных сигналов по их длительности, что обеспечивает обработку импульсных сигналов на фоне помех. При такой организации схемы обработки реализуется непрерывный контроль состояния системы устройство - биообъект. Информационный сигнал с УД 13 поступает на вход ТГ 1 и управляет начальной фазой рабочего импульса, сдвигая его в том направлении, пока напряжение на выходе УД 13 не станет минимальным. Этим достигается автоматическая регулировка/настройка устройства на требуемый режим соотношения начальных фаз источника светового потока и собственных колебаний раковой клетки и его поддержание в процессе сеанса лечения.
Требуемая длина волны ПЛД 3, которая является априори, обеспечивается специальным каналом контроля, настройки и автоматического поддержания. Конструктивно ПЛД 3 имеет встроенные систему контроля состояния активного элемента, системы грубой и точной настройки рабочей длины волны, что облегчает задачу управления таким прибором. Система контроля состояния активного элемента выдает информационный сигнал, который поступает на АЦП 14 и может быть дешифрирован с отображением на табло-индикаторе 15. Каждый экземпляр ПЛД 3 имеет паспортную характеристику излучаемой длины волны в зависимости от информационного сигнала встроенной контролирующей системы. Двоичный код с АЦП 14 разделяется на элементы старшего и младшего разрядов. ППЗУ 17 хранит двоичные коды резонансных частот различных раковых тканей, которые будут применяться в процессе лечения. Информационные коды старших разрядов АЦП 14 и ППЗУ 17 сравниваются в первом УС 16 и сигнал ошибки несовпадения кодов поступает на первую СУ 19. Выходной сигнал первой СУ 19 управляет первым ВИП 21, который с помощью системы грубой настройки изменяет длину волны в направлении, пока не совпадут коды старших разрядов в первом УС 16. Информационные коды младших разрядов АЦП 14 и ППЗУ 17 сравниваются во втором УС 18 и сигнал ошибки несовпадения кодов поступает на вторую СУ 20. Выходной сигнал второй СУ 20 управляет вторым ВИП 22, который с помощью системы точной настройки изменяет длину волны в направлении, пока не совпадут коды младших разрядов в втором УС 18.
Из приведенного описания устройства видно, что оно состоит преимущественно из стандартных элементных устройств, что делает его общедоступным в монтаже. Простота устройства и автоматика поддержания его в рабочем положении при наличии помех обеспечивает самое широкое его внедрение и применение при реализации способа лечения раковых заболеваний различных биосистем на любой стадии.
Источники информации, принятые во внимание при составлении описания
1. Эмануэль Н.М., Кавецкий Р.Е., Тарусов Б.Н., Сидорик Е.П. Биофизика рака. - Киев: Наук. думка, 1976. - 296 с.
2. United States Patent 5634922. Jun. 3, 1997. Hirano et al. Cancer Diagnosis and Device Having Laser Beam Generator. Hamamatsu Photonics K.K.
Устройство для лечения раковых тканей, содержащее полупроводниковый лазерный диод, полупрозрачное зеркало для разделения светового потока на рабочий и контрольный и табло-индикатор, отличающееся тем, что выход тактового генератора соединен с первым входом первого усилителя постоянного тока, выход которого связан с первым входом полупроводникового лазерного диода и первым входом сравнивающего устройства, первый фотоприемник соединен со входом второго усилителя постоянного тока, выход которого подключен ко второму входу сравнивающего устройства, а его выход связан со вторым входом первого усилителя постоянного тока, второй фотоприемник соединен со входом третьего усилителя постоянного тока, выход которого подключен на вход дифференцирующего усилителя, первый выход последнего соединен с инверсным входом усилителя дискриминатора, а второй соединен через линию задержки с нормальным входом усилителя дискриминатора, выход усилителя дискриминатора соединен со входом тактового генератора, выход полупроводникового лазера соединен со входом аналого-цифрового преобразователя, первый выход которого подключен к табло/индикатору, второй выход - к первому входу первого устройства сравнения двоичных кодов, третий выход - к первому входу второго устройства сравнения двоичных кодов, ко второму входу первого устройства сравнения двоичных кодов подключен первый выход программируемого постоянного запоминающего устройства, ко второму входу второго устройства сравнения двоичных кодов подключен второй выход программируемого постоянного запоминающего устройства, выход первого устройства сравнения двоичных кодов подключен ко входу первой схемы управления вторичным источником питания, выход которой соединен со входом первого вторичного источника питания, а выход второго устройства сравнения двоичных кодов подключен ко входу второй схемы управления вторичным источником питания, выход которой соединен со входом второго вторичного источника питания, выход первого вторичного источника питания соединен со вторым входом полупроводникового лазерного диода, а выход второго - соответственно с третьим входом полупроводникового лазерного диода, при этом полупрозрачное зеркало расположено по пути рабочего светового потока между излучателем полупроводникового лазерного диода и вторым фотоприемником.