Фармацевтические композиции и их применения
Иллюстрации
Показать всеНастоящее изобретение относится к области медицины и фармацевтики и касается фармацевтической композиции для профилактики и лечения нейродегенеративных болезней, содержащей 3-(2-цианофенил)-1-фенил-5-(2-пиридил)-1,2-дигидропиридин-2-он, его соль или гидрат и интерферон-бета, комбинации, содержащей 3-(2-цианофенил)-1-фенил-5-(2-пиридил)-1,2-дигидропиридин-2-он, его соль или гидрат и интерферон-бета, и способам лечения нейродегенеративных болезней с их помощью. Изобретение обеспечивает высокую эффективность лечения. 5 н. и 18 з.п. ф-лы, 2 ил., 4 табл.
Реферат
Настоящее изобретение относится к лечению демиелинизирующих расстройств (разрушение миелинового слоя нервных волокон) и нейродегенеративных болезней и к композициям для вышеупомянутого использования.
Большая часть возбуждающих синаптических ответов в ЦНС млекопитающих выявляется аминокислотами, такими как L-глутамат или L-аспартат, которые принимают участие в деятельности нервов, включая узнавание (распознавание), память, движение, дыхание, сердечно-сосудистую коррекцию и ощущение. Для выражения их физиологической активности взаимодействие с конкретным (специфическим) рецептором является важным. Эти рецепторы могут быть подразделены на четыре различных подтипа рецепторов. Три из этих рецепторов связаны с ионофорами и известны как рецепторы N-метил-D-аспартата (NMDA), AMPA (α-амино-3-гидрокси-5-метил-4-изоксазолпропионата) и каинатные рецепторы. Четвертый подтип рецептора связан с фосфоинозитольным метаболизмом и известен как метаботропный глутаматный рецептор.
Рецептор NMDA связан с каналами высокой проводимости, проницаемыми для Na+, K+ и Ca2+. Он модулируется глицином (коагонист) и полиаминами (позитивный модулятор) и блокируется Mg2+ в ответ на изменение мембранного потенциала, за генерацию и распространение которого вдоль мембран нервных клеток ответственны ионные каналы. Полагают, что функциональный рецептор NMDA образован как пентамерная конструкция из субъединиц, состоящая из выборки субъединиц из семейств NR1 (восемь изоформ) и NR2 (четыре изоформы). Тип субъединиц, образующих канал NMDA, определяет его биофизические свойства и физиологическую функцию. AMPA- и каинатный рецепторы являются проницаемыми для Na+ и K+. AMPA рецептор-зависимый ионный канал образован из четырех различных субъединиц, обозначенных как GluR1-GluR4 (в двух альтернативных вариантах сплайсинга - flip и flop) в тетрамерной конструкции субъединиц. Фармакологические свойства AMPA рецептор-зависимых ионных каналов определяются выбором субъединиц. Конструкции каналов, испытывающие недостаток в субъединицах GluR2, помимо проницаемости в отношении Na+ и K+, являются проницаемыми для Ca2+. Гибридизация in situ обнаружила различную экспрессию субъединиц глутаматного рецептора по всему головному мозгу и во время развития.
Известно, что аминокислота как возбуждающий нейротрансмиттер индуцирует нейротоксичность, например, посредством аномального возбуждения центральных нервов. Было отмечено, что указанная токсичность является настолько серьезной, насколько она сопровождается гибелью нервных клеток, вызывая при этом различные нервные заболевания. Основными нервными болезнями, которые широко известны, являются церебральная ишемия, травма головы, спинномозговая травма, болезнь Альцгеймера, болезнь Паркинсона, боковой амиотрофический склероз (ALS), хорея Гентингтона, нервное расстройство, обусловленное СПИД; эпилепсия, нейродегенерация, наблюдаемая после состояния гипоксии; психическое расстройство, нарушение подвижности, боль, мышечные спазмы, нервное расстройство, вызванное пищевым отравлением; различные нейродегенеративные болезни, различные болезни, связанные с нарушением умственного развития, хроническая боль, мигрень, карциноматозная боль и боль, вызванная диабетическим нервным расстройством. Все перечисленные выше заболевания являются серьезными болезнями, многие механизмы возникновения и т.д. которых еще не выяснены и эффективные терапевтические фармацевтические средства для которых еще не обнаружены, однако полагают, что вышеупомянутые механизмы тесно связаны с чрезмерным высвобождением/аккумуляцией возбуждающих нейромедиаторов, изменениями в картине экспрессии рецепторов и т.д. Например, сообщалось, что концентрация глутамата в цереброспинальной жидкости увеличивается при ударе, церебральной ишемии, травме головы и спинномозговом повреждении. Имеется сообщение о том, что нейропатия происходит, когда глутамат, NMDA, AMPA, каинат и т.д. чрезмерно атакуют нервные клетки. Имеются сообщения, что при болезни Альцгеймера β-амилоидный белок усиливает нейротоксичность глутамата и что он промотирует высвобождение глутамата. В случае болезни Паркинсона имеются сообщения, что гидроксид L-дофы активирует рецептор AMPA и усиливает нейротоксичность. Имеется и другое сообщение, что L-дофа промотирует генерацию свободных радикалов, что приводит к повышению окислительного стресса. В случае хореи Гентингтона имеются данные, что вещество, которое ингибирует высвобождение глутамата, оказывается эффективным для улучшения симптомов (положительной динамики заболевания). В случае ALS (боковой амиотрифический склероз) имеется ряд сообщений, свидетельствующих об участии глутамата в патогенезе заболевания. Имеется несколько случаев, когда пациенты, страдающие СПИД, испытывают нарушение функции нерва, ответственного за узнавание, и даже в такой болезни нерва подтверждается участие глутамата. Например, сообщается, что gp 120, который представляет собой гликопротеин, присутствующий в оболочке вируса ВИЧ (HIV), подавляет включение глутамата астроцитами, в то время как вещество, которое ингибирует высвобождение глутамата, подавляет нейродегенерацию, вызываемую gp 120. В отношении аллергического энцефаломиелита имеется сообщение, что у мышей, у которых имеет место вышеуказанное воспаление, обнаружен недостаток в ферменте, который разрушает глутамат, экспонированный с наружной стороны клеток. Оливопонтоцеребеллярная атрофия представляет собой болезнь, которую иногда объединяют с болезнью Паркинсона, и было обнаружено антитело против GluR2, одной из субъединиц, составляющих рецептор AMPA, и высказано предположение о наличии связи между оливопонтоцеребеллярной атрофией и рецептором AMPA. Относительно эпилепсии имеется сообщение, что у мышей, которые не способны создать GluR2-субъединицу в рецепторе AMPA, проницаемость Ca2+ через рецептор AMPA возрастает, в результате чего возрастает вероятность наступления внезапного приступа, приводящего к смерти. Кроме вышесказанного, сообщается, что NBQX (2,3-дигидрокси-6-нитро-7-сульфамоилбенз[f]хиноксалин) и другие соединения, являющиеся ингибиторами по отношению к рецепторам AMPA, имеют транквилизирующее и противосудорожное действие, и, кроме того, имеются данные относительно связи рецептора AMPA/каинатного рецептора с расстройством мочеиспускания, лекарственным злоупотреблением (токсикоманией), болью и т.д.
Терапевтические подходы к нейродегенеративным болезням и демиелинизирующим расстройствам в значительной степени оказались неудовлетворяющими, несмотря на то, что в случае последнего (демиелинизирующего расстройства) использование иммунодепрессантов, таких как кортикостероиды и циклофосфамид, которые хотя и позволяют получить пациентам ограниченную пользу, может быть ассоциировано с потенциально возможными серьезными побочными действиями. Введение препаратов интерферона обеспечивало эффективность в лечении некоторых демиелинизирующих расстройств (например, рассеянного склероза). Благоприятные воздействия, отмеченные в этом случае, связывают с иммуномодуляторными действиями интерферонов. Однако, поскольку благоприятное воздействие оказывается реализованным только для части подгруппы пациентов, специально отобранных для лечения, проблема, связанная с недостаточным контролем за болезнью с помощью вышеуказанных препаратов, остается нерешенной. Ограниченная эффективность современной терапии с использованием иммуномодуляторов для демиелинизирующих расстройств (например, рассеянный склероз) может быть связана с неспособностью указанных средств противодействовать дегенерации олигодендроглиальных клеток, нейронов и аксонов, ассоциируемой с этой болезнью.
Можно ожидать, что вещества, проявляющие антагонистическое действие в отношении стимулирующих нейротрансмиттеров, могут быть полезными для лечения вышеупомянутых болезней. В настоящее время полагают, что вещества, имеющие антагонистическое действие в отношении не-NMDA рецепторов, таких как рецептор AMPA и каинатный рецептор, будут особенно полезными. Например, сообщается, что ингибиторы взаимодействия глутамата с комплексом AMPA и/или каинатным рецепторов являются полезными для лечения демиелинизирующих рассстройств (WO 00/01376). Кроме того, сообщается, что антагонисты AMPA и/или каинатного рецепторов оказались эффективными в уменьшении интенсивности симптомов экспериментального аутоиммунного энцефаломиелита (EAE), животной модели, которая репродуцирует многие из патологических и клинических признаков рассеянного склероза. Хотя нейрозащитный потенциал антагонистов AMPA и/или каинатного рецепторов признан в нейронной/аксонной дегенерации, являющейся следствием гипоксии/ишемии, гипогликемии, конвульсий и травмы головы или спинного мозга, эти данные [WO 00/01376] были первыми, которые обеспечили доказательство в поддержку участия (вовлечения) глутамата в патогенез демиелинизирующих расстройств. Кроме того, улучшенный клинический результат для EAE, полученный при лечении с использованием агонистов AMPA и/или каинатного рецепторов, оказался независимым от противовоспалительных или иммуномодуляторных воздействий, что свидетельствует о наличии альтернативного механизма действия, в основе которого лежит защита олигодендроглиальных клеток и аксонов.
Решение проблемы недостатка клинической эффективности современных терапий демиелинизирующих расстройств заключается в использовании комбинации иммунорегуляторного или противовоспалительного средства и средства, защищающего нейроны, аксоны и/или олигодендроглиальные клетки. В соответствии с этим задачей настоящего изобретения является исследование и обнаружение соединений, которые ингибируют рецептор(ы) AMPA и/или каинатный рецептор(ы) и которые при объединении с иммуномодуляторным или противовоспалительным средством подавляют токсичность возбуждающих нейромедиаторов в отношении нейронов, аксонов и олигодендроглиальных клеток и обеспечивают их защиту как фармацевтические средства, которые можно использовать в качестве терапевтических, профилактических или улучшающих симптомы заболевания (положительная динамика заболевания) средств для различных нейродегенеративных и демиелинизирующих болезней.
В данном случае показано, что (благодаря достигнутому реверсированию паралича на in vivo модели демиелинизирующего и нейродегенеративного расстройства) имеются клинические преимущества в лечении нейродегенеративных и демиелинизирующих расстройств с использованием комбинации антагониста AMPA и/или каинатного рецепторов с иммунорегуляторным средством, при этом эффективность предлагаемой терапии оказывается выше, чем ожидаемое аддитивное действие любого одного средства из двух.
Таким образом, в одном аспекте изобретение относится к композиции, содержащей:
I) соединение, описанное в настоящем описании, и
II) иммунорегуляторное или противовоспалительное средство.
Соединения настоящего изобретения включают соединения 1,2-дигидропиридин-2-она, такие как, например, 3-(2-цианофенил)-1-фенил-5-(2-пиридил)-1,2-дигидропиридин-2-он, 3-(2-цианофенил)-5-(2-пиридил)-1-(3-пиридил)-1,2-дигидропиридин-2-он, 3-(2-фтор-3-пиридил)-5-(2-пиридил)-1-фенил-1, 2-дигидропиридин-2-он, 3-(2-фтор-3-пиридил)-5-(2-пиридил)-1-(3-пиридил)-1,2-дигидропиридин-2-он, 3-(2-цианофенил)-1-фенил-5-(2-пиримидинил)-1,2-дигидропиридин-2-он, 3-(2-цианофенил)-1-(3-пиридил)-5-(2-пиримидинил)-1,2-дигидропиридин-2-он, 3-(2-фторпиридин-3-ил)-1-фенил-5-(2-пиримидинил)-1,2-дигидропиридин-2-он,
3-(2-цианопиридин-3-ил)-1-фенил-5-(2-пиримидинил)-1,2-дигидропиридин-2-он.
Дополнительные соединения настоящего изобретения и их синтез описаны в представленных ниже примерах.
Композиция, определенная здесь, может дополнительно включать фармацевтически приемлемый носитель или наполнитель.
Согласно настоящему изобретению, иммунорегуляция может быть определена как контроль специфических иммунных ответов и взаимодействий между клетками лимфоидной и миеловидной линии дифференцировки; кроме того, иммунорегуляция может включать иммуносупрессию и иммуномодуляцию, где иммуносупрессия может быть определена как предупреждение или препятствие развитию иммунологического ответа и может включать миелосупрессию, и где иммуномодуляция может быть определена как корректирование иммунного ответа до желаемого уровня. Согласно настоящему изобретению, термин “противовоспалительный” может быть определен как уменьшение воспаления.
Иммунорегуляторные или противовоспалительные средства согласно изобретению могут представлять, например, интерферон (IFN; IFN-бета-1a, например Ребиф и Авонекс; IFN-бета-1b, например Бетасерон и Бетаферон; IFN-альфа-2а, например Альфаферон; IFN-альфа-2b, например Вираферон), кортикотропин (например, Актар; Кортрозин), синтетический стероид (например, дексаметазон, например Декадрон; преднизолон, например Дельтакортеф; метилпреднизолон, например А-метапред, Солу-Медреол), химиотерапевтическое средство (например, митозантрон, например Новантрон; циклофосфамид, например цитоксан, неосар; паклитаксел, например Таксол; метотрексат, например флоекс), азотиоприн (например, имуран), циклоспорин (например, Сандиммун, Неорал), пеницилламин (например, депен), ингибитор фосфодиэстеразы (например, циломиласт, рофлумиласт), антитело или вакцина против поверхностной молекулы лейкоцитов, эндотелиальных или глиальных клеток (например, интегрин) или адгезирующая молекула (например, антегрин (натализумаб)); рецептор или ко-стимулятор Т-клетки, синтетический полипептид (например, глатирамер ацетат, сополимер-1, Copaxone; лиганд измененного пептида), толерантность-индуцирующее средство (например, в основном состоящий из миелина белок), ингибитор металлопротеиназы тканевого матрикса (ММР) (например, основанные на гидроксамовой кислоте ингибиторы ММР), антагонист ингибитора или рецептора цитокина или хемокина (например, ингибитор фактора некроза опухолей (TNF), например Талидомид; гибридный белок TNF-рецептора и иммуноглобулина, нестероидное противовоспалительное средство (например, ингибитор фосфолипазы, циклооксигеназы (например, салициловая кислота, ацетаминифен, индометацин (например, Индоцин), сульдинак (например, Клинорил), феманаты (например, Понстел, Толектин, Торадол, Волтарин), производные арилпропионовой кислоты (например, Ибупрофен, Напроксен), рофекоксиб (например, Целебрекс)) или липоксигеназа (например, Зилеутон; антагонист рецептора лейкотриена (например, Зафирлукаст, Мотелукаст), простагландин, фактор активации тромбоцитов (PAF) или тромбоксан (например, Сератродаст); антигистамин).
Таким образом, в другом аспекте изобретение относится к композиции, определенной здесь, пригодной для профилактики или лечения нейродегенеративной болезни. Все ссылки на нейродегенеративную болезнь могут быть отнесены к ее острому или хроническому течению. Композиции настоящего изобретения могут быть использованы для лечения человека и в ветеринарии. Лечение может носить профилактический или терапевтический характер. Соответственно композиции настоящего изобретения являются полезными для лечения, профилактики и улучшения (состояния) различных нервных болезней и являются полезными, например, в качестве терапевтических и профилактических средств для острых нейродегенеративных болезней (инсульт острой стадии, травма головы, спинномозговая травма (как, например, повреждение спинного мозга), нейропатия, вызванная гипоксией или гипогликемией), хронические нейродегенеративные болезни (такие как болезнь Альцгеймера, болезнь Паркинсона, хорея Гентингтона, боковой амиотрофический склероз и дегенерация нервных волокон, относящихся к спинному мозгу и мозжечку), эпилепсия, печеночная энцефалопатия, периферическая нейропатия, синдром Паркинсона, спастический паралич, боль, невралгия, шизофрения, тревога, злоупотребление (любыми) лекарственными средствами, тошнота, рвота, расстройство мочеиспускания, зрительное расстройство (нарушение зрения) вследствие глакомы; слуховое расстройство (нарушение слуха), обусловленное антибиотиками; пищевое отравление, инфекционный энцефаломиелит (такой как цереброспинальный менингит (например, ВИЧ-индуцированный цереброспинальный менингит), церебрососудистая деменция, деменция или нервные симптомы, обусловленные менингитом.
В данном тексте нейродегенеративная болезнь может представлять демиелинизирующее расстройство. Используемый здесь термин “демиелинизирующее расстройство” включает любое расстройство, которое приводит к снижению уровня миелинизации (образование миелинового слоя), например энцефалит, острый рассеянный энцефаломиелит, острая демиелинизирующая полинейропатия (синдром Гийена-Барре), хроническая воспалительная демиелинизирующая полинейропатия, рассеянный склероз, болезнь Маркиафавы-Биньями), миелинолиз центрального пути варолиева моста мозга, синдром Девика, болезнь Бало, ВИЧ-миелопатия; индуцированная вирусом человеческого Т-клеточного лейкоза (HTLV) миелопатия; прогрессирующая многоочаговая лейкоэнцефалопатия, или вторичное демиелинизирующее расстройство, т.е. где потеря миелина происходит, как следствие вторичного патологического процесса. Примерами вторичных демиелинизирующих болезней являются красная волчанка с поражением ЦНС, нодозный (узелковый) полиартериит, синдром Шегрена, саркоидная гранулема или изолированный церебральный васкулит.
Фактически нейродегенерация, основной коррелят перманентного клинического бессилия при рассеянном склерозе, возникает резко во время активной демиелинизации и может привести к более чем 75% потере аксонов в хронической фазе болезни. Аналогично, дегенерация нейронов и аксонов также является патологическим компонентом острой и хронической моделей EAE.
Соединение настоящего изобретения и иммунорегуляторное или противовоспалительное средство могут быть использованы раздельно, одновременно или последовательно для лечения нейродегенеративной болезни, например демиелинизирующего расстройства. Сочетание вышеуказанных активных компонентов может обеспечить синергически (действующую) эффективную комбинацию.
На протяжении всего этого описания профилактика и/или лечение любой болезни или расстройства означает любой результат, который облегчает любое нарушение или любое медиальное расстройство, до некоторой степени, и включает профилактику и/или лечение как таковые. Кроме того, термин 'лечение' означает любое уменьшение интенсивности симптомов заболевания, расстройства, синдрома, состояния, боли, симптома или комбинации двух или большего числа из вышеперечисленного.
Поэтому изобретение, кроме того, обеспечивает применение описанного здесь соединения и иммунорегуляторного или противовоспалительного средства для получения лекарственного препарата для профилактики или лечения нейродегенеративной болезни. Нейродегенеративная болезнь может представлять демиелинизирующее расстройство. При таком использовании соединение, раскрытое здесь, и иммунорегуляторное или противовоспалительное средство могут вводиться раздельно, одновременно или последовательно.
Кроме того, настоящее изобретение относится к способу профилактики или лечения нейродегенеративной болезни, и этот способ включает введение пациенту определенной здесь композиции. Пациент особо нуждается в введении такой композиции. Способы настоящего изобретения могут осуществляться для профилактики или лечения, например, демиелинизирующего расстройства. В таких способах иммунорегуляторное или противовоспалительное средство может вводиться раздельно, одновременно или последовательно.
Композиции настоящего изобретения вводят, или используют, или получают для использования в количестве, достаточном для профилактики и/или лечения симптомов состояния, болезни или расстройства. Для всех аспектов изобретения, в частности медицинских аспектов, применение композиции предусматривает наличие определенной схемы приема лекарственного средства, которая, обычно, в конечном счете, определяется штатным врачом больницы с учетом таких факторов, как тип соединения, подлежащий использованию, тип животного, возраст, масса тела, тяжесть симптомов, способ введения, побочные реакции и/или другие противопоказания. Конкретные диапазоны доз могут быть установлены посредством клинических испытаний по определенной программе, предусматривающей полный контроль за развитием болезни и восстановлением состояния пациента. Такие испытания могут использовать схему построения эксперимента с возрастающей дозой, используя низкий процент от максимальных предельно допустимых доз для животных в качестве исходной дозы для человека.
Физиологически приемлемые соединения в композициях настоящего изобретения могут вводиться на протяжении длительного периода времени в случае непрерывной терапии, например недели или более, месяца или более, года или более, или неограниченного времени.
Следующий аспект изобретения относится к набору, включающему первый контейнер, содержащий определенное в настоящем описании соединение, и второй контейнер, содержащий иммунорегуляторное или противовоспалительное средство, необязательно, с инструкциями по использованию, и этот набор может дополнительно включать приемлемый носитель или наполнитель (комбинированный с соединением в первом контейнере и/или средством во втором контейнере или отдельный носитель для каждого контейнера).
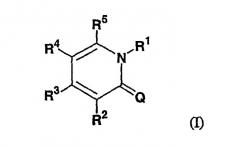
Соединения настоящего изобретения могут быть представлены нижеследующей формулой, его солью или его гидратами.
В формуле Q означает NH, O или S; и R1, R2, R3, R4 и R5 являются одинаковыми или отличными друг от друга и каждый представляет собой атом водорода, атом галогена, C1-6алкильную группу или группу, представленную формулой -X-A (где X означает простую связь, необязательно замещенную C1-6алкиленовую группу, необязательно замещенную
C2-6алкениленовую группу, необязательно замещенную C2-6алкиниленовую группу, -O-, -S-, -CO-, -SO-, -SO2-, -N(R6)-, -N(R7)-CO-, -CO-N(R8)-, -N(R9)-CH2-, -CH2-N(R10)-, -CH2-CO-, -CO-CH2-, -N(R11)-S(O)m-, -S(O)n-N(R12)-, -CH2-S(O)p-,
-S(O)q-CH2-, -CH2-O-, -O-CH2-, -N(R13)-CO-N(R14)- или -N(R15)-CS-N(R16)- (где R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16 означают атом водорода, C1-6алкильную группу или C1-6алкоксигруппу; и m, n, p и q означает целое число, равное независимо 0, 1 или 2); и A означает C3-8 циклоалкильную группу, C3-8 циклоалкенильную группу, 5-14-членную неароматическую гетероциклическую группу, C6-14 ароматическую циклическую углеводородную группу или 5-14-членную ароматическую гетероциклическую группу, которая может быть замещена соответственно при условии, что 3 группы среди R1, R2, R3, R4 и R5 являются всегда одинаковыми или отличными друг от друга и каждая означает -X-A; а остальные 2 группы всегда означают атом водорода, атом галогена или C1-6алкильную группу). Из вышеупомянутых определений исключены случаи, когда (1) Q представляет собой O; R1 и R5 представляют атомы водорода и R2, R3 и R4 представляют фенильные группы, (2) Q представляет собой O; R1 и R4 представляют атомы водорода и R2, R3 и R5 представляют фенильные группы, и (3) Q представляет собой O; R1 и R2 представляют атомы водорода и R3, R4 и R5 представляют фенильные группы.
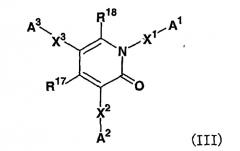
Т.е. настоящее изобретение относится к (1) соединению, представленному вышеупомянутой формулой (I), его соли или его гидратам; (2) соединению согласно вышеупомянутому (1), его соли или его гидратам, которое представлено формулой
где Q означает NH, O или S; X1, X2 и X3 являются одинаковыми или отличными друг от друга и каждый означает простую связь, необязательно замещенную C1-6алкиленовую группу, необязательно замещенную C2-6алкениленовую группу, необязательно замещенную C2-6алкиниленовую группу, -O-, -S-, -CO-, -SO-, -SO2-,
-N(R6)-, -N(R7)-CO-, -CO-N(R8)-, -N(R9)-CH2-, -CH2-N(R10)-, -CH2-CO-, -CO-CH2-,
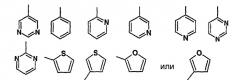
-N(R11)-S(O)m-, -S(O)n-N(R12)-, -CH2-S(O)p-, -S(O)q-CH2-, -CH2-O-, -O-CH2-, -N(R13)-CO-N(R14)- или -N(R15)-CS-N(R16)- (где R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16 означают атом водорода, C1-6алкильную группу или C1-6алкоксигруппу и m, n, p и q являются независимыми друг от друга и каждый означает целое число, равное 0, 1 или 2); A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая означает необязательно замещенную C3-8 циклоалкильную группу, C3-8 циклоалкенильную группу, 5-14-членную неароматическую гетероциклическую группу, C6-14 ароматическую циклическую углеводородную группу или 5-14-членную ароматическую гетероциклическую группу и R17 и R18 являются одинаковыми или отличными друг от друга и каждая означает атом водорода, атом галогена или C1-6алкильную группу; (3) соединению согласно вышеупомянутому (2), его соли или его гидратам, где X1, X2 и X3 представляют (1) простую связь, (2) C1-6алкиленовую группу, C2-6алкениленовую группу или C2-6алкиниленовую группу, которая может быть необязательно замещена, соответственно, одной или несколькими группами, выбранными из нижеследующей группы-заместителя a, (3) -O-, (4) -S-, (5) -CO-, (6) -SO-, (7) -SO2-, (8) -N(R6)-, (9) -N(R7)-CO-, (10) -CO-N(R8)-, (11) -N(R9)-CH2-, (12) -CH2-N(R10)-, (13) -CH2-CO-, (14) -CO-CH2-, (15) -N(R11)-S(O)m-, (16) -S(O)n-N(R12)-, (17) -CH2-S(O)p-, (18) -S(O)q-CH2-, (19) -CH2-O-, (20) -O-CH2-, (21) -N(R13)-CO-N(R14)- или (22) -N(R15)-CS-N(R16)- (где R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16, m, n, p и q имеют значения, определенные выше); и A1, A2 и A3 представляют C3-8циклоалкильную группу, C3-8циклоалкенильную группу, 5-14-членную неароматическую гетероциклическую группу, C6-14ароматическую циклическую углеводородную группу или 5-14-членную ароматическую гетероциклическую группу, которая может быть необязательно замещена одной или несколькими группами, выбранными из нижеследующей группы-заместителя b (группа-заместитель a: группа, состоящая из гидроксигруппы, атома галогена и нитрильной группы; и группа-заместитель b: группа, состоящая из (1) гидроксигруппы, (2) атома галогена, (3) нитрильной группы, (4) нитрогруппы, (5) C1-6алкильной группы, C2-6алкенильной группы или C2-6алкинильной группы, которая может быть необязательно замещена одной или несколькими группами, выбранными из группы, состоящей из гидроксигруппы, нитрильной группы, атома галогена, C1-6алкиламиногруппы, ди(C1-6алкил)аминогруппы, C2-6алкениламиногруппы, ди(C2-6алкениламино)группы, C2-6алкиниламиногруппы, ди(C2-6алкиниламино)группы, N-C1-6алкил-N-C2-6алкениламиногруппы, N-C1-6алкил-N-C2-6алкиниламиногруппы, N-C2-6алкенил-N-C2-6алкиниламиногруппы, аралкилоксигруппы, TBDMS-оксигруппы, C1-6алкилсульфониламиногруппы, C1-6алкилкарбонилоксигруппы, C2-6алкенилкарбонилоксигруппы, C2-6алкинилкарбонилоксигруппы, N-C1-6алкилкарбамоильной группы, N-C2-6алкенилкарбамоильной группы и N-C1-6алкинилкарбамоильной группы, (6) C1-6алкоксигруппы, C2-6алкенилоксигруппы или C2-6алкинилоксигруппы, которая может быть необязательно замещена соответственно одной или несколькими группами, выбранными из группы, состоящей из C1-6алкиламиногруппы, аралкилоксигруппы и гидроксигруппы, (7) C1-6алкилтиогруппы, C2-6алкенилтиогруппы или C2-6алкинилтиогруппы, которая может быть необязательно замещена соответственно одной или несколькими группами, выбранными из группы, состоящей из гидроксигруппы, нитрильной группы, атома галогена, C1-6алкиламиногруппы, аралкилоксигруппы, TBDMS-оксигруппы, C1-6алкилсульфониламиногруппы, C1-6алкилкарбонилоксигруппы и C1-6алкилкарбамоильной группы, (8) карбонильной группы, замещенной группой, выбранной из группы, состоящей из C1-6алкоксигруппы, аминогруппы, C1-6алкиламиногруппы, ди(C1-6алкил)аминогруппы, C2-6алкениламиногруппы, ди(C2-6алкенил)аминогруппы, C2-6алкиниламиногруппы, ди(C2-6алкинил)аминогруппы, N-C1-6алкил-N-C2-6алкениламиногруппы, N-C1-6алкил-N-C2-6алкиниламиногруппы и N-C2-6алкенил-N-C2-6алкиниламиногруппы, (9) аминогруппы, которая может быть необязательно замещена одной или двумя группами, выбранными из группы, состоящей из C1-6алкильной группы, C2-6алкенильной группы, C2-6алкинильной группы, C1-6алкилсульфонильной группы, C2-6алкенилсульфонильной группы, C2-6алкинилсульфонильной группы, C1-6алкилкарбонильной группы, C2-6алкенилкарбонильной группы и C2-6алкинилкарбонильной группы, (10) C1-6алкилсульфонильной группы, (11) C2-6алкенилсульфонильной группы, (12) C2-6алкинилсульфонильной группы, (13) C1-6алкилсульфинильной группы, (14) C2-6алкенилсульфинильной группы, (15) C2-6алкинилсульфинильной группы, (16) формильной группы, (17) C3-8циклоалкильной группы или C3-8циклоалкенильной группы, которая может быть необязательно замещена соответственно одной или несколькими группами, выбранными из группы, состоящей из гидроксигруппы, атома галогена, нитрильной группы, C1-6алкильной группы, C1-6алкилоксигруппы, C1-6алкилоксиC1-6алкильной группы и аралкильной группы, (18) 5-14-членной неароматической гетероциклической группы, которая может быть необязательно замещена одной или несколькими группами, выбранными из группы, состоящей из гидроксигруппы, атома галогена, нитрильной группы, C1-6алкильной группы, C1-6алкилоксигруппы, C1-6алкилоксиC1-6алкильной группы и аралкильной группы, (19) C6-14ароматической циклической углеводородной группы, которая может быть необязательно замещена одной или несколькими группами, выбранными из группы, состоящей из гидроксигруппы, атома галогена, нитрильной группы, C1-6алкильной группы, C1-6алкилоксигруппы, C1-6алкилоксиC1-6алкильной группы и аралкильной группы, и (20) 5-14-членной ароматической гетероциклической группы, которая может быть необязательно замещена одной или несколькими группами, выбранными из группы, состоящей из гидроксигруппы, атома галогена, нитрильной группы, C1-6алкильной группы, C1-6алкилоксигруппы, C1-6алкилоксиC1-6алкильной группы и аралкильной группы); (4) соединению согласно вышеупомянутому (2), его соли или его гидратам, где A1, A2 и/или A3 являются одинаковыми или отличными друг от друга и каждая представляет собой необязательно замещенный C3-8циклоалкил, C3-8циклоалкенил или 5-14-членную неароматическую гетероциклическую структуру; (5) соединению согласно вышеупомянутому (2), его соли или его гидратам, где A1, A2 и/или A3 являются одинаковыми или отличными друг от друга и каждая представляет собой необязательно замещенную C6-14ароматическую углеводородную циклическую структуру или 5-14-членную ароматическую гетероциклическую структуру; (6) соединению согласно вышеупомянутому (2), его соли или его гидратам, где А1, А2 и А3 являются одинаковыми или отличными друг от друга и каждая представляет собой фенильную группу, пирролильную группу, пиридильную группу, пиридазинильную группу, пиримидинильную группу, пиразинильную группу, тиенильную группу, тиазолильную группу, фурильную группу, нафтильную группу, хинолильную группу, изохинолильную группу, индолильную группу, бензимидазолильную группу, бензотиазолильную группу, бензоксазолильную группу, имидазопиридильную группу, карбазолильную группу, циклопентильную группу, циклогексильную группу, циклогексенильную группу, диоксинильную группу, адамантильную группу, пирролидинильную группу, пиперидинильную группу, пиперазинильную группу или морфолильную группу, которые могут необязательно иметь один или несколько заместителей соответственно; (7) соединению согласно вышеупомянутому (2), его соли или его гидратам, где A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая представляет собой группу, представленную формулой
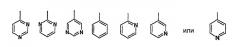
которые могут быть замещенными; (8) соединению согласно вышеупомянутому (2), его соли или его гидратам, где A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая необязательно замещена гидроксильной группой, атомом галогена, аминогруппой или нитрильной группой; (9) соединению согласно вышеупомянутому (7), его соли или его гидратам, где заместители A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая представляет собой гидроксильную группу, атом галогена или аминогруппу, нитрильную группу или нитрогруппу; (10) соединению согласно вышеупомянутому (1) или (2), его соли или его гидратам, где Q представляет собой кислород; (11) соединению согласно вышеупомянутому (1) или (2), его соли или его гидратам, где X1, X2 и X3 являются одинаковыми или отличными друг от друга и каждая представляет собой простую связь, -CH2-, -CH(OH)-, -CH2-CH2-, -CH=CH-, -C≡C-, -O- или -CO-; (12) соединению согласно вышеупомянутому (2), его соли или его гидратам, где X1, X2 и X3 представляют простые связи; (13) соединению согласно вышеупомянутому (2), его соли или его гидратам, где R17 и R18 являются одинаковыми или отличными друг от друга и каждая представляет собой атом водорода, фтор, хлор, бром, йод, метильную группу, этильную группу, н-пропильную группу или изопропильную группу; (14) соединению согласно вышеупомянутому (2), его соли или его гидратам, где R17 и R18 представляют атом водорода; (15) соединению согласно вышеупомянутому (1) или (2), его соли или его гидратам, которое представлено формулой
где X1, X2, X3, A1, A2, A3, R17 и R18 имеют такие же значения, как определено в вышеупомянутом (2); (16) соединение согласно вышеупомянутому (15), его соли или его гидратам, где A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая представляет собой необязательно замещенную C6-14 ароматическую углеводородную циклическую структуру или 5-14-членную ароматическую гетероциклическую структуру; (16) соединению согласно вышеупомянутому (15), его соли или его гидратам, где A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая представляет собой необязательно замещенную C6-14ароматическую углеводородную циклическую структуру или 5-14-членную ароматическую гетероциклическую структуру; (17) соединению согласно вышеупомянутому (15), его соли или его гидратам, где A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая представляет собой необязательно замещенную фенильную группу, пирролильную группу, пиридильную группу, пиридазинильную группу, пиримидинильную группу, пиразинильную группу, тиенильную группу, тиазолильную группу, фурильную группу, нафтильную группу, хинолильную группу, изохинолильную группу, индолильную группу, бензимидазолильную группу, бензотиазолильную группу, бензоксазолильную группу, имидазопиридильную группу, карбазолильную группу, циклопентильную группу, циклогексильную группу, циклогексенильную группу, диоксинильную группу, адамантильную группу, пирролидинильную группу, пиперидинильную группу, пиперазинильную группу или морфолильную группу; (18) соединению согласно вышеупомянутому (15), его соли или его гидратам, где A1, A2 и A3 являются одинаковыми или отличными друг от друга и каждая представляет собой группу, представленную нижеследующей формулой