Капсулы, содержащие водные наполняющие композиции, стабилизированные производным циклодекстрина
Иллюстрации
Показать всеИзобретение относится к лекарственным средствам и касается капсул для доставки биологически активного агента, содержащих: а) водорастворимую, размываемую, разрушаемую и/или набухающую оболочку; и b) водную наполняющую композицию, включающую один или более активных агентов, воду, находящуюся в количестве от по меньшей мере приблизительно 10% масс./масс. до менее приблизительно 70% масс./масс; и водорастворимое производное циклодекстрина, присутствующее в количестве по меньшей мере 30% масс./масс. в пересчете на общую массу воды и производного циклодекстрина в наполняющей композиции, где количество производного циклодекстрина достаточно для подавления растворения, размывания, разрушения и/или набухания оболочки, вызываемых водой в наполняющей композиции, и где капсула имеет срок хранения, по меньшей мере, одну неделю. Также раскрыт способ стабилизации капсулы. Изобретение направлено на создание капсул с устойчивыми к растворению, размыванию, разрушению и набуханию оболочками. 11 н. и 40 з.п. ф-лы, 11 ил., 11 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к капсуле, содержащей производное циклодекстрина в водном наполнителе, где циклодекстрин присутствует в количестве, достаточном для придания устойчивости оболочке капсулы в отношении размывания, растворения, набухания или разрушения под действием воды наполнителя.
Уровень техники, к которому относится изобретение
Широко известны капсулы с жидким или полужидким наполнением. Данные, наполняющие композиции, обычно предпочтительны по сравнению с капсулами с твердым наполнением, поскольку легче получить более высокую степень однородности для капсул с жидким или полужидким наполнением, чем для капсул с твердым наполнением.
Наполняющие композиции капсулы могут быть водными или неводными. Обычно применяемые вещества для наполняющих композиций капсулы включают: 1) несмешивающиеся с водой летучие и нелетучие жидкости, 2) смешивающиеся с водой летучие и нелетучие жидкости, 3) разнообразные носители, такие как глицерин, пропиленгликоль, вода и спирты с низкой молекулярной массой, кетоны, кислоты, амины и сложные эфиры. Суспензии активных агентов часто включаются в растительные или неорганические масла, триглицериды, гликоли, такие как полиэтиленгликоли и пропиленгликоль, поверхностно-активные вещества, такие как полисорбаты, или их сочетания.
Вещество, образующее оболочку капсулы, выбирают так, чтобы довести до максимума стабильность оболочки по отношению к наполняющей композиции при поддержании в то же самое время желаемого профиля высвобождения активного агента. Неводные наполняющие композиции широко применяются, потому что оболочка капсулы должна быть растворимой в воде, размываемой или разрушаемой для того, чтобы быть пригодной для применения в водной среде, например, для перорального введения субъекту. Довольно часто, однако, желательным является включение воды в наполняющую композицию для того, чтобы получить желаемый профиль высвобождения активного агента, увеличить растворимость активного агента в наполняющей композиции и/или довести до максимума стабильность ингредиентов наполняющей композиции. Когда применяют водную наполняющую композицию, оболочку капсулы обычно изготовляют из вещества, которое более устойчиво к растворению в воде, размыванию или разрушению.
Известен ряд различных относительно стабильных в отношении воды композиций оболочки. Данные композиции оболочки обычно включают вещества или изготовлены с помощью методов, которые снижают нестабильность оболочки в отношении воды в наполняющей композиции. Например, Banner Pharmacaps и Cardinal Health предлагают капсулы, которые являются в некоторой степени стабилизированными, одни - в отношении липофильного наполнителя, другие - в отношении гидрофильного наполнителя. Однако применение таких оболочек приводит к изменению характеристик состава капсулы. Соответственно, фармацевт должен тщательно сопоставлять количество воды, включенной в наполняющую композицию, и характеристики водной стабильности оболочки. Более того, известные водные наполняющие композиции ограничиваются по количеству воды и сочетанию активных агентов и носителей, которые могут быть в них включены. Другими словами известные оболочки, содержащие наполняющие композиции с высоким содержанием воды, все еще разрушаются, растворяются, набухают или размываются при хранении.
В ряде ссылок раскрываются дозированные формы в виде капсул, наполненных водной жидкостью или полутвердым носителем, активным агентом и другим компонентом, добавленным для снижения или прекращения растворения, размывания или разрушения оболочки наполняющей композицией.
Kuentz et al. (International Journal of Pharmaceutics (2002) 236(1-2), 145-152) раскрывает капсулы, наполненные жидкой композицией, включающей воду, ПЭГ и поли(винилпирролидон), или включающей воду, глицериды (LABRASOL®) и коллоидный диоксид кремния (AEROSIL®). Компоненты добавлены для определения, какое их сочетание будет способно снизить или остановить растворение, размывание или разрушение оболочки наполняющей композицией. Kuentz et al. не раскрывают применение циклодекстринов.
Bowtle (презентация, озаглавленная “Liquid-encapsulation technology for oral delivery”) раскрывает применение гидрогенизированного сиропа глюкозы в качестве вещества, подходящего для применения в капсулах с жидким наполнением. Bowtle не раскрывает применение циклодекстринов для снижения или прекращения растворения, размывания или разрушения оболочки наполняющей композицией.
В японском патенте No. JP 61207329, принадлежащем Mochizuki et al., раскрывается мягкая желатиновая капсула, наполненная водным жидким носителем, сахаром и активным агентом. Сахар присутствует в количестве ≥55 мас.% по отношению к наполняющей композиции. Раскрыты сахара, такие как сахароза, глюкоза, фруктоза и мальтоза. Сахар присутствует в количестве, достаточном для снижения или прекращения растворения, размывания или разрушения оболочки наполняющей композицией. Mochizuki et al. не раскрывают применение циклодекстринов для снижения или прекращения растворения, размывания или разрушения оболочки наполняющей композицией.
В патенте Германии No. DE 19545043, принадлежащем Lucks et al., раскрывается мягкая желатиновая капсула с жидким наполнением. Жидкость присутствует в одной фазе. Наполняющая композиция включает 1-20 мас.% полиола (такого как глицерин, пропандиол или ПЭГ) или бензиловый спирт, 1-20 мас.% поверхностно-активного вещества, 79-98 мас.% сопутствующего поверхностно-активного вещества (такого как глицериды), <5 мас.% этанола и <10 мас.% воды. Lucks et al. не раскрывает циклодекстрины. Вода присутствует в количестве, достаточно низком для сведения к минимуму растворения, размывания или разрушения оболочки наполняющей композицией. Lucks et al. не раскрывают применение циклодекстринов для снижения или прекращения растворения, размывания или разрушения оболочки наполняющей композицией.
В патенте США No. 5037698, принадлежащем Brunel, раскрывается капсула с твердым или полутвердым наполнением, в которой наполняющая композиция включает воду (0,1-10 мас.%), загущающий агент (≥35 мас.%), гигроскопический или разжижающийся агент (0,1-50 мас.%) и, необязательно, агент для сохранения равновесия (0,1-15 мас.%). Вода присутствует в или приблизительно в стехиометрических количествах в отношении гигроскопического или разжижающегося агента так, чтобы мог образовываться гидрат, но разрушение оболочки водой сводилось к минимуму. Загущающий агент представляет собой твердый, размягчающийся при нагревании или полутвердый эксципиент. Агент для сохранения равновесия включает соединения, такие как алифатические или ароматические гидроксисоединения, включая, например, смягчающие агенты (глицерин) и масла. Brunel не раскрывает применение циклодекстринов.
В патенте США No. 5707648, принадлежащем Yiv, раскрывается двухфазная капсула с жидким наполнением, содержащая масляную фазу и водную фазу. Водная фаза включает воду (2-30 мас.%) и ПЭГ (60-95 мас.%), где отношение ПЭГ к воде составляет ≥2:1 или 2:1-99:1. Композиция также нуждается в поверхностно-активном веществе и активном агенте. ПЭГ присутствует в количестве, достаточном для снижения или прекращения растворения, размывания или разрушения оболочки наполняющей композицией. Yiv не раскрывает применение циклодекстринов.
В публикации предварительного патента США No. 2003/0133974, принадлежащей Curatolo et al., раскрывается инкапсулированная дозированная форма, содержащая сертралин, однако, данная дозированная форма включает несмешиваемую с водой среду носителя.
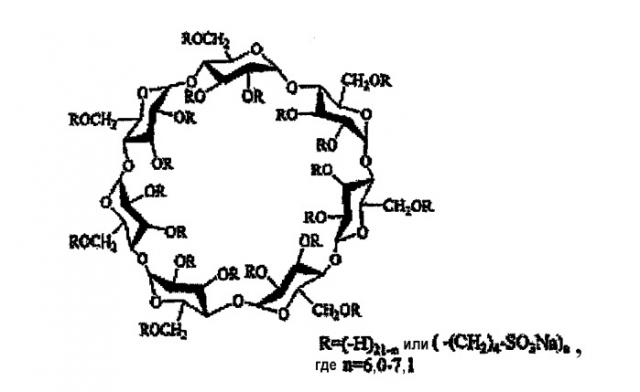
Циклодекстрины и их производные широко применяются в жидких композициях для увеличения растворимости в воде гидрофобных соединений. Циклодекстрины представляют собой циклические углеводы, происходящие от крахмала. Немодифицированные циклодекстрины различаются по количеству глюкопиранозных единиц, соединенных вместе в цилиндрическую структуру. Родительские циклодекстрины содержат 6, 7 или 8 глюкопиранозных единиц и обозначаются как α-, β- и γ-циклодекстрин, соответственно. Каждая субъединица циклодекстрина имеет вторичные гидроксильные группы в положениях 2 и 3 и первичную гидроксильную группу в положении 6. Циклодекстрины могут быть изображены как полые усеченные конусы с гидрофильными внешними поверхностями и гидрофобными внутренними полостями. В водных растворах данные гидрофобные полости дают укрытие гидрофобным органическим соединениям, которые могут подгонять полностью или частично свою структуру под данные полости. Данный процесс, известный как комплексообразование (образованием комплекса включения), может приводить к увеличенной кажущейся водной растворимости и стабильности образующего комплекс лекарственного средства. Комплекс стабилизируется с помощью гидрофобных взаимодействий и не вовлекает образование каких-либо ковалентных связей.
Химическая модификация родительских циклодекстринов (обычно в гидроксильных частях) приводит у производных иногда к улучшенной безопасности при сохранении или улучшении способности к образованию комплекса циклодекстрина. В настоящее время доступен ряд различных производных циклодекстрина, включая производные сульфобутилового сложного эфира, такие как SBE1-β-CD и SBE4-β-CD (степень замещения ~4), SBE7-β-CD (степень замещения ~7, циклодекстрин CAPTISOL®); гидроксипропильные производные, такие как ENCAPSIN™ (степень замещения ~4; HP4-β-CD) и MOLECUSOL™ (степень замещения ~8; HP8-β-CD); карбоксилированные производные; сульфатированные производные; алкилированные производные; гидроксиалкилированные производные; метилированные производные; и карбокси-β-циклодекстрины, например, сукцинил-β-циклодекстрин, 6A-амино-6A-дезокси-N-(3-карбоксипропил)-β-циклодекстрин.
SAE-CD представляют собой класс отрицательно заряженных циклодекстринов, которые различаются по природе алкильного спейсера, солевой форме, степени замещения и исходному родительскому циклодекстрину. Натриевая соль сульфобутилового эфирного производного бета-циклодекстрина в среднем с приблизительно 7 заместителями на молекулу циклодекстрина (SBE7-β-CD) коммерчески доступен от CyDex, Inc. (Kansas) в виде циклодекстрина CAPTISOL®.
Сульфобутиловый эфир β-циклодекстрина (Captisol ® )
Анионный сульфобутиловый эфирный заместитель существенно улучшает растворимость в воде родительского циклодекстрина. Обратимое, нековалентное комплексообразование лекарственных средств с циклодекстрином CAPTISOL® обычно позволяет достичь повышенной растворимости и стабильности лекарственных средств в водных растворах.
В ряде ссылок раскрываются капсульные дозированные формы, включающие наполняющую композицию, включающую циклодекстрин, водный или неводный носитель, активный агент и другие фармацевтические эксципиенты.
В патентах США No. 6287594, принадлежащем Wilson et al., и No. 6365180, принадлежащем Meyer et al., раскрываются пероральные жидкие композиции, которые могут быть включены в капсульные дозированные формы. Жидкие композиции включают кислый активный агент, разрыхляющий агент, солюбилизирующий агент (0-90% или 60-90 мас.%), необязательное поверхностно-активное вещество (0-10 мас.%) и необязательный пластифицирующий агент (0-25 мас.%). Разрыхляющим агентом может быть агент на основе углеводов, например, «производное циклодекстрина». Солюбилизирующий агент представляет собой воду или поли(этиленгликоль). Отношение активного агента к разрыхляющему агенту составляет от приблизительно 3:1 до приблизительно 1:30. Патенты не раскрывают того, что циклодекстрин может снизить или прекратить растворение, размывание или разрушение оболочки водной наполняющей композицией. Более того, не раскрыты примеры, включающие циклодекстрин.
В патенте США No. 6383471, принадлежащем Chen et al., раскрывается жидкая композиция, включающая ионизируемый гидрофобный активный агент, ионизирующий агент, поверхностно-активное вещество и необязательно солюбилизаторы, триглицериды и нейтрализующие агенты. Жидкая композиция может быть применена в капсулах. Chen et al. раскрыли, что солюбилизаторы могут включать циклодекстрины среди многих других соединений. Сульфобутиловый эфир циклодекстрина перечислен в качестве примера циклодекстрина. Chen et al. не раскрыли или предположили, что циклодекстрин присутствует в количестве, достаточном для снижения или прекращения растворения, размывания или разрушения оболочки водной наполняющей композицией.
В патентах США No. 6046177 и No. 5874418, принадлежащих Stella et al., раскрываются капсульные дозированные формы, содержащие неводную твердую физическую смесь SAE-CD и активного агента. Физическая смесь не является жидкой или полутвердой композицией и вода не включается в физическую смесь для того, чтобы снизить образование комплекса включения между циклодекстрином и активным агентом. Stella et al. не раскрывают того, что циклодекстрин может присутствовать в количестве, достаточном для снижения или прекращения растворения, размывания или разрушения оболочки водой в наполняющей композиции.
В патентах США No. 5376645 и No. 5134127, принадлежащих Stella et al., раскрываются фармацевтические композиции, включающие активный агент, SAE-CD и жидкий или твердый носитель. SAE-CD и активный агент присутствуют в виде комплекса включения. Stella et al. обычно раскрывают «мягкие желатиновые капсулы, в которых активный ингредиент (смесь, содержащая соединение включения SAE-CD и активного агента) смешивают с водой или маслом». Они также раскрывают, что «Фармацевтические составы, подходящие для перорального введения, в которых носитель является жидким, могут просто присутствовать в виде раствора в водной жидкости или неводной жидкости, или в виде жидкой эмульсии масло в воде или вода в масле». Stella et al. не раскрывают или предполагают, что SAE-CD может присутствовать в водной наполняющей композиции (для капсул) в количестве, достаточном для снижения или прекращения растворения, размывания или разрушения оболочки водой в наполняющей композиции. Более того, Stella et al. раскрывают сочетания, в которых SAE-CD должен образовывать комплекс включения с активным агентом.
В патенте США No. 3426011, принадлежащем Parmerter et al., раскрываются анионные циклодекстриновые производные, имеющие сульфоалкиловые эфирные заместители. Parmerter et al. не раскрывают применение сульфоалкиловых простых эфиров циклодекстринов в водной композиции, содержащейся в капсуле. Lammers et al. (Recl. Trav. Chim. Pays-Bas (1972), 91(6), 733-742); Staerke (1971), 23(5), 167-71) раскрывают производные в виде сульфоалкиловых простых эфиров циклодекстринов; однако, они не раскрывают применение циклодекстринов для снижения или прекращения растворения, размывания или разрушения оболочки водной наполняющей композицией.
Сохраняется потребность в усовершенствованных наполняющих композициях капсул, которые придают оболочке устойчивость в отношении растворения, размывания, набухания или разрушения водой наполняющей композиции. Ни кем в данной области техники не раскрыто или предложено изобретение, которое заявлено в данном описании. В предшествующем уровне техники не раскрывается водная наполняющая композиция для капсулы, где наполняющая композиция содержит производное циклодекстрина, такое как SAE-CD, активный агент и водный носитель, и производное циклодекстрина присутствует в количестве, достаточном для снижения или прекращения растворения, размывания или разрушения оболочки капсулы водой в наполняющей композиции. Более того, в предшествующем уровне техники не раскрыт или предложен способ стабилизации растворимой в воде, размываемой, набухающей или разрушаемой оболочки капсулы, окружающей водную наполняющую композицию, путем включения производного циклодекстрина в наполняющую композицию.
Сущность изобретения
Настоящее изобретение позволяет преодолеть некоторые или все недостатки, присущие другим известным композициям. В изобретении предлагается коммерчески конкурентнопособная композиция для применения в твердых или мягких капсулах, позволяющая получать и хранить капсулы, наполненные водной наполняющей композицией, без существенного разрушения, размывания, набухания или растворения оболочки капсулы в течение приемлемого срока хранения наполненной капсулы. В изобретении предлагается капсульная дозированная форма и водная наполняющая композиция для нее. Капсула включает мягкую или твердую оболочку. В одном аспекте изобретения предлагается водная наполняющая композиция на основе сульфоалкилового простого эфира циклодекстрина (SAE-CD) (на основе производного циклодекстрина). Наполняющая композиция включает водный наполнитель, сульфоалкиловый простой эфир циклодекстрина (SAE-CD), активный агент и другие необязательные ингредиенты. Оболочку обычно делают из растворимого в воде, размываемого, набухающего или разрушаемого вещества(в); однако может быть также применено вещество оболочки, которое не является растворимым в воде, размываемым, набухающим или разрушаемым. SAE-CD или другое производное циклодекстрина присутствует в количестве, достаточном для снижения или прекращения растворения, размывания, набухания или разрушения оболочки водой в наполняющей композиции. Другими словами, производное циклодекстрина снижает растворение, размывание, набухание или разрушение оболочки наполняющей композицией по сравнению со сходной наполняющей композицией без производного циклодекстрина, т.е. в которой производное циклодекстрина заменено водой или другим веществом, не стабилизирующим оболочку. В отсутствие другого вещества(в), стабилизирующего оболочку, SAE-CD стабилизирует оболочку капсулы в отношении растворения, размывания, набухания или разрушения, вызываемых водой в наполняющей композиции.
Капсульная дозированная форма включает оболочку и водную наполняющую композицию, включающую SAE-CD или растворимое в воде производное циклодекстрина. В отсутствие других веществ, стабилизирующих оболочку, и в зависимости от веществ, которые составляют оболочку, наполняющая композиция может включать, по меньшей мере, приблизительно 30 мас.% SAE-CD или производного циклодекстрина от суммарной массы воды и присутствующего SAE-CD или производного циклодекстрина. Количество производного циклодекстрина, требуемое для обеспечения желаемого уровня стабилизации оболочки, должно варьироваться в соответствии с композицией оболочки и веществами, составляющими наполняющую композицию. Чем более стабильна оболочка в отношении воды, тем меньше количество производного циклодекстрина, которое может потребоваться. Чем менее стабильна оболочка в отношении воды, тем больше количество производного циклодекстрина, которое может потребоваться. В отсутствие других веществ, стабилизирующих оболочку, наполняющая композиция включает менее чем приблизительно 70 мас.% воды от суммарной массы присутствующей воды и SAE-CD. Минимальный срок хранения наполненной капсулы составляет, по меньшей мере, приблизительно 1 неделю, 2 недели, 3 недели, 1 месяц, 3 месяца, 6 месяцев или 1 год или более чем приблизительно 1 год.
В изобретении также предлагается способ стабилизации растворимой, размываемой или разрушаемой оболочки капсулы, окружающей водную наполняющую композицию. Способ включает стадию включения SAE-CD или производного циклодекстрина в наполняющую композицию, так чтобы SAE-CD или производное циклодекстрина присутствовали в количестве, достаточном для снижения или прекращения растворения, размывания, набухания или разрушения оболочки капсулы, вызываемых водой в наполняющей композиции.
Наполняющая композиция может содержать другие вещества, стабилизирующие оболочку, и/или другие вещества, уменьшающие воздействие воды. Наполняющая композиция может также включать другие ингридиенты, пригодные для использования в таких композициях.
Для активного агента не является необходимым образование комплекса с производным циклодекстрина для того, чтобы производное циклодекстрина проявляло свой стабилизирующий эффект на оболочку капсулы. Наполняющая композиция может включать один или более активных агентов, и каждый активный агент независимо может образовывать комплекс или нет с производным циклодекстрина.
В настоящем изобретении может быть применено любое вещество, образующее оболочку, пригодное для применения в твердых и мягких оболочках капсул или для инкапсулирования наполняющей композиции.
Композиция SAE-CD имеет очень высокую стабильность при применении в качестве коммерческого продукта. Композиция может быть получена в виде чистой водной композиции, которая стерилизуется с помощью стерильной фильтрации (например, размер пор фильтра менее или равен 0,22 мкм) и другими общепринятыми способами. Водная композиция стабильна в разнообразных условиях хранения. SAE-CD может быть применен для увеличения растворимости активных агентов путем нековалентного ионного связывания и/или путем комплексообразования через образование комплексов включения.
Наполняющая композиция может быть или не быть чистой в зависимости от идентичности и количеств включенных в нее ингредиентов. При хранении чистота наполняющей композиции может или не может изменяться. Другими словами, один или более компонентов наполняющей композиции может дополнительно растворяться или осаждаться при хранении. Наполняющая композиция, которая представляет собой содержащую воду композицию, может быть гелем, сиропом, жидкостью, полутвердой, твердой, суспензией, эмульсией, пастой или стекловидным веществом.
Соответственно, в одном аспекте изобретения предлагается водная наполняющая композиция в размываемой водой, разрушаемой, набухающей или растворимой оболочке (или инкапсулирующем веществе), причем наполняющая композиция включает воду, одно или более производных циклодекстрина, необязательно один или более активных агентов и необязательно один или более эксципиентов, где производное циклодекстрина присутствует в количестве, достаточном для снижения или прекращения размывания, разрушения, набухания или растворения оболочки наполняющей композицией.
Конкретные варианты осуществления изобретения включают те, в которых: 1) производное циклодекстрина представляет собой SAE-CD и присутствует в количестве, по меньшей мере, приблизительно 30 мас.% от суммарной массы воды и SAE-CD; 2) наполняющая композиция дополнительно включает вещество, стабилизирующее оболочку; 3) наполняющая композиция имеет рН в диапазоне приблизительно 1-11; 4) наполняющая композиция включает один или более эксципиентов; 5) оболочка является мягкой оболочкой; 6) оболочка является твердой оболочкой; 7) активность воды наполняющей композиции составляет менее приблизительно 0,95 при измерении согласно подробно представленным здесь методикам; 8) наполняющая композиция дополнительно включает агент, усиливающий растворимость; 9) SAE-CD образует комплекс с одним или более активными агентами; 10) SAE-CD не образует комплекс с одним или более активными ингредиентами; 11) наполняющая композиция дополнительно включает жидкий носитель, отличный от воды; 12) наполняющая композиция представляет собой жидкость; 13) наполняющая композиция является полутвердой; 14) наполняющая композиция является твердой; 15) наполняющую композицию получают при температуре 5°С или выше, 25°С или выше, 35°С или выше, 45°С или выше или 50°С или выше; 16) композиция получена при температуре, приближающейся к температуре окружающей среды; 17) SAE-CD или производное циклодекстрина снижает активность воды водной наполняющей композиции; 18) оболочка представляет собой твердую желатиновую оболочку и наполняющая композиция включает, по меньшей мере, 60 мас.% производного циклодекстрина; 19) оболочка представляет собой мягкую желатиновую оболочку и наполняющая композиция включает, по меньшей мере, 50 мас.% производного циклодекстрина; 20) оболочка представляет собой твердую оболочку, включающую целлюлозу, производное целлюлозы, крахмал, производное крахмала или их сочетание и необязательно другие эксципиенты, и наполняющая композиция включает, по меньшей мере, 30 мас.% производного циклодекстрина; и/или 21) наполняющая композиция дополнительно включает вещество, снижающее активность воды.
В изобретении также предлагается первая капсула внутри второй капсулы. В данном случае первая и/или вторая капсула может содержать водную наполняющую композицию.
В другом аспекте изобретения предлагается способ стабилизации капсулы, наполненной водной композицией, в отношении размывания, растворения, набухания или разрушения ее оболочки водой, присутствующей в наполнителе, причем способ включает стадию включения в водный наполнитель производного циклодекстрина, присутствующего в количестве, достаточном для снижения или остановки скорости размывания, растворения, набухания или разрушения оболочки водой в наполняющей композиции по сравнению со скоростью размывания, растворения, набухания или разрушения оболочки сходной наполняющей композиции без производного циклодекстрина, т.е. наполняющей композиции, в которой производное циклодекстрина заменено водой или другим веществом, которое не стабилизирует оболочку (вещество, не стабилизирующее оболочку). Производное циклодекстрина способно стабилизировать оболочку в отношении размывания, растворения, набухания или разрушения оболочки водой в наполняющей композиции либо в отсутствии, либо необязательно в присутствии другого вещества, стабилизирующего оболочку.
В еще одном аспекте в изобретении также предлагается водная наполняющая композиция, заключенная в инкапсулирующее вещество, причем наполняющая композиция включает производное циклодекстрина и водный носитель, где производное циклодекстрина присутствует в количестве, достаточном для снижения активности воды наполняющей композиции, тем самым снижая скорость размывания, набухания или разрушения инкапсулирующего вещества водой, содержащейся в водном наполнителе. Активность воды наполняющей композиции обычно снижают до менее чем приблизительно 0,95±0,025, менее чем 0,95±0,01, менее чем 0,925 или менее чем 0,90. Предпочтительная величина активности воды может варьироваться в соответствии с компонентами, присутствующими в наполнителе и в соответствии с композицией самой оболочки капсулы. Наблюдаемая величина активности воды может также варьироваться в соответствии с прибором, применяемым для ее измерения, а также калибровкой прибора и воспроизводимостью измерений (что выражается величиной стандартного отклонения), получаемой на приборе. Предпочтительная величина активности воды должна также варьироваться в соответствии с композицией оболочки. Обычно, чем более стабильна в отношении воды оболочка, тем выше может быть активность воды наполняющей композиции, и чем менее стабильна в отношении воды оболочка, тем ниже должна быть активность воды наполняющей композиции, если наполняющая композиция не содержит какого-либо другого вещества(в), стабилизирующего оболочку.
Конкретные варианты осуществления изобретения включают те, в которых: 1) производное циклодекстрина представляет собой SAE-CD, HPCD, растворимое в воде производное циклодекстрина, способное снижать активность воды наполняющей композиции или их смеси; 2) наполняющая композиция дополнительно включает вещество, стабилизирующее оболочку; 3) наполняющая композиция дополнительно включает агент, снижающий активность воды; 4) наполняющая композиция дополнительно включает активный агент; и/или 5) наполняющая композиция дополнительно включает один или более фармацевтических эксципиентов.
В изобретении также предлагается способ снижения активности воды водной композиции, причем способ включает стадию включения растворимого в воде производного циклодекстрина в водную композицию в концентрации, достаточной для снижения активности воды.
В изобретении также предлагаются составы капсулы, которые обеспечивают высвобождение активного агента в соответствии с контролируемым, поддерживаемым, продолжительным, медленным, быстрым, пульсирующим, синхронизированным (заданным по времени), направленным профилем высвобождения, профилем высвобождения в ободочной кишке, профилем высвобождения нулевого порядка, псевдо-нулевого порядка, первого порядка, псевдо-первого порядка и/или профилем высвобождения в кишечнике, где высвобождение активного агента после попадания в среду применения начинается быстро (менее чем за 30 минут) или после периода задержки (≥30 мин). Другими словами, первоначальное высвобождение лекарственного средства может быть немедленным или замедленным, а также оно может высвобождаться в соответствии с модифицированными указанными в данном описании профилями высвобождения. Композиция капсулы может представлять собой капсулу с покрытием, капсулу без покрытия, осмотическую капсулу, капсулу в капсуле или многослойную капсулу.
В изобретении также предлагается капсула, содержащая:
растворимую в воде, размываемую, разрушаемую и/или набухающую оболочку; и
водную наполняющую композицию, включающую воду, присутствующую в количестве, достаточном для растворения, размывания, разрушения и/или набухания оболочки, один или более активных агентов и растворимое в воде производное циклодекстрина, присутствующее в количестве, достаточном для подавления растворения, размывания, разрушения или набухания оболочки водой наполняющей композиции, где капсула имеет срок хранения, по меньшей мере, одну неделю.
В другом варианте осуществления изобретения предлагается композиция стабилизированной капсулы, имеющей срок хранения, по меньшей мере, одну неделю, причем композиция содержит:
растворимую в воде, размываемую, набухающую и/или разрушаемую оболочку, и
водную наполняющую композицию, включающую растворимое в воде производное циклодекстрина, водный носитель и необязательно один или более активных агентов, где композиция капсулы имеет увеличенный срок хранения по сравнению с аналогичной композицией капсулы, не содержащей производного циклодекстрина и любого другого стабилизирующего вещества; воду в водном носителе, которая присутствует в количестве, достаточном, по меньшей мере, для частичного растворения, размывания, набухания и/или разрушения оболочки; и производное циклодекстрина, присутствующее в количестве, достаточном для снижения скорости или прекращения растворения, размывания, набухания или разрушения оболочки водой водного носителя.
В еще одном варианте осуществления изобретения предлагается
водная наполняющая композиция, заключенная в растворимое в воде, размываемое, набухающее и/или разрушаемое инкапсулирующее вещество, причем композиция включает:
водный носитель, присутствующий в количестве, достаточном, по меньшей мере, для частичного растворения, размывания, набухания и/или разрушения инкапсулирующего вещества;
растворимое в воде производное циклодекстрина, присутствующее в количестве, которое само по себе не достаточно для прекращения растворения, размывания, набухания и/или разрушения инкапсулирующего вещества водным носителем;
вещество, стабилизирующее оболочку, присутствующее в количестве, которое само по себе не достаточно для прекращения растворения, размывания, набухания и/или разрушения инкапсулирующего вещества водным носителем;
необязательно один или более активных агентов; и
необязательно один или более эксципиентов; где
производное циклодекстрина и вещество, стабилизирующее оболочку, синергично, по меньшей мере, снижают скорость или прекращают растворение, размывание, набухание и/или разрушение инкапсулирующего вещества водным носителем.
В конкретных вариантах осуществления: 1) водная наполняющая композиция является смешиваемой с водой; 2) активный агент присутствует в терапевтически эффективном количестве; 2) активный агент присутствует в субтерапевтически эффективном количестве; 3) активный агент умеренно растворим, незначительно растворим, очень мало растворим, практически не растворим или нерастворим в воде; 4) активный агент более растворим в водной наполняющей композиции, чем в воде; 5) активный агент растворим, легко растворим или очень хорошо растворим в воде; 6) активный агент образует комплексы с производным циклодекстрина с образованием комплекса включения и/или нековалентного ионного комплекса; 7) активный агент выбран из раскрытых здесь активных агентов или терапевтических категорий; 8) наполняющая композиция дополнительно содержит спирт; 9) наполняющая композиция дополнительно содержит смешиваемое с водой вещество, содержащее гидроксильную часть, например, полиол, гликоль, полимерный гликоль, спирт или гликолизированные глицериды, ПЭГ 660 12-гидроксистеарат (SOLUTOL™-15); 10) растворимое в воде производное циклодекстрина присутствует в количестве, достаточном для растворения активного агента, когда он высвобождается в среду применения, такую как желудочно-кишечный тракт или водная жидкая среда.
Другие характеристики, преимущества и варианты осуществления изобретения будут ясны специалистам в данной области техники из последующего описания и прилагаемых примеров.
Краткое описание фигур
Следующие фигуры являются частью настоящего описания и включены для дополнительной иллюстрации определенных аспектов изобретения. Изобретение может быть лучше понято со ссылкой на одну или более из данных фигур в сочетании с подробным описанием представленных здесь конкретных вариантах осуществления.
На фиг.1 представлен график зависимости H.S.I.T. от концентрации производного циклодекстрина (SBE-CD или HPCD), находящегося в наполняющей композиции, для оценки мягких желатиновых капсул LFB (оболочки для липофильного наполнителя от Banner) и HFC (оболочки для гидрофильного наполнителя от Cardinal), содержащих наполняющую композицию, по отношению к активности воды наполняющей композиции.
На фиг.2 представлен график зависимости H.S.I.T. от концентрации циклодекстрина, находящегося в наполняющей композиции, для оценки мягких желатиновых капсул HFB (оболочки для гидрофильного наполнителя от Banner) и HFC (оболочки для гидрофильного наполнителя от Cardinal), содержащих наполняющую композицию, по отношению к активности воды наполняющей композиции.
На фиг.3 представлен график зависимости H.S.I.T. от концентрации производного циклодекстрина (SBE-CD или HPCD), находящегося в наполняющей композиции, для оценки разных отличающихся оболочек капсул HGC (твердой желатиновой капсулы от Capsugel), HGS (твердой желатиновой капсулы от Shionogi), HPC (твердой гидроксипропилметилцеллюлозной капсулы от Capsugel), HPS (твердой гидроксипропилметилцеллюлозной капсулы от Shionogi), SSS (мягкой крахмальной капсулы от Swisscaps).
На фиг.4 представлен график оценки H.S.I.T. различных водных наполняющих композиций, включающих разные циклодекстрины и производные циклодекстринов, при приведении их в контакт с мягкой желатиновой капсулой для гидрофильного наполнителя.
На фиг.5 представлен график зависимости H.S.I.T. от концентрации ПЭГ (поли(этиленгликоля)) в наполняющей композиции, для оценки наполняющей композиции для мягкой желатиновой капсулы, содержащей наполняющую композицию, по отношению к активности воды наполняющей композиции.
На фиг.6a-6b представлены тройные графики зависимости H.S.I.T. от концентрации циклодекстрина, концентрации ПЭГ и концентрации воды, для оценки мягких желатиновых капсул, признаваемых их производителями как подходящие для применения с гидрофильной наполняющей композицией.
На фиг.7a-7b представлены тройные графики зависимости H.S.I.T. от концентрации циклодекстрина, концентрации ПЭГ и концентрации воды, для оценки мягких желатиновых капсул, признаваемых их производителями как подходящие для применения с липофильной наполняющей композицией.
На фиг.8 представлен график зависимости H.S.I.T. от концентрации воды в наполняющей композиции, включающей SBE, для оценки наполняющей композиции для мягкой желатиновой капсулы, содержащей наполняющую композицию, по отношению к активности воды наполняющей композиции. Различные линии представляют различные концентрации ПЭГ.
На фиг.9 представлен график зависимости H.S.I.T. от концентрации поли(винилпирролидон)а (ПВП) в наполняющей композиции для оценки наполняющей композиции для мягкой желатиновой к