Алмаз-углеродный материал и способ его получения
Иллюстрации
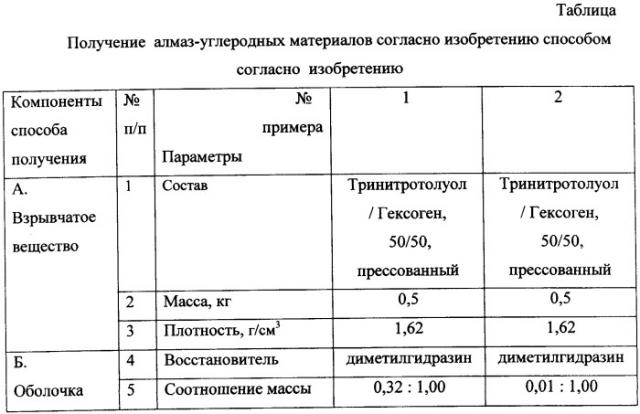
Показать всеИзобретение может быть использовано при изготовлении полировально-финишных композиций, пленочных покрытий, радиационно-стойких материалов. Алмаз-углеродный материал содержит углерод в виде алмазной кубической модификации и в рентгеноаморфной фазе в соотношении (40-80):(60-20) по массе соответственно и имеет следующий состав, мас.%: углерод 89,1-95,2; водород 1,2-5,0; азот 2,1-4,8; кислород 0,1-4,7; несгораемые примеси 1,4-4,8. Этот материал получают детонацией углеродсодержащего взрывчатого вещества с отрицательным кислородным балансом, помещенного в оболочку из конденсированной фазы, содержащей восстановитель при соотношении массы восстановителя в конденсированной фазе к массе используемого углеродсодержащего взрывчатого вещества не менее 0,01:1, в замкнутом объеме в газовой среде, инертной к углероду. Образцы полученного алмаз-углеродного материала подготавливают для исследования его элементного состава путем выдержки при 120-140°С под вакуумом 0,01-10,0 Па в течение 3-5 ч и последующей обработки при 1050-1200°С потоком кислорода со скоростью, обеспечивающей его сжигание в течение 40-50 с. Изобретение позволяет получить продукт, обладающий прогнозируемыми свойствами и элементным составом при высоком содержании углерода в желаемых фазовых состояниях. 3 н. и 1 з.п. ф-лы, 1 табл.
Реферат
Область техники
Изобретение относится к химии углерода, в частности к композиционным углеродным материалам, содержащим углерод кубической алмазной модификации и рентгеноаморфной углеродной фазы, а также к технологии их получения, в частности детонационным способам получения алмаз-углеродных материалов.
Предшествующий уровень техники
Известны различные композиционные материалы, получаемые способами детонационного синтеза из углеродсодержащих взрывчатых веществ и содержащие углерод в различных фазах.
Например, специалистам в области химии углерода известен конденсированный углерод (далее КУ), представляющий собой композиционный углеродный материал, содержащий углерод в различных модификациях и при этом, в зависимости от условий детонации углеродсодержащих взрывчатых веществ, содержащий или не содержащий углерод в кубической алмазной фазе.
Такой КУ может быть получен при детонации углеродсодержащих взрывчатых веществ с отрицательным кислородным балансом в специальной среде в условиях, позволяющих сохранить конденсированные углеродные продукты взрыва (Лямкин А.И., Петров Е.А., Ершов А.П. и др. Получение алмазов из взрывчатых веществ, ДАН СССР, 1988, т.302, с.611-613; Greiner N.R., Phillips D.S., Johnson F.J.D. Diamonds in detonation soot, Nature, 1988, vol.333, p.440-442; Петров В.А., Сакович Г.В., Брыляков П.М. Условия сохранения алмазов в процессе детонационного получения, ДАН СССР, 1990, т.313, №4, с.862-864; В.Ю.Долматов. Ультрадисперсные алмазы детонационного синтеза: свойства и применение. Успехи химии, 2001, т.70 (7), с.687-708; В.Ю.Долматов. Ультрадисперсные алмазы детонационного синтеза, Санкт-Петербург, СПбГПУ, 2003, 344 с.).
Известно, что способ получения КУ или алмаз-углеродного материала может включать подрыв заряда углеродсодержащего взрывчатого вещества в различной среде, например:
- в газовой среде, инертной к углероду, например в среде азота, углекислого газа, газообразных продуктов предыдущих подрывов (US, 5916955, C1);
- в водяной пене (Петров В.А., Сакович Г.В., Брыляков П.М. Условия сохранения алмазов в процессе детонационного получения, ДАН СССР, 1990, т.313, №4, с.862-964);
- при орошении заряда водой (RU, 2036835, С1);
- в водяной оболочке (US, 5353708, С1);
- во льду (RU, 2230702, С1).
Из существующих способов подрыва углеродсодержащих взрывчатых веществ наиболее эффективным с точки зрения выхода КУ и собственно алмазной модификации является подрыв заряда в водяной или ледяной оболочке (В.Ю.Долматов. Ультрадисперсные алмазы детонационного синтеза. Санкт-Петербург, СПбГПУ, 2003, 344 с.; RU, 2230702, С).
При этом полученный КУ представляет собой нанодисперсный углеродсодержащий порошок, обладающий специфическими свойствами и структурой. Например, КУ отличается высокой дисперсностью, большой удельной поверхностью, наличием образовавшихся дефектных углеродных структур, повышенной реакционной способностью.
Известен синтетический алмаз-углеродный материал (US, 5861349, А), состоящий в основном из сгруппированных круглых и неправильной формы частиц в диапазоне диаметров, не превышающем 0,1 µ, в котором:
a) элементный состав, мас.%: углерод от 75,0 до 90,0; водород от 0,8 до 1,5; азот от 0,8 до 4,5; кислород - до баланса;
b) фазовый состав, мас.%: аморфный углерод от 10 до 30, алмаз кубической модификации - до баланса;
c) пористая структура материала, имеющая поры объемом 0,6-1,0 см3/г;
d) поверхность материала с наличием на 10-20% поверхности метильных, нитритных, первичных и вторичных гидроксильных групп, имеющих различные химические сдвиги в области спектра ядерного магнитного резонанса и одну или более оксикарбоксильных функциональных групп, выбранных из группы, состоящей из карбонильных групп, карбоксильных групп, гуиноновых групп, гидропероксидных групп и лактоновых групп на 1-2% поверхности материала, связанных с атомами углерода некомпенсированными связями; и
e) специальная поверхность от 200 до 450 м2/г.
При этом указанный материал получают способом детонационного синтеза в закрытом объеме взрывчатого заряда, содержащего в основном углеродсодержащее взрывчатое вещество или смесь таких веществ, имеющего отрицательный кислородный баланс, при этом детонация заряда инициируется в присутствии частиц углерода в концентрации от 0,01 до 0,015 кг/м3 в среде, состоящей из кислорода от около 0,1 до 6% по объему и газа, инертного к углероду, при температуре от 303 до 363 K (US, 5861349, А). Способ осуществляют в камере давления с зарядом, имеющим отрицательный кислородный баланс и состоящим в основном из, по меньшей мере, одного углеродсодержащего твердого взрывчатого вещества.
Известен КУ, получивший название «алмаз-углеродный материал» (US, 5916955, А), содержащий углерод, водород, азот, кислород и различные несгораемые примеси и при этом содержащий углерод кубической модификации, углерод в рентгеноаморфной фазе и углерод кристаллической не алмазной модификации в соотношении фазовых модификаций углерода, мас.%:
| Углерод кубической модификации (алмазная фаза) | 30-75 |
| Рентгеноаморфная углеродная фаза | 10-15 |
| Углерод кристаллической модификации | остальное, |
при следующем элементном составе, мас.%:
| Углерод | 84,0-89,0 |
| Водород | 0,3-1,1 |
| Азот | 3,1-4,3 |
| Кислород | 2,0-7,1 |
| Несгораемые примеси | 2,0-5,0 |
Способ получения указанного алмаз-углеродного материала (US, 5916955, А) включает в себя стадию детонации заряда, состоящего из углеродсодержащего взрывчатого вещества, в замкнутом пространстве в атмосфере, содержащей газ, инертный к углероду, с образованием продуктов детонации, содержащих углерод кубической модификации (алмазная фаза), рентгеноаморфную углеродную фазу и углерод кристаллической модификации. При этом охлаждение продуктов детонации производят со скоростью от 200 до 6000 град/мин, и атмосфера содержит газовую среду, содержащую газы, образованные при взрыве первоначального заряда углеродсодержащего вещества.
Однако указанный выше способ получения алмаз-углеродного материала имеет низкий выход алмаз-углеродного материала - до 7,8 мас.% и при этом не позволяет получить материал с высокой эффективностью высокого качества, так как из-за низкого содержания важнейшего в алмаз-углеродном материале элемента - углерода - получаемый продукт содержит большое количество гетероатомов, в основном кислорода, присутствующего в виде лактонных, эфирных и альдегидных групп, что приводит к слишком высокой химической активности алмаз-углеродного материала. Это обстоятельство увеличивает вероятность деструктивных процессов в композициях с использованием алмаз-углеродного материала, например, в полимерных и масляных композициях, особенно при повышенных рабочих температурах.
Раскрытие изобретения
Целью настоящего изобретения является разработка технологии получения алмаз-углеродного материала, обладающего прогнозируемыми свойствами и прогнозируемым элементным составом при высоком содержании углерода в желаемых фазовых состояниях.
При создании изобретения была поставлена задача разработки способа получения алмаз-углеродного материала, имеющего высокую концентрацию углерода желаемых модификаций и желаемого фазового состава, из углеродсодержащего материала с помощью детонационного синтеза в условиях, препятствующих окислению поверхности алмаз-углеродного материала и обеспечивающих сохранность полученной алмазной фазы.
Поставленная задача была решена получением алмаз-углеродного материала, содержащего углерод, водород, азот и кислород, отличающегося тем, что материал содержит углерод в виде алмазной кубической модификации и в рентгеноаморфной фазе в соотношении (40-80):(60-20) по массе углерода, соответственно, и при этом содержит, мас.%:
| Углерод | 89,1-95,2 |
| Водород | 1,2-5,0 |
| Азот | 2,1-4,8 |
| Кислород | 0,1-4,7 |
| Несгораемые примеси | 0,1-1,5 |
Поставленная задача была также решена разработкой способа получения алмаз-углеродного материала, включающего детонацию углеродсодержащего взрывчатого вещества с отрицательным кислородным балансом в замкнутом объеме в газовой среде, инертной к углероду, в окружении конденсированной фазы, отличающегося тем, что осуществляют детонацию углеродсодержащего взрывчатого вещества, помещенного в оболочку из конденсированной фазы, содержащей восстановитель при количественном соотношении массы восстановителя в конденсированной фазе к массе используемого углеродсодержащего взрывчатого вещества не менее 0,01:1, и получают продукт, содержащий, мас.%:
| Углерод | 89,1-95,2 |
| Водород | 1,2-5,0 |
| Азот | 2,1-4,8 |
| Кислород | 0,1-4,7 |
| Несгораемые примеси | 0,1-1,5, |
при этом в массе углерода содержащий углерод алмазной кубической модификации и углерод в рентгеноаморфной фазе в соотношении (40-80):(60-20) мас.%, соответственно.
При этом согласно изобретению целесообразно в качестве восстановителя использовать неорганическое или органическое соединение, предпочтительно не содержащее атомов кислорода и галогенов.
Поставленная задача была также решена разработкой способа подготовки алмаз-углеродного материала, полученного способом детонационного синтеза из углеродсодержащих взрывчатых веществ, к последующим исследованиям по определению элементного состава, включающего выдержку указанного конечного продукта при температуре 120-140°С под вакуумом 0,01-10,0 Па в течение 3-5 часов и последующую его обработку при температуре 1050-1200°С потоком кислорода со скоростью, обеспечивающей его сжигание в течение 40-50 с.
Лучший вариант осуществления изобретения
Процесс образования алмаз-углеродного материала согласно изобретению способом согласно изобретению можно разделить на четыре стадии.
1. Первая стадия детонационного превращения углеродсодержащего взрывчатого вещества при его взрыве в основном происходит в пределах объема заряда, ограниченного его наружными поверхностями, и особенности среды, окружающей заряд, не оказывают влияния на процесс превращения.
Как показали исследования, выбор состава взрывчатых веществ с отрицательным кислородным балансом приводит к образованию «лишнего» углерода, который остается в конденсированном виде. Часть этого «лишнего» углерода при взрыве превращается в алмаз кубической модификации.
Размещение заряда в окружении среды в жидком или твердом агрегатном состоянии, например при подрыве в бассейне, наполненном водой или льдом, препятствующими разлету продуктов детонации, создает условия для повышения длительности существования образующегося при детонации комплекса сверхвысокого давления и высокой температуры, являющихся областью существования жидкого углерода и алмаза.
Размещение заряда внутри оболочки, содержащей конденсированную фазу в жидком или твердом агрегатном состоянии, например в виде воды, льда, позволяет также более продолжительное время удерживать продукты детонации в объеме исходного заряда, что приводит к более продолжительному существованию плазмы, содержащей продукты детонации, и способствует более полному переходу «лишнего» углерода в алмазную фазу.
2. Во второй стадии превращения, наступающей после завершения процесса детонации, очень важным является обеспечение быстрого газодинамического охлаждения продуктов детонации для сохранения алмазов кубической модификации, образовавшихся в зоне химических превращений.
Известно, что при взрыве в вакууме вследствие высоких скоростей разлета наблюдается наиболее быстрое газодинамическое охлаждение продуктов детонации. Однако при последующем ударе продуктов детонации о стенки взрывной камеры их кинетическая энергия переходит в тепловую энергию, и температура в камере быстро растет, достигая очень высоких значений, и после затухания всех ударных волн в полости камеры устанавливается температура ~3500 K, близкая к температуре детонации. А поскольку давление в камере падает во много раз быстрее, чем температура, алмазы кубической модификации полностью превращаются (переходят) в графит. Затем при длительном воздействии высоких температур весь КУ газифицируется. Именно поэтому при взрыве в вакууме алмазы кубической модификации не сохраняются.
Наиболее медленное газодинамическое охлаждение наблюдается при разлете продуктов детонации, окруженных массивными водяными или ледяными оболочками. При этом максимальная установившаяся температура продуктов детонации не превышает 500-800 K из-за эффективного отбора энергии водой (RU, 2230702, С; В.А.Мазанов. Макрокинетика сохранения конденсированного углерода и детонационного наноалмаза в герметичной взрывной камере. Физика твердого тела, 2004, т.46, вып.4, с.614-620).
Взрыв в среде инертного газа по интенсивности газодинамического охлаждения занимает промежуточное положение между взрывом в вакууме и взрывом в оболочке из конденсированной фазы в виде воды или льда, так как скорость разлета продуктов детонации в газовой среде меньше, чем в вакууме, но больше, чем при наличии водной оболочки или ледяной оболочки.
Поскольку существование КУ в значительной степени определяется остаточной температурой во взрывной камере, - чем меньше температура, тем выше выход алмаз-углеродного материала, - то оптимальным является использование конденсированных оболочек вокруг заряда, создающих наибольшее охлаждение.
3. Третья стадия детонационного синтеза алмаз-углеродного материала наступает после отражения ударных волн от стенок камеры: происходит циркуляция ударных волн, распространяющихся со сверхзвуковой скоростью, сопровождающихся процессами резкого увеличения плотности вещества, давления и температуры, и турбулентное перемешивание продуктов детонации со средой в полости камеры.
Максимально установившаяся температура среды в полости камеры зависит от отношения масс взрывчатых веществ и от состава газовой среды, то есть химической активности среды и теплоемкости газов.
4. На четвертой стадии процесса детонационного синтеза среда, нагретая взрывом углеродсодержащего взрывчатого вещества и ограниченная холодной оболочкой, интенсивно охлаждается. После взрыва и высвобождения продуктов детонации в камере, кроме разного вида газообразных продуктов (СО2, СО, О2, Н2, N2, CH4, NO, NO2, NH3, H2O) также находится высокодисперсная взвесь частиц КУ, которые обладают большой излучающей способностью. Поэтому процесс охлаждения такой среды характеризуется совместным переносом тепла конвекцией и излучением.
Известно, что с помощью использования метода измерения профиля электропроводности в детонационной волне было установлено, что время образования алмазной кубической модификации не превышает 0,2-0,5 мкс, что соответствует ширине зоны химической реакции в смесевых композициях взрывчатых веществ тринитротолуол-гексоген, как в литьевых, так и в прессованных (Ставер A.M., Ершов А.П., Лямкин А.И. Исследование детонационного превращения конденсированных взрывчатых веществ методом электропроводности. Физика горения и взрыва, 1984, т.20, №3, с.79-82).
Поскольку часть образовавшихся на первой стадии детонации твердых частиц КУ превращается в газы под воздействием образующихся при взрыве газообразных окислителей: CO2, Н2О, СО, O2, N2O3, NO2, то можно говорить о «сохранившихся частицах» КУ, которые не успели газифицироваться, в том числе из-за недостатка количества этих газообразных окислителей.
Так как любые не прореагировавшие твердые частицы углерода КУ имеют покров из функциональных групп, то взаимодействие поверхностных функциональных групп с газообразными окислителями способно изменить первичные функциональные группы, в том числе не содержащие кислорода, на кислородсодержащие группы, так как все окислители имеют в своем составе кислород.
При этом использование важной функции восстановителя - связать окислитель, предотвращая окисление углерода, создает условия для препятствия окислению поверхности углеродных частиц. Это создает условия для существенного увеличения содержания углерода в алмаз-углеродном материале. Это увеличение достигается как раз за счет уменьшения содержания кислорода, так как исследования показывают, что содержание водорода и азота меняется мало.
Следует отметить, что высокое содержание кислорода в алмаз-углеродном материале препятствует его эффективному использованию в ряде технологий. Например, при использовании алмаз-углеродного материала в качестве присадок к техническим маслам наличие большого количества кислорода увеличивает окислительную способность материала.
Известно, что при подрыве углеродсодержащего взрывчатого вещества в газовой среде в условиях установившейся в полости камеры температуры 1500±150 K выход КУ максимален и равен ~12%. С увеличением температуры в полости камеры до 3000-3500 K выход КУ падает практически до нуля (В.А.Мазанов. Макрокинетика сохранения конденсированного углерода и детонационного наноалмаза в герметичной взрывной камере. Физика твердого тела, 2004, т.46, вып.4, с.614-620).
Возможности сохранения полученных алмазов кубической модификации и элементный состав алмазо-углеродного материала зависят от интенсивности протекания в полости камеры гетерофазных эндотермических реакций газификации КУ диоксидом углерода (1) и водяным паром (2), которые можно представить единой брутто-реакцией (3):
При высокой температуре в полости камеры происходят 2 конкурирующих процесса: газификация КУ - в первую очередь, не алмазного углерода, как более активного, и графитизация образовавшихся алмазов кубической модификации.
Поэтому авторы сочли целесообразным разработать условия проведения синтеза, которые обеспечивали бы минимальные возможности влияния продуктов детонации на полученный при детонации продукт и максимально возможную скорость охлаждения продукта для исключения его газификации.
Согласно изобретению введение восстановителя в состав окружающей заряд конденсированной оболочки позволяет достичь нескольких эффектов:
1. Восстановитель препятствует окислению поверхности углеродных частиц на третьей стадии детонационного процесса, связывая окислители как наиболее химически активные вещества в полости камеры. При этом содержание главного мешающего последующему использованию КУ гетероатома - кислорода, резко падает до 0,1%, а его место занимает достаточно инертный и ничему не мешающий водород. Содержание углерода соответственно увеличивается до 95,2%.
2. За счет частичного разложения восстановителя при высоких температурах происходит падение температуры в камере, что, в свою очередь, уменьшает процесс газификации (реакции 1-3) и «замораживает» фазовый переход алмаз - графит.
Таким образом, введение восстановителя позволяет увеличить выход КУ.
Настоящее изобретение может быть проиллюстрировано примерами осуществления способа получения алмаз-углеродного материала согласно изобретению.
Обычно для синтеза КУ используют смесевые углеродсодержащие взрывчатые вещества, например смесь тринитротолуола с гексогеном или октогеном при содержании тринитротолуола от 30 до 70%. Возможно использование тринитротриаминобензола в смеси с октогеном, гексогеном или тринитротолуолом.
Для испытаний в качестве углеродсодержащих взрывчатых веществ были выбраны:
- заряды из смеси тринитротолуола с гексогеном, сформированные прессованием при давлении прессования 1500 кг/см2 в соотношении 50/50 (примеры 1-18) и плавлением в соотношении 65/35 (примеры 19, 20);
- заряды из смеси тринитротолуола и октогена, сформированные прессованием при давлении прессования 1500 кг/см2 в соотношении 60/40 (пример 21);
- заряды из смеси триаминотринитробензола с октогеном, сформированные прессованием при давлении прессования 1500 кг/см2 в соотношении 50/50 (пример 22).
При этом форма заряда была выбрана традиционная, в виде сплошного цилиндра, диаметр цилиндрической шашки 48,5 мм, длина заряда 167,1 мм.
Подрыв заряда осуществляли с помощью электродетонатора, размещенного с торца заряда внутри него.
Заряд углеродсодержащего взрывчатого вещества помещали в оболочку их конденсированной фазы, представляющую собой раствор восстановителя в воде в жидком агрегатном состоянии (примеры 1-16, 18, 19, 21, 22) или в состоянии льда (пример 20), или в оболочку, представляющую собой бронировку заряда, выполненную из прессованного твердого восстановителя (пример 17). При этом масса оболочки составляла от 4,0 до 6,0 кг, и оболочки, имеющие жидкое агрегатное состояние конденсированной фазы, представляли собой цилиндрические мешки из полиэтилена, наполненные конденсированной фазой раствора восстановителя, и заряд подвешивали (размещали) в центре мешка. В случае твердого агрегатного состояния оболочки с использованием в качестве восстановителя адамантана оболочка имела вид наружной бронировки заряда по всем поверхностям.
В качестве восстановителей были использованы диметилгидразин (примеры 1-5, 19), уротропин (примеры 6-10, 20-22), аммиак (примеры 11-13), мочевина (примеры 14-16), адамантан (пример 17), ацетонитрил (пример 18) при различных, в диапазоне (0,01-10,0):1,0, соотношениях массы используемого восстановителя и массы используемого углеродсодержащего взрывчатого вещества, соответственно.
Испытания проводили следующим образом: заряд в оболочке помещали через верхний люк во взрывную камеру, выполненную из нержавеющей стали, объемом 1 м3, заполненную газообразными продуктами предыдущего подрыва, камеру закрывали и заряд подрывали.
Через 3 минуты после подрыва осуществляли разгрузку полученной водной суспензии продукта через нижний клапан в приемную емкость. Водную суспензию пропускали затем через сито с размером ячейки 200 мкм и высушивали. Высушенный продукт дробили и просеивали через сито с размером ячейки 80 мкм и затем образцы полученного продукта подготавливали способом подготовки согласно изобретению для проведения последующих исследований их элементного состава.
Для этого образцы полученных продуктов выдерживали при температуре 120-140°С под вакуумом 0,01-10,0 Па в течение 3-5 часов и затем подвергали обработке при температуре 1050-1200°С потоком кислорода со скоростью, обеспечивающей его сжигание в течение 40-50 секунд.
С помощью исследований было установлено, что алмаз-углеродный материал содержит от 8 до 14 мас.% летучих примесей (в основном, воду, окислы азота и углерода). Удаление таких примесей, прочно связанных адсорбционными силами в микропорах, обычным нагревом на воздухе при температуре 120-125°С невозможно. Повышение температуры прогрева до более высоких температур на воздухе опасно из-за разложения, возможности воспламенения и возгорания частиц не алмазного углерода.
Для полного удаления летучих примесей следует применять вакуум при остаточном давлении 0,01-10,0 Па. При этом температуру необходимо поддерживать в диапазоне 120-140°С.
При вакууме 0,01 Па достаточно поддерживать температуру 120°С, а при давлении 10,0 Па - 140°С. Давление менее 0,01 Па поддерживать нецелесообразно по экономическим причинам, а выше 10,0 Па - из-за возможного неполного удаления летучих примесей. Повышение температуры свыше 140°С может вызвать распад части нестойкого не алмазного углерода. Время прогрева в течение 3-5 часов гарантирует также полное удаление летучих примесей. При давлении 0,01 Па и 120°С достаточно 3-х часов выдержки, а при 10,0 Па и 140°С целесообразнее выдерживать 5 часов.
Для определения элементного состава алмаз-углеродного материала обычно используют стандартную методику органической химии: температура нагрева в токе кислорода 850-900°С в течение 5 с. Однако алмаз-углеродный материал сильно отличается по своей стойкости к окислению от любых органических соединений. Поэтому указанных выше условий недостаточно для полного окисления элементов, составляющих алмаз-углеродный материал. Температура, обеспечивающая полное сгорание (окисление) алмаз-углеродного материала, составляет 1050-1200°С, при этом время прогрева должно составлять 40-50 секунд. Эти условия достижимы, например, на приборе №185 фирмы "Hewlett Packard" (США).
Подготовленные описанным выше способом образцы продуктов синтеза были подвергнуты следующим исследованиям:
- исследованию с помощью метода малоуглового рассеяния для определения количественного распределения частиц материала по их размерам;
- исследованию с помощью полярографического титрования для определения наличия и состава поверхностных кислородсодержащих, аминных и амидных функциональных групп. При этом гидроксильные, карбоксильные, аминные и амидные группы идентифицируются по значениям соответствующих восстановительных потенциалов, а также по данным ИК-спектроскопии;
- исследованию с помощью газохроматографического анализа наличия поверхностных метильных групп, идентифицируемых по составу выделенных газов при нагревании при температуре 663-673 K в течение 3 часов, по количеству выделенного метана. При этом полученные продукты перед газохроматографическим анализом были прогреты при 473 K в вакууме (0,1 Па) до получения продукта постоянного веса (в течение 24 часов), при этом адсорбированные ранее поверхностью полученного продукта летучие продукты, в том числе газы, были удалены, и выделяющиеся при газохроматографическом анализе газы СН4, H2, CO2, СО, O2, N2 и NH3 являлись газами, образующимися при разрушении химически связанных с КУ поверхностных групп;
- исследованию с помощью рентген-фотоэлектронной спектроскопии (XPES) для анализа распределения углеродных форм в полученном продукте;
- исследованию с помощью метода малоуглового рассеяния (Свергун Д.И., Фейгин Л.А. Рентгеновское и нейтронное малоугловое рассеяние. М.: Наука, 1986, 280 с.);
- исследованию с помощью метода определения удельной поверхности порошков путем низкотемпературной сорбции азота (далее БЭТ) (Герасимов Я.И. и др. Курс физической химии. T.1, издание 2-ое., М.: Химия, 1969, стр.592).
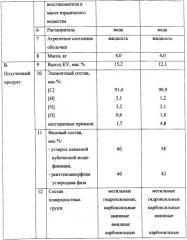
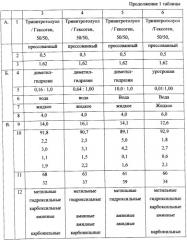
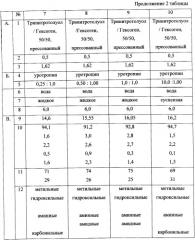
Результаты испытаний приведены в таблице.
В результате исследований было установлено, что полученный способом согласно настоящему изобретению алмаз-углеродный материал представляет собой порошок черного цвета и имеет следующие параметры:
- удельную поверхность от 150 до 550 м2/г, деленную с помощью метода определения удельной поверхности порошков путем низкотемпературной сорбции азота (далее БЭТ) (Герасимов Я.И. и др. Курс физической химии. T.1, издание 2-ое исправл., М.: Химия, 1969, стр.592),
- средний размер частиц 2-6 нм, определен с помощью метода малоуглового рассеяния,
- удельный вес в пределах 2,0-2,6 г/см3.
Содержание в полученном продукте несгораемых частиц, представляющих собой в основном окислы и карбиды металлов, зависит от условий детонационного синтеза, состава материалов стенок взрывной камеры и степени изношенности этой камеры и может составлять 1,4-4,8 мас.%.
Исследования показали, что рентгенограммы изученных образцов алмаз-углеродного материала содержат наряду с тремя линиями, относящимися к алмазной фазе углерода, и широкий максимум с d=0,42 нм, относящийся к рентгеноаморфной фазе углерода, при этом наличие последнего максимума ясно выделяется после частичного окисления КУ либо кислородом воздуха при температуре 673 K в течение 1-5 часов, либо при травлении 98%-ной азотной кислотой при кипении в течение 3-8 часов.
Распределение частиц материала было исследовано с помощью метода малоуглового рассеяния. Исследования показали, что распределение по размерам частиц характеризуется единственным максимумом в области между 40 и 60 Å, то есть углеродные фазы не разделяются по размерам частиц.
ИК-спектры позволили идентифицировать гидроксильные, карбоксильные, карбонильные, аминные и амидные группы на поверхности частиц КУ.
По данным газохроматографического анализа было установлено, что при нагревании в вакууме при 663-673 K в течение 3 часов из образца исследуемого продукта массой 1,0 г выделяются следующие газы:
- метан - 0,12-0,60 см3/г,
- водород - 0,18-0,33 см3/г,
- двуокись углерода - 0,01-0,46 см3/т,
- окись углерода - 0,01-0,13 см3/г,
- кислород - 0,00-0,02 см3/г,
- азот - 0,39-2,04 см3/г,
- аммиак - 0,06-0,21 см3/г.
Общее выделение газа составляет 0,82-3,22 см3/г.
На основании полученных данных можно сделать заключение, что на поверхности полученных КУ имеются следующие поверхностные группы: метильные (по выделению метана), карбоксильные (по выделению двуокиси и окиси углерода), аминные (по выделению аммиака), амидные, карбонильные, гидроксильные.
На основании полярографического титрования было установлено присутствие карбоксильных групп на многих образцах и карбонильных групп на некоторых образцах.
Специалистам в области химии наноалмазов известно, что травление окислителями - это послойный съем материала с оболочки частицы алмаз-углеродного материала при обработке его сильными окислителями.
Поскольку кислород и водород сосредоточены в верхних слоях частиц, то, естественно, при послойном съеме материала их процентное содержание в оставшейся после травления частице будет уменьшаться, а процентное содержание углерода в оставшейся после травления частице возрастет. Поскольку азот равномерно распределен по частице, то его процентное содержание не изменится.
Таким образом, при любом травлении окислителями частиц алмаз-углеродного материала процентное содержание азота в оставшемся материале практически не меняется и при этом, в отличие от известного алмаз-углеродного материала, описанного выше (US, 5916955, А), азот достаточно равномерно распределен по объему как алмазной фазы углерода, так и рентгеноаморфной фазы углерода.
На основании данных, приведенных в таблице, можно сделать следующие выводы:
1. Присутствие в оболочке из конденсированной фазы восстановителя в количестве от 0,01 мас.% до 10 мас.% по отношению к массе используемого взрывчатого вещества дало заметный положительный эффект, заключающийся в существенном изменении элементного состава: углерод более 91,5 мас.%, водород более 1,5 мас.%, кислород - менее 1,5 мас.%, азот - в пределах 2,2-2,9 мас.%.
Введение восстановителя в количестве, большем в 10 раз, чем количество взрывчатого вещества, нецелесообразно по экономическим соображениям. При соотношении массы взрывчатого вещества к массе восстановителя 1:10,0 выход КУ и содержание в нем углерода кубической модификации достигают максимальных значений, и дальнейшее увеличение количества восстановителя приведет к техническим сложностям по извлечению алмаз-углеродного материала из камеры и его переработке.
Физико-химические свойства алмаз-углеродных материалов, полученных способом согласно изобретению, позволяют использовать их в качестве наноразмерного компонента высокоэффективных композиционных материалов.
Были проведены сравнительные испытания использования алмаз-углеродных материалов, полученных различными способами.
При этом были изготовлены масла для погружных нефтяных насосов, в которых в качестве присадок были использованы:
А) алмаз-углеродные материалы, полученные способом согласно изобретению, имеющие следующий состав, мас.%: углерод 94,5%, водород - 1,2%, азот - 2,5 %, кислород - 0,8%, несгораемые примеси - 1,0% при содержании в них углерода в алмазной кубической модификации - 72% и углерода в рентгеноаморфной модификации - 28%.
Б) алмаз-углеродные материалы, полученные способом детонации, описанным выше (US, 5916955, А), имеющие следующий состав, мас.%: углерод 88,8%, водород - 1,1%, азот - 3,1%, кислород - 4,9%, несгораемые примеси - 2,1%, при содержании в массе углерода: углерода в алмазной кубической фазе - 42% и в других формах углерода - 58%.
Результаты сравнительных испытаний показали, что использование масел с присадками из материала Б в погружных нефтяных насосах при замкнутом цикле маслопотока привело к полному осмолению масла за 18 часов работы и выходу из строя насоса вследствие катастрофического износа поверхностей.
Использование масел с присадками из материала А по данному изобретению не приводило к осмолению масла и конденсации (слипанию) алмазных частиц с последующим износом поверхности.
Таким образом, алмаз-углеродные материалы согласно изобретению, полученные способом детонационного синтеза согласно изобретению, обладают улучшенными элементным и фазовым составом по сравнению с известными алмаз-углеродными материалами, что приводит к более стабильным прогнозируемым свойствам композиций и материалов при их использовании в различных областях науки и технологии.
Образцы полученного алмаз-углеродного материала подготавливали способом подготовки согласно изобретению для последующего определения его элементного состава.
Примеры конкретного выполнения.
Пример 23. Алмаз-углеродный материал, полученный способом детонационного синтеза из углеродсодержащих взрывчатых веществ по примеру 1, или 3, или 15, выдерживают при температуре 120°С под вакуумом 10,0 Па в течение 3-х часов, а затем обрабатывают при температуре 1050°С потоком кислорода со скоростью, обеспечивающей его сжигание в течение 40 с.
Пример 24. Аналогично примеру 23. Используют алмаз-углеродный материал, полученный по примеру 4, или 7, или 20. Условия выдержки: температура - 140°С, вакуум - 0,01 Па, время - 4 часа. Последующую обработку материала проводят при 1200°С потоком кислорода со скоростью, обеспечивающей его сжигание в течение 50 с.
Пример 25. Аналогично примеру 23. Используют алмаз-углеродный материал, полученный по примеру 9, или 19, или 22. Условия выдержки: температура - 130°С, вакуум - 1 Па, время - 5 часов. Последующую обработку материала проводят при 1100°С потоком кислорода со скоростью, обеспечивающей его сжигание в течение 45 с.
Промышленная применимость
Алмаз-углеродные материалы согласно изобретению могут найти широкое применение в различных технологиях, например в полировально-финишных композициях, пленочных покрытиях, в составе радиационно-стойких материалов.
Алмаз-углеродные материалы согласно изобретению могут быть получены способом согласно изобретению, который может быть осуществлен с использованием имеющегося технологического оборудования и известных взрывчатых веществ.
1. Алмаз-углеродный материал, содержащий углерод, водород, азот и кислород, отличающийся тем, что содержит углерод в виде алмазной кубической модификации и в рентгеноаморфной фазе в соотношении (40-80):(60-20) по массе углерода соответственно, и при этом содержит, мас.%:
| Углерод | 89,1-95,2 |
| Водород | 1,2-5,0 |
| Азот | 2,1-4,8 |
| Кислород | 0,1-4,7 |
| Несгораемые примеси | 1,4-4,8 |
2. Способ получения алмаз-углеродного материала, включающий детонацию углеродсодержащего взрывчатого вещества с отрицательным кислородным балансом в замкнутом объеме в газовой среде, инертной к углероду, в окружении конденсированной фазы, отличающийся тем, что осуществляют детонацию углеродсодержащего взрывчатого вещества, помещенного в оболочку из конденсированной фазы, содержащей восстановитель при количественном соотношении массы восстановителя в конденсированной фазе к массе используемого углеродсодержащего взрывчатого вещества не менее 0,01:1, при этом получаемый продукт содержит, мас.%:
| Углерод | 89,1-95,2 |
| Водород | 1,2-5,0 |
| Азот | 2,1-4,8 |
| Кислород | 0,1-4,7 |
| Несгораемые примеси | 1,4-4,8, |