Маркер рака предстательной железы
Иллюстрации
Показать всеИзобретение относится к области биотехнологии и может быть использовано в диагностике рака предстательной железы, а также в дифференциальной диагностике между раком предстательной железы и доброкачественной гиперплазии. Маркер рака предстательной железы состоит из белка молекулярной массы 28,5 кДа и видимой изоэлектрической точкой 6,92, выделяемого из опухолевой ткани предстательной железы. Выделенный маркерный белок включает пептиды MPADLPSLAADFVESK; DVFLGMFLYEYAR; VFDEFKPLVEEPQNLIK; FQNALLVR; VPQVSTPTLVEVSR и AVMDDFAAFVEKCCK. Изобретение позволяет повысить точность диагностики рака простаты. 1 табл., 2 ил.
Реферат
Изобретение относится к медицинской диагностике и может использоваться для дифференциальной диагностики между раком предстательной железы человека и доброкачественной гиперплазией.
Одна из важных проблем поддержания здоровья в стареющих популяциях современного общества - онкологические заболевания, среди которых особое место принадлежит раку предстательной железы (РПЖ). Известно, что более 50% мужчин с возрастом в диапазоне 51-60 лет имеют признаки гиперплазии простаты, что рассматривается как предраковое состояние.
Возможности эффективного (хирургического, химиотерапевтического и др.) лечения РП в первую очередь определяются своевременностью и точностью диагностики, в которой первостепенное значение имеет определение молекулярных маркеров рака.
В настоящее время для диагностики РПЖ предложен и используется целый ряд совершенно разных клинических и инструментальных методов: способ диагностики путем пальцевого ректального исследования, способ на основе трансректального ультразвукового исследования (пат. РФ 2256924, 2259163), по результатам магниторезонансной томографии предстательной железы, анализ радиоизлучений тела больного (авт.св. 1738261, 1767434, 1655467), цветной допплерографии, рентгенодиагностики, морфологической диагностики, гистологии срезов биоптатов (пат. РФ 2156977, 2018829), иммуногистохимической (пат. РФ №2276672) и цитологической диагностики (пат. РФ 2151397), определение концентрации рубидия и цинка в секрете предстательной железы (авт. св. №764660), ИК-спектроскопии (пат. РФ №№2246898, 2018829).
Однако указанные клинические и инструментальные методы не обладают необходимыми качествами для обеспечения ранней и эффективной диагностики РПЖ; их применение обычно позволяет уточнить диагноз только на развернутых стадиях заболевания, а для ранней диагностики требуется использование молекулярных маркеров, о чем свидетельствует значительный опыт, накопленный отечественными и зарубежными специалистами (Злокачественные новообразования в России в 2002 году. Заболеваемость и смертность. Ред. В.И.Чиссов, В.В.Старинский, Г.В.Петрова, М., Из-во "МЕДпресс-информ". 2004. С.5-22).
Как следствие, на протяжении уже не одного десятилетия ведутся активные поиски эффективных молекулярных маркеров РПЖ разной природы в тканях предстательной железы и в биологических жидкостях, а обнаруживаемые потенциальные маркеры используются для разработки новых способов диагностики РПЖ.
Достаточно давно известен опухолевый молекулярный маркер RSP, предложенный как универсальный маркер для обнаружения различных опухолей, в том числе и РПЖ (пат. РФ 2025734, дата подачи 1990).
Описан способ дифференциальной диагностики между доброкачественной гиперплазией и РПЖ (пат. РФ №2151397, 1999 г.), включающий исследование биологического материала на содержание фосфатидилинозит-3-фосфатов (ФИФ); при этом из цельной крови выделяют липидную фракцию, в которой методом проточной горизонтальной хромотографии определяют уровень ФИФ. При значении 0,1-0,08 нмоль фосфора ФИФ 1 на 1 мг белка ставится диагноз доброкачественной гиперплазии, а при значении 0,04-0,01 нмоль фосфора ФИФ 1 на 1 мг белка диагностируют РПЖ.
Патентом РФ №2234942, 1999 г. защищен ряд полинуклеотидов, выделенных из опухолевой ткани предстательной железы и способных кодировать опухолевые полипептиды предстательной железы. Нуклеотидные последовательности этих полинуклеотидов приведены в патенте под номерами SEQ ID NO: 225 и SEQ ID NO: 326. Описанные в патенте композиции могут быть использованы в качестве маркеров прогрессирования рака.
Патентом РФ №2258710, 2000 г. защищен выделенный полипептид - новый цитокин zalpha11-лиганд, содержащий последовательность аминокислотных остатков, которая по меньшей мере на 90% идентична остаткам 41 (Gln) - 148 (Ile) в последовательности, приведенной в патенте под номером SEQ ID NO:2, причем остаток в положении 44 является Asp, остаток в положении 47 является Asp, а остаток в положении 135 является Glu. Полипептид связывает zalpha11-рецептор, показанный в последовательности под номером SEQ ID NO: 115. Альтернативно полипептид zalpha11 может служить в качестве дополнительного маркера клеточной поверхности или секретируемого маркера, ассоциированного со стадиоспецифической экспрессией в ткани. Появление или исчезновение полипептидов, регулирующих клеточную подвижность, может быть использовано в диагностике и прогнозировании рака предстательной железы.
Обнаружен человеческий ген (патент США 6300479, опубл. 2001 г.), который кодирует новый белок из семейства бета тимозинов (далее тимозин β-15); показано, что этот белок обладает способностью связывать и удерживать (арестовывать) глобулярный актин, подобно другим членам семейства бета тимозинов, но в отличие от других членов семейства бета тимозинов он непосредственно регулирует клеточную подвижность у клеток карциномы (рака) простаты. Имеется предложение использовать тимозин β-15, как молекулярный маркер для диагностики РПЖ (Hutchinson L.M. et al. Use of thymosin beta15 as a urinary biomarker in human prostate cancer. Prostate. 2005. V.64. 116-127).
Известны неинвазивные методы для определения присутствия нуклеиновых кислот со специфичными последовательностями, так же как и модификаций и повреждений нуклеиновых кислот в образцах анализируемой мочи для установления присутствия трансренальных почечных нуклеиновых кислот (патент США 6492144, 2002 г.). Предлагаемый способ включает методы определения специфичных фетальных нуклеиновых кислот, последовательности которых содержат модифицированные нуклеотиды в анализируемом мочевом материале для установления присутствия фетальных нуклеиновых кислот. Кроме того, данный способ предлагается использовать для диагностики не только раковых заболеваний, но и патогенных инфекций, а также для определения генетической предрасположенности к различным болезням, для мониторинга за лечением рака и для контроля за успешностью трансплантаций клеток, тканей и органов.
Однако перечисленные методы оказались недостаточно специфичными, трудно воспроизводимыми и не нашли до настоящего времени клинического применения (Злокачественные новообразования в России в 2002 году. Заболеваемость и смертность. / Ред. В.И.Чиссов, В.В.Старинский, Г.В.Петрова, М., Из-во "МЕДпресс-информ". 2004. С.5-22).
Наиболее близким аналогом является широко применяемый в клинике биохимический способ диагностики РПЖ по определению уровня сывороточного простатспецифического антигена (далее ПСА) в плазме или сыворотке крови (Kuriyama М. Prostate-specific antigen in prostate cancer. // Int. J. Biol. Markers. 1986. 1(2). P.67-76.; Parekh D.J., Ankerst D.P., Troyer D., Srivastava S., Thompson I.M. Biomarkers for prostate cancer detection.). Однако имеются и убедительные данные о недостаточной диагностической значимости этого маркера (Stamey T.A. et al. J. The prostate specific antigen era in the United States is over for prostate cancer: what happened in the last 20 years? J. Urol. 2004. 172. 1297-1301), который, в основном, отражает степень гиперплазии простаты. В целом, по результатам определения ПСА в крови пациентов регистрируется 40-60% ложноположительных тестов и около 10% ложноотрицательных тестов (Kuriyama М. Prostate-specific antigen in prostate cancer. // Int. J. Biol. Markers. 1986. 1(2). P.67-76).
Вместе с тем за последние 3-4 года с помощью протеомных технологий показано, что при РПЖ в опухолевых клетках предстательной железы обнаруживается повышенный синтез десятков различных белков, большинство из которых не проявляют свойств, необходимых для специфичных диагностических маркеров, но поиски таких белков активно продолжаются.
Задачей изобретения является разработка способа диагностики рака простаты по выявлению специфического белкового маркера в малигнизированной ткани с целью повышения точности диагностики.
Поставленная цель достигается за счет использования в качестве маркера рака предстательной железы, состоящего из белка, выделенного из опухолевой ткани предстательной железы, молекулярной массы 28,5 кДа и видимой изоэлектрической точкой 6,92, который включает пептиды MPADLPSLAADFVESK; DVFLGMFLYEYAR; VFDEFKPLVEEPQNLIK; FQNALLVR; VPQVSTPTLVEVSR; AVMDDFAAFVEKCCK.
Авторы выделяли заявляемый белок из опухолевой ткани предстательной железы методикой, аналогичной описанной в статье Ahram M. et al. Proteomic analysis of human prostate cancer. Molecular carcinogenesis. 2002. V.33. 9-15. Ниже представлена данная методика проведения анализа.
Белки из образцов эпителия рака простаты (стадия по Глисону 8-9) и 12 здоровых лиц экстрагировались лизис-буфером и фракционировались двумерным электрофорезом по О' Фарреллу, используя в первом направлении (IPG) иммобилизованные полоски с нелинейным градиентом рН 3-10 и последующим разделением SDS-ЭФ ПААГ с градиентом 9-18% с окрашиванием азотнокислым серебром или флуоресцентным красителем Sypro Ruby. Белковые пятна, проявляющие качественные и количественные изменения при раке простаты, вырезались из полиакриламидных гелей, подвергались триптическому гидролизу и анализировались, используя HPLC и тандемную масс-спектрометрию. Полученные массы триптических пептидов использовались для поиска белков-кандидатов по белковым последовательностям с использованием программы PepFrag. Сорок опухоль-специфических изменений были идентифицированы, включая белки клеточной морфологии (тропомиозин бета), метаболизма (альдолаза А, М-цепь лактат дегидрогеназы) и сигнальной трансдукции (рецептор ламинина 67 кДа, белок взаимодействия фосфосерин-треонин-тирозина).
Авторы данного изобретения провели поиск с помощью аналогичного набора приведенных выше протеомных технологий потенциальных белковых маркеров РПЖ в ходе сравнительных исследований белков в биоптатах и операционных материалах, полученных от двух групп больных с послеоперационными морфологически подтвержденными диагнозами: рак простаты (РПЖ, n=20) и гиперплазия (ГП, n=18), где n - количество пациентов. Результаты исследований сведены в таблицу 1. В таблице 1 приведены также данные о пооперационных клинико-морфологических диагнозах этих больных и результаты определения у них ПСА, которые в подавляющем большинстве случаев соответствовали так называемой «серой зоне» («СЗ» - от 4 до 10 нг/мл). Только у трех пациентов с послеопреационным диагнозом аденокарцинома уровень ПСА превышал верхнюю границу «серой зоны». При этом у четырех человек обследованной выборки показатель ПСА оказался меньше нижней границы «серой зоны».
Дооперационный клинико-морфологический диагноз во всех случаях был поставлен с использованием комплекса инструментальных методов, включая многоигольную биопсию с последующим гистологическим исследованием биоптатов.
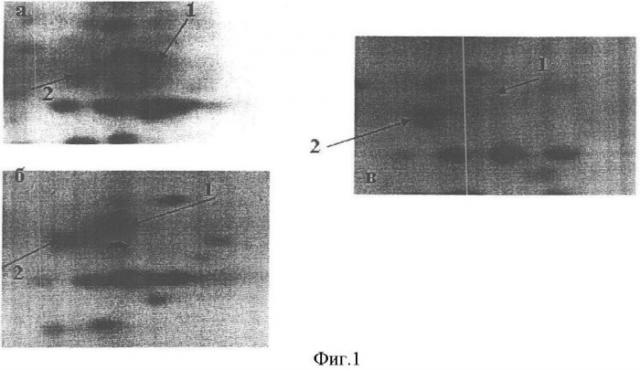
Сравнительный анализ этих двух групп образцов показал наличие специфичного качественного отличия между тканями с ГП и РПЖ, заключавшегося в том, что в последних присутствовал заявляемый белок с молекулярной массой - 28,5 кДа и с видимой изоэлектрической точкой - 6,92. В целом у 19 из 20 обследованных пациентов с послеоперационным диагнозом «аденокарцинома» при протеомном анализе регистрировался заявляемый белок и при этом соответствующий белок был найден только у 1 пациента с гиперплазией. На фиг.1 в качестве примера показаны соответствующие фрагменты двумерных электрофореграмм, полученных при протеомном анализе белковых экстрактов двух пациентов с РПЖ и одного пациента с гиперплазией предстательной железы.
По результатам MALDI TOF масс-спектрометрического анализа триптических пептидов заявляемого белка (показанного стрелкой №1 на фиг.1) было выявлено несколько пептидов, входящих в состав альбумин-родственных доменов, что позволило идентифицировать заявляемый белок как альбумин-родственный карциномный протеин 1 (фиг.2).
Таким образом, заявляемый белок предлагается использовать, как маркер при диагностике РПЖ, определяя присутствие указанного белка в биоматериалах с помощью протеомных технологий. Определение заявляемого маркера при высокой специфичности (более 90%) позволит снизить число ложно положительных тестов с 40-60% (при определении простатспецифического антигена плазме или сыворотке крови) до 5-10% (при исследовании заявляемого маркера).
Заявленный маркер никогда ранее не использовался для диагностики рака. Его применение оказывается предпочтительней для более точной постановки диагноза.
| Таблица 1. | ||||
| Результаты определения ПСА и заявляемого белка у пациентов с послеоперационным гистологическим диагнозом. | ||||
| №№ | Дооперационный клинико-морфологический диагноз | ПСА | Заявляемый белок | Послеоперационный морфологический диагноз |
| 1 | Рак | «СЗ» | рак | Аденокарцинома |
| 2 | Рак | «СЗ» | рак | Аденокарцинома |
| 3 | Рак | «СЗ» | рак | Аденокарцинома |
| 4 | Рак | «СЗ» | рак | Аденокарцинома |
| 5 | Рак | «СЗ» | Рак | Аденокарцинома |
| 6 | Рак | «СЗ» | Рак | Аденокарцинома |
| 7 | Рак | «СЗ» | Рак | Аденокарцинома |
| 8 | Рак | «СЗ» | рак | Аденокарцинома |
| 9 | Рак | Рак | Рак | Аденокарцинома |
| 10 | Рак | Рак | Рак | Аденокарцинома |
| 11 | Рак | «СЗ» | рак | Аденокарцинома |
| 12 | Рак | «СЗ» | Рак | Аденокарцинома |
| 13 | гиперплазия | Норма | Рак | Аденокарцинома |
| 14 | гиперплазия | Норма | Рак | Аденокарцинома |
| 15 | Рак (?) | «СЗ» | Рак | Аденокарцинома |
| 16 | Рак (?) | «СЗ» | Рак | Аденокарцинома |
| 17 | Рак | Рак | Рак | Аденокарцинома |
| 18 | Рак | «СЗ» | Рак | Аденокарцинома |
| 19 | Рак (?) | «СЗ» | Рак | Аденокарцинома |
| 20 | Рак | «СЗ» | Не определен | Аденокарцинома |
| 21 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 22 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 23 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 24 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 25 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 26 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 27 | Аденома (Гиперплазия) | Норма | Не определен | Гиперплазия |
| 28 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 29 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 30 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 31 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 32 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 33 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 34 | Рак (?) | «СЗ» | Не определен | Гиперплазия |
| 35 | Аденома (Гиперплазия?) | «СЗ» | Не определен | Гиперплазия |
| 36 | Аденома (Гиперплазия?) | Норма | Не определен | Гиперплазия |
| 37 | Аденома (Гиперплазия) | «СЗ» | Не определен | Гиперплазия |
| 38 | Аденома (Гиперплазия?) | «СЗ» | Рак | Гиперплазия |
Фиг.1. Фрагменты двумерных электрофореграмм белков простаты человека: а - пациент «К» с РПЖ; б - пациент «П» с РПЖ; в - пациент «С» с гиперплазией. Стрелкой №1 показан белок, специфично появляющийся при раке и идентифицированный как неизвестный белковый продукт гена PRO2675, содержащий С-концевой альбуминовый домен. Стрелкой №2 показан реперный белок, идентифицированный как цепь B триозофосфат изомеразы.
Фиг.2. Результаты MALDI TOF масс-спектрометрического анализа триптических пептидов дополнительного белка (показанного стрелкой №1 на Фиг.1). Определение структуры пептидов, выявленных по масс-спектрам, с помощью опции “Peptide Fingerprint” программы Mascot (Matrixscience, США).
Маркер рака предстательной железы, состоящий из белка, выделенного из опухолевой ткани предстательной железы, молекулярной массы 28,5 кДа и с видимой изоэлектрической точкой 6,92, включает пептиды MPADLPSLAADFVESK; DVFLGMFLYEYAR; VFDEFKPLVEEPQNLIK; FQNALLVR; VPQVSTPTLVEVSR; AVMDDFAAFVEKCCK.