Способ получения гидроталькитоподобных соединений
Иллюстрации
Показать всеИзобретение относится к области химии, в частности к способам получения синтетических слоистых гидроксидов. Способ получения слоистых гидроксидов формулы Mg(1-x)Mex 3+(OH)2(CO3)x/2·nH2O, где трехвалентным металлом является скандий Sc3+ или одновременно железо и алюминий в виде FeyAlx-y, причем «у» меньше «х», а «х» не выше 0,4, заключается в том, что в раствор, содержащий хлориды или нитраты Mg2+ и Sc3+, или в раствор, содержащий хлориды или нитраты Mg2+ и Al3+ и сульфаты или хлориды, или нитраты Fe3+, добавляют раствор-осадитель, содержащий гидроксид натрия и карбонат натрия, при этом соотношение ионов Me3+:Mg2+:[ОН-]:[СО3 2-] в растворе составляет 1:3:8:1. Выпавший осадок термостатируют в маточном растворе при 96-98°С в течение двух суток. После охлаждаения до комнатной температуры маточные растворы с осадком декантируют, затем осадок трижды подвергают анионному обмену с Na2CO3. После отстаивания растворы декантируют и осадок промывают дистиллированной водой до получения отрицательного результата на наличие иона натрия, сушат при 80-105°С. Общая концентрация солей металлов в растворе-осадителе составляет не более 3 М, и общая концентрация раствора-осадителя составляет не более 3 М. Изобретение позволяет получить хорошо закристаллизованные гомогенные образцы гидроталькитоподобных соединений, что позволяет расширить сферу их применения. 4 ил.
Реферат
Изобретение относится к методам синтеза гидроталькитоподобных веществ.
Для идентификации слоистой структуры гидроксидов используют рентгенофазовый анализ. Рентгеновские дифрактограммы слоистых гидроксидов имеют характерный вид: набор из 5 пиков, расстояние между которыми зависит от состава слоистого гидроксида, а интенсивность пиков убывает с увеличением угла дифракции два тета. При больших углах (более 56°) имеется дуплет из шестого и седьмого пика, который также входит в характеристическую дифракционную картину для идентификации слоистой структуры.
Степень окристаллизованности вещества можно оценить по ширине пиков. Узкие интенсивные пики указывают на высокую степень кристалличности образцов, а также на однородность образцов и, следовательно, изотропность их физико-химических свойств.
Известен способ синтеза слоистых гидроксидов, например гидроксосульфата магния-алюминия (Краснобаева О.Н., Носова Т.А., Елизарова Т.А., Данилов В.П. Двойные гидроксосульфаты магния-алюминия со слоистой структурой. // Ж. неорганической химии, 2001, - т.46, - №6, - с.899-902), включающий осаждение из 2N растворов сульфатов магния и алюминия раствором 2N гидроксида натрия при 50-70°С до рН 7,5-7,8, выдерживание смеси при 60-75°С на масляной бане в закрытых колбах в течение 2 недель, отделение осадков от раствора фильтрованием и промывку 50% водным раствором ацетона.
Данный способ обладает следующими недостатками: длительное термостатирование, использование для промывки ацетона и при этом недостаточная кристаллизация конечного продукта и низкая упорядоченность анионов в межслоевом пространстве готового продукта.
Наиболее близким по существу является способ синтеза (Елисеев А.А., Лукашин А.В., Вергетел А.А., Тарасов В.П., Третьяков Ю.Д. Исследование процессов кристаллизации слоистых двойных гидроксидов Mg-Al. // Доклады академии наук. - 2002. - т.387, - №6, - с.777-781), включающий осаждение гидроталькитоподобных соединений из растворов нитратов магния и алюминия (Mg2+:Al3+=3:1, общая концентрация катионов 1М), раствором карбоната и гидроксида натрия ([CO3 2-]:[OH-]=1:6, общая концентрация анионов 3М), при постоянном значении рН 10,0±0,1, термостатирование при 80°С в течение 5 суток.
Недостатком данного способа является также длительность процесса, необходимость поддержания постоянного рН, при этом недостаточная кристаллизация и низкая упорядоченность анионов в межслоевом пространстве, что может являться причиной неоднородности физико-химических свойств готового продукта.
Задача изобретения заключается в расширении арсенала способов получения синтетических гидроталькитоподобных соединений с общей формулой
Mg(1-х)Мех(ОН)2(СО3)х/2·nН2O, где в качестве трехвалентного металла выступают скандий Sc3+ или в любом соотношении одновременно алюминий Al3+и железо Fe3+.
Техническим результатом является получение синтетических гидроталькитоподобных слоистых магний-скандиевого гидроксида и магний-железо-алюминиевого гидроксида с улучшенными характеристиками, такими как высокая кристалличность и упорядоченность анионов в межслоевом пространстве.
Предложенное изобретение от указанного способа, включающего осаждение гидроталькитоподобных соединений из раствора солей двухвалентного магния и трехвалентного металла раствором-осадителем, содержащим карбонат и гидроксид натрия, термостатирование выпавшего осадка, отличается тем, что:
- раствор для осаждения содержит хлориды или нитраты Mg2+ и скандия Sc3+;
- раствор для осаждения содержит хлориды или нитраты Mg2+ и Al3+ и сульфаты или хлориды или нитраты Fe3+;
- концентрация как раствора для осаждения, так и раствора-осадителя не должна быть более 3М, т.к. повышение концентрации приводит к повышенной густоте реакционной смеси и невозможности из-за этого равномерного прохождения реакции по всему объему, что в конечном итоге препятствует получению необходимой гомогенности конечного продукта;
- соотношение ионов в растворе для осаждения и в растворе-осадителе должно соответствовать: Ме3+:Мe2+:[СО3 2-]:[ОН-]=1:3:1:8;
- термостатирование проводят при 96-98°С в течение 2 суток, полученный осадок гидроталькитоподобного соединения трижды подвергают анионному обмену с Nа2СО3, после промывают дистиллированной водой до отрицательной качественной реакции на ион Na+, сушку производят при 80-105°С.
Критерии «новизна» и «изобретательский уровень» предложенного способа получения заявленных слоистых гидроксидов подтверждают следующие признаки:
- выявленная возможность при приготовлении раствора солей для осаждения слоистых гидроксидов использовать в качестве анионов - хлориды или нитраты Mg2+ и Sс3+ или хлориды или нитраты Mg2+ и Al3+ и сульфаты или хлориды или нитраты Fe3+;
- соотношение ионов в растворе для осаждения и в растворе-осадителе, соответствующее Me3+:Ме2+:[СО3 2-]:[ОН-]=1:3:1:8;
- проведение термостатирования при 96-98°С, что позволяет сократить длительность термостатирования до 2 суток. Снижение температуры увеличивает длительность термостатирования и ухудшает характеристику готового продукта, а повышение температуры термостатирования выше 100°С требует использования специального оборудования, т.е. дополнительных затрат. При указанной температуре уже через двое суток характеристики готового продукта, полученные на рентгеновской дифрактограмме, подтверждают высокое качество готового продукта;
- декантирование маточных растворов с осадком слоистых гидроксидов после охлаждения до комнатной температуры, которые затем трижды подвергают анионному обмену с Na2CO3, после отстаивания растворы декантируют и промывают дистиллированной водой до получения отрицательного результата на наличие иона натрия, а сушку производят при 80-105°С.
Способ позволяет получить синтетические гидроталькитоподобные соединения с улучшенными характеристиками, т.е. высокой кристалличностью и упорядоченностью анионов в межслоевом пространстве, что подтверждается наличием высоких и узких характеристических пиков на рентгеновских дифрактограммах.
Заявленное изобретение характеризуют на фиг.1-4.
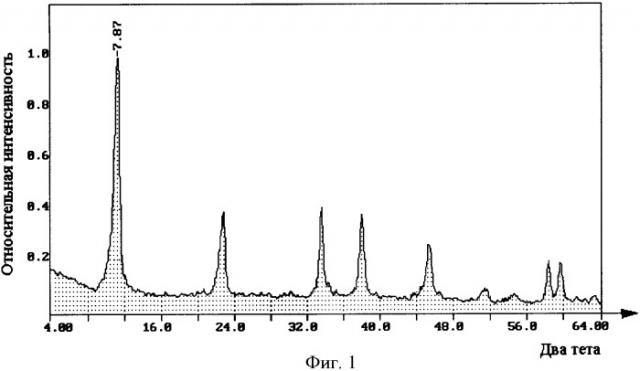
Фиг.1 - рентгеновская дифрактограмма магний-скандиевого слоистого гидроксида, полученного предложенным способом;
Фиг.2 - рентгеновская дифрактограмма магний-железо-алюминиевого слоистого гидроксида, полученного предложенным способом с соотношением А13+:Fe3+=9:1 в растворе для осаждения;
Фиг.3 - рентгеновская дифрактограмма магний-железо-алюминиевого гидроксида, полученного предложенным способом с соотношением Al3+:Fe3+=99:1 в растворе для осаждения;
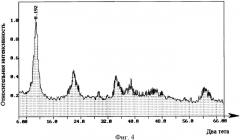
Фиг.4 - рентгеновская дифрактограмма магний-железо-алюминиевого гидроксида, полученного предложенным способом с соотношением Al3+:Fe3+=9:1 в растворе для осаждения, но при температуре термостатирования 80°С.
Примеры использования предложенного способа для получения синтетических гидроталькитоподобных соединений
Пример 1
При синтезе магний-скандиевого слоистого гидроксида к смеси растворов нитрата скандия и нитрата магния прикапывали со скоростью 3-5 мл/мин при комнатной температуре раствор-осадитель, который содержал гидроксид натрия и карбонат натрия. Общая концентрация солей металлов равна 2М, а общая концентрации раствора-осадителя составляет 1М. Навески веществ для приготовления растворов рассчитаны из соотношения: Sc3+:Mg2+:[ОН-]:[СО3 2-]=1:3:8:1.
Осажденные образцы термостатировали в маточном растворе при 96°С в течение двух суток.
Затем после охлаждения до комнатной температуры маточный раствор декантировали и осадок слоистого гидроксида подвергали анионному обмену с Na2CO3, с целью замещения остаточных NO3 --анионов в межслоевом пространстве на СО3 2-. Операцию повторили три раза. После отстаивания растворы декантировали и многократно промывали дистиллированной водой, пока качественная реакция на натрий не даст отрицательный результат. Образцы высушивали при 99°С.
Проведенный химический и термогравиметрический анализ позволил рассчитать химическую формулу полученного продукта: Mg0,677Sc0,323(OH)2(CO3)0,162·0,805Н2O, который имеет характеристику дифракции рентгеновских лучей с высокими и узкими пиками, представленную на фиг.1
Пример 2
При синтезе магний-железо-алюминиевого слоистого гидроксида к смеси растворов хлорида железа, нитрата алюминия и нитрата магния прикапывали со скоростью 3-5 мл/мин при комнатной температуре раствор-осадитель, который содержал гидроксид натрия и карбонат натрия. Общая концентрация солей металлов равна 3М, а общая концентрация раствора-осадителя составляет 2М. Навески веществ для приготовления растворов рассчитаны из соотношения: Ме3+:Mg2+:[ОН-]:[СО3 2-]=1:3:8:1, где в качестве трехвалентного металла выступают одновременно Al3+ и Fe3+ в соотношении 9:1.
Осажденные образцы термостатировали в маточном растворе при 97°С в течение двух суток.
Затем после охлаждения до комнатной температуры маточный раствор декантировали и осадок слоистого гидроксида подвергали анионному обмену с Na2CO3. Операцию повторили три раза. После отстаивания раствор декантировали и многократно промывали дистиллированной водой, пока качественная реакция на натрий не даст отрицательный результат. Образцы высушивали при 99°С.
Проведенный химический и термогравиметрический анализ позволил рассчитать химическую формулу полученного продукта: Mg0,764Al0,219Fe0,017(OH)2(CO3)0,118·0,886Н2O. Данный продукт имеет характеристику дифракции рентгеновских лучей с высокими и узкими пиками, представленную на фиг.2.
Пример 3
При синтезе магний-железо-алюминиевого слоистого гидроксида к смеси растворов сульфата железа, хлорида алюминия и нитрата магния прикапывали со скоростью 3-5 мл/мин при комнатной температуре раствор-осадитель, который содержал гидроксид натрия и карбонат натрия. Общая концентрация солей металлов равна 3М, а общая концентрация раствора-осадителя составляет 1М. Навески веществ для приготовления растворов рассчитаны из соотношения: Me3+:Mg2+:[ОН-]:[СО3 2-]=1:3:8:1, где в качестве трехвалентного металла выступают одновременно Al3+:Fe3+ в соотношении 99:1.
Осажденные образцы термостатировали в маточном растворе при 98°С в течение двух суток.
Затем после охлаждения до комнатной температуры маточный раствор декантировали и осадок слоистого гидроксида подвергали анионному обмену с Na2CO3. Операцию повторили три раза. После отстаивания раствор декантировали и многократно промывали дистиллированной водой, пока качественная реакция на натрий не даст отрицательный результат. Образцы высушивали при 105°С.
Проведенный химический и термогравиметрический анализ позволил рассчитать химическую формулу полученного продукта: Mg0,714Al0,282Fe0,004(OH)2(CO3)0,146·0,820Н2O. Данный продукт имеет характеристику дифракции рентгеновских лучей с высокими и узкими пиками, представленную на фиг.3.
Пример 4
При синтезе магний-железо-алюминиевого слоистого гидроксида к смеси растворов хлорида железа, нитрата алюминия и нитрата магния прикапывали со скоростью 3-5 мл/мин при комнатной температуре раствор-осадитель, который содержал гидроксид натрия и карбонат натрия. Общая концентрация солей металлов равна 3М, а общая концентрация раствора-осадителя составляет 2М. Навески веществ для приготовления растворов рассчитываются из соотношения: Me3+:Mg2+:[ОН-]:[СО3 2-]=1:3:8:1, где в качестве трехвалентного металла выступают одновременно А13+:Fe3+ в соотношении 9:1.
Осажденные образцы термостатировали в маточном растворе при 80°С в течение двух суток.
Затем после охлаждения до комнатной температуры маточный раствор декантировали и осадок слоистого гидроксида подвергали анионному обмену с Na2CO3. Операцию повторили три раза. После отстаивания раствор декантировали и многократно промывали дистиллированной водой, пока качественная реакция на натрий не даст отрицательный результат. Образцы высушивали при 99°С.
Данный продукт имеет характеристику дифракции рентгеновских лучей, представленную на фиг.4. Из рентгеновской дифрактограммы видно, что при данной температуре за 2 суток не удается достичь той же степени кристалличности, как в примере 2 при термостатировании при 97°С и прочих равных условиях.
Приведенные примеры 1-3 подтверждают, что предложенный способ позволяет получить новые синтетические гидроталькитоподобные соединения с общей формулой Mg(1-x)Mex(OH)2(CO3)x/2·nН2O, где х не выше 0,4, a Me - трехвалентный металл, в качестве которого выступают скандий, или одновременно железо и алюминий с любыми соотношениями между собой.
Пример 4 показывает, что снижение температуры ухудшает характеристику полученного продукта, что подтверждают пики на рентгеновской дифрактограмме (фиг.4).
Таким образом, предложенный способ позволяет за короткий промежуток времени получить хорошо закристаллизованные образцы новых гидроталькитоподобных соединений с общей формулой Mg(1-x)Mex(OH)2(CO3)x/2·nH2O, где x не выше 0,4, а в качестве трехвалентного металла выступает скандий Sc или одновременно железо и алюминий в виде FeyAlx-y. Высокие и узкие характеристические пики рентгеновских дифрактограмм данных соединений говорят о гомогенности образцов и, следовательно, об изотропности их физико-химических свойств, что позволит расширить сферу их применения.
Способ получения слоистых гидроксидов формулыMg(1-x)Mex 3+(OH)2(CO3)x/2·nH2O,где трехвалентным металлом является скандий Sc3+ или одновременно железо и алюминий в виде FeyAlx-y, причем «у» меньше «x», а «x» не выше 0,4, заключающийся в том, что в раствор, содержащий хлориды или нитраты Mg2+ и Sc3+, или в раствор, содержащий хлориды или нитраты Mg2+ и Al3+ и сульфаты или хлориды, или нитраты Fe3+, добавляют раствор-осадитель, содержащий гидроксид натрия и карбонат натрия, при этом соотношение ионов Me3+:Mg2+:[ОН-]:[CO3 2-] в растворе составляет 1:3:8:1, выпавший осадок термостатируют в маточном растворе при 96-98°С в течение двух суток, после охлаждения до комнатной температуры маточные растворы с осадком декантируют, затем трижды подвергают анионному обмену с Na2CO3, после отстаивания растворы декантируют и осадок промывают дистиллированной водой до получения отрицательного результата на наличие иона натрия, сушку производят при 80-105°С.
2. Способ п.1, отличающийся тем, что общая концентрация солей металлов в растворе-осадителе составляет не более 3 М, и общая концентрация раствора-осадителя составляет не более 3 М.