Гипо- и гиперацетилированные менингококковые капсульные сахариды
Иллюстрации
Показать всеКапсульные сахариды, полученные из серогрупп W135 и Y Neisseria meningitidis, имеют измененные уровни O-ацетилирования в положениях 7 и 9 остатков их сиаловых кислот. Модифицированный менингококковый капсульный сахарид серогруппы W135, где (а) ≤29% остатков сиаловых кислот в сахариде являются O-ацетилированными в 7 положении; и/или (b) ≥26% остатков сиаловых кислот в сахариде являются O-ацетилированными в 9 положении и модифицированный менингококковый капсульный сахарид серогруппы Y, где а) ≤9% остатков сиаловых кислот в сахариде являются O-ацетилированными в 7 положении; и/или (b) ≥29% или ≤27% остатков сиаловых кислот в сахариде являются O-ацетилированными в 9 положении могут быть использованы для создания иммуногенных композиций - композиций для индукции образования антител у млекопитающих и продуктов конъюгирования с белками-носителями. Конъюгаты производных демонстрируют повышенную иммуногенность по сравнению с природными полисахаридами. 14 н. и 15 з.п. ф-лы, 3 табл., 6 ил.
Реферат
Все приведенные документы полностью включены сюда в качестве ссылки.
Техническая область
Это изобретение относится к области менингококковых капсульных сахаридов и их конъюгированных производных.
Предшествующий уровень техники
Полисахариды представляют собой важные биологические молекулы, и их широко применяли в фармацевтической промышленности для предотвращения и лечения заболеваний. Например, в течение многих лет капсульные полисахариды применяли в вакцинах против инкапсулированных бактерий, таких как менингококк (Neisseria meningitidis), пневмококк (Streptococcus pneumoniae) и Hib (Haemophilus influenzae типа B).
Разработаны конъюгатные вакцины для усиления иммуногенности капсульных полисахаридов, особенно у детей. Конъюгатные вакцины включают в себя капсульный сахарид, конъюгированный с белком-носителем [например, ссылки 1-3]. Конъюгация превращает Т-независимые антигены в Т-зависимые антигены.
Капсульный сахарид серогруппы W135 Neisseria meningitidis ("MenW135") включает в себя полимер из дисахаридных мотивов сиаловая кислота-галактоза:
→4)-D-Neup5Ac(7/9OAc)-α-(2→6)-D-Gal-α-(1→,
где "Neu" означает нейраминовую кислоту, общеизвестную как сиаловая кислота.
Аналогичным образом, капсульный сахарид серогруппы Y Neisseria meningitidis (MenY) включает в себя полимер из дисахаридных мотивов сиаловая кислота-глюкоза:
→4)-D-Neup5Ac(7/9ОAc)-α-(2→6)-D-Glc-б-(1→.
Обнаружено, что в природе эти капсульные сахариды O-ацетилированы по некоторым 7 и 9 положениям некоторых остатков сиаловых кислот. В ссылке 4 "впервые сообщили" об O-ацетилировании сахарида W135, с O-ацетилированием в положениях O-7 и O-9. Также в положениях O-7 и O-9 наблюдали ацетилирование сахарида серогруппы Y, хотя авторы заметили, что в предыдущей работе указано на O-ацетилирование в O-7, O'-3 или O'-4 положениях. О дальнейших исследованиях содержания O-ацетилов в сахаридах сообщено в ссылке 5.
В ссылке 5 сообщают, что для серогруппы W135 "существует растущий объем данных, что O-ацетилирование не важно для вызова защитного ответа антителами". В отличие от этого, в ссылке 6 сообщают, что "существует доказательство того, что O-ацетилирование оказывает влияние на иммуногенность полисахаридных вакцин". Однако авторы ссылки 5 исследовали ацетилирование в серогруппах W135 и Y в предположении, что "O-ацетилирование CPS [капсульного полисахарида] может быть не важным для активации защитного иммунитета". Среди своих результатов они наблюдали отсутствие изменений в O-ацетилировании для этих двух серогрупп после хранения в основных условиях в течение 9 суток при комнатной температуре.
В ссылке 7 сообщают, что ранее "не сообщали о "состоянии O-ацетилирования штаммов W135 и Y", применяемых в тетравалентных полисахаридных вакцинах". В ссылке 8 авторы продолжили сообщение того, что "о состоянии O-ацетилирования серогрупп W135 и Y известно немного", и они указали, что дальнейшая работа "может обеспечить полезные представления для оптимального формулирования вакцин", хотя сущность такой дальнейшей работы и возможные представления не конкретизированы. В ссылке 9 сообщают, что для серогруппы W135 "важность O-ацетилирования для разработки вакцин остается неопределенной". Ссылка 6 выражает мнение, что данные “о влиянии O-ацетилирования полисахаридов на иммуногенность серогруппы W-135 или Y пока еще недоступны” (январь 2004 г.).
Эти неопределенность и отсутствие информации для серогрупп W135 и Y отличаются от двух других серогрупп, для которых в настоящее время применяют сахаридные вакцины. С большими промежутками сообщалось [10, 11] о вариации O-ацетилирования капсульного полисахарида серогруппы C Neisseria meningitidis, но, по-видимому, это не оказывает никакого отрицательного влияния на иммуногенность, так как эффективны оба продукта, как MenjugateTM, так и NeisVac-CTM. В отличие от этого, де-O-ацетилирование полисахарида серогруппы A связано со "значительным снижением иммуногенности" [12].
Объектом изобретения является представление производных капсульного сахарида, которые можно применять для создания иммуногенных композиций, в частности, при конъюгировании с белками-носителями, и, особенно для менингококковых серогрупп W135 и Y.
Описание изобретения
Несмотря на неясность относительно роли O-ацетилирования в вакцинах для серогрупп W135 и Y менингококков, авторы изобретения обнаружили, что O-ацетилирование действительно может являться значимым, особенно для получения конъюгатных вакцин. Изобретение основано на открытии того, что полученные из MenW135 и MenY модифицированные капсульные сахариды с измененными уровнями O-ацетилирования в 7 и 9 положениях остатков сиаловых кислот можно применять для создания иммуногенных композиций. Относительно немодифицированных нативных сахаридов, производные по изобретению предпочтительно выбирают при конъюгировании с белками-носителями. Кроме того, конъюгаты этих производных демонстрируют увеличенную иммуногенность по сравнению с нативными полисахаридами.
Модифицированные сахариды
Таким образом, изобретение относится к модифицированному менингококковому капсульному сахариду серогруппы W135, где (a) ≤x% остатков сиаловых кислот в сахариде являются O-ацетилированными в 7 положении; и/или (b) ≥y% остатков сиаловых кислот в сахариде являются O-ацетилированными в 9 положении.
Подобно этому изобретение относится к модифицированному капсульному сахариду менингококковой серогруппы Y, где a) ≤x% остатков сиаловых кислот в сахариде являются O-ацетилированными в 7 положении; и/или (b) ≥y% или ≤z% остатков сиаловых кислот в сахариде являются O-ацетилированными в 9 положении.
Значение x зависит от серогруппы: для серогруппы W135, x менее или равно 29 (например, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0); для серогруппы Y, x менее или равно 9 (например, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0).
Значение y также зависит от серогруппы: для серогруппы W135, y более или равно 26 (например, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100); для серогруппы Y, y более или равно 29 (например, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100).
Значение z менее или равно 27 (например, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0).
Предпочтительно x>m, где m выбрано из 0, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10.
Предпочтительно z>p, где p выбрано из 0, 0,5, 1, 2, 3, 4, 5, 6, 7, 8, 9 и 10.
Сахариды по изобретению
В широком смысле изобретение относится к модифицированному менингококковому капсульному сахариду, необязательно конъюгированному с белком-носителем, где сахарид включает в себя n или более повторяющихся мотивов дисахаридной единицы {[сиаловая кислота]-[гексоза]}, где гексоза представляет собой галактозу или глюкозу и n представляет собой целое число от 1 до 100, и где (a) ≤x% остатков сиаловых кислот в указанном n или более повторяющихся единиц являются O-ацетилированными в 7 положении; и/или (b) когда гексоза представляет собой галактозу, ≥y% остатков сиаловых кислот в указанном n или более повторяющихся единиц являются O-ацетилированными в 9 положении, и когда гексоза представляет собой глюкозу, ≥y% или ≤z% остатков сиаловых кислот в указанном n или более повторяющихся единиц являются O-ацетилированными в 9 положении.
Значение x зависит от гексозы: когда гексоза представляет собой галактозу, x менее или равно 29 (например, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0); когда гексоза представляет собой глюкозу, x менее или равно 9 (например, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0).
Значение y зависит от гексозы: когда гексоза представляет собой галактозу, y более или равно 26 (например, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100); когда гексоза представляет собой глюкозу, y более или равно 29 (например, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100).
Значение z менее или равно 27 (например, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0).
Предпочтительно x>m, как описано выше. Предпочтительно z>p, как описано выше.
Предпочтительно сиаловые кислоты представляют собой N-ацетилнейраминовую кислоту.
Предпочтительно дисахаридный мотив {[сиаловая кислота]-[гексоза]} представляет собой:
→4)-D-Neup5Ac(7/9OAc)-б-(2→6)-D-Gal-б-(1→,
когда гексоза представляет собой галактозу.
Предпочтительно дисахаридный мотив {[сиаловая кислота]-[гексоза]} представляет собой:
→4)-D-Neup5Ac(7/9OAc)-α-(2→6)-D-Glc-α-(1→,
когда гексоза представляет собой глюкозу.
Предпочтительно модифицированный менингококковый капсульный сахарид конъюгирован с белком-носителем. В таких конъюгатах: (i) предпочтительно от 2 до 9%, более предпочтительно от 4 до 8%, более предпочтительно от 5 до 7%, еще более предпочтительно около 6% остатков сиаловых кислот O-ацетилированы в 7 положении; (ii) предпочтительно от 35 до 55%, более предпочтительно от 40 до 50%, более предпочтительно от 42 до 46%, еще более предпочтительно около 43% (когда гексозой является Gal) или около 45% (когда гексозой является Glc) остатков сиаловых кислот O-ацетилированы в 9 положении.
По изобретению также представлена композиция, включающая в себя a молекул капсульного сахарида менингококковой серогруппы W135, где среднее количество остатков сиаловых кислот в молекуле капсульного сахарида представляет собой b, и где (a) ≤x% a·b остатков сиаловых кислот серогруппы W135 в композиции O-ацетилированы в 7 положении; и/или (b) ≥y% a·b остатков сиаловых кислот серогруппы W135 в композиции O-ацетилированы в 9 положении, и где x и y представляют собой, как определено выше.
Также изобретение относится к композиции, включающей в себя a молекул капсульного сахарида менингококковой серогруппы Y, где среднее количество остатков сиаловых кислот в молекуле капсульного сахарида представляет собой b, и где (a) ≤x% a·b остатков сиаловых кислот серогруппы Y в композиции O-ацетилированы в 7 положении; и/или (b) ≥y% или ≤z% a·b остатков сиаловых кислот серогруппы Y в композиции O-ацетилированы в 9 положении, и где x и y представляют собой, как определено выше.
Сахариды в указанных группах могут быть конъюгированы с белками-носителями и/или быть свободны в растворе.
Предпочтительно сахариды или конъюгаты по изобретению находятся в очищенной форме, например, преимущественно в отсутствие нативного полисахарида.
Описания структур
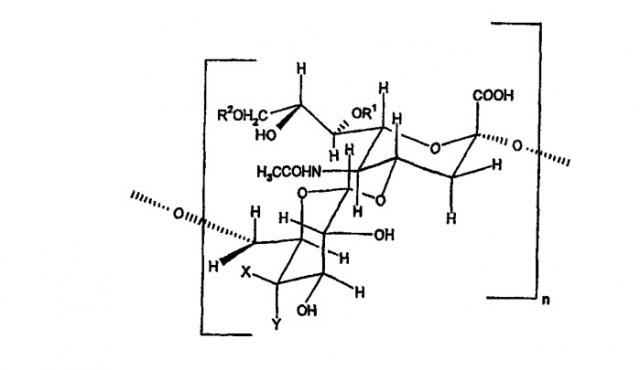
По этому изобретению также представлен сахарид, необязательно конъюгированный с белком-носителем, включающим в себя n или более повторов следующего дисахаридного мотива:
где - n представляет собой целое число от 1 до 100,
- X и Y представляют собой разные группы, выбранные из -H и -OH,
- R1 независимо выбран из -H и -COCH3 и может быть одним и тем же или разным в каждой дисахаридной единице,
- R2 независимо выбран из -H и -COCH3 и может быть одним и тем же или разным в каждой дисахаридной единице, и когда
- X представляет собой -OH и Y представляет собой -H, (a) ≤x% R1 представляют собой -COCH3 и/или (b) ≥y% R2 представляют собой -COCH3,
- X представляет собой -H и Y представляет собой -OH, (a) ≤x% R1 представляют собой -COCH3 и/или (b) ≥y% или ≤z% R2 представляют собой -COCH3.
Когда X представляет собой -OH и Y представляет собой -H, x менее или равно 29 (например, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0) и y более или равно 26 (например, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100).
Когда X представляет собой -H и Y представляет собой -OH, x менее или равно 9 (например, 8, 7, 6, 5, 4, 3, 2, 1 или 0,5), y более или равно 29 (например, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100) и z менее или равно 27 (например, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1, 0,5 или 0).
Предпочтительно x>m, где m, как определено выше. Предпочтительно z>p, где p, как указано выше.
Предпочтительно сахарид конъюгирован с белком-носителем.
Когда сахарид конъюгирован с белком-носителем, и X представляет собой -OH и Y представляет собой -H: (a) предпочтительно приблизительно 2-10%, более предпочтительно приблизительно 4-8%, более предпочтительно приблизительно 5-7%, еще более предпочтительно приблизительно 6% R1 представляют собой -COCH3; и/или (b) предпочтительно приблизительно 35-55%, более предпочтительно приблизительно 40-50%, более предпочтительно приблизительно 42-44%, еще более предпочтительно приблизительно 43% R2 представляют собой -COCH3.
Когда сахарид конъюгирован с белком-носителем и X представляет собой -H и Y представляет собой -OH: (a) предпочтительно приблизительно 2-9%, более предпочтительно приблизительно 4-8%, более предпочтительно приблизительно 5-7%, еще более предпочтительно приблизительно 6% R1 представляют собой -COCH3; и/или (b) предпочтительно приблизительно 35-55%, более предпочтительно приблизительно 40-50%, более предпочтительно приблизительно 42-46%, еще более предпочтительно приблизительно 45% R2 представляют собой -COCH3.
Состояние O-ацетилирования остатков сиаловых кислот в положениях 7 и 9 в сахаридах и конъюгатах по изобретению можно измерять с применением 1D и 2D протонного ЯМР, как описано ниже. HPAEC можно применять для измерения общего O-ацетилирования, но он не может провести различия между различными положениями [234]. Для анализа O-ацетилирования MenA применяли MС с распылением ионов [235].
Способ получения модифицированного сахарида
Изобретение также относится к способу получения иммуногенных конъюгатов, включающему в себя стадии (1) предоставления исходного менингококкового капсульного сахарида и белка-носителя, любой или оба из которых необязательно модифицированы для приведения его/их в состояние реактивности по отношению друг к другу; (2) формирования ковалентной связи между сахаридом и белком-носителем; и (3) очистки полученных гликоконъюгатов, где между стадиями (1) и (3) (например, при реакции стадии (2)) увеличивается степень O-ацетилирования остатков сиаловых кислот в положении 9 в исходном сахариде.
Менингококковый капсульный сахарид предпочтительно происходит из серогрупп W135 или Y.
Исходное сырье капсульного сахарида
Модифицированные капсульные сахариды по изобретению получают из сахаридов, обнаруженных в капсуле серогрупп W135 или Y N.meningitidis. Таким образом, сахариды по изобретению предпочтительно представляют собой модифицированные сахариды серогруппы W135 N.meningitidis и модифицированные сахариды серогруппы Y N.meningitidis.
Менингококковые капсульные полисахариды обычно получают посредством способа, включающего в себя стадии преципитации полисахарида (например, с применением катионного детергента), фракционирования этанолом, экстракции холодным фенолом (для удаления белков) и ультрацентрифугирования (для удаления LPS) [например, ссылка 13].
Более предпочтительный способ [14] включает в себя преципитацию полисахарида с последующим растворением осажденного полисахарида с применением низшего спирта. Осаждение (или преципитацию) можно выполнять с применением катионного детергента, такого как тетрабутиламмоний и цетилтриметиламмониевые соли (например, бромидные соли) или гексадиметрина бромид и миристилтриметиламмониевые соли. Особенно предпочтителен бромид цетилтриметиламмония ('CTAB') [15]. Растворение осажденного вещества можно выполнять с применением низшего спирта, такого как метанол, пропан-1-ол, пропан-2-ол, бутан-1-ол, бутан-2-ол, 2-метилпропан-1-ол, 2-метилпропан-2-ол, диолы, и т.д., но особенно подходит для растворения комплексов CTAB-полисахарид этанол. К выпавшему в осадок полисахариду предпочтительно добавляют этанол для получения конечной концентрации (основанной на общем содержании этанола и воды) от 50% до 95%.
После повторного растворения полисахарид можно дополнительно обработать для удаления примесей. Это особенно важно в ситуациях, когда недопустима даже незначительная примесь (например, получение вакцины для человека). Обычно это включает в себя одну или несколько стадий фильтрации, например глубокую фильтрацию, фильтрацию через активированный уголь, фильтрацию по размеру и/или ультрафильтрацию. После фильтрации для удаления примесей полисахарид можно осаждать для дополнительной обработки и/или переработки. Это можно удобно выполнять посредством обмена катионов (например, посредством добавления солей кальция или натрия).
Сахариды по изобретению могут представлять собой полисахариды или олигосахариды. Олигосахариды имеют меньшую степень полимеризации по сравнению со степенью полимеризации, обнаруженной в нативных капсульных полисахаридах, представленных в бактериях.
По изобретению предпочтительно применяют олигосахариды. Предпочтительно они имеют среднюю степень полимеризации, меньшую 30, например от 15 до 25, предпочтительно приблизительно 15-20. Степень полимеризации можно удобно измерять посредством ионообменной хроматографии или посредством колориметрического анализа [16].
Олигосахариды обычно получают посредством фрагментации очищенного капсульного полисахарида (например, посредством гидролиза, посредством мягкой кислотной обработки, посредством нагревания и т.д.), обычно с последующей очисткой фрагментов желательного размера. При выполнении гидролиза, как правило, для удаления коротких олигосахаридов гидролизат разделяют по размеру. Этого можно достичь различными способами, такими как ультрафильтрация с последующей ионообменной хроматографией. Для серогрупп W135 и Y предпочтительно удаляют олигосахариды со степенью полимеризации менее чем приблизительно 4.
В качестве альтернативы очистке из нативных источников капсульные сахариды (и, в частности, олигосахариды) можно получать посредством полного или частичного синтеза, например синтез Hib, как описано в ссылке 17, и синтез MenA по ссылке 18.
Ковалентное конъюгирование
Модифицированные сахариды по изобретению можно подвергать любой обычной применяемой к сахаридам дальнейшей обработке (например, получение производных, конъюгирование, фрагментация и т.д.). Предпочтительно модифицированные сахариды по изобретению конъюгируют с белком-носителем для усиления иммуногенности. Конъюгирование с белками-носителями особенно полезно для педиатрических вакцин [19] и представляет собой хорошо известный способ [например, рассмотренный в ссылках от 20 до 28 и т.д.].
Таким образом, изобретение относится к конъюгату белка-носителя и сахарида по изобретению.
Предпочтительные белки-носители представляют собой бактериальные токсины или анатоксины, такие как дифтерийный анатоксин или столбнячный анатоксин. Особенно предпочтителен производный CRM197 дифтерийного анатоксина [29-31]. Другие пригодные белки-носители включают в себя наружный белок мембраны N.meningitidis [32], синтетические пептиды [33, 34], белки теплового шока [35, 36], коклюшные белки [37, 38], цитокины [39], лимфокины [39], гормоны [39], факторы роста [39], синтетические белки, содержащие множество эпитопов человеческих CD4+ T-клеток из различных происходящих из патогенных организмов антигенов [40], таких как белок N19 [41], белок D из H.influenzae [42, 43], пневмококковый поверхностный белок PspA [44], пневмолизин [45], захватывающие железо белки [46], токсин A или B из C.difficile [47], мутантные бактериальные токсины (например, холерный токсин 'CT' или E.coli термолабильный токсин 'LT'), такой как CT с заменой Glu-29 [48] и т.д. Предпочтительные носители представляют собой дифтерийный анатоксин, столбнячный анатоксин, белок D H.influenzae и CRM197.
В композиции по изобретению можно применять более одного белка-носителя, например, для снижения риска супрессии носителя. Таким образом, можно применять разные белки-носители для различных серогрупп, например, сахариды серогруппы W135 можно конъюгировать с CRM197, тогда как сахариды серогруппы Y можно конъюгировать со столбнячным анатоксином. Также можно применять более одного белка-носителя для конкретного сахаридного антигена, например, сахариды серогруппы Y могут принадлежать двум группам, конъюгированные с CRM197 сахариды и конъюгированные со столбнячным анатоксином сахариды. Однако в большинстве случаев предпочтительно применять один и тот же белок-носитель для всех серогрупп, предпочтительным вариантом является CRM197.
Один белок-носитель может нести более одного сахаридного антигена [49]. Например, один белок-носитель может быть конъюгирован с сахаридами серогрупп W135 и Y. Однако в большинстве случаев предпочтительно иметь отдельные конъюгаты для каждой серогруппы.
Предпочтительны конъюгаты с соотношением сахарид:носитель (мас./мас.) от 1:5 (т.е. избыток белка) до 5:1 (т.е. избыток сахарида). Предпочтительны соотношения от 1:2 до 5:1, хотя более предпочтительны соотношения от 1:1,25 до 1:2,5. Для конъюгатов MenW135 отношение может быть приблизительно 1,1 и для конъюгатов MenY 0,7. Предпочтительно конъюгаты содержат от 6,6-20 мкг носителя CRM197 исходя из количества 10 мкг сахарида MenW135 или MenY.
Конъюгаты можно применять вместе со свободным белком-носителем [50]. Когда в композиции по изобретению данный белок-носитель присутствует в свободной и конъюгированной формах, предпочтительно, чтобы неконъюгированная форма составляла не более 5% от общего количества белка-носителя в композиции в целом, и более предпочтительно присутствие менее 2% по массе.
Где необходимо, можно применять любую пригодную реакцию конъюгирования с любым пригодным линкером.
Как правило, сахарид активируют или функционализируют до конъюгирования. Активация может включать в себя, например, цианилирующие реагенты, такие как CDAP (например, 1-циано-4-диметиламинотетрафторборат пиридина [51, 52 и т.д.]). В других пригодных способах применяют карбодиимиды, гидразиды, активные сложные эфиры, норборан, p-нитробензойную кислоту, N-гидроксисукцинимид, S-NHS, EDC, TSTU; также см. введение к ссылке 26.
Выполнять связывания через линкерную группу можно с применением любого известного способа, например способов, описанных в ссылках 3 и 53. Один тип связывания включает в себя восстановительное аминирование полисахарида, связывающее возникшую аминогруппу с одним концом линкерной группы адипиновой кислоты и затем связывающее белок с другим концом линкерной группы адипиновой кислоты [24, 54, 55]. Предпочтительный тип связывания представляет собой карбонильный линкер, который можно формировать реакцией свободной гидроксильной группы модифицированного сахарида с CDI [56, 57] с последующей реакцией с белком для формирования карбаматной связи. Еще один предпочтительный тип связывания представляет собой линкер из адипиновой кислоты, формируемый связыванием свободной -NH2 группы на модифицированном сахариде с адипиновой кислотой (с применением, например, диимидной активации), и затем связыванием белка с полученным промежуточным соединением сахарида и адипиновой кислоты) [24, 54, 58]. Еще один тип связывания можно формировать посредством реакции свободной гидроксильной группы сахарида с цианилирующим агентом (например, п-нитрофенилцианат, 1-циано-4-(диметиламино)тетрафторборат пиридина (CDAP), N-тетрафторборат цианотриэтиламмония (CTEA)) или с последующей реакцией с аминогруппой белка (необязательно через спейсер, например, через гидразин) [59, 60]. Другие линкеры включают в себя B-пропионамид [61], нитрофенилэтиламин [62], галогенацилгалогениды [63], гликозидные связи [2, 64], 6-аминокапроновую кислоту [65], ADH [66], от C4 до C12 вещества [67], и т.д. В качестве альтернативы связыванию с применением линкера можно применять прямую связь. Прямые связи с белком могут включать в себя окисление полисахарида с последующим восстановительным аминированием белком, как описано, например, в ссылках 2 и 68.
Конъюгирование может включать в себя восстановление аномерного конца в первичную гидроксильную группу, необязательную защиту/снятие защиты первичной гидроксильной группы; реакцию первичной гидроксильной группы с CDI с образованием CDI карбаматного промежуточного соединения; и связывание карбаматного промежуточного соединения CDI с аминогруппой белка.
Предпочтителен процесс, включающий в себя введение аминогрупп в сахарид (например, посредством замещения концевых =О групп на -NH2) с последующим получением производных адипинового диэфира (например, N-гидроксисукцинимидодиэфира адипиновой кислоты) и реакцией с белком-носителем. В еще одной предпочтительной реакции применяют активацию CDAP с белком-носителем D.
После конъюгирования свободные и конъюгированные сахариды можно разделить. Существует множество пригодных способов, включающих в себя гидрофобную хроматографию, тангенциальную ультрафильтрацию, диафильтрацию и т.д. [также см. ссылки 69 и 70, и т.д.].
Предпочтительно, чтобы получение олигосахарида предшествовало конъюгированию в случаях, когда композиция по изобретению включает в себя конъюгированный олигосахарид.
Фармацевтические композиции
Изобретение относится к иммуногенной композиции (например, вакцине), содержащей (a) модифицированный капсульный сахарид по изобретению и/или конъюгат по изобретению и (b) фармацевтически приемлемый носитель. В данной области хорошо известны основанные на сахаридах или конъюгатах сахарид-белок вакцины, включающие в себя конъюгаты, основанные на де-O-ацетилированных сахаридах (NeisVac-C™). Вакцины по изобретению могут быть профилактическими (т.е. для предотвращения инфекции) или терапевтическими (т.е. для лечения инфекции), но, как правило, являются профилактическими.
"Фармацевтически приемлемые носители" включают в себя любой носитель, не индуцирующий самостоятельно образование антител, опасных для индивидуума, получающего фармацевтическую композицию. Как правило, пригодные носители представляют собой большие, медленно метаболизируемые макромолекулы, такие как белки, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимерные аминокислоты, трегалозные липидные агрегаты [71] (такие как масляные капли или липосомы), и неактивные вирусные частицы. Такие носители хорошо известны специалисту в данной области. Также вакцины могут содержать разбавители, такие как вода, солевой раствор, глицерол и т.д. Кроме того, могут присутствовать вспомогательные вещества, такие как увлажняющие или эмульгаторы, забуферивающие pH вещества и т.п. Полное обсуждение фармацевтически приемлемых наполнителей доступно в ссылке 72.
Как правило, фармацевтические композиции получают в виде инъекций или в виде жидких растворов или суспензий; также можно получать твердые формы, пригодные для растворения или суспендирования в жидких носителях до инъекции. Также композицию можно эмульгировать или инкапсулировать в липосомы для усиления эффекта адъюванта. Как правило, прямая доставка фармацевтических композиций является парентеральной (например, посредством инъекции, либо подкожно, внутрибрюшинно, внутривенно или внутримышечно, или доставлена в интерстициальное пространство ткани). Также фармацевтические композиции можно вводить в участок повреждения. Другие способы введения включают в себя пероральное и легочное введение, ректальное (суппозитории) и трансдермальные аппликации или аппликации чрескожные [например, ссылка 73], иглы и безыгольные шприцы.
Предпочтительно pH композиции составляет от 6 до 8, предпочтительно приблизительно 7. Стабильный pH можно поддерживать посредством применения буфера. Предпочтительно применение гистидинового буфера, когда композиция включает в себя соль гидроксида алюминия [74]. Композиция должна быть стерильной и/или апирогенной. Композиции по изобретению должны быть изотоническими по отношению к человеку.
Композиции по изобретению могут быть в водной форме (т.е. растворы или суспензии) или в сухой форме (например, лиофилизированные порошки). Жидкая форма позволяет вводить композицию прямо из ее упакованной формы, без необходимости восстановления в водной среде, что, таким образом, идеально для инъекции. Такие композиции можно помещать в ампулы или в готовые заполненные шприцы. Шприцы могут быть снабжены иглами или без игл. Шприц включает в себя однократную дозу композиции, тогда как ампула может включать в себя однократную дозу или многократные дозы.
Жидкие композиции по изобретению также пригодны для восстановления других вакцин из лиофилизированных форм, например для восстановления лиофилизированных антигенов Hib или DTP. Когда композицию по изобретению следует применять для такого экстемпорального восстановления, по изобретению предоставлен набор, который может включать в себя две ампулы, или может содержать один готовый заполненный шприц и одну ампулу с содержанием шприца, применяемого для восстановления содержимого ампулы до инъекции.
Сухие композиции по изобретению характеризуются стабильностью при хранении, но их до введения необходимо восстанавливать в жидкую форму. По изобретению предоставлен набор, включающий в себя, во-первых, контейнер, содержащий сухую композицию по изобретению и, во-вторых, контейнер, содержащий водную композицию для восстановления содержимого первого контейнера. Водная композиция во втором контейнере может содержать антигены (например, неменингококковый) или может содержать только наполнители. Обычно первый контейнер представляет собой ампулу; второй контейнер также может представлять собой ампулу или может являться готовым заполненным шприцем.
При получении сухих композиций можно применять стабилизаторы, например дисахариды, такие как трегалоза и сахароза, или сахарные спирты, такие как маннитол. Эти компоненты добавляют до лиофилизации, и они находятся в восстановленной композиции.
Дополнительные компоненты композиций включают в себя хлорид натрия (для тоничности), например, приблизительно 9 мг/мл; детергент, например, Tween (полисорбат), такой как Tween 80, обычно в небольших количествах, например, <0,01%; и солевые буферы, например, фосфатный буфер. Композиция может включать в себя антибиотическое средство.
Композиции по изобретению можно фасовать в форме единичной дозы или в форме многократных доз. Для форм жидких многократных доз ампулы предпочтительно представляют собой предварительно заполненные шприцы. Эффективные дозы можно установить обычным способом, но для человека обычная доза композиции для инъекции имеет объем 0,5 мл.
Иммуногенные композиции, применяемые в качестве вакцин, содержат иммунологически эффективное количество антигена(ов), а также любых других необходимых компонентов. Под "иммунологически эффективным количеством" понимают, что введение такого количества индивидууму в виде однократной дозы или части серии эффективно для лечения или профилактики. Это количество варьирует в зависимости от самочувствия и физического состояния подлежащего лечению индивидуума, возраста, таксономической группы подлежащего лечению индивидуума (например, не являющийся человеком примат, примат и т.д.), способности иммунной системы индивидуума синтезировать антитела, степени желательной защиты, формулирования вакцины, оценки лечащим врачом медицинской ситуации и других значимых факторов. Ожидают, что количество находится в достаточно широком интервале, который можно определить посредством обычных исследований.
Обычное количество каждого менингококкового сахаридного антигена на дозу составляет от 1 мкг до 20 мкг, например, приблизительно 1 мкг, приблизительно 2,5 мкг, приблизительно 4 мкг, приблизительно 5 мкг или приблизительно 10 мкг (выраженного в виде сахарида).
Каждый сахарид может присутствовать, по существу, в том же количестве на дозу. Однако может быть предпочтительным избыток сахарида MenY, например, соотношение MenY:MenW135 (мас./мас.) 1,5:1 или более.
Когда присутствует конъюгат, композиция также может содержать свободный белок-носитель [50]. Предпочтительно свободный белок-носитель составляет менее 5% от массы композиции; более предпочтительно он составляет менее 2% от массы.
Композиции по изобретению обычно содержат один или несколько адъювантов. Такие адъюванты включают в себя в качестве неограничивающих примеров
А. Содержащие минералы композиции
Содержащие минералы композиции, пригодные для применения в качестве адъювантов по изобретению, включают в себя минеральные соли, такие как соли алюминия и кальция. Минеральные соли по изобретению включают в себя соли, такие как гидроксиды (например, оксигидроксиды), фосфаты (например, гидроксифосфаты, ортофосфаты), сульфаты и т.д. [например, см. главы 8 и 9 ссылки 75], или смеси различных минеральных соединений с соединениями, принимающими любую пригодную форму (например, гель, кристаллическую, аморфную и т.д.), и предпочтительно с адсорбцией. Содержащие минералы композиции также можно получать как часть соли металла [76].
В. Масляные эмульсии
Композиции в форме масляных эмульсий, пригодные для применения в качестве адъювантов по изобретению, включают в себя сквален-водные эмульсии, такие как MF59 [глава 10 ссылки 75; также см. ссылку 77] (5% сквален, 0,5% Tween 80 и 0,5% Span 85, формулированная в субмикронные частицы с применением микрофлюидизатора). Также можно применять полный адъювант Фрейнда (CFA) и неполный адъювант Фрейнда (IFA).
С. Препараты сапонина [глава 22 ссылки 75]
Препараты сапонина также можно применять в качестве адъювантов по изобретению. Сапонины представляют собой гетерогенную группу стероидных гликозидов и тритерпеноидных гликозидов, обнаруженных в коре, листьях, стеблях, корнях и даже цветках широкого спектра видов растений. Сапонин из коры дерева Quillaia saponaria Molina широко изучали в качестве адъювантов. Также сапонин можно промышленно получать из Smilax ornata (сарсапарель), Gypsophilla paniculata (brides veil) и Saponaria officianalis (мыльный корень). Препараты адъюванта сапонина включают в себя очищенные препараты, такие как QS21, а также липидные препараты, такие как ISCOM. QS21 продается как Stimulon™.
Композиции сапонина очищают с применением HPLC и RP-HPLC. С применением этих способов идентифицировали определенные очищенные фракции, включая QS7, QS17, QS18, QS21, QH-A, QH-B и QH-C. Предпочтительно сапонин представляет собой QS21. Способ получения QS21 сообщают в ссылке 78. Препараты сапонина также могут содержать стирол, такой как холестерин [79].
Можно применять сочетания сапонинов и холестеринов для формирования особых частиц, названных иммуностимулирующими комплексами (ISCOM) [глава 23 ссылки 75]. Обычно ISCOM также включают в себя фосфолипид, такой как фосфатидилэтаноламин или фосфатидилхолин. Любой известный сапонин можно применять в ISCOM. Предпочтительно ISCOM включают в себя один или несколько QuilA, QHA и QHC. ISCOM описаны далее в ссылках 79-81. Необязательно ISCOM можно лишать дополнительного детергента [82].
Рассмотрение разработки основанных на сапонине адъювантов можно найти в ссылках 83 и 84.
D. Виросомы и вирусоподобные частицы
Виросомы и вирусоподобные частицы (VLP) также можно применять в качестве адъювантов по изобретению. Как правило, эти структуры содержат один или несколько вирусных белков, необязательно сочетаемых или формулируемых с фосфолипидом. Как правило, они непатогенные, нереплицирующиеся и, как правило, не содержат никакого нативного вирусного генома. Вирусные белки можно рекомбинантно продуцировать или выделять из целых вирусов. Эти пригодные для применения в виросомах или VLP вирусные белки включают в себя белки, полученные из вируса гриппа (такие как HA или NA), вируса гепатита B (такие как ядерные или капсидные белки), вируса гепатита E, вируса кори, вируса Sindbis, ротавируса, вируса ящура, ретровируса, вируса Norwalk, вируса папилл