Способ получения рентгеноаморфной модификации карведилола
Иллюстрации
Показать всеНастоящее изобретение относится к способам получения рентгеноаморфной модификации карведилола [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин}пропан-2-ол] и может быть использовано в фармацевтической промышленности. Способ состоит в том, что исходную субстанцию карведилола испаряют в вакуумной установке при температуре 80-200°С, остаточном давлении 5-5×10-4 Торр в потоке инертного газа, подающегося со скоростью от 10 до 100 мл/мин, с последующей конденсацией при -196 - +25°С. Технический результат - получение порошка рентгеноаморфной модификации карведилола [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин}пропан-2-ол] с размером частиц менее 5 мкм и повышенной биоактивностью. 8 ил.
Реферат
Настоящее изобретение относится к способам получения рентгеноаморфной модификации карведилола [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин)пропан-2-ол] и может быть использовано в фармацевтической промышленности.
Известен способ получения рентгеноаморфной модификации карведилола нагреванием при температуре 135°С в вакуумной печи до полного перехода в расплав, быстрым охлаждением до комнатной температуре в эксикаторе, растиранием в порошок и просеиванием через сито с величиной ячейки 60 меш [Venkatesh G.M., Bamett M.E., Owusu-Fordjour С., Galop M. Pharmaceutical Research, 2001, vol.18, No 1, p.98-103].
Недостатком этого способа является наличие стадий растирания и просеивания полученного лекарственного порошка через сито, что может привести к загрязнению лекарственного вещества материалами растирающих аппаратов и сит. Кроме того, получить этим методом лекарственный порошок с диаметром частиц менее 5-10 мкм невозможно. Известно, что биодоступность лекарственных средств определяется, в том числе, размером частиц порошков. Чем меньше размер порошка лекарственного средства, тем выше его биоактивность.
Задачей настоящего изобретения является получение порошка рентгеноаморфной модификации карведилола с размером частиц менее 5 мкм.
Данная задача решается настоящим изобретением, состоящим в том, что рентгеноаморфную модификацию карведилола получают нагреванием исходной субстанции в вакууме с последующим охлаждением, причем согласно изобретению исходную субстанцию испаряют в вакуумной установке при температуре 80-200°С, остаточном давлении 5-5×10-4 Торр в потоке инертного газа, подающегося со скоростью от 10 до 100 мл/мин и последующей конденсацией на поверхности при 25-196°С. При этом под исходной субстанцией понимается препарат кристаллического карведилола (получен согласно НД 42-11503-01) с размером частиц более 10 мкм
Отличиями предложенного способа являются величины интервалов: температуры испарения исходной кристаллической субстанции карведилола, остаточного давления, скорости подачи инертного газа и температуры конденсации.
При уменьшении температуры испарения ниже 80°С процесс протекает медленно, из-за этого получается частично закристаллизованный карведилол, что увеличивает размер частиц порошка больше 5-10 мкм и уменьшает биоактивность получаемого препарата. Увеличение температуры испарителя выше 200°С приводит к частичному термическому разложению исходного препарата, что приводит к загрязнению получаемого порошка.
При увеличении остаточного давлении выше 5 Торр процесс испарения замедляется. Это приводит к тому, что испаряющийся карведилол частично кристаллизуется, увеличивается размер частиц порошка и уменьшается его биоактивность. Уменьшение остаточного давления в реакторе ниже 5×10-4 Торр нецелесообразно из-за экономических и аппаратурных затруднений.
Уменьшение скорости подачи инертного газа ниже 10 мл/мин приводит к замедлению процесса испарения, как следствие - появлению кристаллического карведилола, увеличению размера частиц порошка и уменьшению биоактивности получаемого препарата. При увеличении скорости подачи инертного газа выше 100 мл/мин исходная субстанция карведилола уносится частично без испарения, что приводит к появлению кристаллов в получаемом продукте и, как следствие, - увеличению размеров кристаллитов больше 5-10 мкм и уменьшению биоактивности. В качестве инертного газа возможно использование любых химически не активных в данных условиях сред, таких как азот, аргон, гелий, углекислый газ и другие.
При повышении температуры конденсации получаемого порошка выше 25°С размер частиц становится больше 5 мкм, появляется частично закристаллизованный карведилол, биоактивность понижается. Понижение температуры конденсации ниже -196°С нецелесообразно из-за экономических и аппаратурных затруднений.
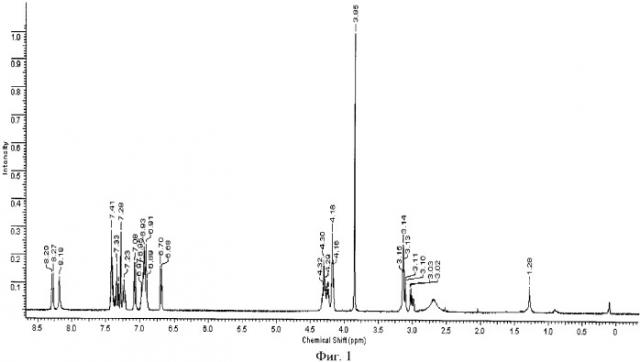
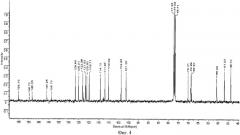
Для идентификации полученного вещества был проведен комплекс физико-химических методов анализа. Первоначально методом ядерного магнитного резонанса (ЯМР 13С - 1H была установлена идентичность химических формул исходного [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин)пропан-2-ол] (карведилола) и полученного рентгеноаморфного порошка. Определение химических сдвигов исходного и полученного предложенным способом вещества было проведено в их насыщенных растворах в дейтерированном хлороформе на ЯМР-спектрометре высокого разрешения VXR-400 фирмы "VARIAN" (США). Полученные данные приведены на фиг.1, 2. Сравнение полученных результатов показывает, что полученное вещество является карведилолом - [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин)пропан-2-ол].
Анализ полученного препарата на чистоту был проведен методом тонкослойной хроматографии (ТСХ) на пластинах Силикагель 60F254 (Merk) в системе растворителей этилацетат-вода-бутанол (40:10:50), а также методом ВЭЖХ ОФ на микроколоночном хроматографе Милихром А-02 (ЗАО ЭкоНова, Новосибирск, Россия) с колонкой 2×75 мм и сорбентом Pronto SIL-120-5-C18 с одновременным детектированием при длинах волн 220, 246, 254 и 280 нм. Оказалось, что суммарное содержание примесей в полученном карведилоле не превышает 1%, что соответствует нормативному документу НД 42-11503-01 на лекарственную субстанцию карведилола.
Таким образом, полученные методами ЯМР-спектроскопии, ТСХ и ВЭЖХ экспериментальные результаты однозначно свидетельствуют о том, что полученное вещество является карведилолом [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин}пропан-2-ол].
Для подтверждения того, что полученное по предлагаемому способу вещество отличается от исходной субстанции карведилола, были проведены рентгенофазовый анализ, ИК-спектроскопические исследования и дифференциальная сканирующая калориметрия.
По данным рентгенофазового анализа (РФА), проведенного на установке "Дрон-3М" на Cu Кα - излучении при скорости вращения гониометра 2 град./мин, полученное вещество является рентгеноаморфным (фиг.3). Об этом свидетельствует рентгеноаморфное гало в малоугловой области рентгеновского спектра, идентичное представленному в прототипе [Venkatesh G.M, Barnett М.Е., Owusu-Fordjour С., Galop M. Pharmaceutical Research, 2001, vol.18, No 1, p.98-103]. На этом же чертеже приведен спектр исходной кристаллической субстанции карведилола, который характеризуется наличием набора дифракционных максимумов.
ИК-спектроскопическое исследование, проведенное на ИК-Фурье-спектрофотометре «ИКАР» (ФИАН, Россия) в таблетке диаметром 13 мм с КВr при концентрации исследуемого вещества 1,5-2,0 мг на 300 мг бромида калия показало, что спектры исходного и полученного по предлагаемому способу карведилола (фиг.4 и 5) различаются в области 1000-800 см-1.
Результаты дифференциальной сканирующей калориметрии (ДСК), полученные на приборе ДСМ-2М (Россия) на воздухе со скоростью нагрева 4 град./мин с использованием в качестве держателей образцов алюминиевых микро-контейнеров, показали (фиг.6), что процесс плавления исходной субстанции карведилола характеризуется одним эндотермическим эффектом при температуре 114°С, а процесс плавления полученного по предлагаемому способу карведилола фиксированной температуры не имеет. Полученные данные аналогичны результатам, представленным в прототипе [Venkatesh G.M, Barnett М.Е., Owusu-Fordjour С., Galop M. Pharmaceutical Research, 2001, vol.18, No 1, p.98-103].
Таким образом, экспериментальные результаты РФА, ИК-спектроскопии и ДСК однозначно свидетельствуют о том, что полученное предлагаемым способом вещество отличается от исходной субстанции и аналогично представленному в прототипе рентгеноаморфному карведилолу [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин}пропан-2-ол].
Предлагаемое изобретение иллюстрируется, но не исчерпывается следующими иллюстрациями и примерами:
На фиг.1 изображен ЯМР 1Н спектр образца карведилола, полученный по предлагаемому способу.
На фиг.2 изображен ЯМР 1H спектр образца карведилола - исходной субстанции.
На фиг.3 изображен ЯМР 13С спектр образца карведилола, полученный по предлагаемому способу.
На фиг.4 изображен ЯМР 13С спектр образца карведилола - исходной субстанции.
На фиг.5 изображены рентгенограммы образцов карведилола, полученных: по предлагаемому способу - А) и исходной субстанции - В).
На фиг.6 изображен ИК-спектр образца карведилола, полученного по предлагаемому способу.
На фиг.7 изображен ИК-спектр исходной субстанции карведилола.
На фиг.8 изображены термограммы образцов карведилола, полученных по предлагаемому способу - А) и исходной субстанции - Б).
Пример 1. 0,5 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 80°С, остаточном давлении 4×10-2 Торр в потоке газообразного азота, подающегося со скоростью 30 мл/мин. Пары сконденсировали на охлажденной до -196°С поверхности.
Выход продукта составил 87,3 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 1-2 мкм.
Пример 2. 2,0 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 200°С, остаточном давлении 0,3 Торр в потоке газообразного азота, подающегося со скоростью 90 мл/мин. Пары сконденсировали на поверхности с температурой 25°С. Выход продукта составил 94,7 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 0,5 мкм.
Пример 3. 1,0 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 120°С, остаточном давлении 5×10-4 Торр в потоке газообразного аргона, подающегося со скоростью 10 мл/мин. Пары сконденсировали на охлажденной до -36°С поверхности. Выход продукта составил 85,9 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 3-4 мкм.
Пример 4. 1,5 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 150°С, остаточном давлении 5 Торр в потоке газообразного гелия, подающегося со скоростью 100 мл/мин. Пары сконденсировали на охлажденной до -78°С поверхности. Выход продукта составил 88,2 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 0,4 мкм.
Пример 5. 2,0 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 180°С, остаточном давлении 2×10-3 Торр в потоке газообразного азота, подающегося со скоростью 50 мл/мин. Пары сконденсировали на охлажденной до -196°С поверхности. Выход продукта составил 96,5 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 0,7 мкм.
Пример 6. 1,0 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 100°С, остаточном давлении 7×10-4 Торр в потоке газообразного аргона, подающегося со скоростью 70 мл/мин. Пары сконденсировали на охлажденной до -36°С, поверхности. Выход продукта составил 83,6 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 2-3 мкм.
Пример 7. 3,0 г карведилола по НД 42-11503-01 с размером частиц более 10 мкм испарили в вакуумной установке при температуре 200°С, остаточном давлении 9×10-4 Торр в потоке газообразного углекислого газа, подающегося со скоростью 45 мл/мин. Пары сконденсировали на охлажденной до -180°С поверхности. Выход продукта составил 91,6 мас.%. По данным РФА полученное вещество является рентгеноаморфным. Температура плавления полученного вещества размыта и фиксированного значения не имеет. По данным микроскопического анализа размер частиц полученного порошка 0,2 мкм.
Определение биоактивности карведилола, полученного предложенным способом, проводили определением артериального давления при введении непосредственно в желудок крысам самцам линий Wistar массой 350-400 г. Животных содержали в стандартных условиях согласно требованиям европейской ассоциации FELASA/ICLAS. Все животные имели неограниченный доступ к воде и корму. После вживления катеторов животных рассаживали по отдельным клеткам. В первый день эксперимента животных взвешивали и делили на 2 группы по 4 крысы в каждой. Первая экспериментальная группа получала ежедневно в течение четырех дней исходную субстанцию карведилола в дозе 12 мкг/кг в виде взвеси в 0,5 мас.% растворе метилцеллюлозы, вторая группа получала карведилол, полученный по предлагаемому способу, в той же дозе и также в виде взвеси в растворе 0,5 мас.% метилцеллюлозы. Взвеси вводились внутрижелудочно с помощью зонда.
Регистрацию системного артериального давления проводили через катетор, имплантированный в левую бедренную артерию. Для введения веществ катетор имплантировали в левую бедренную вену. Оказалось, что использование полученного по предлагаемому способу рентгеноаморфного карведилола по сравнению с исходной кристаллической субстанцией позволяет увеличить межимпульсный интервал у животных, что, по всей видимости, обусловлено блокадой β1-адренорецепторов сердца. Это приводит к снижению коэффициента барорефлекса на введение фенилэфрина и изопротеренола в животных, что свидетельствует об увеличении биоактивности рентгеноаморфного карведилола, полученного по предлагаемому способу.
Таким образом, предлагаемый способ по сравнению с прототипом позволяет получать рентгеноаморфный порошок карведилола [(±)-1-(9Н-карбазол-4-илокси)-3-{[2-(2-метоксифенокси)этил]амин}пропан-2-ол] с размером частиц менее 5 мкм и обладающий повышенной биоактивностью.
Способ получения рентгеноаморфной модификации карведилола нагреванием исходной субстанции в вакууме с последующим охлаждением, отличающийся тем, что исходную субстанцию испаряют в вакуумной установке при температуре 80-200°С, остаточном давлении 5-5·10-4 Торр в потоке инертного газа, подающегося со скоростью от 10 до 100 мл/мин и последующей конденсацией на поверхности при (-196) - (+25°)С.