Фармацевтическая композиция на основе пептида, нормализующего мочеиспускание, и способ ее применения
Иллюстрации
Показать всеИзобретение относится к лекарственным средствам, нормализующим мочеиспускание, и может быть использовано как средство для коррекции дизурических расстройств различного генеза, в том числе вследствие воздействия инфекционно-воспалительных и нейроэндокринных факторов. Заявлена фармацевтическая композиция, нормализующая мочеиспускание, содержащая в качестве действующего вещества эффективное количество пептида глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1] и фармацевтически приемлемый носитель. Заявлено средство, содержащее пептид-аспарагиновая кислота общей формулы H-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1], обладающий биологической активностью, проявляющейся в нормализации мочеиспускания. Предлагается способ регуляции функции детрузорно-сфинктерной системы мочевого пузыря, заключающийся во введении пациенту фармацевтической композиции, содержащей в качестве действующего вещества эффективное количество пептида глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1]. Заявленное изобретение обеспечивает нормализацию мочеиспускания путем регуляции детрузорно-сфинктерной системы мочевого пузыря. 3 н. и 2 з.п. ф-лы, 3 табл., 2 ил.
Реферат
Изобретение относится к лекарственным средствам, нормализующим мочеиспускание, и может быть использовано как средство для коррекции дизурических расстройств различного генеза, в том числе вследствие воздействия инфекционно-воспалительных и нейроэндокринных факторов.
Наиболее частыми проявлениями нарушений мочеиспускания являются затруднение и задержка мочеиспускания, учащенное мочеиспускание, частые и повелительные позывы мочиться, непроизвольное мочеиспускание и недержание мочи, которые существенно ухудшают качество жизни людей и создают большие психологические проблемы. Любой тип дисфункции мочеиспускания определяется аномальными изменениями анатомической и функциональной сохранности мочевыводящих путей, прежде всего, мочевого пузыря и его сфинктеров, предстательной железы, а также нервных структур, регулирующих акт мочеиспускания.
Для медикаментозного лечения нарушения мочеиспускания известны лекарственные препараты различных фармакологических групп, среди которых в основном применяются α-адреноблокаторы, такие как альфузозин, доксазозин, тамсулозин и теразозин (Энциклопедия лекарств. - М.: Издательство ООО «РЛС-2004. - С.68, 314, 827, 839); антихолинэстеразные препараты, такие как убретид (Энциклопедия лекарств. - М.: Издательство ООО «РЛС-2004» - С.887), калимин (Лекарственные препараты в России: Справочник Видаль. - М.: Издательство ЗАО «АстраФармСервис», 2003. - С.451); ингибиторы 5-α редуктазы, например финастерид (Энциклопедия лекарств. - М.: Издательство ООО «РЛС-2004. - С.919); а также фитотерапевтические агенты, такие как липидостериновый экстракт Serenoa repens, экстракты корня Pygeum africanum, Hypoxis rooperi, Cucurbita pero, Populus tremula, Echinacea purpurea и Secale cereale (Аляев Ю.Г., Григорян В.А., Гаджиева З.К. Расстройства мочеиспускания. - М.: Издательство Литтерра, 2006. - С.208).
Однако необходимо отметить, что вышеперечисленные лекарственные средства в той иной степени обладают либо побочным действием, либо низкой эффективностью.
Для медикаментозного лечения дизурических расстройств у женщин используется терапия, основанная на применении эстрогенных препаратов. Как установлено, эстроген эффективен для повышения внутриуретрального давления и изменения структуры слизистой мембраны и сосудов. При этом необходимо отметить, что хорошо известны побочные эффекты, наблюдаемые при лечении эстрогеном.
Известны композиции, включающие пептиды, используемые для медикаментозного лечения дизурических расстройств (WO 9933482, опубл. 08.07.1999; WO 9803189, опубл. 29.01.1999 и WO 2004004701, опубл. 15.01.2004). Следует отметить, что известные средства позволяют решать эту проблему только в ограниченном ряде случаев (недержание мочи). В связи с тем, что лечение дизурических расстройств является сложной и во многом еще нерешенной задачей, в настоящее время остается актуальной разработка эффективных лекарственных средств, в том числе соединений, обладающих биологической активностью, проявляющейся в регуляции детрузорно-сфинктерной системы мочевого пузыря.
Известен пептид формулы H-Glu-Asp-OH различных конфигураций под регистрационными номерами RN 3918-84-1 и RN 3914-66-7 (STN int. BD Registry Chemical abstract). Из уровня техники известен пептид глутамил-аспарагиновая кислота (The unitcell dimensions and the space group of L-glutaminyl-L-aspagine. Pasternak R.A. et.al. March 1954-Д2).
Настоящим изобретением решена задача получения средства пептидной природы, обладающего биологической активностью, проявляющейся в регуляции детрузорно-сфинктерной системы мочевого пузыря, а также фармацевтической композиции, содержащей в качестве действующего вещества этот пептид, использование которой нормализует мочеиспускание субъекта, нуждающегося в этом.
«Субъект, нуждающийся в этом» означает млекопитающее, например человека (пациента), имеющего одно или более проявлений дизурических расстройств, при которых применение предлагаемого средства целесообразно с позиций современных биомедицинских знаний.
Технический результат изобретения заключается в создании средства, обладающего биологической активностью, проявляющейся в нормализации мочеиспускания путем регуляции функции детрузорно-сфинктерной системы мочевого пузыря, а также фармацевтической композиции, содержащей указанный пептид в качестве действующего вещества, которая может быть использована для регуляции функции детрузорно-сфинктерной системы мочевого пузыря.
Для решения поставленной задачи и достижения указанного технического результата предложена группа изобретений, объединенных общим изобретательским замыслом.
В одном из своих аспектов настоящее изобретение относится к фармацевтической композиции, нормализующей мочеиспускание, содержащей в качестве действующего вещества эффективное количество пептида глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1] и фармацевтически приемлемый носитель. При этом фармацевтическая композиция находится в форме, подходящей для парентерального введения.
В еще одном аспекте настоящее изобретение относится к пептиду глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1].
В другом аспекте настоящее изобретение относится к средству, содержащему пептид глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1], обладающему биологической активностью, проявляющейся в нормализации мочеиспускания путем регуляции функции детрузорно-сфинктерной системы мочевого пузыря.
Следующий аспект настоящего изобретения касается способа регуляции функции детрузорно-сфинктерной системы мочевого пузыря, заключающегося во введении пациенту фармацевтической композиции, содержащей в качестве действующего вещества эффективное количество пептида глутамил-аспарагиновая кислота общей формулы Н-Glu-Asp-OH последовательности 1 [SEQ ID NO: 1] в дозе от 0,01 мкг/кг до 100 мкг/кг массы тела однократно ежедневно в течение 10 дней. При этом введение осуществляют внутримышечно.
Пептид глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH получают классическим методом пептидного синтеза в растворе.
Средство, содержащее пептид глутамил-аспарагиновая кислота общей формулы H-Glu-Asp-OH, проявляет биологическую активность, выражающуюся в нормализации мочеиспускания, а именно в регулировании функции детрузорно-сфинктерной системы мочевого пузыря, оказывая нормализующее влияние на характер мочеиспускания. Возможность объективного проявления технического результата при использовании изобретения подтверждена достоверными данными, приведенными в примерах, которые содержат сведения экспериментального и клинического характера, полученные в процессе проведения исследований по методикам, принятым в данной области.
Изучение биологической активности пептида H-Glu-Asp-OH проводили по его влиянию на рост эксплантатов стенки мочевого пузыря, на гладкомышечные клетки детрузора, характер мочеиспускания, урофлоуметрические показатели у больных пожилого и старческого возраста с дизурическими расстройствами, а также больных хроническим простатитом.
Нормализующее действие средства, содержащего пептид H-Glu-Asp-OH, на характер мочеиспускания выявлено при его экспериментальном и клиническом изучении.
Для получения фармацевтической композиции, отвечающей изобретению, эффективное количество пептида H-Glu-Asp-OH как действующее вещество смешивают с фармацевтически приемлемым носителем согласно принятым в фармацевтике способам компаундирования.
Понятие «эффективное количество» подразумевает использование такого количества действующего вещества, которое в соответствии с его количественными показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме. В качестве носителя могут использоваться различные вещества в зависимости от лекарственной формы препарата, желаемой для введения в организм. Для парентерального введения в качестве носителя обычно используют физиологический раствор или стерильную воду.
Сущность изобретения иллюстрируется чертежами и поясняется табл.1-3.
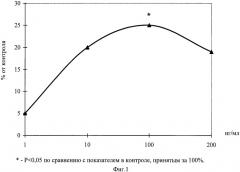
На фиг.1 показано влияние пептида H-Glu-Asp-OH на рост эксплантатов стенки мочевого пузыря.
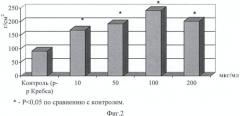
На фиг.2 показано влияние пептида H-Glu-Asp-OH на гладкомышечные клетки детрузора in vitro.
В табл.1 представлено влияние фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH на морфологические и биохимические показатели периферической крови морских свинок при изучении хронической токсичности.
В табл.2 представлено влияние пептида H-Glu-Asp-OH, используемого в фармацевтической композиции в качестве действующего вещества, на состояние уродинамики больных хроническим простатитом.
В табл.3 представлено влияние фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH, на состояние уродинамики больных пожилого и старческого возраста с дизурическими расстройствами.
Изобретение иллюстрируется примером получения пептида классическим методом синтеза пептида H-Glu-Asp-OH в растворе (пример 1), примерами, подтверждающими проявление пептидом биологической активности (примеры 2, 3), примером изучения токсичности пептида H-Glu-Asp-OH, используемого в качестве действующего вещества в фармацевтической композиции (пример 4). Кроме того, примерами результатов клинического применения фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH (примеры 5 и 6), демонстрирующими ее фармакологические свойства и подтверждающими возможность достижения терапевтического эффекта.
Пример 1. Синтез пептида H-Glu-Asp-OH
1. Название соединения: глутамил-аспарагиновая кислота.
2. Структурная формула H-Clu-Asp-ОН
3. Брутто-формула без противоиона: C9H14N2O7.
4. Молекулярный вес без противоиона: 262,21.
5. Противоион: ацетат.
6. Внешний вид: белый аморфный порошок без запаха.
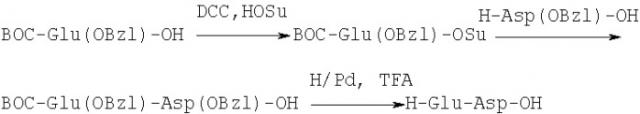
7. Способ синтеза: пептид получен классическим методом синтеза в растворе по схеме:
BOC - трет.бутилоксикарбонильная группа,
OSu - N-оксисукцинимидный эфир,
DCC -N'N'-дициклогексилкарбодиимид,
OBzl - бензиловый эфир,
TFA - трифторуксусная кислота,
8. Характеристики готового препарата:
- содержание основного вещества: 98,33% (по ВЭЖХ, 220 нм);
- ТСХ - индивидуален, Rf=0,24 (ацетонитрил-вода 2:1).
- содержание влаги: 6%.
- pH 0,01% раствора: 4,3.
- Удельное оптическое вращение: [α]D22:+31° (с=1, H2O), "Polamat A", Carl Zeiss Jena.
Пример синтеза:
1) BOC-Glu(OBzl)-OSu, N-оксисукцинимидный эфир N-трет.бутилоксикарбонил-(γ-бензил)глутаминовой кислоты (I)
N-трет.бутилоксикарбонил-(γ-бензил)глутаминовую кислоту BOC-Glu(OBzl)-OH (33,7 г, 0,1 моль) растворяли в 50 мл N,N'-диметилформамида, охлаждали до температуры минус 10°С, добавляли при перемешивании охлажденные до температуры 4-6°С растворы N,N'-дициклогексилкарбодиимида (23,0 г, 0,11 моль) в 30 мл N,N'-диметилформамида и N-гидроксисукцинимида (13,0 г, 0,11 моль) в 20 мл N,N'-диметилформамида. Реакционную смесь перемешивали в течение 12 ч при охлаждении льдом и далее в течение суток при комнатной температуре. Выпавшую N,N'-дициклогексилмочевину отфильтровывали и полученный раствор активированного эфира использовали без выделения на следующей стадии.
2) BOC-Glu(OBzl)-Asp(OBzl)-OH, N-трет.бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартат (II)
(β-бензил)аспарагиновую кислоту H-Asp(OBzl)-OH (28,0 г, 0,12 моль) и 36 мл (0,12 моль) триэтиламина суспендировали в 50 мл N,N'-диметилформамида и перемешивали в течение 1 ч. Затем добавляли порциями раствор активированного эфира ВОС-Glu(OBzl)-OSu (I), полученный на предыдущей стадии. Реакционную смесь перемешивали при комнатной температуре в течение 2 суток. Затем подкисляли 0,5 н. раствором серной кислоты до pH 2-3 и экстрагировали этилацетатом 4×50 мл. Вытяжки объединяли и последовательно промывали 0,5 н. раствором H2SO4 3×50 мл, водой 2×50 мл, 5% раствором NaHCO3 2×50 мл, водой 2×50 мл, насыщенным раствором NaCl 2×50 мл. Органический слой сушили над Na2SO4, упаривали растворитель в вакууме, остаток кристаллизовали под гексаном. Получено 50 г продукта (92%). Rf=0,34 (бензол-ацетон 2:1).
3) H-Glu-Asp-OH (III), глутамил-аспарагиновая кислота
Защищенный дипептид BOC-Glu(OBzl)-Asp(OBzl)-OH (II) (5,4 г) (0,01 моль) растворяли в смеси метиловый спирт - вода (4:1) (50 мл) и гидрировали над катализатором Pd/C (5%) в течение 4 ч. Катализатор отфильтровывали, растворитель упаривали в вакууме, остаток сушили в вакууме над КОН и Р2O5. Далее продукт растворяли в 25 мл смеси хлористый метилен-трифторуксусная кислота (5:1) и выдерживали при комнатной температуре в течение 2 ч. Полноту прохождения реакции деблокирования контролировали по ТСХ в системе ацетонитрил-вода (1:3). Растворитель упаривали в вакууме, остаток сушили в вакууме над KOH.
Для очистки 320 мг препарата растворяли в 4 мл 0,01% раствора трифторуксусной кислоты и подвергали высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50×250 мм Diasorb-130-C16T, 7mkm. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module. Условия хроматографирования - A: 0,1% TFA; В: MeCN/0,1% TFA, градиент В 0 → 50% за 100 мин. Объем пробы 5 мл, детекция при длине волны 215 нм, сканирование при длинах волн 190-600 нм, скорость потока 10 мл/мин. Отбирали фракцию основного пика. Растворитель упаривали в вакууме при температуре не выше 40°С, упаривание многократно (5 раз) повторяли с 10 мл 10% раствора уксусной кислоты.
Окончательно остаток растворяли в 20 мл деионизованной воды и лиофилизовывали.
Получено 250 мг очищенного препарата в виде аморфного белого порошка без запаха.
4) Анализ готового препарата
- Содержание основного вещества определяли методом ВЭЖХ на колонке Phenomenex С 18 LUNA 4,6×150 mm. A: 0,1% TFA, В: MeCN; grad.B 0-100% in 10 min. Скорость потока 1 мл/ мин. Детекция при длине волны 220 нм, сканирование при длинах волн 190-600 нм, проба 20µl. Содержание основного вещества 98,33%.
- ТСХ: индивидуален, Rf=0,24 (ацетонитрил-вода 2:1, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1 ВЭ 8-12 мкм, проявление хлор/бензидин).
- Содержание влаги: 6% (гравиметрически по потере массы при сушке 20 мг при температуре 100°С).
- pH 0,01% раствора: 4,3 (потенциометрически).
- Удельное оптическое вращение: [α]D22:+31° (с=1, H2O), "Polamat A", Carl Zeiss Jena.
Пример 2. Влияние пептида H-Glu-Asp-OH на развитие эксплантатов стенки мочевого пузыря
Эксперименты проведены на 26 фрагментах стенки мочевого пузыря крыс линии «Wistar» с массой тела 150-200 г. Питательная среда для культивирования эксплантатов состояла из 35% раствора Игла, 25% фетальной сыворотки теленка, 35% раствора Хенкса, 5% куриного эмбрионального экстракта, в среду добавляли глюкозу (0,6%), инсулин (0,5 ед./мл), пенициллин (100 ед./мл), глютамин (2 мМ). Фрагменты стенки мочевого пузыря помещали в эту среду и культивировали в чашках Петри в термостате при температуре 36,7±0,2°С в течение 2 суток. В экспериментальную среду с целью выявления эффективной концентрации добавляли пептид H-Glu-Asp-OH в концентрациях 1, 10, 100 и 200 нг/мл. Критерием биологической активности служил индекс площади (ИП)-соотношение площади всего эксплантата вместе с зоной роста к исходящей площади фрагмента стенки мочевого пузыря. Значения ИП выражали в процентах, контрольное значение ИП принималось за 100%.
На фиг.1 показано влияние пептида H-Glu-Asp-OH на развитие эксплантатов стенки мочевого пузыря.
Установлено, что через 1 сутки культивирования происходило распластывание эксплантатов на коллагеновой подложке и начиналось выселение пролиферирующих и мигрирующих клеток по периферии эксплантата. На 3-й сутки культивирования при концентрации пептида H-Glu-Asp-OH 100 нг/мл наблюдалось достоверное повышение ИП эксплантатов на 25% по сравнению с контрольными значениями ИП (фиг.1). При исследовании эксплантатов стенки мочевого пузыря на более длительных сроках культивирования (7 дней) было выявлено аналогичное стимулирующее действие пептида Н-Glu-Asp-OH в той же концентрации.
Таким образом, в отношении ткани стенки мочевого пузыря пептид H-Glu-Asp-OH оказывал тканеспецифическое действие, проявляющееся в стимуляции роста эксплантатов.
Пример 3. Влияние пептида H-Glu-Asp-OH на гладкомышечные клетки детрузора мочевого пузыря in vitro
Эксперименты проводили на полоске детрузора мочевого пузыря крыс, установленной между фиксированным стержнем и датчиком силы, помещенной в специальную ванночку с раствором Кребса. В раствор добавляли пептид H-Glu-Asp-OH в концентрациях 1, 5, 10 и 20 мкг/мл, затем регистрировали авторитмическую сократительную активность полоски мочевого пузыря.
На фиг.2 показано влияние пептида H-Glu-Asp-OH на напряжение полоски детрузора мочевого пузыря крысы in vitro.
Установлено, что под действием пептида H-Glu-Asp-OH происходит дозозависимое изменение фазно-тонических сокращений гладкомышечных клеток детрузора мочевого пузыря (фиг.2).
Максимальное напряжение, развиваемое мышцей в ответ на действие пептида Н-Glu-Asp-OH, возрастало по мере увеличения его концентрации в перфузате до 100 мкг/мл. Так, если в контрольном растворе максимальное напряжение равнялось 91,6 г/см2, то при действии пептида H-Glu-Asp-OH в концентрации 100 мкг/мл значение показателя возрастало до 241,2 г/см2 (фиг.2).
Пример 4. Изучение токсичности пептида H-Glu-Asp-OH
Общетоксическое действие пептида H-Glu-Asp-OH исследовали в соответствии с требованиями «Руководства по экспериментальному (доклиническому) изучению новых фармакологических веществ» (2005): острой токсичности при однократном введении препарата, а также подострой и хронической токсичности при длительном введении пептида.
Исследование по изучению острой токсичности проведено на 60 белых беспородных мышах-самцах с массой тела 18-20 г. Животные были рандомизированно разделены на 6 равных групп. Препарат вводили животным однократно внутримышечно в дозах 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг в 0,25 мл стерильного 0,9% раствора NaCl. Животным контрольной группы в том же объеме вводили стерильный 0,9% раствор NaCl.
Исследования по изучению подострой токсичности проведено на 50 белых беспородных крысах-самцах с массой тела 180-220 г. Ежедневно однократно животным подопытных групп вводили препарат внутримышечно в течение 90 дней в дозах 0,01 мг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл стерильного 0,9% раствора NaCl. Животным контрольной группы вводили в том же объеме стерильный 0,9% раствор NaCl. До введения препарата, на 30, 60 и 90 сутки после начала введения препарата у животных исследовали морфологический состав и свойства периферической крови. При завершении эксперимента исследовали биохимические и коагулологические показатели крови.
Исследования по изучению хронической токсичности проводили в течение 6 месяцев, исходя из длительности рекомендуемого клинического назначения препарата, на 76 морских свинках-самцах с массой тела 290-320 г. Животные подопытных групп получали ежедневно однократно внутримышечно пептид в течение 6 месяцев в дозах 0,01 мг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл стерильного 0,9% раствора NaCl. В контрольной группе животным вводили по аналогичной схеме стерильный 0,9% раствор NaCl в том же объеме. У животных в периферической крови общепринятыми методами определяли: количество эритроцитов, гемоглобина, ретикулоцитов, тромбоцитов, лейкоцитов, лейкоцитарную формулу, скорость оседания эритроцитов (СОЭ), резистентность эритроцитов. Наряду с этим определяли содержание в сыворотке крови общего белка по методу Лоури, калия и натрия методом плазменной спектрофотометрии. После завершения эксперимента проводили патоморфологическое исследование головного и спинного мозга, спинномозговых ганглиев, щитовидной железы, паращитовидных желез, надпочечников, семенников, гипофиза, сердца, легких, аорты, печени, почки, мочевого пузыря, поджелудочной железы, желудка, тонкой кишки, толстой кишки, тимуса, селезенки, лимфатических узлов, костного мозга.
При изучении острой токсичности установлено, что однократное введение исследуемого пептида животным в дозе, превышающей терапевтическую, рекомендованную для клинического применения, более чем в 5000 раз, не вызывает токсических реакций, что свидетельствует о большой терапевтической широте препарата.
Изучение подострой и хронической токсичности пептида свидетельствует об отсутствии побочных эффектов при длительном применении препарата в дозах, превышающих терапевтическую в 100-1000 раз. При исследовании не отмечено достоверного влияния исследуемого пептида на морфологические, биохимические показатели в периферической крови, а также на СОЭ и резистентность эритроцитов (табл.1).
В табл.1 показано влияние пептида H-Glu-Asp-OH на морфологические и биохимические показатели периферической крови морских свинок при изучении хронической токсичности.
При оценке общего состояния животных, морфологических и биохимических показателей периферической крови, морфологического состояния внутренних органов, состояния сердечно-сосудистой и дыхательной систем, функции печени и почек патологические изменения в организме не обнаружены.
Отсутствие общетоксического действия позволяет рекомендовать фармацевтическую композицию, содержащую пептид H-Glu-Asp-OH в качестве действующего вещества, для проведения клинических испытаний.
Пример 5. Эффективность применения фармацевтической композиции, содержащей пептид H-Glu-Asp-OH, у больных хроническим простатитом
В исследовании приняли участие 56 больных хроническим простатитом в стадии обострения в возрасте от 24 до 45 лет. Основными проявлениями заболевания были ноющие боли типичной локализации, различные нарушения мочеиспускания (болезненность при мочеиспускании, учащенное и/или затрудненное мочеиспускание), расстройства способности к совершению половых сношений и признаки невротического состояния.
Всех пациентов обследовали по следующему диагностическому алгоритму: пальцевое ректальное исследование; трансректальное УЗИ простаты; надлобковое УЗИ мочевого пузыря для определения остаточной мочи; общий анализ мочи и крови; микроскопия секрета предстательной железы; бактериологическое исследование секрета и мочи; вычисление индекса симптомов хронического простатита - NIH - CPSI, 1999 г.; определение урофлоуметрического индекса (скорость мочеиспускания). Перечисленные параметры определяли у всех пациентов до и после окончания лечения.
Всем пациентам до назначения антибактериальных препаратов была проведена ПЦР диагностика для выявления флоры, передающейся половым путем. Пациенты, у которых была выявлена специфическая инфекция (хламидии, уреоплазма, микоплазма, трихомонады и т.д.), в настоящее клиническое исследование включены не были.
Больные методом рандомизации были разделены на 2 группы. В контрольную группу вошли 20 человек, которые получали общепринятое лечение, включавшее антибактериальные препараты (антибиотики), спазмолитики (но-шпа, баралгин), стимуляторы обменных процессов (раверон), препараты, улучшающие микроциркуляцию крови (трентал, эскузан).
36 пациентов основной группы были разделены на 3 подгруппы в зависимости от степени выраженности дизурических расстройств.
Пациентам, отмечавшим наиболее выраженные нарушения мочеиспускания в виде болезненности и учащения мочеиспускания до 15-20 раз, особенно в ночные часы (до 10 раз), дополнительно к приведенному выше общепринятому лечению, назначали внутримышечно фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 5 мг в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней.
При средней степени выраженности дизурических расстройств (умеренной болезненности и учащении мочеиспускания до 10 раз в день) пациенты получали дополнительно к общепринятым средствам внутримышечно фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 100 мкг в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней.
Пациентам, отмечавшим умеренные нарушения мочеиспускания, выражавшиеся в учащении мочеиспускания в ночное время до 5 раз, назначали дополнительно к общепринятому лечению внутримышечно фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 1 мкг в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней.
При сравнении показателей пациентов контрольной и основной групп более выраженная положительная динамика отмечена в группе пациентов, получавших фармацевтическую композицию, содержащую в качестве действующего вещества пептид Н-Glu-Asp-OH, как компонент комплексной терапии.
При оценке динамики субъективных показателей все пациенты, получавшие дополнительно к общепринятым средствам фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, оценили свое состояние как «улучшенное». По шкале симптомов это соответствует позициям «хорошо» - 72% и «удовлетворительно» - 28%. Пациентов, не отметивших улучшения состояния, в основной группе не было.
При этом из 20 пациентов контрольной группы только 38% считали свое состояние «удовлетворительным», хороший эффект отметили 32% пациентов, а 30% пациентов контрольной группы отметили «отсутствие явного улучшения» при оценке эффекта от лечения.
По окончании лечения с применением фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH, болевые ощущения при мочеиспускании полностью исчезли у 62,0% пациентов основной группы и значительно уменьшились у 34,7% пациентов, предъявлявших соответствующие жалобы (в контрольной группе 46,2% и 32,4% соответственно). У 3,3% пациентов лечение не дало ожидаемого эффекта, и динамики болевых ощущений не наблюдалось (в контрольной группе 21,4% пациентов).
Поллакиурия (учащение мочеиспускания) полностью перестала беспокоить 82,3% пациентов основной группы, кроме того, у них также исчезла потребность ночного мочеиспускания.
Странгурия (затрудненное мочеиспускание) перестала беспокоить 74,8% пациентов основной группы, 15,9% отметили заметное усиление струи мочи и облегчение акта мочеиспускания.
Следует отметить, что больных контрольной группы поллакиурия и странгурия, особенно потребность ночного мочеиспускания, продолжали беспокоить и после окончания курса лечения хронического простатита общепринятыми средствами.
Данные, приведенные в табл.2, в которой показано влияние фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH, на состояние уродинамики больных хроническим простатитом, позволяют сделать следующие выводы.
У пациентов контрольной группы, получавших общепринятую терапию, урофлоуметрический индекс практически не изменился после лечения.
В группе пациентов основной группы, получавших фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH как компонент комплексной терапии, урофлоуметрический индекс увеличился почти в 2 раза, что является подтверждением положительного влияния пептида как действующего вещества на характер мочеиспускания.
Следует отметить, что урофлоуграммы, записанные после лечения у больных хроническим простатитом I и II стадии, показали восстановление основных параметров мочеиспускания до нормальных значений под действием фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 1 мкг или 100 мкг в 1 мл физиологического раствора соответственно (табл.2). При III стадии болезни полной нормализации показателей мочеиспускания препятствовало снижение эластичности шейки мочевого пузыря из-за склеротических изменений ткани предстательной железы, но тем не менее у этих пациентов, получавших фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 5 мг в 1 мл физиологического раствора, наблюдалось заметное усиление струи мочи и сокращение потребности в ночном мочеиспускании до 3-4 раз.
Таким образом, результаты проведенного исследования свидетельствуют о терапевтической эффективности фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH в дозе 5 мг, 100 мкг и 1 мкг (в зависимости от степени выраженности нарушения мочеиспускания) в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней и целесообразности его применения в комплексном лечении воспалительных заболеваний предстательной железы, сопровождающихся дизурическими расстройствами.
Пример 6. Эффективность применения фармацевтической композиции, содержащей пептид H-Glu-Asp-OH, у больных пожилого и старческого возраста с дизурическими расстройствами
В исследовании приняли участие 67 пациентов, страдающих нарушением мочеиспускания, в том числе 43 мужчины в возрасте от 68 до 82 лет и 24 женщины в возрасте от 58 до 84 лет. Все пациенты пожилого и старческого возраста предъявляли жалобы на учащенное мочеиспускание до 10-20 раз в сутки, особенно с ночные часы (до 5-10 раз), что существенно снижало качество жизни пожилых людей и затрудняло их социальную адаптацию.
Эффективность лечения оценивали на основании динамики жалоб больных и показателей уродинамики. Определяли максимальную, среднюю скорость и время мочеиспускания, время достижения максимальной скорости мочевыделения, оценивали урофлоуметрический индекс.
Больные методом рандомизации были разделены на 2 группы. В контрольную группу вошли 25 человек (17 мужчин, 8 женщин), которые получали общепринятое лечение, включавшее препараты спазмолитического (спазмекс, спазмол, спазмовералгин Нео) и холинолитического (детрузитол) действия.
Составившую основную группу 42 пациента (26 мужчин, 16 женщин) были разделены на 3 подгруппы в зависимости от степени выраженности нарушения мочеиспускания. Пациентам, отмечавшим наиболее выраженные дизурические расстройства в виде учащения мочеиспускания до 15-20 раз в сутки, особенно в ночные часы (до 10 раз), назначали внутримышечно фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 5 мг в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней.
При средней степени выраженности дизурических расстройств (учащении мочеиспускания до 10 раз в день, в том числе до 5 раз в ночные часы) больные получали внутримышечно фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 100 мкг в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней. Пациентам, отмечавшим умеренные нарушения мочеиспускания, выражавшиеся в учащении мочеиспускания в ночное время до 5 раз, назначали внутримышечно фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 1 мкг в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней.
При сравнении показателей пациентов контрольной и основной групп выраженная положительная динамика отмечена в группе пациентов, получавших фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH.
При оценке динамики субъективных показателей все пациенты, получавшие фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, оценили свое состояние как «улучшенное». Поллакиурия (учащение мочеиспускания) полностью перестала беспокоить 86,8% больных основной группы, кроме того, у них также исчезла потребность ночного мочеиспускания. У 13,2% больных основной группы поллакиурия значительно уменьшилась до 7-8 раз в сутки, а потребность ночного мочеиспускания сократилась до 2-3 раз.
Данные, приведенные в табл.3, в которой показано влияние фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH, на состояние уродинамики у пациентов пожилого и старческого возраста с дизурическими расстройствами, позволяют сделать следующие выводы.
Следует отметить, что у пациентов контрольной группы не наблюдалось положительной динамики функции мочевого пузыря как по субъективным, так и по объективным показателям, несмотря на применение общепринятых средств.
У пациентов контрольной группы, получавших общепринятую терапию, урофлоуметрический индекс практически не изменился после лечения.
В группе пациентов основной группы, получавших фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, урофлоуметрический индекс увеличился почти в 2 раза, что является подтверждением положительного влияния пептида как действующего вещества на характер мочеиспускания.
Следует отметить, что урофлоуграммы, записанные после лечения у больных пожилого и старческого возраста с умеренными дизурическими расстройствами, показали восстановление основных параметров мочеиспускания до нормальных значений под действием фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 1 мкг или 100 мкг в 1 мл физиологического раствора соответственно.
У пациентов старческого возраста с выраженными проявлениями дизурических расстройств полной нормализации показателей мочеиспускания препятствовало возрастное снижение эластичности шейки мочевого пузыря, но тем не менее у этих пациентов, получавших фармацевтическую композицию, содержащую в качестве действующего вещества пептид H-Glu-Asp-OH, в дозе 5 мг в 1 мл физиологического раствора, наблюдалось заметное усиление струи мочи и сокращение потребности в дневном мочеиспускании до 7-8 раз, а в ночном - до 2-3 раз.
Таким образом, результаты проведенного исследования свидетельствуют о терапевтической эффективности фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH в дозах 5 мг, 100 мкг и 1 мкг (в зависимости от степени выраженности дизурических расстройств) в 1,0 мл физиологического раствора однократно ежедневно в течение 10 дней и целесообразности его применения в лечении пациентов с дизурическими расстройствами различного генеза.
Также необходимо отметить, что примеры клинического применения фармацевтической композиции, содержащей в качестве действующего вещества пептид H-Glu-Asp-OH у пациентов с дизурическими расстройствами различного генеза, наглядно подтверждают, что в отличие от известных из уровня техники средств предлагаемая фармацевтическая композиция характеризуется способностью при ее введении обеспечить улучшенную активность в отношении детрузорно-сфинктерной системы мочевого пузыря при низких концентрациях действующего вещества, а также отсутствием побочных эффектов.
| Таблица 1Фармацевтическая композиция на основе пептида, нормализующего мочеиспускание, и способ ее применения | ||||
| Показатели | Контроль | Введение пептида H-Glu-Asp-OH в течение 6 мес | ||
| 1 мкг/кг | 0,1 мг/кг | 1 мг/кг | ||
| Эритроциты, ×1012/л | 5,3±0,4 | 5,2±0,4 | 5,3±0,4 | 5,4±0,6 |
| Гемоглобин, г/л | 14,1±0,5 | 14,3±0,5 | 14,7±0,5 | 14,3±0,9 |
| Ретикулоциты, % | 1,12±0,03 | 1,20±0,06 | 1,15±0,08 | 1,11±0,01 |
| Тромбоциты, ×109/л | 143,2±8,4 | 152,4±7,5 | 147,3±8,5 | 146,5±10,2 |
| Лейкоциты, ×109/л | 9,1±0,4 | 10,1±0,5 | 9,8±0,4 | 9,6±0,4 |
| Нейтрофилы палочкоядерные, % | 0,42±0,03 | 0,34±0,03 | 0,35±0,04 | 0,37±0,08 |
| Нейтрофилы сегментоядерные, % | 45,3±4,9 | 42,4±3,7 | 45,7±3,6 | 46,1±3,9 |
| Эозинофилы, % | 0,82±0,04 | 0,54±0,05 | 0,72±0,07 | 0,68±0,05 |
| Базофилы, % | 0,81±0,03 | 0,63±0,05 | 0,62±0,05 | 0,79±0,06 |
| Моноциты, % | 2,52±0,04 | 1,82±0,03 | 1,94±0,06 | 2,28±0,03 |
| Лимфоциты, % | 46,3±2,5 | 42,8±3,9 | 47,4±2,1 | 49,2±1,9 |
| СОЭ, мм/ч | 2,11±0,03 | 1,93±0,07 | 1,92±0,06 | 2,17±0,01 |
| Резистентность эритроцитов, % NaCl | ||||
| - максимальная | 0,42±0,03 | 0,41±0,05 | 0,43±0,03 | 0,43±0,02 |
| - минимальная | 0,34±0,03 | 0,27±0,03 | 0,32±0,05 | 0,31±0,01 |
| Общий белок в сыворотке, г/л | 72,4±3,9 | 72,5±3,8 | 72,3±3,8 | 72,1±4,2 |
| Натрий в сыворотке, ммоль/л | 152,6±7,6 | 152,1±6,2 | 152,6±7,1 | 152,3±7,5 |
| Калий в сыворотке, ммоль/л | 5,2±2,3 | 5,3±2,7 | 5,2+1,4 | 5,3±1,9 |
| Таблица 2Фармацевтическая композиция на основе пептида, нормализующего мочеиспускание, и способ ее применения | |||
| Показатель | До лечения | После лечения с применением общепринятых средств | После лечения с применением фармацевтической композиции, содержащ |