Модуль половолоконных мембран и способ его изготовления
Иллюстрации
Показать всеИзобретение относится к половолоконным мембранным модулям, которые особенно подходят для использования в очистителях крови, а также к способу их изготовления. Модуль половолоконных мембран включает селективно проницаемые половолоконные мембраны полисульфонового типа, которые в качестве основных компонентов содержат смолу на основе полисульфона и гидрофильный полимер. Содержание гидрофильного полимера в самом верхнем слое внутренней поверхности указанной половолоконной мембраны, по меньшей мере, в 1,1 раза больше, чем его содержание в ближайшем слое внутренней поверхности мембраны. Содержание гидрофильного полимера в самом верхнем слое наружной поверхности мембраны, по меньшей мере, в 1,1 раза больше, чем его содержание в самом верхнем слое внутренней поверхности мембраны. Указанный модуль половолоконных мембран подвергают воздействию радиоактивного излучения при условии, что концентрация кислорода в окружающей атмосфере вокруг указанных половолоконных мембран составляет от 0,001 до 0,1% и что отношение содержания влаги в мембранах к массе составляет от 0,2 до 7 мас.%. Технический результат: получение надежных, безопасных и стабильно функционирующих модулей половолоконных мембран. 2 н. и 25 з.п. ф-лы, 2 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к мембранным половолоконным модулям, включающим селективно-проницаемые половолоконные мембраны полисульфонового типа, которые надежны в плане безопасности и стабильности функционирования, которые можно легко включить в модуль и которые особенно подходят для использования в очистителях крови, а также к способам их изготовления.
Описание предшествующего уровня техники
При очищении крови для терапии почечной недостаточности и т.д., такие модули как гемодиализаторы, гемофильтры и гемодиафильтры, которые включают диализные мембраны или ультрафильтрационные мембраны в качестве сепараторов, широко используются для удаления мочевых токсических веществ и продуктов жизнедеятельности из крови. Диализные мембраны и ультрафильтровочные мембраны в качестве сепараторов изготовлены из натуральных материалов, таких как целлюлоза или ее производные (например, диацетат целлюлозы, триацетат целлюлозы и т.д.), или из синтетических полимеров, таких как полисульфон, полиметилметакрилат, полиакрилонитрил и т.д. Модули, включающие половолоконные мембраны в качестве сепараторов, имеют очень большое значение в области диализаторов, ввиду таких преимуществ, как уменьшение количества экстракорпоральной циркулирующей крови, высокую эффективность удаления нежелательных веществ из крови и высокую производительность изготовления модулей.
Среди перечисленных выше мембранных материалов, смолы на основе полисульфона с высокой проницаемостью для воды привлекли общественное внимание, потому что такие смолы больше всего подходят для современной диализной технологии. Однако полупроницаемые мембраны, изготовленные из одной смолы на основе полисульфона, обладают низким аффинитетом к крови, включая феномены воздухонепроницаемости, поскольку смола на основе полисульфона является гидрофобной. Поэтому такие полупроницаемые мембраны, как таковые, нельзя непосредственно использовать для обработки крови.
Для разрешения этой проблемы предлагается способ придания мембране гидрофильности смешиванием смолы на основе полисульфона с гидрофильным полимером: например, к смоле на основе полисульфона добавляют многоатомный спирт, такой как полиэтиленгликоль или ему подобный (см. патентную ссылку 1 и патентную ссылку 2);
или иначе, к смоле на основе полисульфона добавляют поливинилпирролидон (см. патентную ссылку 3 и патентную ссылку 4).
Эти способы эффективны для разрешения обсужденной выше проблемы. Однако очень важен поиск оптимальных условий методики придания гидрофильности смешиванием гидрофильного полимера, потому что концентрация гидрофильного полимера на внутренней поверхности половолоконной мембраны на контактирующей с кровью стороне и концентрация гидрофильного полимера на ее наружной поверхности оказывают значительное влияние на производительность половолоконной мембраны. Например, совместимость половолоконной мембраны с кровью можно надежно получить увеличением концентрации гидрофильного полимера на внутренней поверхности мембраны, хотя слишком высокая концентрация гидрофильного полимера на внутренней поверхности мембраны увеличивает количество гидрофильного полимера, вымываемого в кровь. Накопление вымываемого гидрофильного полимера в течение длительного периода диализной терапии вызывает нежелательные побочные эффекты или осложнения.
С другой стороны, слишком высокая концентрация гидрофильного полимера на наружной поверхности мембраны нарушает функцию адсорбции эндотоксина и создает возможность инфильтрации эндотоксина в диализат на стороне контакта с кровью. В результате вызываются побочные эффекты, такие как лихорадка и т.д., или гидрофильный полимер на наружных поверхностях половолоконных мембран обеспечивает возможность прилипания таких мембран друг к другу во время сушки мембран, что приводит к новой проблеме, так что включение таких мембран в модуль затрудняется.
Напротив, предпочтительна более низкая концентрация гидрофильного полимера на наружной поверхности половолоконной мембраны, поскольку можно подавить инфильтрацию эндотоксина на стороне контакта с кровью. Однако гидрофильность наружной поверхности половолоконной мембраны снижается, что вызывает проблему, заключающуюся в том, что снижается совместимость наружной поверхности половолоконной мембраны с физиологическим солевым раствором, используемым для смачивания мембраны, когда пучок высушенных половолоконных мембран смачивается и вставляется в модуль. В результате происходит нежелательное снижение эффективности первичного заполнения мембран (удаление воздуха из мембран при их смачивании).
Описан способ разрешения этих проблем (см. патентную ссылку 5): то есть концентрация гидрофильного полимера в плотном слое внутренней поверхности половолоконной мембраны доводится до определенного диапазона, содержание гидрофильного полимера в плотном слое внутренней поверхности мембраны, по меньшей мере, в 1,1 раза больше, чем содержание гидрофильного полимера на наружной поверхности мембраны. В частности, этот способ основан на технической идее увеличения содержания гидрофильного полимера в плотном слое внутренней поверхности мембраны и, посредством этого, улучшения ее совместимости с кровью и уменьшения содержания гидрофильного полимера на наружной поверхности мембраны для подавления, посредством этого, прилипания половолоконных мембран, которое произошло бы при сушке мембран. Эта методика разрешает одну из проблем: то есть подавляется инфильтрация эндотоксина, содержащегося в диализате, на стороне контакта с кровью. Однако еще остается нерешенная проблема того, что имеется тенденция к снижению первичного заполнения мембраны, ввиду очень низкого содержания гидрофильного полимера на наружной поверхности мембраны. Поэтому необходимо разрешить эту проблему.
Описан другой способ разрешения проблемы инфильтрации эндотоксина в диализат, на стороне контакта с кровью (см. патентный источник 6). В этом способе содержание гидрофильных полимеров в ближайшем слое внутренней поверхности, наружной поверхности и в промежуточном слое половолоконной мембраны, имеющих равномерную мембранную структуру, определено таким образом, чтобы подавить инфильтрацию эндотоксина на стороне контакта с кровью. Однако этот способ также не может разрешить проблему снижения первичного заполнения мембраны, как и указанный выше способ. Кроме того, существует еще одна проблема, состоящая в том, что поры более крупного размера наружной поверхности половолоконной мембраны снижают сопротивление мембраны нарастанию потока при повышении давления. Поэтому такая мембрана связана с возможностью разрыва при использовании для гемофильтрации или тому подобного, при которой давление жидкости выше, чем давление, применяемое для обычных способов лечения.
Кроме того, описаны способы повышения совместимости мембран с кровью и уменьшения количества гидрофильных полимеров, вымываемых в кровь, обеспечением определенного содержания гидрофильных полимерам на внутренних поверхностях половолоконных мембран (см. патентные ссылки 7-9).
Однако ни в одной из приведенных выше патентных ссылок не идет речь о содержании гидрофильного полимера, присутствующего на наружной поверхности половолоконной мембраны, и таким образом, ни одно из изобретений указанных выше публикаций не способно уменьшить все проблемы, связанные с содержанием гидрофильного полимера, присутствующего на наружной поверхности половолоконной мембраны.
Из обсужденных выше проблем раскрыт способ решения проблемы инфильтрации эндотоксина на стороне мембраны, контактирующей с кровью (см. патентную ссылку 10). Этот способ разработан с использованием преимущества свойств эндотоксина, который имеет гидрофильную часть в молекуле и который склонен к адсорбции на гидрофобный материал. В частности, в этом способе соотношение между гидрофильным полимером и гидрофобным полимером в наружной мембране половолоконной мембраны доводится до интервала от 5 до 25%. Действительно, этот способ эффективен для подавления инфильтрации эндотоксина в мембрану на стороне, контактирующей с кровью. Однако необходимо удалить гидрофильный полимер в наружной поверхности мембраны промыванием с тем, чтобы придать мембране этот признак. Соответственно, для этого промывания требуется длительное время обработки, что неблагоприятно ввиду увеличения затрат. Например, в примере осуществления изобретения по указанной выше патентной публикации, половолоконную мембрану в течение 1 часа промывают потоком горячей воды при 60°С и в течение 1 часа промывают горячей водой при 110°С.
Этот способ снижения количества гидрофильного полимера на наружной поверхности мембраны эффективен для ингибирования инфильтрации эндотоксина в мембрану на стороне, контактирующей с кровью. Однако гидрофильность наружной поверхности мембраны снижается, что вызывает следующий недостаток: когда пучок половолоконных мембран, высушенных для включения в модуль, снова смачивается, то половолоконные мембраны становятся низко совместимыми с физиологическим солевым раствором для смачивания мембран. Этот способ может вызвать нежелательное плохое первичное заполнение, то есть недостаточное удаление воздуха из мембран на стадии смачивания мембран. Например, описаны способы уменьшения этой проблемы, при которых производится смешивание с гидрофильным соединением, таким как глицерин или ему подобное (см. патентную ссылку 11 и патентную ссылку 12). Однако эти способы связаны с проблемами, заключающимися в том, что гидрофильное соединение ведет себя как инородный материал во время диализа, а также имеет тенденцию к порче под воздействием света или подобных факторов, что оказывает неблагоприятное влияние на устойчивость модуля при хранении, а также в том, что гидрофильное соединение препятствует связыванию клеем для фиксации пучка половолоконных мембран в модуле, когда мембраны вставляются в модуль.
Описаны способы устранения прилипания половолоконных мембран, то есть еще одной проблемы из указанных выше проблем: в любом из этих способов соотношение между площадями пор наружной поверхности мембраны доводится до 25% или более (см. патентную ссылку 6 и патентную ссылку 13). Хотя эти способы действительно эффективны в предотвращении прилипания половолоконных мембран, прочность мембран снижается ввиду более высокого соотношения между площадями пор, что может привести к утечке крови или подобным проблемам.
Кроме того, описан способ определения соотношения между площадями пор и площади пор наружной поверхности мембраны (см. патентную ссылку 14).
Между тем, когда модуль, заполненный половолоконными мембранами, используется в качестве медицинского устройства, необходима его стерилизация. Хотя обычно используются такие способы стерилизации, как стерилизация с использованием газообразного оксида этилена или сжатого пара, недавно стали широко использоваться способы стерилизации путем воздействия радиоактивного излучения, потому что воздействие радиоактивного излучения оказывает высокий стерилизационный эффект и легко обеспечивает возможность стерилизации материала, заключенного в упаковку. Однако стерилизация путем воздействия радиоактивного облучения вызывает разрушение веществ из половолоконных мембран и экранирующих материалов, и вымывание таких разрушенных веществ может вызвать побочные эффекты при клиническом применении. Известна мембрана, заполненная водой, и стерилизованная воздействием гамма-излучения, которая проявляет высокую проницаемость для воды и которая поперечно сшита для ингибирования вымывания из нее гидрофильного полимера. Однако эта мембрана тяжелая ввиду заполняющей ее воды и, таким образом, с ней трудно манипулировать.
Для разрешения этой проблемы описан способ стерилизации воздействием радиоактивного излучения без использования воды (см. патентную ссылку 15). В этом способе на половолоконную мембрану с концентрацией кислорода, установленной в интервале от 0,1 до 3,6%, и содержанием влаги, установленным, по меньшей мере, на 4%, воздействуют радиоактивным излучением. В соответствии с этим способом половолоконная мембрана оценивается как обеспечивающая низкое вымывание и высокую безопасность, когда количество израсходованного водного раствора перманганата калия меньше, чем заданная величина. Однако стерилизация половолоконной мембраны, имеющей относительно высокую концентрацию кислорода от 0,1 до 3,6% путем воздействия радиоактивным излучением, связана с возможностью возбуждения кислородных радикалов под действием радиоактивного излучения с последующим ускорением окислительного разрушения материалов, вызванного возбужденными кислородными радикалами, что частично может привести к низкой устойчивости при хранении.
Патентная ссылка 1: JP-A-61-232860
Патентная ссылка 2: JP-A-58-114702
Патентная ссылка 3: JP-B-5-54373
Патентная ссылка 4: JP-B-6-75667
Патентная ссылка 5: JP-A-6-165926
Патентная ссылка 6: JP-A-2001-38170
Патентная ссылка 7: JP-A-6-296686
Патентная ссылка 8: JP-A-11-309355
Патентная ссылка 9: JP-A-2000-157852
Патентная ссылка 10: JP-A-2000-254222
Патентная ссылка 11: JP-A-2001-190934
Патентная ссылка 12: патент № 3193262
Патентная ссылка 13: JP-A-7-289863
Патентная ссылка 14: JP-A-2000-140589
Патентная ссылка 15: JP-A-2003-245526
Описание изобретения
Целью настоящего изобретения является предоставление модуля половолоконных мембран, который является легким и незамораживаемым, ввиду отсутствия использования заполняющей жидкости, и который включает селективно проницаемые половолоконные мембраны полисульфонового типа, которые надежны в плане безопасности и стабильности функционирования и которые можно легко вставить в модуль, и которые особенно подходят для использования в очистителе крови. Другими целями настоящего изобретения являются предоставление мембранного половолоконного модуля, который не связан с возможностью вымывания веществ в результате разрушения половолоконных мембран, экранирующего материала и т.д. вследствие воздействия радиоактивного излучения, и разработка способа изготовления указанного модуля.
Средства для решения проблем
То есть настоящее изобретение относится к модулю половолоконных мембран, который включает половолоконные мембраны полисульфонового типа, включающие в качестве основных компонентов смолу на основе полисульфона и гидрофильный полимер, и этот модуль отличается тем, что
(А) содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны полисульфонового типа, по меньшей мере, в 1,1 раза больше, чем содержание гидрофильного полимера в ближайшем слое внутренней поверхности мембраны;
(В) содержание гидрофильного полимера в самом верхнем слое наружной поверхности половолоконной мембраны полисульфонового типа, по меньшей мере, в 1,1 раза больше, чем содержание гидрофильного полимера в самом верхнем слое внутренней поверхности мембраны; на контактирующей с кровью стороне; и
(С) половолоконная мембрана, в которой отношение содержания влаги к массе составляет от 0,2 до 7 мас.%, подвергается воздействию радиоактивного излучения в условиях окружающей атмосферы, имеющей концентрацию кислорода от 0,001 до 0,1%.
Настоящее изобретение также относится к способу изготовления половолоконного мембранного модуля, который включает стадию указанного выше радиационного воздействия.
В одном аспекте настоящего изобретения содержание гидрофильного полимера в самом верхнем слое внутренней поверхности мембраны в целом составляет предпочтительно от 5 до 60 мас.%, предпочтительнее, от 10 до 55 мас.%, еще предпочтительнее, от 20 до 40 мас.%. Содержание гидрофильного полимера в ближайшем слое, прилегающем к самому верхнему слою, составляет в целом от примерно 2 до примерно 37 мас.%, оптимально, от примерно 5 до примерно 20 мас.%. Далее, содержание гидрофильного полимера в наружной поверхности половолоконной мембраны составляет от примерно 25 до примерно 50 мас.%. Что достаточно для регулирования содержания гидрофильного полимера в самом верхнем слое наружной поверхности мембраны, которое должно быть, по меньшей мере, в 1,1 раза больше, чем содержание гидрофильного полимера в самом верхнем слое внутренней поверхности мембраны. Содержание гидрофильного полимера в соответствующих слоях, как указано выше, выбрано так, что количество гидрофильного полимера, вымываемого из половолоконной мембраны, может составлять 10 ч/млн или менее.
Эффект изобретения
Половолоконный мембранный модуль по настоящему изобретению высоко надежен в плане безопасности и стабильности его функции и имеет высокую проницаемость для воды, подходящую для терапии хронической почечной недостаточности. Половолоконный мембранный модуль по настоящему изобретению можно использовать в сухом состоянии, и таким образом, он имеет легкий вес и лишен возможности замораживания. Поэтому половолоконным мембранным модулем по настоящему изобретению легко манипулировать, и он подходит для высокоэффективного очистителя крови. Далее, половолоконный мембранный модуль по настоящему изобретению безопасен в качестве медицинского устройства, поскольку можно ингибировать инфильтрацию вымываемых веществ в качестве инородных материалов для организма человека.
Лучшие способы осуществления изобретения
Далее, настоящее изобретение будет объяснено более детально.
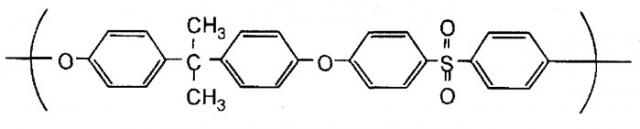
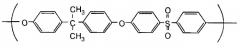
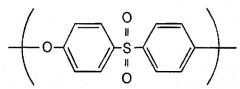
Половолоконный мембранный модуль, подлежащий использованию в настоящем изобретении, включает смолу на основе полисульфона, содержащую гидрофильный полимер. Смола на основе полисульфона, указанная в настоящем изобретении, представляет собой родовой термин смол, имеющих сульфоновые связи. Предпочтительные примеры смолы на основе полисульфона включают, но не ограничиваются, смолы на основе полисульфона и смолы на основе полиэфирсульфона, которые обе имеют повторяющиеся единицы, представленные формулой [I] или [II], и которые можно легко приобрести.
Химическая формула 1
Химическая формула 2
Примеры гидрофильного полимера, упоминаемого в настоящем изобретении, включают материалы, такие как полиэтиленгликоль, поливиниловый спирт, поливинилпирролидон, карбоксиметилцеллюлоза, полипропиленгликоль, глицерин, крахмалы и их производные. Предпочтительно, поливинилпирролидон, имеющий средневесовую молекулярную массу от 10000 до 1500000, используется ввиду безопасности и эффективности затрат. Конкретно, предпочтительно используются поливинилпирролидон, имеющий молекулярную массу 9000 (К17), поливинилпирролидон, имеющий молекулярную массу 45000 (К30), поливинилпирролидон, имеющий молекулярную массу 450000 (К60), поливинилпирролидон, имеющий молекулярную массу 900000 (К80), и поливинилпирролидон, имеющий молекулярную массу 1200000 (К90), которые имеются в продаже от BASF. Каждый из указанных выше гидрофильных полимеров можно использовать отдельно или в комбинации с одним или более из указанных выше полимеров, имеющих различные молекулярные массы, или в комбинации с одной или более из различных смол, в соответствии с предназначенным использованием, или для получения предназначенных свойств или структуры.
В настоящем изобретении (А) содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны, по меньшей мере, в 1,1 раза больше, чем содержание гидрофильного полимера в ближайшем слое внутренней поверхности мембраны, как указано выше. Предпочтительно, содержание гидрофильного полимера в ближайшем слое, прилегающем к самому верхнему слою внутренней поверхности мембраны составляет от примерно 2 до примерно 37 мас.%, для регулировки того, чтобы содержание гидрофильного полимера в самом верхнем слое было больше, чем содержание гидрофильного полимера в ближайшем слое, и для оптимального регулирования содержания гидрофильного полимера в самом верхнем слое, составляющего от 20 до 40 мас.%. По этой причине, практически, должное содержание гидрофильного полимера в ближайшем слое внутренней поверхности мембраны составляет от примерно 5 до примерно 20 мас.%. В деталях, постоянный множитель для различия содержания допускался максимум до 10 или такого порядка величины. Когда постоянный множитель превышает этот предел, диффузия и перенос по гидрофильному полимеру может происходить в обратном направлении от самого верхнего слоя к ближайшему слою на поверхности мембраны, и трудно изготовить половолоконную мембрану, имеющую структуру, допускающую такой постоянный множитель. Действительное содержание гидрофильного полимера в самом верхнем слое внутренней поверхности мембраны можно рассчитать просто умножением величины (от 15 до 20 мас.%) правильного содержания гидрофильного полимера в ближайшем слое внутренней поверхности мембраны на величину постоянного множителя от примерно 1,1 до примерно 10. Посредством этого получают оптимальную величину от 20 до 40 мас.%. Предпочтительно, гидрофильный полимер содержится в самом верхнем слое в таком количестве, которое обычно от примерно 1,1 до примерно 5 раз больше, и, что возможно, оптимально от примерно 1,2 до примерно 3 раз больше, чем содержание гидрофильного полимера в ближайшем слое. Практически, постоянный множитель можно необязательно выбирать с учетом емкости половолоконной мембраны. Например, когда содержание гидрофильного полимера в ближайшем слое поверхности мембраны составляет 5 мас.% в качестве нижнего предела, то содержание гидрофильного полимера в самом верхнем слое на поверхности мембраны составляет приблизительно от 20 до 40 мас.%, что эквивалентно величине, в 4-8 раз больше, чем содержание гидрофильного полимера в указанном выше ближайшем слое.
В настоящем изобретении (В) содержание гидрофильного полимера в самом верхнем слое наружной поверхности половолоконной мембраны полисульфонового типа, по меньшей мере, в 1,1 раза больше, чем содержание гидрофильного полимера в самом верхнем слое внутренней поверхности мембраны, как указано выше. В этом отношении содержание гидрофильного полимера в самом верхнем слое наружной поверхности половолоконной мембраны составляет предпочтительно от примерно 25 до примерно 50 мас.%. Когда содержание гидрофильного полимера в этом слое слишком мало, то содержание белка в крови, адсорбированной в опорный слой половолоконной мембраны, имеет тенденцию к увеличению, и, что нежелательно, имеется тенденция снижения совместимости мембраны с кровью и проницаемости мембраны. Напротив, когда содержание гидрофильного полимера в самом верхнем слое наружной поверхности мембраны слишком велико, то может быть большая возможность инфильтрации эндотоксина в диализат на стороне контакта с кровью, что может вызвать у пациента побочные эффекты, такие как лихорадка и т.д., или может вызвать недостаток, заключающийся в том, что мембраны трудно вставить в модуль ввиду слипания таких половолоконных мембран, вызванного гидрофильным полимером на поверхностях мембран, когда мембраны высушены.
В настоящем изобретении содержание гидрофильного полимера в смоле на основе полисульфона определенно не ограничено, и его можно необязательно выбрать, пока половолоконной мембране могут быть приданы достаточная гидрофильность и высокая смачиваемость. Пропорция гидрофильного полимера составляет предпочтительно от 1 до 20 мас.%, предпочтительнее, от 3 до 15 мас.%, относительно к 80-99 мас.% смолы на основе полисульфона. Когда пропорция гидрофильного полимера слишком низкая, эффект придания гидрофильности может быть недостаточным. С другой стороны, когда пропорция гидрофильного полимера слишком высокая, эффект придания гидрофильности вызывает насыщение мембраны, и количество гидрофильного полимера, вымываемого из мембраны, увеличивается и может превышать 10 ч/млн, как будет описано ниже.
Как указано выше, один из признаков настоящего изобретения заключается в том, что (С) концентрация кислорода в окружающей атмосфере вокруг половолоконной мембраны составляет от 0,001 до 0,1%, и в том, что половолоконная мембрана, содержание влаги в которой к ее массе доведено до 0,2-7 мас.%, подвергается воздействию радиоактивного излучения. Предпочтительно, воздействие облучения проводят на модуль половолоконных мембран, обернутой в упаковку. Однако модуль половолоконных мембран может быть подвергнут радиоактивному облучению, и его можно затем завернуть в упаковку.
Воздействие радиоактивного излучения эквивалентно стерилизации, которая представляет собой обязательный процесс для изготовления медицинских устройств, а также эквивалентно переводу в нерастворимую форму гидрофильного полимера путем поперечной сшивки, в качестве одного из предпочтительных способов осуществления настоящего изобретения. Когда воздействие облучения осуществляется в атмосфере, содержащей кислород, кислородные радикалы имеют тенденцию оказывать и увеличивать эффект стерилизации. Однако кислородные радикалы атакуют полимерный материал и могут ускоренно окислить и разрушить полимерный материал. Когда концентрация кислорода в окружающей атмосфере составляет менее 0,001%, то эффект стерилизации становится недостаточным. Когда эта концентрация превышает 0,1%, то имеется тенденция продолжения окисления и разрушения полимерного материала. Когда содержание влаги в половолоконной мембране составляет менее 0,2 мас.%, то становится трудным осуществление поперечной сшивки гидрофильного полимера, и количество вымываемых веществ увеличивается. Когда содержание влаги в мембране превышает 7 мас.%, то масса модуля половолоконных мембран увеличивается; модуль половолоконных мембран становится влажным, что обеспечивает возможность пролиферации бактерий; или экранирующий агент взаимодействует с водой для вспенивания экранирующего агента или для увеличения количества вымываемых веществ.
Описанные выше предпочтительные способы осуществления настоящего изобретения будут более детально описаны на основании технических признаков. То есть в предпочтительных вариантах настоящего изобретения можно получить селективно проницаемую половолоконную мембрану полисульфонового типа, которая содержит гидрофильный полимер и которая одновременно удовлетворяет следующим признакам:
(1) количество гидрофильного полимера, вымываемого из половолоконной мембраны, составляет 10 ч/млн или менее;
(2) содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны полисульфонового типа составляет от 20 до 40 мас.%;
(3) содержание гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны полисульфонового типа составляет от 5 до 20 мас.%; и
(4) содержание гидрофильного полимера в самом верхнем слое наружной поверхности половолоконной мембраны полисульфонового типа составляет от 25 до 50 мас.%, и, по меньшей мере, в 1,1 рза больше, чем содержание гидрофильного полимера в самом верхнем слое внутренней поверхности мембраны.
В настоящем изобретении количество гидрофильного полимера, вымываемого из половолоконной мембране, составляет предпочтительно 10 ч/млн или менее (признак 1). Когда это количество превышает 10 ч/млн, то имеется возможность возникновения побочных эффектов или осложнений вследствие вымываемого гидрофильного полимера в течение длительного периода диализной терапии. Для получения этого признака, например, отношение количества гидрофильного полимера к гидрофобному полимеру в соответствующих слоях регулируется в указанных выше диапазонах, или, иначе, оптимизируются условия изготовления половолоконной мембраны.
В настоящем изобретении, как указано выше, содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны полисульфонового типа составляет предпочтительно от 20 до 40 мас.% (признак 2). Содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны полисульфонового типа можно необязательно выбрать в пределах широкого диапазона от 5 до 60 мас.%, например, от 10 до 50 мас.%. Для преимущественного получения эффекта настоящего изобретения, предпочтительно, самый верхний слой внутренней поверхности половолоконной мембраны включает от 60 до 80 мас.% смолы на основе полисульфона и от 20 до 40 мас.% гидрофильного полимера в качестве основных компонентов. Когда содержание гидрофильного полимера составляет менее 20 мас.%, гидрофильность поверхности половолоконного материала на стороне, контактирующей с кровью, становится ниже, что ведет к плохой совместимости мембраны с кровью, приводя к вероятному свертыванию крови на поверхности половолоконной мембраны. Свернувшийся тромб закупоривает половолоконную мембрану и в последующем нарушает сепарационную способность половолоконной мембраны или увеличивает количество крови, остающейся в ней после проведения гемодиализа. Содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны составляет предпочтительно 21 мас.% или более, предпочтительнее, 22 мас.% или более, еще предпочтительнее, 23 мас.% или более. С другой стороны, когда это содержание превышает 40 мас.%, то количество гидрофильного полимера, вымываемого в кровь, увеличивается, и такой вымываемый гидрофильный полимер имеет возможность оказания побочных эффектов или осложнение в течение длительного периода гемодиализной терапии. Поэтому содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны составляет предпочтительно 39 мас.% или менее, предпочтительнее, 38 мас.% или менее, еще предпочтитлеьнее, 37 мас.% или менее.
В настоящем изобретении, как указано выше, содержание гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны полисульфонового типа составляет предпочтительно от 5 до 20 мас.% (признак 3). Ближайший слой внутренней поверхности половолоконной мембраны полисульфонового типа включает от 60 до 99 мас.% смолы на основе полисульфона и от 1 до 40 мас.% гидрофильного полимера в качестве основных компонентов, которые можно необязательно выбрать соответственно в указанных выше диапазонах. Содержание гидрофильного полимера составляет предпочтительно от 5 до 20 мас.%, а в целом, предпочтительнее, от 7 до 18 мас.%. Содержание гидрофильного полимера в самом верхнем слое внутренней поверхности половолоконной мембраны полисульфонового типа предпочтительно больше, ввиду совместимости с кровью, как указано выше. Однако противоречие состоит в том, что увеличение содержания гидрофильного полимера ведет к увеличению количества гидрофильного полимера, вымываемого в кровь. Поэтому содержание гидрофильного полимера составляет от примерно 20 до примерно 40 мас.%, которое выбрано с учетом его соответствующего диапазона.
Содержание гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны может быть выбрано в относительно широком диапазоне от 1 до 40 мас.%. Однако имеется недостаток, когда содержание гидрофильного полимера в ближайшем слое больше, чем содержание гидрофильного полимера в самом верхнем слое (например, когда содержание гидрофильного полимера в самом верхнем слое составляет 30 мас.%, его содержание в ближайшем слое составляет 35 мас.%): то есть ускоряется диффузия и перенос гидрофильного полимера от ближайшего слоя к самому верхнему слою внутренней поверхности мембраны, что приводит к нежелательному эффекту увеличения содержания гидрофильного полимера в самом верхнем слое до значения, превышающего заданную величину. Подводя итог, с учетом механизма, посредством которого гидрофильный полимер переносится в самый верхний слой количеством гидрофильного полимера, потребляемого в самом верхнем слое, посредством диффузии и переноса гидрофильного полимера, содержание гидрофильного полимера в ближайшем слое поверхности мембраны относительно меньше, чем его количество в самом верхнем слое, и составляет, предпочтительно, например, 19 мас.% или менее, предпочтительнее, 18 мас.% или менее. Когда содержание гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны слишком маленькое, невозможно перенести гидрофильный полимер от ближайшего слоя к самому верхнему слою, что может снизить стабильность удаляющей растворенные вещества способности или совместимости с кровью половолоконной мембраны. Поэтому оптимальное содержание гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны предпочтительнее 6 мас.% или более, еще предпочтительнее, 7 мас.% или более. В целом, содержание гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны несколько больше, чем содержание гидрофильного полимера в основных компонентах, то есть от 80 до 99 мас.% полимера на основе полисульфона и от 1 до 20 мас.% гидрофильного полимера, которые составляют половолоконную мембрану по настоящему изобретению.
Этот признак 3 представляет собой один из факторов, которые обеспечивают возможность преодоления указанного выше противоречия и оптимизации этого явления на более высоком уровне, чем это делала любая из обычных методик. Другими словами, содержание гидрофильного полимера в самом верхнем слое половолоконной мембраны, которое преимущественно воздействует на совместимость мембраны с кровью, устанавливается на самый низкий уровень, который достаточен для обеспечения возможности проявления совместимости с кровью. Однако возникает другая проблема, состоящая в том, что, хотя это содержание гидрофильного полимера в самом верхнем слое может обеспечить возможность проявления первоначальной совместимости с кровью, гидрофильный полимер в самом верхнем слое понемногу вымывается в кровь в течение длительного периода гемодиализа, что постепенно снижает совместимость с кровью в течение длительного периода гемодиализа. Сохранение совместимости с кровью половолоконной мембраны полисульфонового типа улучшается определением содержания гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны. Путем определения содержания гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны можно разрешить указанную выше проблему, которая состоит в уменьшении содержания гидрофильного полимера в самом верхнем слое вследствие вымывания гидрофильного полимера самого верхнего слоя в кровь в связи с продолжением гемодиализа и затянувшегося нарушения совместимости с кровью мембраны, вызываемой указанным выше уменьшением сохранения совместимости с кровью. Этот способ осуществляется на основании технической идеи, заключающейся в том, что перенос гидрофильного полимера в ближайший слой поверхности половолоконной мембраны в самый верхний ее слой может компенсировать снижение содержания гидрофильного полимера в самом верхнем слое. Соответственно, менее 5 мас.% содержания гидрофильного полимера в ближайшем слое внутренней поверхности половолоконной мембраны может быть, возможно, недостаточным для подавления нарушения консистенции совместимости с кровью половолоконной мембраны. С другой стороны, когда содержание гидрофильного полимера в ближайшем слое поверхности половолоконной мембраны на стороне контакта с кровью превышает 20 мас.%, то количество гидрофильного полимера, вымываемого в кровь, имеет тенденцию к увеличению, что, вероятно, может вызвать побочные эффекты или осложнения в течение длительного периода гемодиализной терапии. До настоящего времени ближайший слой поверхности половолоконной мембраны точное содержание гидрофильного полимера в ближайшем слое и диспергирующее состояние гидрофильного полимера, связанное с его структурой, не было выяснено, и настоящее изобретение впервые выяснило эти вопросы на основании его новых данных.
В настоящем изобретении, как указано выше, содержание гидрофильного полимера в самом верхнем слое наружной поверхности половолоконной мембраны полисул