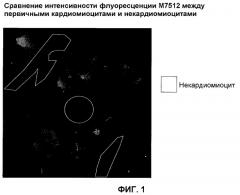
Способ отбора кардиомиоцитов с использованием внутриклеточных митохондрий в качестве индикатора
Иллюстрации
Показать всеИзобретение относится к медицине, в частности к способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов, к способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов, к способу увеличения содержания кардиомиоцитов в содержащей кардиомиоциты смеси клеток без генетического изменения, к способу получения кардиомиоцитов без генетического изменения кардиомиоцитов, к способу оценки содержания кардиомиоцитов в содержащей кардиомиоциты смеси клеток. Вышеописанные способы позволяют эффективно отобрать кардиомиоциты из содержащей кардиомиоциты смеси клеток без их генетического изменения. 4 н. и 16 з.п. ф-лы, 16 ил.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к способу отбора кардиомиоцитов из клеточной популяции, полученной из целого сердца или из популяции стволовых клеток, и способу их применения.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Поскольку кардиомиоцит теряет способность к пролиферации во взрослом организме, то при лечении тяжелых заболеваниях сердца, таких как инфаркт миокарда или кардиомиопатия, необходимо проводить трансплантацию сердца. Однако в настоящее время, поскольку доступно недостаточное количество донорских сердец, существует настоятельная необходимость в разработке способа лечения, отличного от трансплантации сердца. С другой стороны, ожидается, что привлечение продуцируемых ex vivo кардиомиоцитов окажется наиболее перспективным способом оказания помощи пациентам, которым необходима трансплантация сердца.
Разработаны различные способы получения кардиомиоцитов, такие как способ с использованием дифференцированных эмбриональных стволовых клеток, способ стимуляции и дифференцировки стволовых клеток (соматических стволовых клеток), выделенных из живого организма, которые, как полагают, находятся в организме, и так далее. Однако в данной области проблема состоит в том, что характерной особенностью стволовой клетки является то, что в процессе дифференцировки/стимуляции из стволовой клетки в качестве побочного продукта всегда развиваются клетки, отличные от кардиомиоцитов, и что недифференцированная стволовая клетка всегда сохраняется даже после процесса дифференцировки/стимуляции. Таким образом, в данной области полагают, что дифференцированную/индуцированную клеточную популяцию саму по себе нельзя применять в способе лечения. Таким образом, необходимо отбирать кардиомиоциты из дифференцированной/стимулированной клеточной популяции в целях успешного достижения трансплантации в сердце человека.
К настоящему времени в данной области не было сообщений об эффективном способе очистки кардиомиоцитов, кроме способа очистки кардиомиоцитов предварительным встраиванием маркерного гена в геном стволовой клетки (FASEB J., 2000, 14: 2540-2548). Однако поскольку изменение генома включает существенные этические проблемы и приводит к непредсказуемому серьезному риску, включая изменения скорости злокачественных изменений, то изменение генома для использования на практике у человека остается под вопросом.
В данной области известно, что потребность миокарда в кислороде относительно более высокая, чем потребность основных тканей, отличных от сердечной, и что содержание митохондрий в миокарде также относительно более высокое, чем содержание в других тканях (Am. J. Physiol., 1985, 248: R415-421). Кроме того, в данной области хорошо известно, что кардиомиоцит в значительной степени теряет способность к митозу после дифференцировки и созревания клетки. Однако ранее не было известно, что специалисты в данной области предпринимали попытку отбирать кардиомиоциты, используя описанные выше свойства кардиомиоцитов. Кроме того, не было сообщений о непосредственном сравнении трансмембранного потенциала митохондрий кардиомиоцита с трансмембранным потенциалом митохондрий других типов клеток, о сосредоточении внимания на трансмембранном потенциале митохондрий и об отборе кардиомиоцитов с использованием трансмембранного потенциала митохондрий в качестве индикатора кардиомиоцитов.
[непатентный документ 1] FASEB J., 2000, 14: 2540-2548
[непатентный документ 2] Am. J. Physiol., 1985, 248: R415 421
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ЗАДАЧА, РЕШАЕМАЯ ИЗОБРЕТЕНИЕМ
Авторы настоящего изобретения стремились решить задачу разработки способа отбора кардиомиоцитов без генетических изменений из смеси клеток, полученной из целого сердца, и из клеточной смеси, полученной из клеток, способных дифференцироваться в кардиомиоциты с использованием различных типов свойств кардиомиоцитов, напрямую не связанных с отбором кардиомиоцитов.
СПОСОБЫ РЕШЕНИЯ ЗАДАЧИ
Авторы настоящего изобретения успешно решили описанную выше задачу, основываясь на открытиях, что кардиомиоцит содержит относительно более высокое количество митохондрий, чем любой другой тип клеток, и что митохондрии кардиомиоцита обладают относительно более высоким трансмембранным потенциалом, чем любой другой тип клеток. Основываясь на этих открытиях, авторы настоящего изобретения разработали новый способ отбора кардиомиоцитов без генетического изменения кардиомиоцитов, который включает следующие стадии: стадию мечения клеточной смеси, содержащей кардиомиоциты, с использованием специфичного для митохондрий реагента для мечения и стадию измерения относительного содержания митохондрий в клетках и/или трансмембранного потенциала митохондрий.
Конкретно, в первом варианте осуществления настоящее изобретение относится к способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов, на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
Таким образом, в первом варианте осуществления настоящее изобретение относится к
способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов на основе относительного содержания митохондрий в клетках;
способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов на основе также относительного трансмембранного потенциала митохондрий клеток; или
способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов на основе относительного содержания митохондрий в клетках и трансмембранного потенциала.
Этот вариант осуществления способа по настоящему изобретению характеризуется стадиями мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором и измерения относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
В контексте этого изобретения содержащая кардиомиоциты смесь клеток может представлять собой смесь клеток, полученную из целого сердца, или клеточную смесь, полученную из клеток, способных дифференцироваться в кардиомиоцит.
Кроме того, клетка, обладающая способностью дифференцироваться в кардиомиоцит, может быть выбрана из группы, состоящей из стволовой клетки, клетки-предшественника и яйцеклетки.
В этом варианте осуществления после стадии мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором и перед стадией измерения относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток способ по настоящему изобретению может дополнительно включать стадию культивирования меченых клеток в отсутствии митохондриального индикатора.
Более того, митохондриальный индикатор, используемый в этом варианте осуществления настоящего изобретения, может быть выбран из группы, состоящей из A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R648, R14060, R22420, T639, T668, T669 и T3168. В этом варианте осуществления M7512, T3168, T668 или R302 являются предпочтительными в качестве митохондриального индикатора.
Во втором варианте осуществления настоящее изобретение относится к способу увеличения содержания кардиомиоцитов в содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов, где указанный способ включает следующие стадии:
(1) стадию мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором; и
(2) стадию отбора кардиомиоцитов на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клетки.
В контексте второго варианта осуществления настоящего изобретения содержащая кардиомиоциты смесь клеток может представлять собой смесь клеток, полученную из целого сердца, или смесь клеток, полученную из клеток обладающих способностью дифференцироваться в кардиомиоциты.
Кроме того, клетка, обладающая способностью дифференцироваться в кардиомиоцит, может быть выбрана из группы, состоящей из стволовой клетки, клетки-предшественника и яйцеклетки.
Во втором варианте осуществления после стадии (1) и перед стадией (2) способ по настоящему изобретению может дополнительно включать стадию культивирования меченых клеток в отсутствии митохондриального индикатора.
Более того, митохондриальный индикатор, используемый в этом варианте осуществления настоящего изобретения, может быть выбран из группы, состоящей из A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R648, R14060, R22420, T639, T668, T669 и T3168. В этом варианте осуществления M7512, T3168, T668 или R302 являются предпочтительными в качестве митохондриального индикатора.
В третьем варианте осуществления настоящее изобретение относится к способу получения кардиомиоцитов без генетического изменения кардиомиоцитов, где указанный способ включает следующие стадии:
(1) стадию дифференцировки и стимуляции образования кардиомиоцитов из клетки, обладающей способностью дифференцироваться в кардиомиоцит с получением содержащей кардиомиоциты смеси клеток;
(2) стадию мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором; и
(3) стадию отбора кардиомиоцитов на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
В контексте третьего варианта осуществления настоящего изобретения клетка, обладающая способностью дифференцироваться в кардиомиоцит, может быть выбрана из группы, состоящей из стволовой клетки, клетки-предшественника и яйцеклетки.
Кроме того, после стадии (2) и перед стадией (3) способ по настоящему изобретению может дополнительно включать стадию культивирования меченых клеток в отсутствии митохондриального индикатора.
Более того, митохондриальный индикатор, используемый в этом варианте осуществления настоящего изобретения, может быть выбран из группы, состоящей из A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R648, R14060, R22420, T639, T668, T669 и T3168. В этом варианте осуществления настоящего изобретения M7512, T3168, T668 или R302 являются предпочтительными в качестве митохондриального индикатора.
В четвертом варианте осуществления настоящее изобретение относится к способу оценки содержания кардиомиоцитов в содержащей кардиомиоциты смеси клеток, где указанный способ включает следующие стадии:
(1) стадию мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором; и
(2) стадию измерения соотношения кардиомиоцитов и некардиомиоцитов на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
В контексте четвертого варианта осуществления содержащая кардиомиоциты смесь клеток может представлять собой смесь дифференцированных клеток, которая получена из смеси клеток, полученной из целого сердца, или из клеток, обладающих способностью дифференцироваться в кардиомиоциты.
Кроме того, клетка, обладающая способностью дифференцироваться в кардиомиоцит, может быть выбрана из группы, состоящей из стволовой клетки, клетки-предшественника и яйцеклетки.
Более того, митохондриальный индикатор, используемый в этом варианте осуществления настоящего изобретения, может быть выбран из группы, состоящей из A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R648, R14060, R22420, T639, T668, T669 и T3168. В этом варианте осуществления M7512, T3168, T668 или R302 являются предпочтительными в качестве митохондриального индикатора.
Как указано выше, в одном варианте осуществления настоящее изобретение относится к способу отбора кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
Относительное содержание митохондрий в клетках и/или относительный трансмембранный потенциал митохондрий клеток можно измерять мечением содержащей кардиомиоциты смеси клеток митохондриальным индикатором.
Как используется здесь, термин "содержащая кардиомиоциты смесь клеток" означает смесь клеток любых типов, состоящую из кардиомиоцитов и других типов клеток. Например, "содержащая кардиомиоциты смесь клеток" включает, но не ограничивается ими, смесь клеток, полученную из целого сердца, или смесь клеток, полученную из клеток, обладающих способностью дифференцироваться в кардиомиоцит. Как используется здесь, термин "смесь клеток, полученная из целого сердца" означает смесь клеток, состоящую из кардиомиоцитов, эндотелиальных клеток, клеток стромы, гладкомышечных клеток и т.д., которая получена ферментативной обработкой гомогенной или гетерогенной сердечной ткани (сердца) с использованием различных ферментов. Кроме того, как используется здесь, термин "смесь клеток, полученная из клетки, обладающей способностью дифференцироваться в кардиомиоцит," означает смесь клеток, состоящую из кардиомиоцитов, некардиомиоцитов, недифференцированных клеток, нейрональных клеток и эпителиальных клеток, которую получают культивированием клеток, обладающих способностью дифференцироваться в кардиомиоциты (например, стволовых клеток, таких как эмбриональные стволовые клетки и соматические стволовые клетки, клетки-предшественники и яйцеклетки, такие как оплодотворенные яйцеклетки и клоны соматических клеток), в условиях стимуляции дифференцировки клеток из клеток, обладающих способностью дифференцироваться в кардиомиоциты.
Содержание митохондрий в клетках и трансмембранный потенциал митохондрий могут быть количественно определены с помощью мечения внутриклеточных митохондрий митохондриальным индикатором. Однако абсолютное значение для полученного посредством митохондриального индикатора сигнала, который отражает содержание митохондрий и трансмембранный потенциал митохондрий, варьирует в зависимости от стадии созревания кардиомиоцита, подвергающегося анализу, и условий воздействия метки, таких как тип метки и время воздействия метки. Таким образом, важным признаком настоящего изобретения является не абсолютное значение полученного с помощью митохондриального индикатора сигнала, а соотношение между количеством полученного посредством митохондриального индикатора сигнала для кардиомиоцитов и сигнала для некардиомиоцитов. В соответствии с настоящим изобретением можно отбирать клетки, проявляющие относительно более высокую интенсивность флуоресценции, такие как кардиомиоциты. Во-первых, на основе предварительного эксперимента с использованием образца содержащей кардиомиоциты смеси клеток, которая по существу может использоваться в соответствии с настоящим изобретением, определение желательной популяции кардиомиоцитов (т.е. соотношения между содержанием митохондрий и/или степенью трансмембранного потенциала митохондрий кардиомиоцита) проводят должным образом в соответствии с целями этого изобретения. Конкретно, в предварительном эксперименте на основе значений содержания митохондрий и/или степени трансмембранного потенциала митохондрий, используемых в качестве индикаторов, величину полученного посредством митохондриального индикатора сигнала клеток, предназначенных для отбора, классифицируют на несколько групп. Клетки, для которых показано относительно более высокое содержание внутриклеточных митохондрий, и клетки, для которых показан относительно более высокий трансмембранный потенциал митохондрий, должны быть отобраны на основе значений содержания митохондрий и/или степени трансмембранного потенциала митохондрий, используемых в качестве индикаторов.
В соответствии с настоящим изобретением термин "митохондриальный индикатор" означает, но не ограничивается этим, вещество, такое как вещество, которое может специфично метить митохондрии в живой клетке и может отображать содержание митохондрий, вещество, которое может специфично метить митохондрии в живой клетке и может отображать трансмембранный потенциал митохондрий, или вещество, которое может специфично метить митохондрии в живой клетке и может отображать как содержание митохондрий, так и трансмембранный потенциал митохондрий. Например, "митохондриальный индикатор" включает, но не ограничивается ими, (1) вещество, обладающее свойством вызывать флуоресцентное излучение и обладающее способностью связывать структурные компоненты митохондрий (например, белок, липид, цепь сахара, нуклеиновую кислоту или их метаболит и т.д.); (2) вещество, обладающее свойством вызывать флуоресцентное излучение и встраиваться в митохондрии под действием трансмембранного потенциала митохондрий; (3) вещество, которое превращено в форму вещества, обладающего свойством вызывать флуоресцентное излучение под действием структурных компонентов митохондрий; или (4) вещество, которое теряет способность диффундировать из митохондрий наружу под действием структурных компонентов митохондрий.
В соответствии с настоящим изобретением в качестве иллюстративного митохондриального индикатора может использоваться митохондриальный индикатор, такой как, но не ограничиваясь ими, A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R648, R14060, R22420, S7563, T639, T668, T669 или T3168 (номера продуктов для соединений: все доступны в Molecular Probes); более предпочтительно M7514, M7510, M7511, M7512, M7513, M22425, M22426, T668, R302 или T3168; наиболее предпочтительно T668, R302, M7514 или T3168. Химические структуры описанных выше митохондриальных индикаторов, используемых в соответствии с настоящим изобретением, представлены ниже:
[Chem 1]
Структура A1372
Молекулярная формула: C26H38BrN3
Молекулярная масса: 472,51
Номер CAS: 75168-11-5
Название: Акридиний, 3,6-бис(диметиламино)-10-нонил-, бромид
[Chem 2]
Структура D273
Молекулярная формула: C29H37IN2O2
Молекулярная масса: 572,53
Номер CAS: 53213-82-4
Название: бензоксазолий, 3-гексил-2-(3-(3-гексил-2(3H)-бензоксазолиден)-1-пропенил)-, иодид
[Chem 3]
Структура D288
Молекулярная формула: C16H19IN2
Молекулярная масса: 366,24
Номер CAS: 959-81-9
Название: пиридиний, 4-(2-(4-(диметиламино)фенил)этенил)-1-метил, иодид
[Chem 4]
Структура D308
Молекулярная формула: C16H19IN2
Молекулярная масса: 366,24
Номер CAS: 2156-29-8
Название: пиридиний, 2-(2-(4-(диметиламино)фенил)этенил)-1-метил, иодид
[Chem 5]
Структура D378
Молекулярная формула: C31H41N2O2I
Молекулярная масса: 600,58
Номер CAS: нет сведений
Название: нет сведений
[Chem 6]
Структура D426
Молекулярная формула: C17H21IN2
Молекулярная масса: 380,27
Номер CAS: 3785-01-1
Название: пиридиний, 2-(2-(4-диметиламино)фенил)этенил)-1-этил, иодид
[Chem 7]
Структура D632
Молекулярная формула: C21H18N2O3
Молекулярная масса: 346,38
Номер CAS: 109244-58-8
Название: бензойная кислота, 2-(3,6-диамино-9H-ксантен-9-ил)-, метиловый эфир
[Chem 8]
Структура D633
Молекулярная формула: C28H32N2O3
Молекулярная масса: 444,57
Номер CAS: нет сведений
Название: нет сведений
[Chem 9]
Структура D22421
Молекулярная формула: C27H21IN2O3
Молекулярная масса: 532,38
Номер CAS: нет сведений
Название: нет сведений
[Chem 10]
Структура D23806
ИНГРЕДИЕНТ A: дигидрородамин 123
Молекулярная формула: C21H18N2O3
Молекулярная масса: 346,38
Номер CAS: 109244-58-8
Название: бензойная кислота, 2-(3,6-диамино-9H-ксантен-9-ил)-, метиловый эфир
[Chem 11]
Структура L6868
Молекулярная формула: C28H22N4O6
Молекулярная масса: 510,50
Номер CAS: 22103-92-0
Название: 9,9'-биакридиний, 10,10'-диметил-
[Chem 12]
Структура M7502
Молекулярная формула: C34H30Cl3N3O
Молекулярная масса: 602,99
Номер CAS: нет сведений
Название: нет сведений
[Chem 13]
Структура M7510
Молекулярная формула: C24H24Cl2N2O
Молекулярная масса: 427,37
Номер CAS: нет сведений
Название: нет сведений
[Chem 14]
Структура M7511
Молекулярная формула: C24H25ClN2O
Молекулярная масса: 392,93
Номер CAS: нет сведений
Название: нет сведений
[Chem 15]
Структура M7512
Молекулярная формула: C32H32Cl2N2O
Молекулярная масса: 531,52
Номер CAS: 167095-09-2
Название: 1H,5H,11H,15H-ксантено-[2,3,4-ij:5,6,7-i'j']-дихинолизин-18-ий, 9-[4-(хлорметил)фенил]-2,3,6,7,12,13,16,17-октагидро-, хлорид
[Chem 16]
Структура M7513
Молекулярная формула: C32H33ClN2O
Молекулярная масса: 497,08
Номер CAS: 167095-08-1
Название: 1H,5H,9H,11H,15H-ксантено-[2,3,4-ij:5,6,7-i'j']-дихинолизин, 9-[4-(хлорметил)фенил]-2,3,6,7,12,13,16,17-октагидро-
[Chem 17]
Структура M7514
Молекулярная формула: C34H28Cl5N3O
Молекулярная масса: 671,88
Номер CAS: 201860-17-5
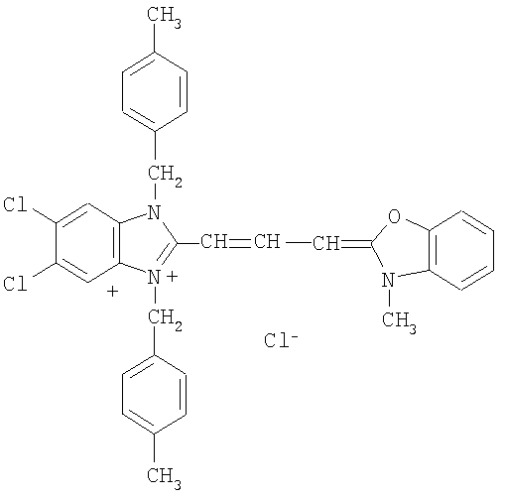
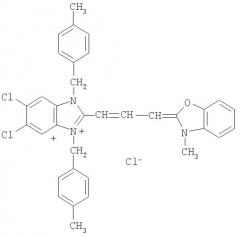
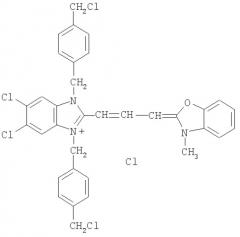
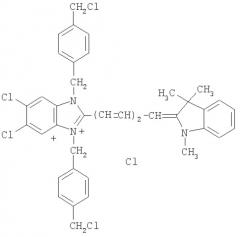
Название: бензоксазолий, 2-[3-[5,6-дихлор-1,3-бис[[4-(хлорметил)фенил]метил]-1,3-дигидро-2H-бензимидазол-2-илиден]-1-пропенил]-3-метил-, хлорид
[Chem 18]
Структура M22422
Молекулярная формула: C35H33ClF6N2O
Молекулярная масса: 647,10
Номер CAS: нет сведений
Название: нет сведений
[Chem 19]
Структура M22423
Молекулярная формула: C26H26ClN3O5
Молекулярная масса: 495,96
Номер CAS: 137993-41-0
Название: 1H,5H,11H,15H-ксантено[2,3,4-ij:5,6,7-i'j']-дихинолизин-18-ий, 9-циано-2,3,6,7,12,13,16,17-октагидро-, перхлорат
[Chem 20]
Структура M22425
Молекулярная формула: C39H36Cl5N3
Молекулярная масса: 724,00
Номер CAS: нет сведений
Название: нет сведений
[Chem 21]
Структура M22426
Молекулярная формула: C34H36Cl2N2
Молекулярная масса: 543,58
Номер CAS: нет сведений
Название: нет сведений
[Chem 22]
Структура R302
Молекулярная формула: C21H17ClN2O3
Молекулярная масса: 380,83
Номер CAS: 62669-70-9
Название: ксантилий, 3,6-диамино-9-(2-(метоксикарбонил)фенил, хлорид
[Chem 23]
Структура R634
Молекулярная формула: C28H31ClN2O3
Молекулярная масса: 479,02
Номер CAS: 989-38-8
Название: ксантилий, 9-(2-(этоксикарбонил)фенил)-3,6-бис(этиламино)-2,7-диметил, хлорид
[Chem 24]
Структура R648
Молекулярная формула: C34H43ClN2O7
Молекулярная масса: 627,18
Номер CAS: нет сведений
Название: нет сведений
[Chem 25]
Структура R14060
Молекулярная формула: C23H19F5N2O
Молекулярная масса: 434,41
Номер CAS: нет сведений
Название: нет сведений
[Chem 26]
Структура R22420
Молекулярная формула: C21H17ClN2O3
Молекулярная масса: 380,83
Номер CAS: 62669-70-9
Название: ксантилий, 3,6-диамино-9-(2-(метоксикарбонил)фенил, хлорид
[Chem 27]
Структура T639
Молекулярная формула: C23H23N2OCl
Молекулярная масса: 378,90
Номер CAS: 6837-70-3
Название: ксантилий, 3,6-бис(диметиламино)-9-фенил, хлорид
[Chem 28]
Структура T668
Молекулярная формула: C25H25ClN2O7
Молекулярная масса: 500,93
Номер CAS: 115532-50-8
Название: ксантилий, 3,6-бис(диметиламино)-9-(2-(метоксикарбонил)фенил)-, перхлорат
[Chem 29]
Структура T669
Молекулярная формула: C26H27ClN2O7
Молекулярная масса: 514,96
Номер CAS: 115532-52-0
Название: ксантилий, 3,6-бис(диметиламино)-9-[2-(этоксикарбонил)фенил]-, перхлорат
[Chem 30]
Структура T3168
Молекулярная формула: C25H27Cl4IN4
Молекулярная масса: 652,23
Номер CAS: 47729-63-5
Название: 1H-бензимидазолий, 5,6-дихлор-2-[3-(5,6-дихлор-1,3-диэтил-1,3-дигидро-2H-бензимидазол-2-илиден)-1-пропенил]-1,3-диэтил-, иодид, (E)-
Кроме того, в качестве митохондриального индикатора также могут использоваться S7563, S7567 и S7585 (номера продуктов для соединений: все доступны в Molecular Probes).
В данной области известно, что каждый митохондриальный индикатор обладает определенной длиной волны возбуждения и вызывает флуоресцентное излучение определенной длины волны. Например, M7514 вызывает флуоресцентное излучение 516 нм, испускаемое при длине волны возбуждения 490 нм, и T3168 вызывает флуоресцентное излучение 590 нм, испускаемое при длине волны возбуждения 535 нм.
Как описано выше, кардиомиоцит проявляет более высокую интенсивность флуоресценции, чем другие типы клеток при мечении содержащей кардиомиоциты смеси клеток митохондриальным индикатором, поскольку кардиомиоцит обладает относительно более высоким содержанием внутриклеточных митохондрий и обладает относительно более высоким трансмембранным потенциалом митохондрий, чем другие типы клеток. Во-первых, в соответствии с настоящим изобретением содержание внутриклеточных митохондрий и/или трансмембранный потенциал митохондрий измеряют для каждой клетки, находящейся в меченой смеси клеток, содержащей кардиомиоциты. Далее, клетки, для которых была показана более высокая интенсивность флуоресценции, определяют как кардиомиоциты. На основе измеренного содержания митохондрий и/или трансмембранного потенциала митохондрий кардиомиоциты выделяют в соответствии со следующим: клеточная популяция, обладающая относительно высоким содержанием митохондрий; клеточная популяция, содержащая митохондрии с относительно высоким трансмембранным потенциалом; или клеточная популяция, состоящая из клеток, обладающих относительно высоким содержанием митохондрий и относительно высоким трансмембранным потенциалом.
Например, если содержащая кардиомиоциты смесь клеток мечена люминесцентными митохондриальными индикаторами c описанной выше флуоресценцией, то кардиомиоциты (для которых показана относительно высокая интенсивность флуоресценции вследствие относительно высокого содержания митохондрий и митохондрий, показывающих относительно высокий трансмембранный потенциал) могут быть отделены от других отличных от кардиомиоцитов типов клеток (т.е. клеток, которые проявляют относительно менее высокую интенсивность флуоресценции на основе метки с митохондриальными индикаторами, вследствие относительно низкого содержания митохондрий или митохондрий, показывающих относительно низкий трансмембранный потенциал) с использованием клеточного сортера. В результате сортировки клеток могут быть отобраны жизнеспособные кардиомиоциты без генетического изменения кардиомиоцитов. Клеточный сортер, используемый по настоящему изобретению, может не ограничиваться конкретным устройством, при условии, что могут быть отсортированы жизнеспособные меченые флуоресцентной меткой клетки. Например, в качестве конкретного устройства для сортировки клеток по настоящему изобретению может использоваться клеточный сортер с активированной флуоресценцией (FACS (зарегистрированный товарный знак); BD, Franklin Lakes, NJ USA) и другие устройства для сортировки клеток (поставляемые Beckman, Coulter, Cytomation и т.д.).
Кардиомиоциты могут быть отобраны непосредственно после мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором. Однако если необходимо отбирать кардиомиоциты из содержащей кардиомиоциты смеси клеток более точно, кардиомиоциты могут быть отобраны после мечения клеток митохондриальным индикатором с последующим культивированием меченых клеток в отсутствии митохондриального индикатора. В процессе культивирования меченых клеток в отсутствии митохондриального индикатора после мечения митохондриальным индикатором содержание митохондриального индикатора, находящегося в одной клетке снижается, поскольку клетка подвергается клеточному делению. Таким образом, с течением времени культивирования пролиферирующих клеток содержание внутриклеточного митохондриального индикатора снижается и интенсивность флуоресценции также снижается. С другой стороны, поскольку кардиомиоцит определяется как клетка, теряющая способность к митозу, или как клетка со значительно сниженным уровнем способности к митозу, то даже после длительного периода времени культивирования содержание митохондриального индикатора, находящегося в отдельной клетке, снижается медленнее, чем в других типах клеток, и таким образом может сохраняться относительно более высокая интенсивность флуоресценции. Таким образом, вследствие различий в интенсивности мечения между кардиомиоцитами и некардиомиоцитами, кардиомиоциты можно выделять более точно после мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором с последующим дополнительным культивированием клеток в отсутствии митохондриального индикатора в течение определенного периода времени, более конкретно в течение нескольких суток.
Кроме того, во втором варианте осуществления настоящее изобретение относится к способу увеличения содержания кардиомиоцитов в содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов, где указанный способ включает следующие стадии:
(1) стадию мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором; и
(2) стадию отбора кардиомиоцитов на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
В контексте этого варианта осуществления содержащая кардиомиоциты смесь клеток может представлять собой смесь клеток, полученную из целого сердца или смесь клеток, полученную из клеток, обладающих способностью дифференцироваться в кардиомиоциты. Поскольку, как используется здесь, термин "смесь клеток, полученная из целого сердца" означает смесь кардиомиоцитов и некардиомиоцитов, то "смесь клеток, полученная из целого сердца" может вызывать клинический риск тяжелых побочных эффектов на сердечную ткань (сердце) реципиента вследствие существования некардиомиоцитов, если смесь используется для трансплантации в сердце без предварительной обработки. Таким образом, для более безопасной и надежной трансплантации кардиомиоцитов реципиенту предпочтительно увеличить процентную долю кардиомиоцитов в содержащей кардиомиоциты смеси клеток, т.е. максимально увеличить содержание кардиомиоцитов перед трансплантацией. Кроме того, например, клетка, обладающая способностью дифференцироваться в кардиомиоцит, может быть выбрана из группы, состоящей из стволовой клетки, клетки-предшественника и яйцеклетки.
Для безошибочного увеличения содержания кардиомиоцитов в этом способе после стадии (1) и перед стадией (2) способ по настоящему изобретению может дополнительно включать стадию культивирования меченых клеток в отсутствии митохондриального индикатора. Эта стадия обеспечивает увеличение уровня относительной внутриклеточной интенсивности флуоресценции кардиомиоцита относительно сниженного уровня интенсивности флуоресценции других типов клеток и более точно приводит к увеличению количества кардиомиоцитов.
Как описано выше, митохондриальный индикатор, используемый в этом варианте осуществления настоящего изобретения, может быть выбран из группы, состоящей из A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R648, R14060, R22420, T639, T668, T669 и T3168. В этом варианте осуществления настоящего изобретения M7512, T3168, T668 или R302 являются предпочтительными в качестве митохондриального индикатора.
Кроме того, в третьем варианте осуществления настоящего изобретения настоящее изобретение относится к способу получения кардиомиоцитов из содержащей кардиомиоциты смеси клеток без генетического изменения кардиомиоцитов, где указанный способ включает следующие стадии:
(1) стадию дифференцировки и стимуляции получения кардиомиоцитов из клеток, обладающих способностью дифференцироваться в кардиомиоциты с получением содержащей кардиомиоциты смеси клеток;
(2) стадию мечения содержащей кардиомиоциты смеси клеток митохондриальным индикатором; и
(3) стадию отбора кардиомиоцитов на основе относительного содержания митохондрий в клетках и/или относительного трансмембранного потенциала митохондрий клеток.
В контексте этого варианта осуществления содержащая кардиомиоциты смесь клеток может представлять собой смесь клеток, полученную из целого сердца или смесь клеток, полученную из клеток, обладающих способностью дифференцироваться в кардиомиоцит. Поскольку, как используется здесь, термин "смесь клеток, полученная из целого сердца" означает смесь кардиомиоцитов и некардиомиоцитов, то "смесь клеток, полученная из целого сердца" может вызывать клинический риск тяжелых побочных эффектов на сердечную ткань реципиента (сердце) вследствие существования некардиомиоцитов, если смесь используется для трансплантации в сердце без какой-либо предварительной обработки. Таким образом, для более безопасной и надежной трансплантации кардиомиоцитов реципиенту предпочтительно увеличить процентную долю кардиомиоцитов в содержащей кардиомиоциты смеси клеток, т.е. максимально увеличить содержание кардиомиоцитов перед трансплантацией. Кроме того, например, клетка, обладающая способностью дифференцироваться в кардиомиоцит, может быть выбрана из группы, состоящей из стволовой клетки, клетки-предшественника и яйцеклетки.
Для безошибочного получения кардиомиоцитов в этом способе после стадии (1) и перед стадией (2) способ по настоящему изобретению может дополнительно включать стадию культивирования меченых клеток в отсутствии митохондриального индикатора.
Как описано выше, митохондриальный индикатор, используемый в этом варианте осуществления, также может быть выбран из группы, состоящей из A1372, D273, D288, D308, D378, D426, D632, D633, D22421, D23806, L6868, M7502, M7510, M7511, M7512, M7513, M7514, M22422, M22423, M22425, M22426, R302, R634, R64