Способ и устройство для оценки гемодинамики печени
Иллюстрации
Показать всеИзобретение относится к медицине, а именно к гепатологии, и предназначено для оценки гемодинамики печени. Устанавливают пять электродов в определенных точках на теле пациента для регистрации электрического импеданса тканей. После установки электродов на теле пациента выполняют функциональные пробы: запись №1 с задержкой дыхания на полувыдохе; запись №2 с задержкой дыхания на глубоком вдохе; запись №3 спустя 1,5-2 минуты после приема нитроглицерина. По указанным записям проводят оценку базового сопротивления тканей, амплитуды и формы реоволн и осуществляют анализ этих данных с помощью системы бинарных оценок. Способ позволяет повысить чувствительность и специфичность исследования гемодинамики печени. 10 ил., 2 табл.
Реферат
Изобретение относится к области медицины, в частности к гепатологии, и может использоваться для оценки гемодинамики печени как портопеченочной, так и центральной.
На сегодняшний день пациентам, у которых имеются подозрения на заболевания печени (на основании жалоб, анамнеза заболевания, данных объективного обследования), предлагают провести ультразвуковое исследование (УЗИ) брюшной полости. С помощью УЗИ возможно выявить гепатомегалию, спленомегалию, асцит, уточнить размеры вены порта, селезеночной вены. Увеличение диаметра селезеночной вены более 10 мм, воротной - более 15 мм лишь косвенно свидетельствует о наличии портальной гипертензии. Поэтому для оценки гемодинамических расстройств портопеченочного кровотока более широко используют методы, основанные на определении объемного тока крови (электромагнитная флуометрия или электрозвуковая флуометрия (TTF)). TTF является более точной методикой и в настоящее время используется в качестве стандарта исследования портопеченочного кровотока. Несмотря на то что кровоток в печеночной и воротной вене может быть оценен одновременно, кровоток микроциркуляторного русла печени может значительно отличаться от полученных данных, так как он во многом определяется степенью интрапеченочного шунтирования. Другой сложностью является то, что объемный кровоток недооценивается, когда используется зонд неподходящего размера. (Например, используется зонд слишком большого размера, что может давать большую недооценку реального тока крови). Также следует учитывать, что при проведении коррекции печеночного кровотока теоретически связь сосуда и зонда должна быть одинакова, от одного эксперимента до другого (для минимизации артефактов, зависящих от угла между зондом и сосудом), что, по мнению многочисленных экспертов, нереально. Также следует помнить, что постановка зонда имеет много ограничивающих факторов, особенно когда нарушения гемодинамики обусловлены блоком на уровне портальных трактов (Bolondi L: The value of Doppler US in the study of hepatic hemodynamics. Consensus conference. J Hepatol 10:353-355, 1990. Bosch J, Navasa M, Garcia-Pagan JC, et al.: Portal hypertension. Med Clin North Am 73:931-953, 1989. Bru С, Bosch J, Navasa M, et al.: Pulsed Doppler measurements of portal blood flow in man: Applications in the non-invasive evaluation of pharmacological therapy of portal hypertension. Proceedings of the Sixth Congress of the European Federation of Societies for Ultrasound in Medicine and Biology, Helsinki, p.66, 1987. Bru С, Feu F, Gilabert R, et al.: Usefulness of color Doppler US in the monitoring of transjugular intrahepatic portosystemic shunt (TIPS). J Ultrasound Med 13:S31, 1994. Matsutani S, Kimura K, Ohto M, et al.: Ultrasonography in the diagnosis of portal hypertension. In Okuda K, Benhamou JP (eds): Portal Hypertension. Berlin, Springer-Verlag, 1991, pp.197-205).
Компьютерная томография и ядерно-магнитный резонанс не менее точны в определении состояния печени, а также четкости визуализации портальной вены или обнаружения тромбозов портальной вены. В то же время, TTF является предпочтительным первичным исследованием из-за его низкой стоимости и высокой точности (Sabba С, Weltin GG, Cicchetti DV, et al.: Observer variability in echo-Doppler measurements of portal flow in cirrhotic patients and normal volunteers. Gastroenterology 98:1603-1611, 1990. Sacerdoti D, Gaiani S, Buonamico P, et al: Interobserver and interequipment variability of hepatic, splenic, and renal arterial Doppler resistance indices in normal subjects and patients with cirrhosis. J Hepatol 27:986-992, 1997).
Среди других методов исследования необходимо выделить ангиографию. Ангиография, включающая ретроградную портальную венографию, является техникой, которая обычно используется для осмотра портальной вены. Однако ультразвуковые методы исследования, по мнению многочисленных экспертов, отличаются высокой точностью и являются более предпочтительным первичным исследованием (Bosch J, Navasa M, Garcia-Pagan JC, et al.: Portal hypertension. Med Clin North Am 73:931-953, 1989. Leyendecker J.R., Rivera E., Washbum W.K. et al.: MR angiography of the portal venous system: Techniques, interpretation, and clinical applications. Radiographics 17:1425-1443, 1997 Debernardi-Venon W, Bandi JC, Garcia-Pagan JC, et al.: CO2 wedged hepatic venography in the evaluation of portal hypertension. Gut 46:856-860, 2000).
Состояние печени можно также оценить по клиренсу коллоидных препаратов, меченных нуклидами при проведении радиоизотопных методов исследования. Для проведения данных исследований используют макроагрегат альбумина, который «захватывается» печенью на 90-95%, или препараты коллоидного золота. Среди указанных методов можно отметить внутривенную радиопортографию (определение кардиопортального времени), а также методы прямого исследования печеночного кровообращения с внутрипеченочным введением нуклидов. Однако радиоизотопные методы исследования в большинстве случаев используются для диагностики объемных процессов, а лучевая нагрузка является не безвредной для больного, что во многом снижает возможности диагностического поиска (Pilette С, Oberti F, Aube С, et al.: Non-invasive diagnosis of esophageal varices in chronic liver diseases. J Hepatol 31:867-873, 1999). Среди широко используемых методов исследований у больных ХЗП является фиброгастродуоденоскопия (ФГДС). С помощью ФГДС можно выявить наличие варикозно расширенных вен пищевода (ВРВ) и начало гастропатии желудка. На согласительном симпозиуме Бавено группа экспертов пришла к заключению, что всем пациентам, страдающим хроническим заболеваниями печени, у которых нет ВРВ, ФГДС должна проводиться 1 раз в 2-3 года, в случае небольшого увеличения ВРВ - 1 раз в год для оценки прогрессирования (Bolondi L, Gatta A, Groszmann RJ, et al.: Baveno II consensus statements: Imaging techniques and hemodynamic measurements in portal hypertension. In De Franchis R (ed): Portal Hypertension II: Proceedings of the Second Baveno International Consensus Workshop on Definitions, Methodology and Therapeutic Strategies. Oxford, Blackwell Science, p.67, 1996. Chalasani N, Imperiale TF, Ismail A, et al.: Predictors of large esophageal varices in patients with cirrhosis. Am J Gastroenterol 94:3285-3291, 1999. De Franchis R: Updating consensus in portal hypertension: Report of the Baveno III Consensus Workshop on Definitions, Methodology and Therapeutic Strategies in Portal Hypertension. J Hepatol 33:846-852, 2000. Garcia-Tsao G, Escorsell A, Zakko M, et al.: Predicting the presence of significant portal hypertension and varices in compensated cirrhotic patients. Hepatology 26:360, 1997. Grace ND, Groszmann RJ, Garcia-Tsao G, et al.: Portal hypertension and variceal bleeding: An AASLD single topic symposium. Hepatology 28:868-880. 1998. Pilette С, Oberti F, Aube C, et al.: Non-invasive diagnosis of esophageal varices in chronic liver diseases. J Hepatol 31:867-873, 1999. The North Italian Endoscopic Club for the Study and Treatment of Esophageal Varices. Prediction of the first variceal hemorrhage in patients with cirrhosis of the liver and esophageal varices. A prospective multicenter study. N Eng1 J Med 319:983-989, 1988).
Однако больший интерес представляет метод эндосонографии (EUS). Стремительное развитие эндоскопической техники в последние годы привело к созданию неинвазивного метода оценки гастрофагальных варикозных вен и кровотока парной вены. Первое исследование EUS было опубликовано в 1988 году. Последующие проводимые исследования показали, что с помощью данного метода можно оценивать увеличение диаметра парной вены и возрастание максимальной скорости кровотока через этот сосуд. Кроме того, EUS оказалась полезной для динамического определения кровотока в парной вене при применении вазоактивных препаратов (соматостатин и т.д.) и является уникальной среди обсуждаемых методик в том, что она может специфически оценивать гастроэфзофагеально расширенные вены. EUS совместно с данными портального давления и определения варикозного тока и диаметра позволяет определить напряжение варикозной стенки. Однако кровоток в гемокапиллярах печени даже при использовании методов математического моделирования может значительно отличаться от полученных данных (Burtin Р, Cales Р, Oberti F, et al.: Endoscopic ultrasonographic signs of portal hypertension in cirrhosis. Gastrointest Endosc 44:257-261, 1996. Caletti GC, Brocchi E, Ferrari A, et al.: Value of endoscopic ultrasonography in the management of portal hypertension. Endoscopy 24 (suppl 1):342-346, 1992).
Известен способ оценки гемодинамики печени с помощью реогепатографии (РГГ). РГГ дает представление о кровенаполнении органа, о тонусе, эластичности и периферическом сопротивлении сосудов печени. Метод прост, неинвазивен, не имеет противопоказаний и может быть использован для динамического контроля и оценки эффективности проводимой терапии. РГГ основана на записи изменений сопротивления живой ткани в переменном электрическом поле высокой частоты, созданном с помощью мостика Уинстна. РГГ впервые была осуществлена М Bettencort в 1956 г. А.С.Логинов и Ю.Т.Пушкарь первыми предложили количественную оценку РГГ при заболеваниях гепатобилиарной системы. Однако большинство экспертов в настоящее время считают, что несмотря на высокую чувствительность метода, получаемые данные отличаются крайне низкой специфичностью, в силу которой РГГ не нашла широкого применение в клинической практике (Щерба Ю.В. Значение реогепатографии в комплексной диагностике хронического вирусного гепатита// Врачебное дело. - 1986, №5. С.114-116. Недогода С.В. Рецепторные механизмы реализации фармакодинамических эффектов кардиоваскулярных средств у больных гипертонической болезнью, сердечной недостаточностью и хроническими заболеваниями печени: Автореф. дис. д-ра мед. наук. - Волгоград, 1995, 36, с.106. Логинов А.С., Пушкарь Ю.Т. Реограмма печени в норме и патологии. Тер. архив - 1962, №3. С.81-87).
В качестве прототипа по наиболее близкой технической сущности выбран Способ оценки гемодинамики печени (Патент №2214158). Способ заключается в совместной оценке кровотока правой, левой долей печени и селезенки. Указанный способ позволяет получать более специфическую информацию о состоянии гемодинамики печени.
Однако оценка гемодинамики печени с помощью способа прототипа в соответствии с заявленными в нем признаками не обеспечивает требуемой достоверности получаемых оценок состояния печени, необходимой врачу для клинической работы, за счет недостаточной чувствительности и специфичности, так как:
1. Способ ограничен оценкой портопеченочной гемодинамики и не дает прямую взаимосвязь их с центральной гемодинамикой.
2. Форма реографической кривой отражает, в первую очередь, соотношение артериовенозного притока и оттока, поэтому по одному исследованию, без проведения функциональных проб практически невозможно судить о преимущественном нарушении артериовенозного притока или нарушенного венозного оттока.
3. Неточность в определении основополагающих показателей не позволяет достоверно судить о стадии и характере поражения печени, исходя из этого невозможно специфично оценить динамику развития процесса.
Известное устройство - Аппаратно-программый комплекс Валента+ - выбрано в качестве прототипа. (Аппаратно-программный комплекс для исследования ЭКГ, РЭО, СВД Валента+. Регистрационное удостоверение №29/02040699/0534-00, внесен в государственный реестр средств измерения медицинского назначения №19266-00. Разработчик - научно-производственное предприятие НЕО г.Санкт-Петербург).
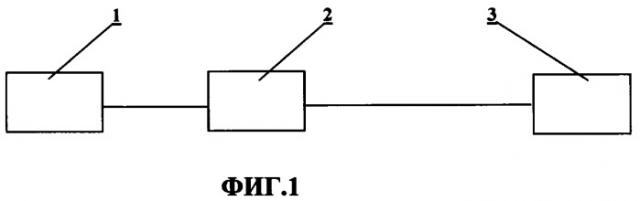
Блок-схема устройства изображена на Фиг.1, где
1 - комплект электродов, выполненных в виде пластин, накладываемых на тело пациента в области печени и селезенки;
2 - цифровой датчик (первичный преобразователь) для формирования сигналов, соответствующих базовой и пульсовой составляющей электрического импеданса тканей в области исследуемого сегмента или органа тела;
3 - регистратор-анализатор сигналов, формируемый на базе персонального компьютера.
Цифровой датчик содержит:
- стабилизированный источник зондирующего переменного тока Iз=1 мА, частотой f=50 кГц;
- детектор электрических сигналов, пропорциональных постоянной и переменной составляющей электрического импеданса зондируемой области тела;
- аналого-цифровой преобразователь и модуль передачи оцифрованных сигналов в регистратор-анализатор сигналов.
Регистратор-анализатор сигналов - это персональный компьютер, выполняющий функции хранения и анализа регистрируемых сигналов (полигепатограмм). Анализ осуществляется с помощью соответствующей компьютерной программы.
С помощью комплекта электродов цепь зондирующего тока замыкается через ткани в области исследуемого сегмента или органа тела (в частности, в области печени и селезенки). Благодаря сравнительно высокой частоте тока электрический импеданс участков цепи, соответствующих преодолению кожных покровов, снижается (вследствие их высокой электрической емкости С и, соответственно, низкого емкостного сопротивления ХC, шунтирующего высокое омическое сопротивлении кожи Rк). При этом измеряемый электрический импеданс Zи определяется преимущественно омическим сопротивлением пульсирующих кровеносных сосудов Rс (зависит от длины L и общего поперечного сечения сосудов Sc).
ХС=1/ωС; ω=2πf; Zи≈Rс≈ρ·L/Sc
Величине импеданса пропорционально значение напряжения (разности потенциалов) на электродах, подключенных к зондируемому участку тела. В первом приближении, изменение этого напряжения характеризует пульсовые изменения кровенаполнения сосудов (пульсации суммарной площади их поперечного сечения), а основной уровень напряжения - базовый уровень кровенаполнения (базовое сопротивление тканей, на фоне которого наблюдаются пульсирующие изменения их сопротивления - волны пульсации кровенаполнения тканей). Измеряемый импеданс (и, соответственно, измеряемое напряжение Uи) складывается из импеданса тканей Zт и импеданса кожи Zк (соизмеримого с Zт). При простой, биполярной схеме подключения электродов эти величины соизмеримы: Zи=Zк+Zт; Uи=Zк·Iз+Zт·Iз; Zк≈Zт
Вклад в измеряемый импеданс Zи величины Zк удается существенно уменьшить за счет применения тетраполярной схемы подключения электродов. В этом случае зондируемый ток подводится с помощью одной пары электродов (токовых), а напряжение измеряется с помощью другой пары электродов (потенциальных), размещаемых на теле пациента внутри зондируемого сегмента. Преимущество достигается за счет того, что в измерительной цепи потенциальных электродов ток Iи может быть гораздо меньше зондирующего тока Iз, и, соответственно этому, уменьшается вклад в измеряемую величину Uи импеданса кожи.
Uи=Zк·Iи+Zт·Iз; Iи<<Iз
В кольцевых электродах, используемых в устройстве-прототипе, рабочие поверхности токовой, потенциальной части и разделяющего их изоляционного материала находятся в одной плоскости, соприкасающейся с кожей пациента. Растекание геля или пота по этой плоскости практически неизбежно, поэтому на величину импеданса (базового сопротивления тканей) существенное влияние оказывает влажность кожных покровов исследуемого, которая у всех пациентов будет различна.
Учитывая неверное определение базового сопротивления, также ошибочными будут суждения об эластичности сосудистого русла печени, оцениваемые по амплитуде реоволны.
Таким образом, устройство, выбранное в качестве прототипа, не обладает достаточной чувствительностью, что не обеспечивает требуемой достоверности выявления особенностей состояния пациента.
Задачей изобретения является повышение диагностической ценности способа оценки гемодинамики печени.
Техническим результатом изобретения является разработка способа и устройства (гепатополиграфа) для оценки гемодинамики печени, повышающего чувствительность и специфичность оценки.
Технический результат достигается тем, что способ оценки гемодинамики печени заключается в регистрации следующих биосигналов: биопотенциалов сердца, тонов сердца, электрического импеданса тканей в области легочной артерии, а также левой, правой доли печени и селезенки. Для регистрации биосигналов электроды устанавливают: электрод №1 под мечевидным отростком на уровне 6-го межреберья, электрод №2 по правой среднеключичной линии в 6-м межреберье, электрод №3 устанавливается на спине, справа от позвоночника, в 6-м межреберье, электрод №4 на уровне 10-го межреберья по левой среднеключичной линии, электрод №5 на уровне 10-го межреберья по левой задней подмышечной линии. После установки электродов на теле пациента выполняют функциональные пробы: запись №1 выполняют при задержке дыхания на полувыдохе; запись №2 выполняют с задержкой дыхания на глубоком вдохе; запись №3 выполняют спустя 1,5-2 минуты после приема нитроглицерина; после проведенного исследования оценивают базовое сопротивление тканей, а также амплитуду и форму реоволны во всех указанных выше отведениях и их динамику при выполнении проб и осуществляют автоматический анализ полученных записей с применением формализованной системы бинарных оценок.
Устройство для оценки гемодинамики печени (гепатополиграф), включающее многоканальный регистратор реограмм (электроимпедансограмм) и контактные электроды для установки на теле пациента, содержит обособленный чип-анализатор с записью ядра программного обеспечения, а электроды выполнены в виде двух контактирующих с телом пациента проводящих частей, разделенных изоляционной канавкой с размерами не менее 2×2 мм.
Способ осуществляется следующим образом.
Географические электроды, которые выполнены в виде двух контактирующих с телом пациента проводящих частей, разделенных изоляционной канавкой с размерами не менее 2×2 мм, устанавливают в области правой доли печени (РЕО 1, электроды Э1 и Э2), левой доли печени (РЕО 2, электроды Э1 и Э3) и в области селезенки (РЕО 3, электроды Э4 и Э5). Кроме того, устанавливают электроды для измерения интегральной реограммы тела (РЕО 4) и реограммы легочной артерии (РЕО 5). Для записи РЕО 4 и РЕО 5 электроды накладывают в соответствии с известными методиками Интегральная реография тела (ИРГТ) и Реография легочной артерии (РЛА).
Для записи ЭКГ выбирается стандартное отведение I или II, в зависимости от того, в каком из них лучше отображается зубец Р. Для записи фонокардиограммы оптимальной оказалась установка микрофона в точке Боткина-Эрба. При этом основные тоны сердца I и II прослушиваются примерно одинаково.
Положение точек установки основных реографических электродов:
электрод №1 под мечевидным отростком на уровне 6-го межреберья,
электрод №2 по правой среднеключичной линии в 6-м межреберье,
электрод №3 устанавливается на спине, справа от позвоночника, в 6-м межреберье,
электрод №4 на уровне 10-го межреберья по левой среднеключичной линии,
электрод №5 на уровне 10-го межреберья по левой задней подмышечной линии.
После установки электродов на теле пациента больного укладывают на кушетку, а электроды соединяют с устройством для оценки гемодинамики печени (гепатополиграфом) и выполняют не менее трех записей полученных биосигналов. При выполнении записей выполняют функциональные пробы:
запись №1 выполняют при задержке дыхания на полувыдохе;
запись №2 выполняют с задержкой дыхания на глубоком вдохе;
запись №3 выполняют спустя 1,5-2 минуты после приема нитроглицерина.
После проведенного исследования оценивают базовое сопротивление тканей, амплитуду и форму реоволны.
Затем осуществляют автоматический анализ полученных записей за счет обособленного чипа-анализатора с записью ядра программного обеспечения с применением формализованной системы бинарных оценок:
1) признаки нарушений портопеченочной и центральной гемодинамики - выявлены или не выявлены;
2) выявленные нарушения портопеченочной и центральной гемодинамики имеют органический или функциональный характер;
3) уровень нарушений портопеченочной и центральной гемодинамики соответствует стадии заболевания - компенсированной или декомпенсированной;
4) динамика состояния печени - выявлена или не выявлена - положительная или отрицательная;
5) этиология заболевания - вирусно-аутоиммунная или токсическая.
Диагностическая значимость заключений о распознаваемых особенностях функционального состояния печени (Self-Descriptiveness, SD) - оценивается независимым экспертом по методу шкалы отношения крайностей: от «бесполезны» (0) до «исчерпывающи» (1)
0<SD<1
Чувствительность распознавания (Sensitivity, Se) - оценивается по формуле Se=QTP/(QTP+QFN), где
QTP (TruePositiveQuantity) - количество истинно положительных заключений
QFN (FolseNegativeQuantity) - количество ложноотрицательных заключений
Прогностическая ценность или достоверность положительного заключения (PositivePredictiveValue или PositivePrediction, PV+ или Р+* (*При принятом нами условии QP=QN критерии ценности и достоверности (PV+ и Р+) тождественны.)) - оценивается по формуле
PV+=QTP/(QTP+QFP*RPN) или Р+=QTP/(QTP+QFP), где
QFN (FolseNegativeQuantity) - количество ложноположительных заключений
RPN (PositoveNegativeRatio) - отношение количества пациентов в сопоставляемых группах RPN=QP/QN, где
QP (PositiveQuantity) и QN (NegativeQuantity) - количество пациентов в группах с наличием распознаваемой особенности состояния и с отсутствием этой особенности.
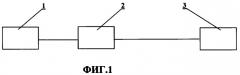
Блок-схема заявляемого устройства представлена на Фиг.2, где
1 - комплект электродов, накладываемых на тело пациента в области печени и селезенки;
2 - цифровой датчик (первичный преобразователь) для формирования сигналов, соответствующих базовой и пульсовой составляющей электрического импеданса тканей в области исследуемого сегмента или органа тела;
3 - регистратор сигналов;
4 - анализатор сигналов.
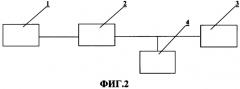
Общий вид электродов представлен на Фиг.3.
Отличительными существенными признаками заявляемого способа и устройства для оценки гемодинамики печени являются:
1. Месторасположение электродов. Электроды устанавливают:
электрод №1 под мечевидным отростком на уровне 6-го межреберья,
электрод №2 по правой среднеключичной линии в 6-м межреберье,
электрод №3 устанавливается на спине, справа от позвоночника, в 6-м межреберье,
электрод №4 на уровне 10-го межреберья по левой среднеключичной линии,
электрод №5 на уровне 10-го межреберья по левой задней подмышечной линии.
2. Выполнение не менее трех записей биосигналов после установки электродов на теле пациента, причем при выполнении записей выполняют функциональные пробы:
запись №1 выполняют при задержке дыхания на полувыдохе;
запись №2 выполняют с задержкой дыхания на глубоком вдохе;
запись №3 выполняют спустя 1,5-2 минуты после приема нитроглицерина.
3. Оценка базового сопротивления тканей, амплитуды и формы реоволны во всех указанных выше отведениях и их динамики при выполнении проб после проведенного исследования.
4. Осуществление автоматического анализа полученных записей с применением формализованной системы бинарных оценок.
5. Выполнение электродов в виде разделенных изоляционной канавкой с размерами не менее 2×2 мм.
6. Наличие в устройстве обособленного чипа-анализатора с записью ядра программного обеспечения.
Причинно-следственная связь между отличительными существенными признаками изобретения и полученным результатом.
Признак 1. Месторасположение электродов позволяет унифицировать методику исследования и выполнить оптимизацию алгоритма анализа регистрируемых кривых в репрезентативной выборке верифицированных записей.
Признак 2. Выполнение не менее трех записей после установки электродов на теле пациента с выполнением функциональных проб позволяет осуществить необходимую детализацию оценки состояния печени. Отбор проб выполнялся с учетом степени отражения в результатах пробы факторов нарушения венозного оттока и артериального притока.
Обоснование применений функциональных проб.
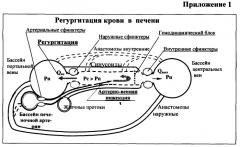
Для обоснования необходимости проведения функциональных проб можно привести конкретную гемодинамическую ситуацию. При прогрессировании патологического процесса в печени происходит существенное ухудшение условий печеночного кровотока, своеобразной реакцией на которое служит механизм повышения перфузионного системного артериального давления, однако вследствие незначительного градиента давления на микроциркуляторном уровне усиленный артериальный кровоток сам может создать дополнительный «гемодинамический» блок, ухудшая прохождение венозной крови через печеночные гемокапилляры и способствуя повышению давления в портальной вене (Приложение 1).
Следовательно, чрезвычайно важно на данном этапе иметь доступную информацию о вкладе артериального кровотока в портопеченочную гемодинамику. При ориентации только на общепринятые в настоящее время методы исследования это представляется довольно сложной задачей. В то же время ПГГ как методика, интегрально оценивающая кровенаполнение органа, оказалась чрезвычайно чувствительна и специфична к изменениям соотношений артериального и венозного притока и венозного оттока, происходящих на микроциркуляторном уровне печени.
В случае сниженного венозного оттока на фоне усиления функции артериального притока при проведении ПГГ на реограммах над областью проекции печени формируется острый артериальный зубец на фоне кривой платообразного вида. В ряде случаев на фоне кривой платообразного вида после острого артериального зубца формировался систолический коллапс. Алгоритм заключений ПГГ, по результатам проведенных функциональных проб с нитроглицерином и на высоте вдоха, достаточно прост. В случае сниженного венозного оттока на высоте вдоха происходит нормализация формы реографической кривой, проявляющаяся уменьшением площади или полном исчезновением систолического коллапса, сокращением площади диастолической части реоволны. В то время как после проведения пробы с нитроглицерином у исследуемых отмечено отсутствие или даже отрицательная динамика изменений формы реограмм. В случае первопричинного снижения венозного притока, на высоте вдоха, наоборот, происходило формирование или увеличение площади систолического коллапса. Одновременно с этим исчезновение или уменьшение площади систолического коллапса после приема нитроглицерина свидетельствовало о функциональном нарушении венозного притока.
Важным элементом в оценке полигепатограмм является отсутствие изменений реограмм в третьем отведении (область проекции селезенки), указывающем на компенсаторные возможности печеночного кровотока (Приложение 1). При проведении пробы с нитроглицерином существенной динамики получено не было.
По результатам проведенного исследования, по динамике изменений формы реографических кривых (полигепатограммы) можно сделать следующей вывод: у исследуемой Ф. формирование острого артериального зубца и систолический коллапс на фоне кривой платообразного вида обусловлены сниженным венозным оттоком на фоне усиления отрицательного вклада артериального притока в печеночный кровоток (Приложение 2). Нарушения венозного оттока имеют функциональный характер. Без проведения функциональных проб по исходной полигепатограмме не возможно дать оценку гемодинамических нарушений портопеченочного кровотока.
Признак 3. Оценка базового сопротивления тканей, амплитуды и формы реоволны во всех указанных выше отведениях и их динамики при выполнении проб после проведенного исследования обеспечивает оптимальное соотношение характеристик значимости, достоверности и чувствительности получаемых оценок состояния печени.
Путем анализа изменений реограмм, отмечаемых при обследовании различных групп пациентов, были отобраны следующие реографические признаки:
- Базовое сопротивление (Rb)
- Форма реографических волн, классифицируемая по видам:
- - артериального вида (вариант нормы)
- - венного вида
- - двухфазная ассиметричная
- - двухфазная симметричная
- - обостренно артериальная
- - нитевидная
- Область, в которой наблюдаются искажения формы реоволны
- - только в области левой доли печени
- - в области обеих долей печени
- - в области правой доли печени и селезенки
Для классификации видов реографической волны использовались значения площади под кривой в интервалах, соответствующих определенным фазам гемодинамического цикла, в том числе:
- механическая систола желудочков сердца
- - фаза максимальной скорости изгнания (ФМИ)
- - фаза редурицированного изгнания (ФРИ)
- механическая диастола желудочков сердца
- - фаза быстрого наполнения желудочков (ФБН)
- - систола предсердий
Было установлено существенное значение для анализа реограмм достоверности измерения величины Rb
Признак 4. Для выявления ряда наиболее информативных и достаточно достоверных заключений об особенностях функционального состояния печени, которые можно распознать методом реографии, была сформирована представительная рондомизированная выборка верифицированных записей. Объем выборки - 504 исследования.
Для каждого исследования были определены реографические признаки и распознаваемые с их помощью особенности функционального состояния печени (на уровне описания особенностей портопеченочной гемодинамики и на уровне клинического описания). Для заключений, полученных по каждой распознаваемой особенности состояния печени, оценивались показатели информативности (SD), чувствительности (Se) и достоверности (Р+). Особенности состояния, заключения о наличие которых получали оценки Se<0,8 или Р+<0,7, отбрасывались. Оставшиеся особенности выстраивались в порядке убывания значений Р+. Отбирались из этого ряда те особенности, совокупность которых обеспечивала, по нашему мнению, наибольшую информативность при приемлемых значениях чувствительности и достоверности получаемых заключений.
Итоговый перечень особенностей функционального состояния печени с применением формализованной системы бинарных оценок:
- признаки нарушений в работе печени - выявлены (не выявлены);
- характер поражения печени - органическое (функциональное);
- наиболее вероятный генез заболевания - токсическое (вирусное или аутоиммунное);
- стадия заболевания - декомпенсированная (компенсированная или субкомпенсированная);
- динамика состояния печени - положительная (отрицательная или отсутствие динамики).
Признак 5. Выполнение электродов в виде разделенных изоляционной канавкой с размерами не менее 2×2 мм позволяет предотвратить замыкание указанных частей через гель на поверхности кожи пациентов, систематически имевшее место при прежней конструкции электродов. Затекание геля между токовой и потенциальной частью электрода приводило к неопределенному завышению измеренного значения величины Rb (на 20…50%). Предлагаемая конструкция электродов позволяет повысить чувствительность прибора за счет повышения достоверности измерения базового сопротивления тканей (одного из важнейших показателей принятой системы анализа реограмм).
Признак 6. Наличие в устройстве обособленного чипа-анализатора с записью ядра программного обеспечения позволяет повысит надежность и защищенность ядра программного обеспечения устройства, а также существенно уменьшить требования к регистратору гепатополиграфа, так как сигнал, который идет от регистратора, оцифровывается, что исключает возникновение помех и артефактов и снижает требования к регистратору.
Совокупность отличительных существенных признаков является новой и позволяет повысить диагностическую ценность способа за счет повышения его чувствительности и специфичности. Способ позволяет определить характер выявленных нарушений не только портопеченочной, но и центральной гемодинамики.
Приводим примеры из клинической практики.
Пример 1.
И/б №342. Больной Д., 32 года, служащий гос. учреждения. Диагноз: Хронический вирусный гепатит С, фаза репликации, минимальная степень активности и фиброзирования.
Последние два года отмечает нарастающую слабость, быструю утомляемость, эпизодические боли в области правого подреберья и эпигастральной области, горечь во рту, изжогу. К врачам не обращался и самостоятельно не лечился. В связи с нарастанием слабости обратился в поликлинику, где были проведены основные клинико-лабораторные и инструментальные исследования, выявлена гепатомегалия. Был рекомендован курс гепатопротекторов. На фоне проводимой терапии продолжала нарастать слабость, в связи с чем больной был госпитализирован в стационар для дальнейшего обследования и лечения.
При поступлении в стационар предъявлял жалобы на выраженную общую слабость, повышенную утомляемость, усталость, эпизодические, ни с чем не связанные боли в области правого подреберья и в эпигастральной области, горечь во рту, изжогу. Объективно: состояние удовлетворительное, кожные покровы чистые, обычной окраски, склеры субиктеричны. Пульс 78 уд/мин, ритмичный. АД 120/80 мм рт.ст. Границы сердца не расширены. Тоны сердца ясные, ритмичные, соотношение тонов не изменено. Дыхание жесткое, хрипов нет. Живот мягкий, безболезненный. Печень увеличена, выступает из-под края реберной дуги на 2 см, край эластичный, закруглен. Размеры селезенки не увеличены. Больному была проведена ПГГ, где на исходной полигепатограмме видно, что величина базового сопротивления выше нормы; амплитуда незначительно снижена; форма реографических кривых в области проекции печени имеет систолическое плато; в области проекции селезенки - увеличение площади диастолической части реоволны (Приложение 3).
После проведения пробы на высоте вдоха зафиксировано, что на фоне незначительного увеличения базового сопротивления существенной динамики изменения формы реографической не было (Приложение 4). В то же время после проведения пробы с нитроглицерином выявлено уменьшение деформации реографических кривых (Приложение 5). Однако полной нормализации формы реографических кривых в РЕО1-2 не произошло, что свидетельствует о стойких нарушениях внутрипеченочного кровотока.
Анализ полигепатограмм.
Таким образом, исходно у больного выявлены нарушения портопеченочной гемодинамики, протекающие на фоне высокого базового сопротивления и снижения амплитуды реографических кривых, что свидетельствует о снижении кровенаполнения печени и эластических свойств сосудистого русла печени. Нарушения формы реографических кривых выявлены: в области проекции правой, левой доли печени и селезенки, что свидетельствует о выраженных гемодинамических нарушениях, сопровождающихся формированием портальной гипертензии. Проведенные функциональные пробы с нитроглицерином свидетельствуют о функциональном снижении венозного притока. В то время как на высоте вдоха положительной динамики получено не было.
Обсуждение: учитывая отсутствие динамики на высоте вдоха и значительном эффекте при приеме нитроглицерина, можно думать о первопричинном сниженном венозном притоке. В то же время, после приема нитроглицерина полной нормализации формы реографических кривых в области проекции печени не произошло, что может указывать о наличии сформировавшихся морфологических изменениях в области портальных трактов. На основании проведенного исследования нарушения портопеченочной гемодинамики можно сопоставить с 1-2 стадией фиброза (перипортальный, порто-портальный фиброз). Учитывая морфофункциональную гетерогенность гепатоцитов (гепатоциты первой зоны печеночного ацинуса ответственны за синтез, поэтому чаще всего поражения в этой зоне связано с вирусной этиологией заболевания), можно предположить вирусную этиологию заболевания. Также проведенные функциональные пробы свидетельствуют о значительных резервных возможностях портопеченочного кровотока и возможностях терапевтической коррекции портопеченочной гемодинамики.
Заключение: Кровенаполнение печени снижено, эластичность сосудистого русла снижена. Нарушения внутрипеченочной гемодинамики обусловлены развитием блока преимущественно на уровне портальных трактов (пресинусоидальная внутрипеченочная гипертензия). Признаки функциональной портальной гипертензии. Нарушения портопеченочной гемодинамики можно сопоставить с 1-2 стадией фиброза (перипортальный, порто-портальный фиброз). Рекомендовано проведение серологических и молекулярно-генетических методов исследований для исключения вирусной природы заболевания1 (1Вирусное поражение печени здесь рассматривается как наиболее распространенное, и не исключена возможность другой этиологии заболевания, характеризующейся такой же локализацией в печеночном гемокапилляре).
При исследовании периферической крови содержание гемоглобина, эритроцитов, лейкоцитов, тромбоцитов не отличалось от нормальных показателей, отмечено повышение СОЭ до 25 мм/ч. Выявлены положительные антитела к вирусу гепатита С (ИФА), HCV-RNA (++) сыворотки крови положительная методом ПЦР. В биохимических исследования крови: АсАТ 0,76 ммоль/л, АлАТ 1,24 ммоль/л, билирубин 23 мкмоль/л, ЩФ 162,6 ед./л, ГГТП 17,8 ед./л, тимоловая проба 1,5 ВСЕ, альбумины - 59,3%, гамма-глобулины - 16,4. В иммунограмме: снижение показателей клеточного иммунного ответа по субпопуляциям CD3 (1,26×109/л.), CD4 (0,740×109/л.), повышение Ig G (16,1 г/л), ЦИК (89 ед.).
Результаты инструментального обследования: по данным УЗИ выявлена гепатомегалия, на ФГДС - признаки хронического гастрита, дуоденита, положительный уреазный тест на Н. Pylori. Ритмокардиография представила признаки усиления п