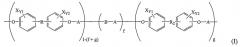Полимерные по существу рентгеноконтрастные продукты для эмболотерапии
Иллюстрации
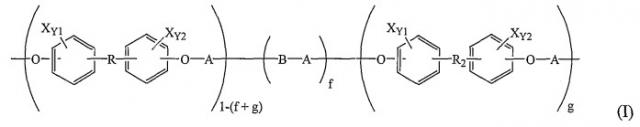
Показать всеИзобретение относится к химико-фармацевтической промышленности, в частности к полимерным рентгеноконтрастным продуктам для эмболотерапии. Описывается эмболотерапевтический продукт, включающий полимер формулы I:
где Х=I или Br; Y1 и Y2=0, 1, 2, 3 или 4; f=0-1; g=0-1; f+g=0-1; А выбран из:
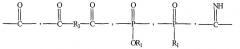
, , , ,
где R1 - H или алкильная группа, содержащая от 1 до 18 углеродных атомов и 0-5 гетероатомов, выбранных из О и N; R3 - алкильная, арильная или алкиларильная группа, содержащая до 18 углеродных атомов и 0-8 гетероатомов, выбранных из О и N; В - алифатическое диоловое или полиалкиленгликолевое звено; R и R2 выбраны из
где R7 - -СН=СН-, -CHJ1-CHJ2- и (-СН2-)а; R8 - -СН=СН-, -CHJ1-CHJ2- и (-СН2-)n;
а и n=0-8; J1 и J2 - Br или I; Q для R2 включает свободную карбоксильную группу и Q для каждого R выбран из группы, состоящей из водорода и сложных эфиров и амидов карбоновых кислот, где полимер включает достаточное количество атомов галогена для придания эмболотерапевтическому продукту рентгеноконтрастности. Предложенный эмболотерапевтический продукт обладает свойствами рентгеноконтрастности, являясь при этом биосовместимым и биоразрушаемым. 3 н. и 72 з.п. ф-лы, 3 ил., 3 табл.
Реферат
В данной заявке заявляется приоритет по 35 U.S.C. §119(e) предварительной заявки США № 60/601677, зарегистрированной 13 августа 2004 г., и предварительной заявки США № 60/505951, зарегистрированной 25 сентября 2003 г. Раскрытия обеих заявок включены здесь в качестве ссылки.
Предпочтительные осуществления настоящего изобретения относятся к полимерным по существу рентгеноконтрастным, биосовместимым и биоразрушаемым частицам и способам применения их для эмболизации полости тела.
Устройства и реагенты для эмболотерапии включают металлические спирали для эмболизации, желеобразную пену, клеи, масла, спирт или полимерные агенты в форме частиц для эмболизации, применяемые, например, для контролирования кровотечения, предотвращения потери крови перед или в течение хирургической процедуры, ограничения или блокирования поступления крови к опухолям и неправильно образованным сосудам, например, в случае фиброзных опухолей матки, опухолей (т.е. хемоэмболизация), геморрагии (например, при травме с кровотечением) и артериовенозных нарушений, фистул и аневризмов. Спирали и частицы для эмболизации применяются наиболее часто.
Традиционные спирали для эмболизации обычно представляют собой свернутые металлические нити, которые сжаты до линейной конфигурации в течение доставки через сосудистый катетер. Они имеют ранее приданную геометрически «спиральную» форму, к которой они возвращаются при выходе из доставляющего катетера. Существует ряд различных моделей и методических вариантов, с использованием металлических спиралей (см., например, патенты США № 6358228 и 6117157); однако металлические спирали для эмболизации создаются для применения при первичном ответе, т.е. когда сгусток крови обусловлен гемодинамическим ответом на физическую обструкцию в кровотоке, и в некоторых случаях при дополнительном ответе, т.е. когда сгусток крови обусловлен биологическим ответом организма на материал спирали, где терапевтическая цель блокирования кровотока достигается образованием сгустка внутри и вокруг металлической спирали.
Хотя металлические спирали для эмболизации имеют ряд благоприятных физико-механических свойств, таких как природная рентгеноконтрастность и память формы (т.е. возвращение к предварительно сформированному спиральному состоянию при развертывании), существует ряд недостатков, связанных с применением металлических спиралей для эмболизации, включая среди прочего хроническое повреждение ткани, тканевую гиперплазию, окклюзию сосудов и постоянное включение в ткань в месте развертывания.
Неметаллические альтернативы включают жидкие и в форме частиц агенты для эмболизации. Однако они также имеют существенные недостатки. Жидкие агенты для эмболизации обычно разделяются на преципитирующие и вступающие в реакцию системы. В первом случае полимер сольватируют в биологически приемлемом растворителе, который рассеивается при доставке через сосуды, оставляя полимер преципитировать in situ (см., например, патент США № 5851508). Такие агенты могут не преципитировать достаточно быстро, тем самым позволяя не застывшему (вязкому) полимеру для эмболизации мигрировать и эмболизировать не предназначенные для этого ткани. Это особенно касается артериовенозных нарушений, где материал может легко входить в венозную систему и вызывать существенную эмболию легких. Другим недостатком является применение растворителей, таких как диметилсульфоксид, для доставки преципитирующих полимеров.
Вступающие в реакцию агенты для эмболизации являются в первую очередь вариантами цианоакрилатных химических систем. Примером утвержденной FDA системы является цианоакрилат для эмболизации TRUFILL® от Cordis. Здесь жидкую мономерную и/или олигомерную цианоакрилатную смесь вводят в участок сосуда через катетер, где полимеризация инициируется под действием имеющейся в крови воды. К сожалению, если время набухания в процессе доставки является слишком большим, цианоакрилатный адгезивный агент может связать наконечник катетера с тканями с серьезными последствиями. Второе касается того, что биоразрушаемые продукты разрушения из данных материалов включают формальдегид, токсичный химический агент.
Терапевтические агенты в форме частиц для эмболизации состоят из частиц с различными размерами, геометрией и составом. Раскрытые Schwarz et al., J. Biomater., 25(21), 5209-15 (2004) деградируемые гидроксиэтилакрилатные (HEA) микросферы были синтезированы и протестированы на животных, но никогда не были поставлены на коммерческую основу. Частицы, применяемые для клинических нужд, обычно суспендируют в рентгеноконтрастирующем растворе, и они доставляются через сосудистый катетер при введении с помощью шприца. Три наиболее часто применяемых в настоящее время агента для эмболизации в форме частиц, представляют собой GELFOAM® (рассасывающиеся желатиновые частицы от Pharmacia & Upjohn), пена из поливинилового спирта (PVA) и трисакриловые желатиновые микросферы (EMBOSPHERE® от Biosphere Medical). В отличие от металлических спиралей данным агентам для эмболизации не присуща рентгеноконтрастность. Действительно, размещение визуализирующего аппарата зависит от результатов рентгеноскопического проточного анализа в течение процедуры эмболизации. Отсутствует прямая возможность визуализировать действующие частицы, как только они попадают внутрь организма. Также в случае PVA или EMBOSPHERE материал может оставаться в организме в течение жизни больного, создавая повышенный риск биологического отторжения. В случае GELFOAM существует возможность тканевого отторжения данного агента животного происхождения.
Агенты в форме частиц для эмболизации могут быть применены, например, для ограничения или блокирования поступления крови, как в случае традиционных применений, которые обычно включают доставку через проводниковый катетер, таких как лечение опухолей и неправильно образованных сосудов, например, в случае фиброзных опухолей матки, раковых опухолей (т.е. хемоэмболизация), геморрагии (например, при травме с кровотечением) и артериовенозных нарушений, фистул и аневризмов.
Биосовместимые, биоразрушаемые, агенты в форме частиц для эмболизации имеют потенциальное преимущество, будучи временными. Эффективное удаление инородного тела в форме частиц с течением времени позволяет ткани вернуться в свое неповрежденное состояние.
Рентгеноконтрастирующие агенты в форме частиц для эмболизации имеют особое потенциальное преимущество, будучи визуализируемыми в течение и после терапевтических процедур эмболизации. В течение процедуры визуализация агента в форме частиц должна позволить врачу достичь точной доставки к целевому сосуду или ткани. Это означает, что врач будет способен убедиться в том, что частицы не задержались в непредназначенных для них местах. Данный уровень контроля должен существенно увеличить безопасность и эффективность эмболотерапии. Как только рентгеноконтрастирующие частицы имплантировались, последующие процедуры могут быть ограничены неинвазивными способами, например, простой рентгеноскопической радиографией. В случае опухоли, например, может быть прослежен ее размер после того, как рентгеноконтрастные эмболизированные срезы покажут стремление к снижению во времени соотношения масса/объем.
Как отмечалось, биосовместимые частицы для эмболизации имеются в настоящее время на рынке. Действительно, биоразрушаемые, биосовместимые агенты для эмболизации доступны в форме GELFOAM®. Как указывалось, однако, существует возможность отторжения из-за животного происхождения данного материала. Более того, GELFOAM® не является одобренным FDA устройством для данного применения.
Были предприняты попытки получения более биосовместимого, деградируемого агента в форме частиц для эмболизации. Также в исследовательских целях были получены рентгеноконтрастирующие агенты для эмболизации и протестированы на животных на их потенциальную применимость. Во всех случаях должны быть добавлены внешние агенты, такие как иодированные контрастирующие среды или металл, или его соль (например, вольфрам, сульфат бария и т.п.), или должна быть придана по существу рентгеноконтрастность с помощью галогенизации биологически неразрушаемых композиций.
Ранее, однако, биосовместимые, биоразрушаемые по природе рентгеноконтрастные частицы для эмболотерапии не испытывались и не испробовались. Соответственно, остается важная неудовлетворенная потребность в разработке биосовместимых, биоразрушаемых по существу рентгеноконтрастных частиц для эмболотерапии, которые могут также давать возможность повторного лечения того же самого места, обходя или ослабляя указанные выше недостатки существующих или испытывающихся агентов в форме частиц для эмболизации.
Соответственно, остается важная неудовлетворенная потребность в разработке биоразрушаемых, рентгеноконтрастирующих агентов для эмболизации, в которых полимерные материалы, применяемые для создания данных агентов, имеют желательные качества металла (например, рентгеноконтрастность), обходя или ослабляя указанные выше недостатки, связанные с применением металлических спиралей или жидких и состоящих из частиц альтернатив для эмболизации.
Краткое изложение существа изобретения
Раскрыт продукт для эмболотерапии в соответствии с предпочтительными осуществлениями настоящего изобретения. Продукт для эмболотерапии включает состав в форме частиц, включающий биосовместимый, биоразрушаемый полимер и необязательно включающий его стереоизомеры, где полимер включает достаточное количество атомов галогена для придания продукту для эмболотерапии по существу рентгеноконтрастности. В некоторых предпочтительных осуществлениях полимер включает гомополимер, гетерополимер или их смесь.
В одном предпочтительном осуществлении продукта для эмболотерапии полимер включает одно или более звеньев, описываемых формулой I:
где X = I или Br; Y1 и Y2 могут независимо = 0, 1, 2, 3 или 4;
где f равно между 0 и менее чем 1; g равно 0-1, включительно; и f+g равно 0-1, включительно;
где A представляет собой либо:
где R1 независимо представляет собой H или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N;
где R3 представляет собой насыщенную или ненасыщенную, замещенную или незамещенную алкильную, арильную или алкиларильную группу, содержащую до приблизительно 18 углеродных атомов и 0-8 гетероатомов, выбранных из O и N;
где B представляет собой алифатическое линейное или разветвленное диоловое или полиалкиленгликолевое звено; и
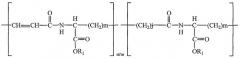
где R и R2 могут быть независимо выбраны из:
где R7 выбран из группы, состоящей из -CH=CH-, -CHJ1-CHJ2- и (-CH2-)a; где R8 выбран из группы, состоящей из -CH=CH-, -CHJ1-CHJ2- и (-CH2-)n; где a и n независимо равны 0-8, включительно; J1 и J2 независимо представляют собой Br или I; и, для R2, Q включает свободную карбоксильную группу, и, для R, Q выбран из группы, состоящей из водорода и сложных эфиров и амидов карбоновых кислот, где указанные сложные эфиры и амиды выбраны из группы, состоящей из алкиловых и алкилариловых сложных эфиров и амидов, где алкильные и алкиларильные группы содержат до 18 углеродных атомов, и из сложных эфиров и амидов биологически и фармацевтически активных соединений.
В варианте данного осуществления формулы I R и R2 могут быть выбраны из групп:
где R1 в каждом R2 представляет собой водород, и R1 в каждом R независимо представляет собой алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из О и N,;
где j и m независимо являются целыми числами 1-8, включительно; и
где Z независимо представляет собой О или S.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может включать одно или более звеньев, описываемых формулой II:
где Х для каждого полимерного звена независимо представляет собой Br или I, Y равен 1-4, включительно, и R4 представляет собой алкильную, арильную или алкиларильную группу, содержащую до 18 углеродных атомов и от 0 до 8 гетероатомов, выбранных из О и N.
В вариантах полимера формулы II все группы Х могут быть в орто-положении и Y может составлять 1 или 2. В другом варианте R4 представляет собой алкильную группу.
В другом варианте R4 имеет структуру:
где R9 для каждого звена независимо представляет собой алкильную, арильную или алкиларильную группу, содержащую до 18 углеродных атомов и 0-8 гетероатомов, выбранных из O и N; и R5 и R6, каждый независимо, выбран из водорода и алкильных групп, имеющих до 18 углеродных атомов и 0-8 гетероатомов, выбранных из O и N.
В другом варианте R4 в формуле II R9 для, по меньшей мере, одного звена включает боковую группу COOR1, где для каждого звена, в котором она присутствует, подгруппа R1 независимо представляет собой водород или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов, содержащую 0-5 гетероатомов, выбранных из O и N.
В другом варианте R4 в формуле II R9 независимо имеет структуру:
где R7 выбран из группы, состоящей из -CH=CH-, -CHJ1-CHJ2- и (-CH2-)a; где R8 выбран из группы, состоящей из -CH=CH-, -CHJ1-CHJ2- и (-CH2-)n; где a и n независимо равны 0-8, включительно; и J1 и J2 независимо представляют собой Br или I; и Q выбран из группы, состоящей из водорода, свободной карбоксильной группы, и сложных эфиров и амидов карбоновых кислот, где указанные сложные эфиры и амиды выбраны из группы, состоящей из алкиловых и алкилариловых сложных эфиров и амидов, где алкильные и алкиларильные группы содержат до 18 углеродных атомов, и из сложных эфиров и амидов биологически и фармацевтически активных соединений.
В другом варианте R4 в формуле II R9 независимо имеет структуру:
где R5a представляет собой алкильную группу, содержащую до 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N; и где m является целым числом 1-8, включительно; и R1 независимо представляет собой водород или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N.
В другом варианте R4 в формуле II R9 независимо имеет структуру:
где j и m независимо являются целыми числами 1-8, включительно, и R1 независимо представляет собой водород или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N.
В некоторых осуществлениях продуктов для эмболотерапии настоящего изобретения полимер может быть сополимеризован с поли(C1-C4алкиленгликолем). Предпочтительно количество поли(C1-C4алкиленгликоля) составляет менее приблизительно 75 вес.%. Более предпочтительно полиалкиленгликоль представляет собой полиэтиленгликоль.
В другом варианте раскрытых в описании полимеров от приблизительно 0,01 до приблизительно 0,99 процентов указанных полимерных звеньев включает боковую группу -COOH.
В другом варианте формулы II R4 может представлять собой арильную или алкиларильную группу. Предпочтительно, чтобы арильная или алкиларильная группа R4 была выбрана так, чтобы полимерные звенья представляли собой дифенолы.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может включать одно или более звеньев, описываемых формулой III:
где X для каждого полимерного звена независимо представляет собой Br или I, Y1 и Y2, каждый независимо, составляют 0-4, включительно, Y1+Y2 для каждого звена независимо составляют 1-8, включительно, и R2 для каждого полимерного звена независимо представляет собой алкильную, арильную или алкиларильную группу, содержащую до 18 углеродных атомов и 0-8 гетероатомов, выбранных из O и N.
В предпочтительных вариантах формулы III все группы X находятся в орто-положении. Предпочтительно, чтобы Y1 и Y2 независимо составляли 2 или менее и Y1+Y2=1, 2, 3 или 4.
В другом варианте формулы III R2 для, по меньшей мере, одного звена может включать боковую группу COOR1, где для каждого звена, в котором присутствует группа COOR1, подгруппа R1 независимо представляет собой водород или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N.
В другом варианте формулы III R2 независимо имеет структуру:
где R7 выбран из группы, состоящей из -CH=CH-, -CHJ1-CHJ2- и (-CH2-)a, где R8 выбран из группы, состоящей из -CH=CH-, -CHJ1-CHJ2- и (-CH2-)n; где a и n независимо равны 0-8, включительно; и J1 и J2 независимо представляют собой Br или I; и Q выбран из группы, состоящей из водорода, свободной карбоксильной группы и сложных эфиров и амидов карбоновых кислот, где указанные сложные эфиры и амиды выбраны из группы, состоящей из алкиловых и алкилариловых сложных эфиров и амидов, алкильные и алкиларильные группы которых содержат до 18 углеродных атомов, и из сложных эфиров и амидов биологически и фармацевтически активных соединений.
В другом варианте формулы III R2 независимо имеет структуру:
где R5a представляет собой алкильную группу, содержащую до 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N; и где m является целым числом 1-8, включительно; и R1 независимо представляет собой водород или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N.
В другом варианте формулы III R2 независимо имеет структуру:
где j и m независимо являются целыми числами 1-8, включительно, и R1 независимо представляет собой водород или алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N.
В предпочтительном варианте формулы III от приблизительно 0,01 до приблизительно 0,99 процентов полимерных звеньев включает боковую группу COOH. Предпочтительно полимер сополимеризован с до 75 вес.% поли(C1-C4алкиленгликоля). Более предпочтительно поли(C1-C4алкиленгликоль) представляет собой полиэтиленгликоль.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может включать одно или более звеньев, описываемых формулой IV:
где каждый X независимо представляет собой I или Br, Y1 и Y2 для каждого дифенольного звена независимо составляют 0-4 включительно, и Y1+Y2 для каждого дифенольного звена независимо составляют 1-8, включительно;
и каждый R и R2 независимо представляет собой алкильную, арильную или алкиларильную группу, содержащую до 18 углеродных атомов и 0-8 гетероатомов, выбранных из O и N, где R2 дополнительно включает боковую группу карбоновой кислоты;
где A представляет собой либо:
где R3 представляет собой насыщенную или ненасыщенную, замещенную или незамещенную алкильную, арильную или алкиларильную группу, содержащую до приблизительно 18 углеродных атомов и от 0 до 8 гетероатомов, выбранных из O и N;
P представляет собой звено поли(C1-C4алкиленгликоля), составляющего приблизительно 75 вес.% или менее; f равно между 0 и менее 1, g равно 0-1, включительно; и f+g равно 0-1, включительно.
В предпочтительных вариантах формулы IV P представляет собой полиэтиленгликоль, который составляет приблизительно 50 вес.% или менее. Более предпочтительно P представляет собой полиэтиленгликоль, который составляет приблизительно 30 вес.% или менее.
В других предпочтительных вариантах формулы IV R и R2 включают боковую группу COOR1; где для R подгруппа R1 независимо представляет собой алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N; и где для R2 подгруппа R1 представляет собой атом водорода.
В других предпочтительных вариантах формулы IV каждый R и R2 независимо имеют структуру:
где R7 выбран из группы, состоящей из -СН=СН-, -CHJ1-CHJ2- и (-СН2-)а, где R8 выбран из группы, состоящей из -СН=СН-, -CHJ1-CHJ2- и (-СН2-)n, где а и n независимо равны 0-8, включительно; и J1 и J2 независимо представляют собой Br или I; и Q для R2 включает свободную карбоксильную группу, и Q для каждого R независимо выбран из группы, состоящей из водорода, сложных эфиров и амидов карбоновых кислот, где указанные сложные эфиры и амиды выбраны из группы, состоящей из алкиловых и алкилариловых сложных эфиров и амидов, где алкильные и алкиларильные группы содержат до 18 углеродных атомов, и из сложных эфиров и амидов биологически и фармацевтически активных соединений.
В других предпочтительных вариантах формулы IV каждый R2 независимо имеет структуру:
где R5a представляет собой алкильную группу, содержащую до 18 углеродных атомов и 0-5 гетероатомов, выбранных из О и N; где m является целым числом 1-8, включительно; и где для каждого R2, R1 представляет, собой водород и для каждого R, R1 независимо представляет собой алкильную группу, содержащую от 1 до 18 углеродных атомов и от 0 до 5 гетероатомов, выбранных из О и N.
В других предпочтительных вариантах формулы IV каждый R2 независимо имеет структуру:
или
где j и m независимо являются целыми числами 1-8, включительно, и где для каждого R2, R1 представляет собой водород и для каждого R, R1 независимо представляет собой алкильную группу, содержащую от 1 до 18 углеродных атомов и 0-5 гетероатомов, выбранных из О и N. Предпочтительно, каждый сложный эфир или амид карбоновых кислот для R представляет собой либо этиловый, либо бутиловый эфир или амид.
В других предпочтительных вариантах формулы IV А представляет собой группу -С(=O)-. В другом предпочтительном варианте формулы III А представляет собой:
где R3 представляет собой С4-С12алкил, С8-С14арил или C8-С14алкиларил. Предпочтительно R3 выбран так, чтобы А представляла собой часть дикарбоновой кислоты, которая является природным метаболитом. Более предпочтительно R3 представляет собой часть, выбранную из -СН2-С(=O)-, -СН2-СН2-С(=O)-, -СН=СН- и (-CH2-)z, где z представляет собой целое число 1-8, включительно.
В других предпочтительных вариантах формулы IV все группы Х находятся в орто-положении. Предпочтительно, чтобы Y1 и Y2 независимо составляли 2 или менее и Y1+Y2=1, 2, 3 или 4.
В других предпочтительных вариантах формулы IV каждый галоген представляет собой йод.
В других предпочтительных вариантах формулы IV f составляет от более 0,1 до приблизительно 0,3. Предпочтительно f составляет от более 0,2 до приблизительно 0,25.
В других предпочтительных вариантах формулы IV поли(C1-C4алкиленгликоль) составляет менее приблизительно 25 вес.%.
В других предпочтительных вариантах формулы IV g составляет от более 0,1 до приблизительно 0,35. Более предпочтительно g составляет от более 0,2 до приблизительно 0,3.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может включать одно или более звеньев, описываемых формулой V:
где каждый X независимо представляет собой йод или бром; каждый y независимо составляет 0-4 включительно, где суммарное число заместителей йода и брома в кольце составляет 1-8 включительно; каждый R4 и R6 независимо представляет собой алкильную, арильную или алкиларильную группу, содержащую до 18 углеродных атомов и от 0 до 8 гетероатомов, выбранных из O и N, R4 дополнительно включает боковую группу карбоновой кислоты;
где A представляет собой либо:
где R3 представляет собой насыщенную или ненасыщенную, замещенную или незамещенную алкильную, арильную или алкиларильную группу, содержащую до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из группы, состоящей из O и N;
P представляет собой поли(C1-C4алкиленгликольное звено), весовая доля которого составляет менее приблизительно 75 вес.%;
f составляет более 0 - менее 1; g составляет 0-1, включительно; и f+g составляет 0-1, включительно.
Предпочтительно P представляет собой звено полиэтиленгликоля.
В предпочтительных вариантах формулы V каждый R4 и R6 указанного полимера содержит боковую группу -COOR1, где для каждого R6 каждая подгруппа R1 независимо представляет собой алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов, выбранных из группы, состоящей O и N, и где для каждого R4 каждая подгруппа R1 представляет собой атом водорода.
В других предпочтительных вариантах формулы V каждый R4 и R6 указанного полимера представляет собой:
где R5a представляет собой алкильную группу, содержащую до 18 углеродных атомов и 0-5 гетероатомов, выбранных из O и N; и где m является целым числом 1-8, включительно; и для каждого R6 каждая подгруппа R1 независимо представляет собой алкильную группу, содержащую от 1 до приблизительно 18 углеродных атомов и 0-5 гетероатомов,, выбранных из О и N, и для каждого R4 каждая подгруппа R1 представляет собой атом водорода.
В других предпочтительных вариантах формулы V каждая подгруппа R1 для R4 указанного полимера представляет собой либо этил, либо бутил.
В других предпочтительных вариантах формулы V А представляет собой группу -С(=O)-. Альтернативно, А может представлять собой:
где R3 представляет собой С4-С12алкил, С8-С14арил или С8-С14алкиларил.
В других предпочтительных вариантах формулы V R3 выбран так, чтобы А представляла собой часть дикарбоновой кислоты, которая является природным метаболитом.
В других предпочтительных вариантах формулы V R3 представляет собой часть, выбранную из группы, состоящей из -СН2-С(=O)-, -СН2-СН2-С(=O)-, -СН=СН- и (-CH2-)z, где z представляет собой целое число 1-8, включительно.
В других предпочтительных вариантах формулы V все группы Х находятся в орто-положении и у составляет 2 или 3.
В других предпочтительных вариантах формулы V каждая группа Х представляет собой йод.
В других предпочтительных вариантах формулы V f составляет от более 0,1 до приблизительно 0,3.
В других предпочтительных вариантах формулы V g составляет от более 0,1 до приблизительно 0,35.
В предпочтительных осуществлениях продукт для эмболотерапии настоящего изобретения, состав в форме частиц может быть сформирован для введения путем инъекции. Состав может включать частицы полимера, выбранные из группы, состоящей из сферических частиц, геометрически неоднородных частиц, пористых частиц, полых частиц, плотных частиц и частиц, имеющих исключаемый диаметр от приблизительно 10 микрон до приблизительно 5000 микрон и их сочетаний.
Альтернативно, состав может включать полимерную гидрогелевую композицию.
В предпочтительном осуществлении продукта для эмболотерапии полимер может дополнительно включать эффективное количество, по меньшей мере, одного терапевтического агента. Предпочтительно, чтобы, по меньшей мере, один терапевтический агент был выбран из группы, состоящей из химиотерапевтического агента, нестероидного противовоспалительного или стероидного противовоспалительного агента.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может дополнительно включать эффективное количество агента, увеличивающего магнитный резонанс.
В предпочтительном осуществлении продукта для эмболотерапии полимер может дополнительно включать эффективное количество рентгеноконтрастирующего агента, выбранного из группы, состоящей из йода, брома, бария, висмута, золота, платины, тантала, вольфрама и их смесей.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может дополнительно включать биосовместимое, биодеградируемое полимерное покрытие, адаптированное к стимуляции селективного биологического ответа. Предпочтительно, чтобы биологический ответ был выбран из группы, состоящей из тромбоза, прикрепления клеток, клеточной пролиферации, прикрепления воспалительных клеток и отложения белков матрикса, ингибирования тромбоза, ингибирования прикрепления клеток, ингибирования клеточной пролиферации, ингибирования воспалительных клеток и ингибирования отложения белков матрикса и их сочетания.
В другом предпочтительном осуществлении продукта для эмболотерапии полимер может включать формулу I:
где X=I или Br; Y1 и Y2 могут независимо = 0, 1, 2, 3 или 4;
где f равно между 0 и менее 1; g равно 0-1, включительно; и f+g равно 0-1, включительно;
где R и R2 могут быть независимо выбраны из
где для R2 R1 представляет собой H и для R R1 представляет собой алифатический углеводород с длинной цепью;
где j и m независимо являются целыми числами 1-8, включительно;
где Z независимо представляет собой O или S;
где A выбран из группы, состоящей из
где R3 представляет собой насыщенную или ненасыщенную, замещенную или незамещенную алкильную, арильную или алкиларильную группу, содержащую до приблизительно 18 углеродных атомов и от 0 до 8 гетероатомов, выбранных из O и N; и
где B представляет собой алифатическое линейное или разветвленное диоловое или полиалкиленгликолевое звено.
В соответствии с другим предпочтительным осуществлением настоящего изобретения раскрыт способ эмболизации полости тела. Способ включает стадию введения в полость тела эффективного количества продукта для эмболотерапии, включающего состав в форме частиц, включающих биосовместимый, биоразрушаемый полимер, где полимер включает эффективное количество атомов галогена для придания продукту для эмболотерапии по существу рентгеноконтрастности.
Предпочтительно стадия введения осуществляется путем инъекции либо через катетер, либо через шприц.
В другом предпочтительном осуществлении настоящего изобретения раскрыт способ лечения варикозных и/или паутинных вен. Способ включает введение в указанные варикозные и/или паутинные вены эффективного количества продукта для эмболотерапии, включающего состав в форме частиц, включающих биосовместимый, биоразрушаемый полимер, где полимер включает достаточное число атомов галогена для придания продукту для эмболотерапии по существу рентгеноконтрастности.
Предпочтительно стадия введения осуществляется путем инъекции либо через катетер, либо через шприц.
В соответствии с предпочтительными осуществлениями настоящего изобретения также раскрыт способ увеличения местной доставки терапевтического агента к ткани. Способ включает стадии: введения в кровеносный сосуд, связанный с тканью, количества продукта для эмболотерапии, достаточного для снижения кровотока через указанную ткань; введения терапевтического агента в кровеносный сосуд отдельно или в сочетании с продуктом для эмболотерапии, так чтобы местная доставка терапевтического агента увеличивалась; и повторения стадий введения продукта для эмболотерапии и терапевтического агента после того, как введенный первоначально продукт для эмболотерапии существенно разрушился, заново создавая свободный доступ к указанному кровеносному сосуду. Продукт для эмболотерапии для применения в данном способе включает состав в форме частиц, включающих биосовместимый, биоразрушаемый полимер, где полимер включает достаточное число атомов галогена для придания продукту для эмболотерапии по существу рентгеноконтрастности.
Раскрыт также способ повторного лечения полости тела. Способ включает стадии: введения в область кровеносного сосуда, связанного с указанной тканью, количества биосовместимого, биоразрушаемого полимерного продукта для эмболотерапии, достаточного для снижения тока крови из ткани в течение некоторого периода времени; и введения в более позднее время какого-либо продукта для эмболотерапии в приблизительно ту же область кровеносного сосуда, связанного с указанной тканью, так чтобы указанную ткань можно было повторно лечить или создавать возможность для других форм повторного воздействия.
В одном осуществлении продукта для эмболотерапии настоящего изобретения полимер включает биоразрушаемый по существу рентгеноконтрастный полимер, который не существует в природе. В другом варианте полимер включает биоразрушаемый по существу рентгеноконтрастный полимер, включающий, по меньшей мере, одну аминокислоту.
Краткое описание чертежей
На фиг. 1A-1C показаны рентгеновские изображения изъятой почки свиньи после введения рентгеноконтрастирующей полимерной композиции для эмболотерапии в соответствии с предпочтительными осуществлениями.
На фиг.2 изображено растворение иллюстративного химиотерапевтического лекарства (паклитакселя) из поли-DTE-карбонатного покрытия, биосовместимого, полимерного покрытия для эмболотерапии в соответствии с предпочтительными осуществлениями в ЗФР с твином 20 при 37°С.
На фиг. 3a-b показано сравнение рентгеновских изображений рентгеноконтрастирующих биоразрушаемых поликарбонатных пленок с трииодированными производными тирозина, демонстрирующее рентгеноконтрастность в соответствии с одним предпочтительным осуществлением настоящего изобретения. Поли(I2DITE-со-20%PEG2k)карбонатные пленки имеют фотоплотность, эквивалентную кости человека.
Лучший вариант осуществления изобретения
В соответствии с предпочтительными осуществлениями настоящего изобретения раскрыты биоразрушаемые полимерные эмболотерапевтические по существу рентгеноконтрастные продукты. Они могут быть применены, например, для временного ограничения или блокирования снабжения кровью, как в случае традиционных применений, которые обычно включают доставку через катетер, таких как лечение опухолей и нарушений образования сосудов, например, в случае фиброзных опухолей матки, опухолей (т.е. хемоэмболизация), геморрагии (например, при травме с кровотечением) и артериовенозных нарушений, фистул и аневризмов. Далее, данные агенты для эмболизации могут быть доставлены с помощью других способов, например, прямо в организм через шприц, или другим некатетерным проводником для обеспечения косметического лечения паутинных вен (непривлекательных или нежелательных маленьких вен, близких к поверхности кожи, которые имеют форму ветвей дерева или паутины и имеют красный или синий цвет), выявляемых как на ногах, так и на лице, или даже варикозных вен (набухших и выступающих выше поверхности кожи).
Продукты для эмболотерапии в соответствии с предпочтительными аспектами настоящего изобретения могут иметь, по меньшей мере, некоторые из следующих свойств: (a) существенную рентгеноконтрастность, чтобы быть видимыми с помощью традиционной рентгеновской флюороскопии, (b) существенную сжимаемость частиц, свойства