Способ получения сульфоксидов каталитическим окислением тиоэфиров
Иллюстрации
Показать всеИзобретение относится к области органической химии, а именно к способу получения сульфоксидов каталитическим окисления тиоэфиров в присутствии пероксида водорода, отличающийся тем, что в качестве катализатора используют соединения цинка, такие как соли цинка Zn(NO3)2·6Н2O или Zn(СН3СОО)2·2Н2O, комплексное соединение цинка Zn(salen), координационные полимеры на основе комплексных соединений цинка, такие как гомохиральные микропористые координационные полимеры состава [Zn2BDC·(L-Lac)·DMF]·(DMF)x, где BDC - дианион терефталевой кислоты, L-Lac-дианион молочной кислоты, DMF-диметилформамид;
[Zn2camph2bipy]·3DMF·H2O, где H2camph - (+)-камфорная кислота, bipy - 4,4'-бипиридил; [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O, где H2bpdc - 4,4'-бифенилдикарбоновая кислота, R-man - R-миндальная кислота; [Zn2camph2bpe]·5DMF·H2O, где bpe-транс-бис(4-пиридил)этилен. Технический результат - разработан способ получения сульфоксидов с высокой конверсией и селективностью. Полученные сульфоксиды широко применяются в синтезе органических соединений, в том числе биологически активных. 4 табл.
Реферат
Изобретение относится к области органической химии, а именно к получению сульфоксидов, которые широко применяются в синтезе органических соединений, в том числе биологически активных соединений /Прилежаева Е.Н. Сульфоны и сульфоксиды в полном синтезе биологически активных природных соединений. // Успехи химии, 2000, Т.69, с.403-446/.
Основным подходом к получению сульфоксидов является окисление сульфидов (тиоэфиров) в мягких условиях, обычно при низких температурах, строго дозируя используемый окислитель и подбирая оптимальный растворитель.
Используются H2O2 в различных средах и с различными каталитическими добавками, органические пероксикислоты, гидропероксиды, различные типы галогенсодержащих окислителей, в том числе свободные галогены, азотная кислота и другие азотсодержащие окислители, свободный кислород и другие более сложные реагенты /Прилежаева Е.Н. Химия сульфоксидов и сульфонов //Получение и свойства органических соединений серы, Л.И.Беленький, ред., Москва, Химия, 1998/. Большинство процессов имеют ряд недостатков, таких как (1) дороговизна (и непригодность для промышленного применения), (2) недостаточная экологическая безопасность, (3) невысокая селективность: на практике зачастую сложно остановить окисление на первой стадии, и большинство каталитических способов окисления приводят к образованию примесей сульфона в продуктах реакции. Поэтому поиск новых высокоселективных каталитических систем на основе доступных незагрязняющих окружающую среду металлов (желательно биоэлементов, таких как Zn, Fe) и дешевых нетоксичных окислителей (например, пероксида водорода) является важной и актуальной задачей.
В данной работе предлагается новый способ получения сульфоксидов, основанный на процессе селективного окисления сульфидов пероксидом водорода, катализируемом соединениями цинка.
Предложен способ окисления тиоэфиров в сульфоксиды пероксидом водорода (либо его аддуктом с карбамидом H2O2·(NH2)2CO, далее обозначенным UHP), в котором в качестве катализатора используют соли цинка, например Zn(NO3)2·6H2O и Zn(СН3СОО)2·2H2O, или комплексные соединения цинка, например, N,N'-бис(3,5-дитретбутилсалицилиден)-1,2-циклогександиамин цинк(II) (Zn(salen)), или координационные полимеры на основе комплексов цинка, например, гомохиральные микропористые координационные полимеры состава: [Zn2BDC(L-Lac)·DMF]·(DMF)x (где BDC - дианион терефталевой кислоты, Z-Lac-дианион молочной кислоты, DMF-диметилформамид, х=0÷1), [Zn2camph2bipy]·3DMF·H2O (где H2camph - (+)-камфорная кислота, bipy - 4,4'-бипиридил), [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O (где H2bpdc - 4,4'-бифенилдикар6оновая кислота, R-man - R-миндальная кислота), [Zn2camph2bpe]·5DMF·H2O (где bpe-транс-бис(4-пиридил)этилен).
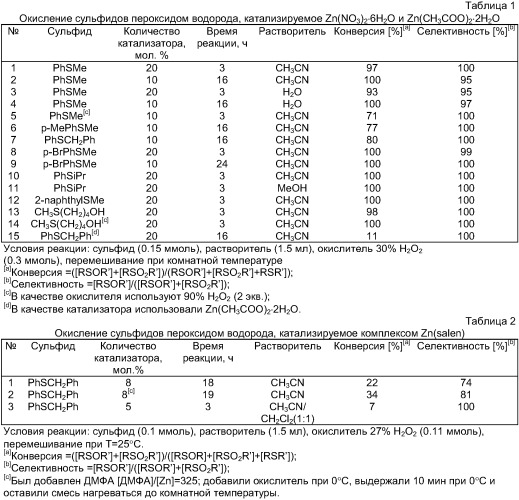
Несмотря на значительное число способов получения сульфоксидов /Прилежаева Е.Н. Химия сульфоксидов и сульфонов // Получение и свойства органических соединений серы, Л.И.Беленький, ред., Москва, Химия, 1998/, в литературе до сих пор не было описано примеров окисления сульфидов (тиоэфиров) в сульфоксиды, катализируемых соединениями цинка. Наши исследования показали, что соли цинка способны катализировать селективное окисление тиоэфиров до сульфоксидов пероксидом водорода. Так, при использовании в качестве катализатора Zn(NO3)2·6H2O окисление алкиларилсульфидов пероксидом водорода происходило с конверсией и селективностью до 100% (таблица 1). Это гомогенный процесс; для растворения Zn(NO3)2·6H2O и пероксида водорода необходимо использовать полярные растворители. Количественное превращение может достигаться при использовании не более 10 моль.% катализатора; оптимальное соотношение окислитель:субстрат равняется двум. Обнаружено также, что другие соли цинка, например
Zn(CH3COO)2·2H2O также проявляют ненулевую каталитическую активность в селективном окислении тиоэфиров в сульфоксиды пероксидом водорода. Конверсия исходного сульфида достигала 11% при селективности 100% при проведении реакции в течение 16 часов (таблица 1 эксперимент 15).
Подобные каталитические свойства характерны не только для солей цинка, но и для комплексных соединений цинка(II). Так, комплекс N,N'-бис(3,5-дитретбутилсалицилиден)-1,2-циклогександиамин цинк(II) (далее обозначенный Zn(salen)) также способен катализировать окисление тиоэфиров в сульфоксиды пероксидом водорода (таблица 2).
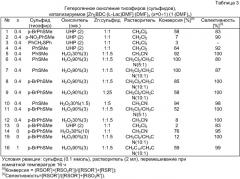
Кроме того, показано, что микропористый координационный полимер [Zn2BDC·(L-Lac)·DMF]·(DMF)x(1·(DMF)x, x=0÷1) /Dybtsev D.N., Nuzhdin A.L., Chun H., Bryliakov K.P., Taisi E.P., Fedin V.P., Kim K. A Homochiral Metal-Organic Material with Permanent Porosity, Enantioselective Sorption Properties, and Catalytic Activity // Angew. Chem. Int. Ed., 2006, v.45, p.916-920/ катализирует селективное гетерогенное окисление тиоэфиров до сульфоксидов дешевым и экологически безопасным окислителем - пероксидом водорода. Результаты гетерогенного окисления сульфидов, катализируемого [Zn2BDC·(L-Lac)·DMF]·(DMF)x(x=0÷1), представлены в таблице 3. В экспериментах по каталитическому окислению тиоэфиров, имеющих небольшие заместители (PhSMe, p-BrPhSMe) с 1·(DMF)x (x=1; ≈0.4) наблюдаются высокие конверсии и высокая селективность окисления после 16 ч каталитической реакции, тогда как тиоэфиры с объемными заместителями (эксперимент №3) окисляются с низкой конверсией. Размерная селективность в каталитических реакциях объясняется тем, что реакция главным образом происходит внутри микропор каркаса 1·(DMF)x. Поскольку PhCH2SPh в силу больших размеров не может проникать в поры 1·(DMF)x, его окисление может происходить только на поверхности полимера, что приводит к чрезвычайно низким величинам конверсии. Раствор, полученный перемешиванием 1·(DMF)0.4 в 2 мл CH2Cl2 в течение 12 ч с последующим отделением твердой фазы с помощью фильтрования и центрифугирования, не проявляет каталитической активности в окислении тиоэфиров. Таким образом, при перемешивании не происходит вымывания активных центров, что также является подтверждением гетерогенного характера каталитической реакции. Каждая формульная единица [Zn2] способна выполнять не менее 30 каталитических циклов. Полимер 1·(DMF)x, из которого практически полностью удален DMF (х=0), демонстрирует низкую конверсию в окислении сульфидов. Вероятно, это связано с частичным разрушением каркаса и схлопыванием пор при удалении значительного количества диметилформамида. Несмотря на то, что полимер 1·(DMF)x обладает свойством гомохиральности (т.к. при его синтезе была использована оптически чистая L-молочная кислота), в результате окисления получается рацемическая смесь сульфоксидов. В случае необходимости рацемическая смесь может быть разделена на чистые энантиомеры любым из известных способов (кристаллизацией, разделением через диастереомеры либо с помощью энантиоселективной хроматографии).
Было установлено, что не только [Zn2BDC·(L-Lac)·DMF]·(DMF)x проявляет каталитическую активность в реакциях селективного окисления тиоэфиров в сульфоксиды. Другие координационные полимеры на основе комплексных соединений цинка, например [Zn2camph2bipy]·3DMF·H2O, [Zn2camph2bpe]·5DMF·H2O и [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O, также проявляют каталитическую активность (см. таблицу 4). Следует отметить, что вышеперечисленные пористые координационные полимеры - первые представители класса координационных полимеров, демонстрирующие каталитическую активность и высокую селективность в реакциях сульфоксидирования.
Таким образом, установлено, что соединения цинка способны катализировать окисление тиоэфиров пероксидом водорода с конверсией и селективностью до 100%. В реакциях окисления каталитическую активность проявляют как соли, так и координационные соединения цинка.
Сущность изобретения иллюстрируется следующими примерами.
Пример 1.
Получение рацемических сульфоксидов окислением соответствующих тиоэфиров пероксидом водорода с Zn(NO3)2·6H2O либо Zn(СН3СОО)2·2H2O в качестве катализатора
Сульфид (тиоэфир) (0.15 ммоль) растворяют в 1.5 мл полярного растворителя (CH3CN, MeOH либо H2O), добавляют катализатор (10-20 мол. %) и H2O2 (0.3 ммоль) и перемешивают в течение 3-24 ч при комнатной температуре. По окончании реакции удаляют растворитель. Продукты реакции выделяют с помощью колоночной хроматографии (SiO2, элюент: гексан/этилацетат) и анализируют с помощью спектроскопии 1Н ЯМР в CCl4 или CDCl3.
В таблице 1 приведены результаты экспериментов по получению рацемического сульфоксидов окислением соответствующих сульфидов пероксидом водорода с применением соли цинка Zn(NO3)2·6H2O и Zn(СН3СОО)2·2H2O в качестве катализатора.
Пример 2.
Получение рацемических сульфоксидов окислением соответствующих тиоэфиров пероксидом водорода с Zn(salen) в качестве катализатора
Сульфид (тиоэфир) (0.1 ммоль) растворяют в 1.5 мл полярного растворителя (CH3CN либо CH3CN/CH2Cl2), добавляют катализатор (5-8 мол. %) и H2O2 (0.11 ммоль) и перемешивают в течение 3-19 ч при Т=25°С. По окончании реакции удаляют растворитель. Продукты реакции выделяют с помощью колоночной хроматографии (SiO2, элюент: гексан/этилацетат) и анализируют с помощью спектроскопии 1Н ЯМР в CCl4.
В таблице 2 приведены результаты экспериментов по получению рацемического сульфоксида окислением соответствующего сульфида пероксидом водорода с применением комплекса цинка Zn(salen) в качестве катализатора.
Пример 3.
Получение рацемических сульфоксидов окислением соответствующих тиоэфиров (сульфидов) пероксидом водорода с [Zn2·BDC·(L-Lac)·DMF]·(DMF)x в качестве катализатора
Смесь сульфида (0.1 ммоль, 1 экв), 1·(DMF)x ([Zn2·BDC·(L-Lac)·DMF]) и окислителя
H2O2 (в виде 90% или 30% водного раствора) либо аддукта H2O2 с мочевиной
H2O2·(NH2)2CO (UHP) растворяют в CH2Cl2 или CH3CN (либо их смеси различного состава). Смесь, общий объем которой был 2 мл, перемешивают 16 ч при комнатной температуре. Полимер отфильтровывают, сорбированный сульфоксид экстрагируют метанолом (3×3 мл). Экстракт и фильтрат комбинируют, удаляют растворитель и DMF в вакууме. Оптический выход и соотношение продуктов реакции определяют с помощью спектроскопии 1Н ЯМР с Eu(hfc)3 в CCl4 или COCl3.
В таблице 3 приведены более подробно условия получения рацемических сульфоксидов окислением соответствующих сульфидов пероксидом водорода с применением координационного соединения цинка [Zn2·BDC·(L-Lac)·DMF]·(DMF)x в качестве катализатора.
Пример 4.
Получение рацемических сульфоксидов окислением соответствующих тиоэфиров (сульфидов) пероксидом водорода с [Zn2camph2bipy]·3DMF·H2O, [Zn2camph2bpe]·5DMF·H2O и [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O в качестве катализатора
Смесь сульфида (0.15 ммоль, 1 экв), соответствующего координационного полимера и окислителя H2O2 (в виде 30% водного раствора) растворяют в CH3CN. Смесь, общий объем которой был 1.5 мл, перемешивают 16 ч при комнатной температуре. Полимер отфильтровывают, сорбированный сульфоксид экстрагируют метанолом (3×3 мл). Экстракт и фильтрат комбинируют, удаляют растворитель и DMF в вакууме. Оптический выход и соотношение продуктов реакции определяют с помощью спектроскопии 1Н ЯМР с Eu(hfc)3 в CCl4 или COCl3.
Результаты каталитических реакций приведены в таблице 4.
| Таблица 4 | |||||
| Гетерогенное окисление тиоэфиров (сульфидов), катализируемое координационными полимерами на основе комплексов цинка [Zn2camph2bipy]·3DMF·H2O и [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O. | |||||
| № | Сульфид | Координационный полимер | Zn:сульфид | Конверсия [%][a] | Селективность[%][b] |
| 1 | PhSMe | [Zn2camph2bipy]·3DMF·H2O | 1:30 | 30 | 97 |
| 2 | PhSCH2Ph | [Zn2camph2bipy]·3DMF·H2O | 1:30 | 17 | 99 |
| 3 | PhSMe | [Zn2camph2bpe]·5DMF·H2O | 1:30 | 28 | 96 |
| 4 | PhSCH2Ph | [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O | 1:30 | 70 | 99 |
| Условия реакции: сульфид (0.15 ммоль), CH3CN (1.5 мл), в качестве катализатора использовали 10 мг полимера, H2O2 30% (0.30 ммоль), перемешивание при комнатной температуре в течение 16 ч | |||||
| [a]Конверсия =([RSOR']+[RSO2R']/([RSOR']+[RSO2R']+[RSR']); | |||||
| [b]Селективность =[RSOR']/([RSOR']+[RSO2R']). |
Способ получения сульфоксидов каталитическим окислением тиоэфиров в присутствие пероксида водорода, отличающийся тем, что в качестве катализатора используют соединения цинка, такие как: соли цинка - Zn(NO3)2·6Н2O или Zn(СН3СОО)2·2Н2O, комплексное соединение цинка - Zn(salen), координационные полимеры на основе комплексных соединения цинка, такие как гомохиральные микропористые координационные полимеры состава: [Zn2BDC·(L-Lac)·DMF]·(DMF)x, где BDC - дианион терефталевой кислоты, L-Lac-дианион молочной кислоты, DMF-диметилформамид; [Zn2camph2bipy]·3DMF·H2O, где H2camph - (+)-камфорная кислота, bipy - 4,4'-бипиридил; [Zn2(bpdc)(R-man)(dmf)]·4DMF·H2O, где H2bpdc - 4,4'-бифенилдикарбоновая кислота, R-man R-миндальная кислота; [Zn2camph2bpe]·5DMF·H2O, где bpe-транс-бис(4-пиридил)этилен.