Способ получения катализатора для паровой конверсии метансодержащих углеводородов
Иллюстрации
Показать всеИзобретение относится к способу получения катализатора, применяемого для процессов конверсии углеводородного сырья в водород и водородсодержащие газы. Описан способ получения катализатора паровой конверсии метансодержащих углеводородов на основе шпинельсодержащего носителя, отличающийся тем, что носитель получают осаждением неорганических компонентов из растворов кислотного травления вермикулитовой руды растворами шелочи с последующей прокалкой полученного осадка при температуре, обеспечивающей получение сложной шпинели типа Mg [Al, Fe]2O4, причем растворы кислотного травления вермикулитовой руды и щелочи берут в количествах, обеспечивающих содержание оксидов магния, железа и алюминия в готовом катализаторе, отвечающее их массовому соотношению 1:0,6:1, носитель выделяют, гранулируют, сушат и прокаливают, после чего наносят никель в количестве 6-15 мас.% в готовом катализаторе и вновь прокаливают. Технический результат - расширение сырьевой базы для производства катализатора паровой конверсии метансодержащих углеводородов. 3 табл., 2 ил.
Реферат
Изобретение относится к способу получения катализатора, применяемого для процессов конверсии углеводородного сырья в водород и водородсодержащие газы.
Паровая конверсия углеводородного сырья является наиболее экономически эффективным методом производства водорода, синтез-газа для оксосинтеза и азотоводородной смеси для получения аммиака.
Технологически метод хорошо разработан и позволяет проводить процесс при высоких давлениях и температуре. Поскольку процесс является каталитическим, важной проблемой остается создание и производство высокоэффективных катализаторов, обладающих повышенными активностью, селективностью и стабильностью.
Современные катализаторы паровой конверсии, выпускаемые различными фирмами, имеют близкие по величине показатели активности и обеспечивают эксплуатацию катализаторов в течение 4-5 лет.
Различия в концентрации никеля в разных марках катализаторов служат, скорее, мерой «элегантности» технических решений, использованных при конструировании этих катализаторов [В.В.Веселов. «Катализаторы конверсии углеводородов», 1979, с.216; Ulmanns Encyclopaedia of Industrial Chemistry, 5th Edn, 1989, vol.A12, p.186 - 202; C.N.Satterfield «Heterogeneous Catalysis in Industrial Practice», McGraw Hill, New York, 1991].
Условия эксплуатации катализаторов паровой конверсии выдвигают достаточно жесткие требования к катализаторам и, соответственно, к носителям для катализаторов. Основу большинства носителей составляет α-Аl2O3, наиболее устойчивая фаза из существующих разновидностей оксида алюминия, с высокой термостабильностью, исключающей возможность структурной химической эрозии носителя под действием водяного пара.
Известен способ получения алюмоникелевого катализатора высокой плотности и механической прочности, описанный в патенте US 5110781 А, B01J 21/04, 05.05.1992.
В качестве исходного материала используют γ-Al2O3, который пропитывают азотнокислым никелем и далее прокаливают для перевода нитрата никеля в оксид.
К недостаткам способа можно отнести высокую температуру прокалки катализатора (1200°С) и низкую удельную поверхность получающейся α-Al2О3.
Известен способ получения Ni-содержащего катализатора паровой конверсии метана, носителем которого является высокочистый α-Al2О3, получаемый из переосажденного оксида алюминия. В качестве диспергатора и промотора активного компонента используют оксид лантана, что повышает устойчивость к зауглероживанию и позволяет работать при низких отношениях пар/углерод.
К недостаткам можно отнести то, что α-Al2O3 имеет низкие значения удельной поверхности, а процессы переосаждения оксида алюминия и введение в систему оксида лантана повышают стоимость катализатора [RU 2185239 С1, кл. В01J 23/83, 20.07.2002].
Достаточно большую группу составляют Ni-содержащие катализаторы на керамических носителях, содержащих помимо α-Al2O3 также алюминаты кальция.
Так, в патенте US 6261991 B1, B01J 23/00, 17.07.2001] описан способ получения никельсодержащего катализатора, согласно которому активный компонент, в частности Ni, наносится методом пропитки на CaAl2O4. Далее полученный материал прокаливают в токе воздуха при температуре 950°С. Испытания полученного катализатора в условиях паровой конверсии показали снижение степени превращения метана на 0,5% в течение 90 часов. Если предположить, что такая тенденция сохранится при более длительной работе, то можно ожидать более существенного снижения активности катализатора.
В патенте US 4906603 A, B01J 23/00, 06.03.1990 сообщается о способе получения катализатора паровой конверсии метана, в котором в качестве носителя используют алюминат кальция в форме гиббонита [CaO(Al2O3)6]. Для создания пористой структуры добавляют выгорающую добавку - графит. Сформованный материал подвергают гидротермальной обработке, затем проходит стадии прокалки и выжигания графита.
Известен способ получения катализатора паровой конверсии метана, носитель которого готовят смешением цемента марки СА-25 с гидроокисью алюминия. Сформованный материал прокаливают при температуре 1300°С и затем наносят активный компонент [US 5773589 A, B01J 23/40, 30.06.1998].
Использование различных алюминатов кальция повышает устойчивость катализаторов к образованию никелевой шпинели, накопление и кристаллизация которой является одной из основных причин дезактивации катализаторов. Недостатком является снижение термостойкости по мере увеличения концентрации алюминатов кальция в носителе.
Известны способы получения катализаторов паровой конверсии метана, носителем которых является шпинель MgAL2O4.
Например, в патенте US 6878667 В2, B01J 23/09, 12.04. 2005 описан способ получения катализатора паровой конверсии метана, в котором различные активные компоненты наносят из их растворов на промышленную шпинель MgAl2O4. Приготовленные таким образом катализаторы после сушки при 110°С подвергают последующей прокалке при 800°С в течение 4 часов. Катализатор, по оценке авторов, имеет высокую активность и механическую прочность.
В патенте US 6958310 В2, B01J 12/00, 02.10.2003 способ получения катализатора, в котором носитель готовят пропиткой γ-Al2О3 раствором нитрата магния с последующей сушкой при 110°С в течение 4 часов и последующей прокалкой при 900°С в течение 2 часов. Далее на полученный носитель методом пропитки наносят активный компонент и полученный катализатор прокаливают при температуре 500°С в течение 3 часов. Катализатор, по мнению авторов, имеет высокую активность и термостабильность.
Однако высокая термическая стабильность магниевой шпинели не защищает ее от нежелательного химического взаимодействия в окислительной среде с никелевым компонентом катализатора, обусловленного диффузионным обменом ионов Mg2+ носителя на ионы Ni2+, имеющие близкие ионные радиусы. Для увеличения стабильности магниевой шпинели предлагается проводить предварительную гидротермальную обработку катализатора при повышенных температуре и давлении. В заявке US 2004265225 А1, кл. В01J 19/00, 30.12.2004 описан способ получения катализатора с использованием гидротермально стабилизированного носителя. Гидротермальную обработку проводят при температуре 900°С, парциальном давлении водяного пара 6-7 атм в течение 24 часов.
Следует отметить, что добавление такой ступени в схему приготовления катализатора неизбежно приведет к увеличению стоимости конечного продукта.
В заявке FR 2857003 А, В01J 21/00, 07.01.2005 разработан способ приготовления катализатора, носителем которого является шпинель со структурной формулой MxM1 1-xAl2O4, где М - Mg, Zn, Mn, a M1 - Fe, Ni, Co. Катализатор демонстрирует высокую активность и термическую стабильность.
Это наиболее близкое техническое решение.
К недостаткам описанного способа можно отнести высокую стоимость промышленных реактивов для приготовления носителя, а также многостадийность метода: а) пропитка исходного γ-Аl2О3 азотнокислыми солями магния и алюминия с последующей сушкой материала при 120°С в течение 15 часов, б) постадийная прокалка носителя при 400°С в течение 2 часов, при 600°С в течение 3 часов, при 900°С в течение 4 часов и далее финишная прокалка при 1000°С в течение 15 часов, в) пропитка носителя солями активного компонента и прокалка готового катализатора при температуре 700°С в течение 5 часов.
Задача предлагаемого изобретения заключается в расширении сырьевой базы для производства катализатора паровой конверсии метансодержащих углеводородов и снижения его себестоимости при сохранении активности на уровне промышленных образцов.
Для решения поставленной задачи предложен способ получения катализатора паровой конверсии метансодержащих углеводородов на основе шпинельсодержащего носителя, в котором носитель получают осаждением неорганических компонентов из растворов кислотного травления вермикулитовой руды растворами щелочи с последующей прокалкой полученного осадка при температуре, обеспечивающей получение сложной шпинели типа Mg[Аl,Fe]2O4, причем растворы кислотного травления вермикулитовой руды и щелочи берут в количествах, обеспечивающих содержание оксидов магния, железа, алюминия в готовом катализаторе, отвечающее их массовому соотношению 1:0,6:1, носитель выделяют, гранулируют, сушат и прокаливают, после чего наносят никель в количестве 6-15 мас.% в готовом катализаторе и вновь прокаливают.
Известны процессы кислотного травления вермикулитовой руды с целью получения пористого сорбента, в которых кислые растворы не использовались и требовали утилизации, описанные в патенте SU 1042794, B01J 20/16, 23.09.1983.
Однако не было известно и авторами впервые обнаружено, что из выделенного по предлагаемому способу осадка, как показывают данные исследования структуры, в ходе термообработки получается сложный оксид со структурой шпинели Mg[Al,Fe]2O4, проявляющий активность в процессе паровой конверсии метансодержащих углеводородов и для образования которого другими методами требуются более высокие затраты энергии и реактивов.
При травлении вермикулита используют, как правило, 10% раствор НСl, в связи с чем требуются небольшие количества щелочи для получения осадка неорганических компонентов, количество которого по массе составляет 50% от исходной вермикулитовой руды.
Ориентировочная стоимость предлагаемого катализатора 30000 руб. за тонну, что на порядок ниже стоимости производства современных промышленных катализаторов.
Учитывая то, что в стране имеются огромные копи вермикулитовой руды, которые на сегодняшний день практически не используются, предлагаемый катализатор имеет выгодную конъюнктуру для реализации выпуска его в стране.
Изобретение иллюстрируется следующими примерами.
Приготовление катализатора
Пример 1
Для получения предлагаемого катализатора из раствора кислотного травления вермикулита методом осаждения готовят шпинельсодержащий носитель. Для этого в раствор травления добавляют 2N раствор NaOH. При достижении значения рН 9,5 образовавшийся осадок тщательно перемешивают в течение 30 минут, отжимают с использованием воронки Бюхнера и промывают репульпацией дистиллированной воды комнатной температуры до отрицательной реакции на ионы хлора.
Выделенный промытый осадок формуют в виде небольших частиц цилиндрической формы диаметром 3 мм, длиной 2-3 мм. Сформованные гранулы сушат на воздухе, в сушильном шкафу при температуре 120°С и прокаливают в муфельной печи при температуре 800°С в течение 2 часов.
Оксид никеля в количестве 6 мас.% (в расчете на никель) вводят в состав катализатора методом пропитки с использованием Ni(NO)36H2O. Готовый катализатор прокаливают при температуре 800°С в течение 2 часов.
По данным элементного анализа в состав полученных гранул входят (мас.%): Fe - 11,81; Mg - 7,26; Al - 8,12, что соответствует массовому соотношению оксидов магния, железа и алюминия в готовом катализаторе, равному 1:0,6:1.
Пример 2
Готовят носитель, как в примере 1, на который наносят никель в количестве 10 мас.% (в расчете на никель) методом пропитки с использованием Ni(NО)36Н2O. Готовый катализатор прокаливают в муфельной печи при температуре 800°С в течение 2 часов.
Пример 3
Готовят носитель, как в примере 1, на который наносят никель в количестве 15 мас.% (в расчете на никель) методом пропитки с использованием Ni(NО)36Н2O. Готовый катализатор прокаливают в муфельной печи при температуре 800°С в течение 2 часов.
Фазовый состав катализаторов определяют методом рентгеновской дифракции на дифрактометре ДРОН-3М с использованием Cu Кα фильтрованного излучения.
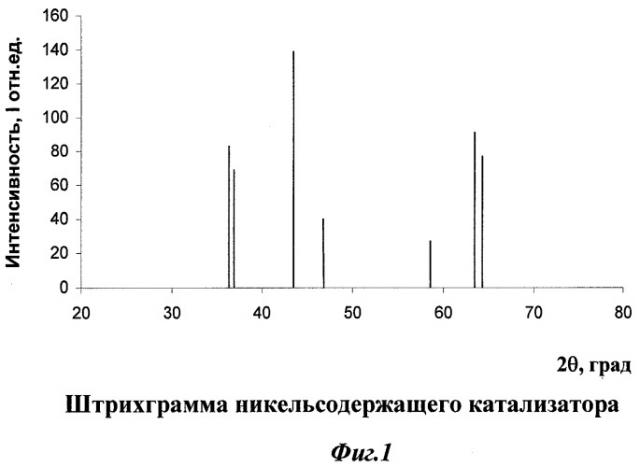
На фиг.1 приведен спектр никельсодержащего катализатора (по оси ординат - интенсивность I в относительных единицах измерения, по оси абсцисс - 2θ, град - удвоенное значение угла рентгеновского излучения при проведении съемки методом рентгеновской дифракции), из которого видно, что катализатор представляет собой систему шпинель - активный компонент.
Линии 2,48; 1,58; 1,45 можно отнести к сложной шпинели типа Mg [Al,Fe]2O4 (13), а линии 2,44; 2,08; 1,47 к фазе NiO (14).
Испытание образцов катализатора в процессе паровой конверсии
Предлагаемый катализатор был испытан в процессе паровой конверсии метана. Опыты проводят в реакторе, изготовленном из жаропрочной стали с внутренним диаметром 30 мм. Во всех экспериментах в реактор загружают 20 см3 испытуемого катализатора.
Пример 5
Катализатор, приготовленный способом, описанным в примере 1, испытывают в процессе паровой конверсии метана под давлением 2,0 МПа, температуре 800°С, соотношении пар/углерод = 4:1 и объемной скорости 4000 ч-1. Результаты испытаний представлены в таблице 1.
Состав конвертированного газа.
| Таблица 1 | |||||
| № пробы | Время, час | Состав конвертированного газа, об.% | |||
| H2 | СО | СO2 | СН4 | ||
| 1 | 1 | 51.6 | 1.6 | 7.6 | 39.2 |
| 2 | 5 | 60.7 | 6,0 | 10.8 | 22.5 |
| 3 | 10 | 66.4 | 6.5 | 10.9 | 16.1 |
| 4 | 15 | 67.1 | 6.6 | 11.0 | 15.3 |
| 5 | 20 | 70.7 | 6.6 | 11.9 | 10.8 |
| 6 | 25 | 71.2 | 6.5 | 11.1 | 11.2 |
| 7 | 30 | 70.5 | 5.5 | 11.8 | 12.2 |
| 8 | 35 | 69.4 | 6.3 | 10.9 | 13.4 |
| 9 | 40 | 71.0 | 6.1 | 12.1 | 10.8 |
| 10 | 45 | 73.1 | 6.2 | 12.0 | 8.7 |
| 11 | 50 | 71.5 | 5.8 | 11.7 | 10.9 |
| 12 | 55 | 71.9 | 6.9 | 11.8 | 9.4 |
| 13 | 60 | 69.2 | 6.2 | 11.9 | 12.7 |
| 14 | 65 | 69.4 | 6.8 | 11.7 | 12.1 |
| 15 | 70 | 70.2 | 6.6 | 11.8 | 11.4 |
Из данных, приведенных в табл.1, видно, что увеличение активности происходит в первые часы работы и обусловлено восстановлением катализатора метанопаровой смесью.
Пример 6
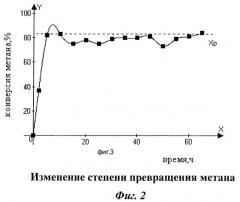
Катализатор, приготовленный способом, описанным в примере 2, был испытан в процессе парой конверсии метана под давлением 2,0 МПа, температуре 800°С, соотношении пар/углерод = 4:1 и объемной скорости 4000 ч-1. Результаты испытаний представлены в таблице 2 и на фиг.2. На фиг.2 приведено изменение степени превращения метана α в течение эксперимента.
Состав конвертированного газа
| Таблица 2 | |||||
| № пробы | Время, час | Состав конвертированного газа, об.% | |||
| H2 | СО | CO2 | CH4 | ||
| 1 | 1 | 61.6 | 6.6 | 7.6 | 24.1 |
| 2 | 5 | 72.1 | 10.6 | 12.1 | 5.2 |
| 3 | 10 | 73.0 | 9.9 | 12.5 | 4.6 |
| 4 | 15 | 71.4 | 10.6 | 10.8 | 7.2 |
| 5 | 20 | 72.2 | 10.1 | 11.6 | 6.1 |
| 6 | 25 | 71.2 | 10.5 | 11.2 | 7.1 |
| 7 | 30 | 72.8 | 11.0 | 10.5 | 5.7 |
| 8 | 35 | 73.1 | 10.8 | 10.6 | 5.5 |
| 9 | 40 | 73.8 | 11.1 | 9.9 | 5.2 |
| 10 | 45 | 73.7 | 11.1 | 10.1 | 5.1 |
| 11 | 50 | 71.6 | 10.8 | 9.7 | 7.9 |
| 12 | 55 | 73.68 | 11.00 | 9.82 | 5.50 |
| 13 | 60 | 74.0 | 10.8 | 10.2 | 5.0 |
| 14 | 65 | 74.7 | 11.4 | 10.1 | 3.8 |
| 15 | 70 | 74.8 | 11.3 | 10.0 | 3.9 |
Из данных, приведенных в табл.2 и на фиг.2, видно, что в начале процесса происходит увеличение активности катализатора, обусловленное его восстановлением. После этого степень превращения метана приближается к равновесной и не снижается в течение всего эксперимента. Следует отметить, что увеличение содержания активного компонента (никеля) до 10% приводит к более быстрой разработке катализатора на выход равновесных концентраций продуктов реакции (сравнение данных табл.1 и 2) по сравнению с катализатором, содержащим 6% Ni.
Пример 7
Катализатор, приготовленный способом, описанным в примере 3, был испытан в процессе паровой конверсии метана под давлением 2,0 МПа, температуре 800°С, соотношении пар/углерод = 4:1 и объемной скорости 4000 ч-1. Результаты испытаний представлены в таблице 3.
| Таблица 3 | |||||
| Состав конвертированного газа | |||||
| № пробы | Время, час | Состав конвертированного газа, об.% | |||
| H2 | СО | СО2 | CH4 | ||
| 1 | 1 | 68.6 | 7.6 | 9.5 | 14.3 |
| 2 | 5 | 72.4 | 10.7 | 11.3 | 5.6 |
| 3 | 10 | 73.1 | 10.0 | 12.4 | 4.5 |
| 4 | 15 | 72.4 | 10.6 | 10.8 | 6.2 |
| 5 | 20 | 72.3 | 10.1 | 11.6 | 6.0 |
| 6 | 25 | 70.1 | 9.5 | 12.1 | 8.3 |
| 7 | 30 | 72.8 | 11.0 | 10.5 | 5.7 |
| 8 | 35 | 73.0 | 10.9 | 10.6 | 5.5 |
| 9 | 40 | 73.8 | 11.1 | 9.9 | 5.2 |
| 10 | 45 | 73.6 | 11.2 | 10.1 | 5.1 |
| 11 | 50 | 71.5 | 10.8 | 9.8 | 7.9 |
| 12 | 55 | 73.7 | 11.2 | 10.0 | 5.1 |
| 13 | 60 | 74.1 | 11.8 | 10.2 | 3.9 |
| 14 | 65 | 75.2 | 11.3 | 10.1 | 3.4 |
| 15 | 70 | 75.4 | 11.4 | 10.0 | 3.2 |
Из данных, приведенных в табл.3, видно, что катализатор разрабатывается так же, как и в примере 6, после чего степень превращения метана приближается к равновесной и не снижается в течение всего эксперимента. Результаты по конверсии метана, полученные в примерах 6 и 7, в которых катализаторы содержат никеля 10 и 15%, достаточно близки.
В этой связи, на основании сопоставления данных, полученных в экспериментах по конверсии метана на катализаторах с различным содержанием никеля как активного компонента, показывает, что наиболее оптимальным является катализатор, содержащий 10 мас.% Ni.
Снижение концентрации активного компонента, в частности, Ni до 6 мас.% ухудшает показатели процесса. Отношение степени превращения метана α (в примере 5) к равновесной для данной температуры - αp составляет α/αp=0,73.
Способ получения катализатора паровой конверсии метансодержащих углеводородов на основе шпинельсодержащего носителя, отличающийся тем, что носитель получают осаждением неорганических компонентов из растворов кислотного травления вермикулитовой руды растворами шелочи с последующей прокалкой полученного осадка при температуре, обеспечивающей получение сложной шпинели типа Mg [Al, Fe]2O4, причем растворы кислотного травления вермикулитовой руды и щелочи берут в количествах, обеспечивающих содержание оксидов магния, железа и алюминия в готовом катализаторе, отвечающее их массовому соотношению 1:0,6:1, носитель выделяют, гранулируют, сушат и прокаливают, после чего наносят никель в количестве 6-15 мас.% в готовом катализаторе и вновь прокаливают.