Пиррольные соединения в качестве ингибиторов erk протеинкиназ, их синтез и промежуточные соединения
Иллюстрации
Показать всеНастоящее изобретение относится к соединениям формулы I
или его фармацевтически приемлемой соли, в которой R1 обозначает С1-6-алифатическую группу, причем R1 может быть замещен заместителями в числе до 2 групп, независимо выбранных из -OR или -С1-3галогеналкила; каждый R независимо обозначает водород или
С1-4-алифатическую группу; R2 обозначает R, фтор или хлор; m обозначает 0, 1 или 2 и R3 обозначает водород, C1-3-алифатическую группу, фтор или хлор, к композиции для ингибирования активности протеинкиназы ERK1 или ERK2 на основе этих соединений, к способу ингибирования активности протеинкиназы ERK1 или ERK2, а также к применению соединений формулы I или композиции на их основе для лечения или уменьшения серьезности заболевания. Технический результат: получены и описаны новые соединения, которые могут быть использованы в качестве ингибиторов протеинкиназ. 5 н.и 6 з.п. ф-лы, 3 табл.
Реферат
ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет на основании Предварительной Заявки на патент Соединенных Штатов 60/571309, поданной 14 мая 2004, все содержание которой тем самым включено в настоящую заявку путем ссылки.
ТЕХНИЧЕСКАЯ ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к соединениям, которые могут быть использованы как ингибиторы протеинкиназ. Изобретение также относится к фармацевтически приемлемым композициям, включающим соединения по изобретению, и к способам применения композиций в лечении различных нарушений.
УРОВЕНЬ ТЕХНИКИ
Поиску новых терапевтических средств значительно помогли в последние годы лучшее понимание структуры ферментов и других биомолекул, связанных с заболеваниями, к лечению которых относится изобретение. Один важный класс ферментов, который был объектом обширных исследований, составляют протеинкиназы.
Протеинкиназы составляют большое семейство структурно родственных ферментов, которые являются ответственными за контроль разнообразных процессов проведения сигналов в пределах клетки (см. Hardie, G. and Hanks, S. (1995) The Protein Kinase Facts Book, I and II, Academic Press, San Diego, CA). Считается, что протеинкиназы эволюционировали от общего генетического предшественника, о чем свидетельствует консерватизм их структуры и каталитической функции. Почти все киназы содержат сходный каталитический домен из 250-300 аминокислот. Киназы могут быть классифицированы по семействам на основании субстратов, которые они фосфорилируют (например, белок-тирозин, белок-серин/треонин, липиды и т.д.). Были идентифицированы звенья последовательности, которые в целом соответствуют каждому из этих семейств киназ (см., например, Hiles et al., Cell, 70:419-429 (1992) Knighton et al., Science, 253:407-414 (1991); Hanks, S.K., Hunter, T., FASEB J., 9:576-596 (1995); Garcia-Bustos et al., EMBO J., 13:2352-2361 (1994 Kunz et al., Cell,73:585-596 (1993)).
В целом, протеинкиназы опосредуют внутриклеточное проведение сигналов, осуществляя перенос фосфорила от нуклеозидтрифосфата к белковому акцептору, который участвует в осуществлении сигнального пути. Эти события фосфорилирования действуют как молекулярный включатель, который может модулировать или регулировать биологическую функцию целевого белка. Эти события фосфорилирования в конечном счете запускаются в ответ на различные внеклеточные и другие раздражители. Примеры таких раздражителей включают сигналы экологического и химического стресса (например, осмотический шок, тепловой шок, ультрафиолетовое излучение, бактериальный эндотоксин и H2O2), цитокины (например, интерлейкин-1 (IL-I) и фактор некроза опухоли (TNF-α)), и факторы роста (например, колониестимулирующий фактор гранулоцита-макрофага (GM-CSF), и фактор роста фибробласта (FGF)). Внеклеточный раздражитель может воздействовать на одну или более клеточных реакций, относящихся к росту, миграции, дифференцировки клеток, секреции гормонов, активации факторов транскрипции, сокращения мышцы, метаболизма глюкозы, контролю синтеза белка и регуляции клеточного цикла.
Многие заболевания связаны с патологическими клеточными реакциями, вызываемыми опосредуемыми протеинкиназой событиями. Эти заболевания включают аутоиммунные заболевания, воспалительные заболевания, заболевания костей, нарушения обмена веществ, неврологические и нейродегенеративные заболевания, рак, сердечно-сосудистые заболевания, аллергии и астму, болезнь Альцгеймера и связанные с гормонами заболевания. Соответственно, в области фармхимии предпринимались усилия для того, чтобы найти ингибиторы протеинкиназ, которые были бы эффективными как терапевтические средства. Однако, учитывая отсутствие в настоящее время доступных вариантов лечения для большинства состояний, связанных с протеинкиназами, все еще существует большая потребность в новых терапевтических средствах, которые ингибируют эти белковые мишени.
Клетки млекопитающих отвечают на внеклеточные раздражители, активируя сигнальные каскады, которые опосредуются семейством митоген-активируемых протеинкиназ (МАР), которые включают регулируемые внеклеточным сигналом киназы (ERK), p38 МАР-киназы и c-Jun N-концевые киназы (JNK). МАР-киназы (MAPK) активируются различными сигналами, включая факторы роста, цитокины, УФ-излучение и стресс-индуцирующие агенты. MAPK представляют собой серин/треонин-киназы, и их активация происходит за счет двойного фосфорилирования треонина и тирозина на сегменте Thr-X-Tyr в активирующей петле. MAPK фосфорилируют различные субстраты, включая факторы транскрипции, которые в свою очередь регулируют экспрессию специфических наборов генов и, таким образом, опосредуют специфический ответ на раздражитель.
ERK2 представляет собой широко распространенную протеинкиназу, которая достигает максимальной активности, когда одновременно Tyr183 и Tyr185 фосфорилируются МАР-киназ-киназой, MEK1 (Anderson et al., 1990, Nature 343, 651; Crews et al., 1992, Science 258,478). После активации ERK2 фосфорилирует многие регуляторные белки, включая протеинкиназы Rsk90 (Bjorbaek et al., 1995, J. Biol. Chem. 270, 18848) и MAPKAP2 (Rouse et al., 1994, Cell 78, 1027), и факторы транскрипции, такие как ATF2 (Raingeaud et al., 1996, Mol. Cell Biol. 16, 1247), Elk-I (Raingeaud et al. 1996), c-Fos (Chen et al., 1993 Proc. Natl. Acad. Sei. USA 90, 10952), и c-Myc (Oliver et al., 1995, Proc. Soc. Exp. Biol. Med. 210, 162). ERK2 также является мишенью на более поздних стадиях Ras/Raf-зависимых путей (Moodie et al., 1993, Science 260, 1658) и передает сигналы от этих потенциально онкогенных белков. Показано, что ERK2 играет роль в отрицательном контроле роста клеток рака молочной железы (Frey and Mulder, 1997, Cancer Res. 57, 628), и сообщалось о гиперэкспрессии ERK2 при раке молочной железы у человека (Sivaraman et al., 1997, J Clin. Invest. 99, 1478). Активированная ERK2 также участвует в пролиферации стимулируемых эндотелином гладких мышечных клеток дыхательных путей, что говорит о роли этой киназы в механизме астмы (Whelchel et al., 1997, Am. J. Respir. Cell MoI. Biol. 16, 589).
Повышенная экспрессия рецептора тирозинкиназ, такого как EGFR и ErbB2 (Arteaga CL, 2002, Semin Oncol. 29, 3-9; Eccles SA, 2001, J. Mammary Gland Biol Neoplasia 6:393-406; Mendelsohn J & Baselga J, 2000, Oncogene 19, 6550-65), а также активирующие мутации в Ras ГТФ-азных белках (Nottage M & Siu LL, 2002, Curr Pharm Des 8, 2231-42; Adjei AA, 2001, J Natl Cancer Inst 93, 1062-74) или мутанты B-Raf (Davies H. et al., 2002, Nature 417, 949-54; Brose et al., 2002, Cancer Res 62, 6997-7000) являются основными причинами рака у человека. Эти генетические альтерации коррелируют с плохим клиническим прогнозом и приводят к активации Raf-1/2/3-MEK1/2-ERK1/2 каскада трансдукции сигнала в обширной группе опухолей у человека. Активированная ERK (то есть ERK1 и/или ERK2) является центральной сигнальной молекулой, которая связана с контролем пролиферации, дифференцировки, независимого от заякоревания выживания клетки и ангиогенеза, внося свой вклад в множество процессов, которые являются важными для формирования и прогрессии злокачественных опухолей. Эти данные позволяют предположить, что ингибитор ERK1/2 будет проявлять плейотропную активность, включая проапоптотические, антипролиферативные, антиметастатические и антиангиогенные эффекты, и предлагают терапевтический подход в отношении очень широкой группы опухолей у человека.
Существует растущий набор очевидных данных о том, что конститутивная активация пути ERK МАРК вовлечена в осуществление онкогенного режима обсуждаемых видов рака. Активирующие мутации Ras обнаруживаются в ~30% всех видов рака, в некоторых, таких как рак поджелудочной железы (90%) и толстого кишечника (50%), достигая особенно высокой частоты мутации. Мутации Ras были также идентифицированы в 9-15% меланом, однако соматические миссенс-мутации B-Raf, придающие конститутивную активацию, являются более частыми и обнаруживаются в 60-66% злокачественных меланом. Активирующие мутации Ras, Raf и MEK способны онкогенно трансформировать фибробласты in vitro, и Ras или Raf мутации, в сочетании с потерей гена супрессора опухоли (например, p16INK4A), могут вызывать спонтанное развитие опухоли in vivo. Увеличенная активность ERK была показана в этих моделях, и о ней также широко сообщалось в отношении соответствующих опухолей у человека. При меланоме зарегистрирована высокая базовая активность ERK, происходящая из B-Raf или N-Ras мутации или аутокринной активации фактора роста, и ее связывают с быстрым ростом опухоли, увеличенной выживаемостью клеток и устойчивостью к апоптозу. Дополнительно, активацию ERK считают главной движущей силой высоко метастатического режима меланомы, связанной с увеличенной экспрессией как протеаз, разлагающих внеклеточную матрицу, так и промотирующих инвазию интегринов, наряду с ингибированием молекул адгезии E-кадгерина, которые в норме опосредуют взаимодействие кератиноцитов, контролируя рост меланоцитов. Эти данные, взятые вместе, показывают, что ERK являются многообещающей терапевтической мишенью в отношении лечения меланомы, в настоящее время не поддающегося лечению заболевания.
КРАТКОЕ СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
В настоящее время обнаружено, что соединения по изобретению и их фармацевтически приемлемые композиции являются эффективными в качестве ингибиторов ERK протеинкиназы. Эти соединения имеют общую формулу I:
или их фармацевтически приемлемую соль, в которой m, R1, R2 и R3 имеют значения, определенные ниже.
Эти соединения и их фармацевтически приемлемые композиции могут быть использованы для лечения или снижения серьезности различных нарушений, особенно пролиферативных нарушений, таких как рак.
Соединения согласно настоящему изобретению также могут быть использованы для исследования киназ в биологических и патологических явлениях и в исследовании путей внутриклеточной трансдукции сигнала, опосредуемых такими киназами, и для сравнительной оценки новых ингибиторов киназ.
ПОДРОБНОЕ ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
1. Общее описание соединений по изобретению
Настоящее изобретение относится к соединению формулы I:
или его фармацевтически приемлемой соли, в которой:
R1 обозначает C1-6 алифатическую группу, причем R1 может быть замещен заместителями в числе до 2 групп, независимо от выбранных из -OR или -C1-3 галогеналкила;
каждый R независимо обозначает водород или C1-4 алифатическую группу;
каждый R2 независимо обозначает R, фтор или хлор;
m обозначает 0, l или 2 и
R3 обозначает водород, C1-3 алифатическую группу, фтор или хлор.
2. Соединения и определения
Соединения по изобретению включают описываемые в целом выше и далее иллюстрируются классами, подклассами и разновидностями, раскрытыми в настоящем описании. В рамках изобретения должны использоваться следующие определения, если не указано иное. В целях этого изобретения, химические элементы идентифицированы в соответствии с Периодической таблицей элементов, версия CAS, Handbook of Chemistry and Physics, 75th Ed.
Дополнительно, общие принципы органической химии описаны в "Organic Chemistry", Thomas Sorrell, University Science Books, Sausalito: 1999, и "March's Advanced Organic Chemistry", 5th Ed., Ed.: Smith, M.B. and March, J., John Wiley & Sons, New York: 2001, все содержание которых тем самым включено в настоящее описание путем ссылки.
В рамках изобретения, термин "пролекарство" относится к производному материнской молекулы лекарственного средства, которое требует трансформации в организме для высвобождения активного лекарственного средства и которое обладает улучшенными физическими свойствами и/или свойствами доставки по сравнению с материнской молекулой лекарственного средства. Пролекарства предназначены для того, чтобы усилить фармацевтические и/или фармакокинетические свойства, связанные с материнской молекулой лекарственного средства. Преимущество пролекарства заключается в его физических свойствах, таких как увеличенная водорастворимость для парентерального введения при физиологическом рН по сравнению с исходным лекарственным средством, или оно усиливает всасывание из пищеварительного тракта, или оно может увеличить стабильность лекарственного средства для длительного хранения. В последние годы несколько типов биообратимых производных были использованы для проектирования пролекарств. Использование сложных эфиров в качестве одного типа пролекарства для препаратов, содержащих карбоксильную или гидроксильную группу, известно в уровне техники и описано, например, в "The Organic Chemistry of Drug Design and Drug Interaction" Richard Silverman, published by Academic Press (1992).
Как описано здесь, соединения по изобретению могут быть в случае необходимости замещены одним или более заместителями, такими как проиллюстрированные выше, или как иллюстрируется особыми классами, подклассами и разновидностями по изобретению. Следует понимать, что фраза «в случае необходимости замещенный» используется взаимозаменяемо с фразой «замещенный или незамещенный». В общем, термин «замещенный», предваряемый или нет термином «в случае необходимости», относится к замене водородных радикалов в данной структуре радикалом указанного заместителя. Если не указано иное, в случае необходимости замещенная группа может иметь заместитель в каждом пригодном для замещения положении группы, и в случае, если более одного положения в любой данной структуре может быть замещено более чем одним заместителем, выбранным из определенной группы, заместитель в каждом положении может быть тем же самым или отличным.
Комбинации заместителей, которые могут быть использованы в соответствии с этим изобретением, предпочтительно являются такими, которые приводят к формированию стабильных или химически возможных соединений. Термин "стабильный" в рамках изобретения относится к соединениям, которые в основном не подвергаются изменениям под действием условий, необходимых для их получения, детекции и, предпочтительно, их рекуперации, очистки и использования для одной или более целей, раскрытых в настоящем изобретении.
В некоторых вариантах осуществления стабильное соединение или химически возможное соединение представляет собой соединение, которое в основном не подвергается изменению при хранении при температуре 40°C или ниже, в отсутствие влажности или в других химически реактивных условиях, в течение по меньшей мере недели.
Термин "алифатический радикал" или "алифатическая группа" в рамках изобретения обозначает прямую (то есть неразветвленную) или разветвленную, замещенную или незамещенную углеводородную цепь, которая является полностью насыщенной или содержит одно или более ненасыщенных звеньев, или моноциклический углеводород, который является полностью насыщенным или содержит одно или более ненасыщенных звеньев, но который не является ароматическим (также упомянутый здесь как "карбоцикл" "циклоалифатический радикал" или "циклоалкил"), который присоединен к остальной части молекулы в одной точке. В некоторых вариантах осуществления алифатические группы содержат 1-6 алифатических атомов углерода, а в других вариантах осуществления алифатические группы содержат 1-4 алифатических атома углерода. В некоторых вариантах осуществления "циклоалифатический радикал" (или "карбоцикл", или "циклоалкил") относится к моноциклическому С3-С6-углеводороду, который является полностью насыщенным или содержит одно или более ненасыщенных звеньев, но который не является ароматическим, который присоединен к остальной части молекулы в одной точке. Подходящие алифатические группы включают, но не ограничены ими, прямой или разветвленный, замещенный или незамещенный алкил, алкенил, алкинил и их гибриды, такие как (циклоалкил)алкил, (циклоалкенил)алкил или (циклоалкил)алкенил.
Термин "ненасыщенный" в рамках изобретения означает, что часть имеет одно или более ненасыщенных звеньев.
Термины "галогеналкил", "галогеналкенил" и "галогеналкокси" означают алкил, алкенил или алкокси, в зависимости от обстоятельств замещенный одним или более атомами галогена. Термин "галоген" означает F, Cl, Br или I.
Термин "арил", использованный отдельно или как часть большего определения, такого как "аралкил", "аралкокси" или "арилоксиалкил", относится к моноциклической, бициклической и трициклической кольцевым системам, имеющим в общей сложности от пяти до четырнадцати кольцевых членов, причем по меньшей мере одно кольцо в системе является ароматическим, и причем каждое кольцо в системе содержит 3-7 кольцевых членов. Термин "арил" может использоваться взаимозаменяемо с термином "арильное кольцо".
Арил (включая аралкил, аралкокси, арилоксиалкил и т.п.) или гетероарил (включая гетероаралкил и гетероарилалкокси и т.п.) может содержать один или более заместителей. Подходящие заместители на ненасыщенном атоме углерода арила или гетероарила выбирают из галогена; R°; OR°; SR°; 1,2-метилен-диокси; 1,2-этилендиокси; фенила (Ph), в случае необходимости замещенного R°; -О(Ph), в случае необходимости замещенного R°; (CH2)1-2(Ph), в случае необходимости замещенного R°; CH=CH(Ph), в случае необходимости замещенного R°; NO2; CN; N(R°)2; NR°C(O)R°; NR°C(О)N(R°)2; NR°CO2R°; -NR°NR°C(O)R°; NR°NR°C(O)N(R°)2; NR°NR°CO2R°; C(O)C(O)R°; C(O)CH2C(O)R°; CO2R°; C(O)R°; C(О)N(R°)2; ОС(O)N(R°)2; С(O)2R°; SO2N(R°)2; С(O)R°; NR°SО2N(R°)2; NR°SO2R°; C(=S)N(R°)2; C(=NH)-N(R°)2; или (CH2)0-2NHC(О)R°, причем каждый R° независимо выбирают из водорода, в случае необходимости замещенного C1-6 алифатического радикала, незамещенных 5-6 членных гетероарила или гетероциклического ядра, фенила, O(Ph) или CH2(Ph), или, несмотря на определение, данное выше, два независимых R°, в том же самом заместителе или в разных заместителях, вместе с атомом(ами), с которым каждая группа R° связана, образуют 3-8-членный циклоалкил, гетероциклил, арил или гетероарил, имеющее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы. Возможные заместители на алифатической группе R° выбраны из NH2, NH(C1-4-алифатической группы), N(C1-4-алифатической группы)2, галогена, C1-4-алифатической группы, ОН, О(C1-4-алифатической группы), NO2, CN, CO2H, CO2(C1-4-алифатической группы), О(галоген-C1-4-алифатической группы) или галоген-C1-4-алифатической группы, причем каждая из указанных C1-4-алифатической группы групп в R° является незамещенной.
Алифатическая или гетероалифатическая группа или неароматическое гетероциклическое ядро могут содержать один или более заместителей. Подходящие заместители на насыщенном углероде алифатической или гетероалифатической группы или неароматического гетероциклического ядра выбраны из упомянутых выше для ненасыщенного углерода арила или гетероарила и дополнительно включают следующее: =О, =S, =NNHR*, =NN(R*)2, =NNHC(О)R*, =NNHCО2(алкил), =NNHSО2(алкил) или =NR*, где каждый R* независимо выбран из водорода или в случае необходимости замещенной C1-6-алифатической группы. Возможные заместители на алифатической группе R* выбраны из NH2, NH(C1-4-алифатической группы), N(C1-4-алифатической группы)2, галогена, C1-4-алифатической группы, ОН, О(C1-4-алифатической группы), NO2, CN, CO2H, CO2(C1-4-алифатической группы), О(галоген- C1-4-алифатической группы) или галоген(C1-4-алифатической группы), причем каждая из указанных C1-4-алифатических групп в R* является незамещенной.
Возможные заместители на азоте неароматического гетероциклического ядра выбраны из R+, N(R+)2, C(O)R+, CO2R+, C(O)C(O)R+, C(O)CH2C(O)R+, SO2R+, SО2N(R+)2, C(=S)N(R+)2, C(=NH)-N(R+)2 или NR+SO2R+; причем R+ обозначает водород, в случае необходимости замещенную C1-6-алифатическую группу, в случае необходимости замещенный фенил, в случае необходимости замещенный O(Ph), в случае необходимости замещенный CH2(Ph), в случае необходимости замещенный (CH2)1-2(Ph); в случае необходимости замещенный CH=CH(Ph); или незамещенный 5-6-членный гетероарил или гетероциклическое кольцо, имеющие один-четыре гетероатома, независимо выбранные из кислорода, азота или серы, или, несмотря на определение, данное выше, два независимых R+, на том же самом заместителе или на разных заместителях, вместе с атомом(ами), с которым каждая группа R+ связана, образуют 3-8-членный циклоалкил, гетероциклил, арил или гетероарил, имеющее 0-4 гетероатома, независимо выбранные из азота, кислорода или серы. Возможные заместители на алифатической группе или фениле R+ выбраны из NH2, NH(C1-4-алифатической группы), N(C1-4-алифатической группы)2, галогена, C1-4-алифатической группы, ОН, О(C1-4-алифатической группы), NO2, CN, CO2H, CO2(C1-4-алифатической группы), О(галоген-C1-4-алифатической группы) или галоген(C1-4-алифатической группы), причем каждая из указанных C1-4-алифатических групп в R+ является незамещенной.
Если не указано иное, структуры, изображенные здесь, также включают все изомерные (например, энантиомерные, диастереомерные и геометрические (или конформационные)) формы структуры; например, конфигурации R и С для каждого центра асимметрии, (Z) и (E) изомеров двойной связи и (Z) и (E) конформационных изомеров. Поэтому отдельные стереохимические изомеры, а также энантиомерные, диастереомерные и геометрические (или конформационные) смеси настоящих соединений находятся в рамках изобретения. Если не указано иное, все таутомерные формы соединений по изобретению также входят в рамки изобретения. Дополнительно, если не указано иное, структуры, изображенные здесь, также включают соединения, которые отличаются только присутствием одного или более изотопически обогащенных атомов. Например, соединения, имеющие структуры по изобретению, за исключением замены водорода дейтерием или тритием или замены углерода 13C- или l4C-обогащенным углеродом, также входят в рамки этого изобретения. Такие соединения могут быть использованы, например, как аналитические инструменты или зонды в биологических анализах.
3. Описание примеров соединений
Согласно одному варианту осуществления настоящее изобретение относится к соединению формулы I, причем указанное соединение имеет формулу Ia или Ib:
или к его фармацевтически приемлемой соли, в которой каждый m, R1, R2 и R3 имеет значение, определенное выше.
Согласно некоторым вариантам осуществления R1 в любой из формул I, Ia и Ib обозначает C1-4-алифатическую группу, в случае необходимости замещенную -OR или -C1-3 галогеналкилом. В некоторых вариантах осуществления R1 в любой из формул I, Ia и Ib обозначает C1-4-алифатическую группу, в случае необходимости замещенную -ОН, -CH2F, -CHF2 или -CF3. В других вариантах осуществления, R1 в любой из формул I, Ia и Ib обозначает C1-4-алифатическую группу, в случае необходимости замещенную -ОН. В других вариантах осуществления R1 является незамещенным.
Согласно другому варианту осуществления R1 в любой из формул I, Ia и Ib обозначает изопропил, 2-бутил, циклопропил или этил, причем каждый из указанных радикалов может быть замещен -ОН, -CHF2, -CH2F или -СF3. В определенных вариантах осуществления в любой из формул I, Ia и Ib может быть замещен -ОН или -CF3.
Другой аспект настоящего изобретения относится к соединению любой из формул I, Ia и Ib, в которой R2 обозначает водород, C1-3-алифатическую группу или хлор. Согласно еще одному аспекту настоящее изобретение относится к соединению любой из формул I, Ia и Ib, в которой R2 обозначает хлор.
В некоторых вариантах осуществления m=1.
В других вариантах осуществления R3 в любой из формул I, Ia и Ib обозначает водород, метил или хлор.
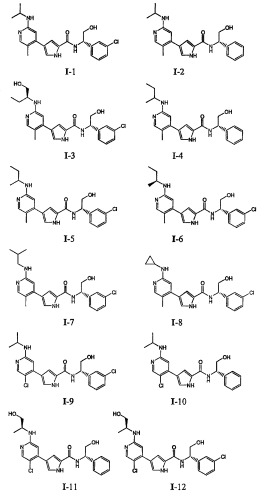
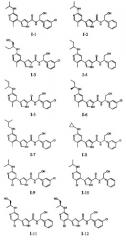
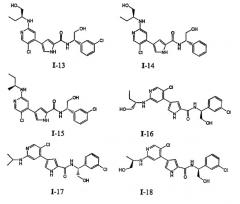
Примеры соединений формулы I сформулированы ниже в Таблице 1.
Таблица 1. Примеры соединений формулы I:
4. Общие способы получения соединений по изобретению
Соединения по изобретению могут быть получены или выделены в общем синтетическими и/или псевдосинтетическими способами, известными специалисту в отношении аналогичных соединений и такими, как иллюстрируется ниже общими Схемами I, II и III и примерами получения, приведенными далее.
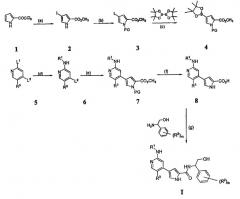
Схема I
Реагенты и условия: (a) iIC1, CH2CL2, iiNaOMe, MeOH; (b) PG-CL, DMAP, триэтиламин; (c) Pd(dppf); (d)R1-NH2; (e) Pd(PPh3)4,4; (f) удаление защитной группы/омыление; (g) условия сочетания.
Общая Схема I, приведенная выше, иллюстрирует общий способ получения соединений согласно настоящему изобретению. В стадии (a) пиррольное соединение 1 йодируют и этерифицируют, получая соединение 2. В стадии (b) пиррольное звено в случае необходимости защищают по -NH- с помощью подходящей аминозащитной группы, получая соединение 3. Аминозащитные группы известны в уровне техники и описаны подробно в Protecting Groups in Organic Synthesis, Theodora W. Greene and Peter G. M. Wuts, 1991, опубликованном John Wiley and Sons, который тем самым в полном объеме включен в настоящее описание путем ссылки. Йод из соединения 3 вытесняют подходящей бороновой кислотой или сложным эфиром. Как изображено выше, используют бис(пинаколато)диборан, получая соединение 4, хотя в этой реакции могут быть использованы другие бороновые кислоты или их эфиры, выбор которых очевиден для специалиста.
Поскольку соединения по изобретению касаются полизамещенного пиридина, рассматривают такой порядок реакции и используют такие способы активации положений в пиридине, чтобы направлять региохимию. В стадии (d) первая удаляемая группа L1 может быть вытеснена по желанию спиртом, амином или тиолом. Для специалиста является очевидным, что различные удаляемые группы L1 могут быть подвергнуты этой реакции. Примеры таких групп включают, но не ограничены ими, галоген и активированные простые эфиры. Эта реакция может сопровождаться, в стадии (e), заменой второй удаляемой группы L2 или с использованием катализируемой металлом реакции сочетания или через нуклеофильное замещение, с получением соединения 7. Для специалиста в данной области очевидно, что различные удаляемые группы L2 могут быть подвергнуты этой реакции. Примеры таких групп включают, но не ограничены ими, галоген, активированные простые эфиры, бороновую кислоту или эфир бороновой кислоты.
В стадии (f) защитную группу на пиррольном звене удаляют способами, подходящими для удаления используемой аминозащитной группы. В зависимости от используемой аминозащитной группы условия, подходящие для этого удаления, могут одновременно приводить к омылению или иначе обеспечить получение карбоксилатного звена, как изображено выше для соединения 8. Если условия, подходящие для удаления аминозащитной группы, не являются подходящими для того, чтобы обеспечить получение карбоксилатного соединения 8, может использоваться другая стадия. Соединения формулы I получают из 8 путем сочетания полученного карбоксилата с желаемым амином, как изображено в стадии (g). Для специалиста в данной области очевидно, что для указанной реакции сочетания пригодны различные условия, и они могут включать стадию образования карбоксилатного звена соединения 8 до или одновременно с обработкой желаемым амином. Такие состояния включают, но не ограничены ими, соединения, описанные подробно в разделе Примеров, приведенном ниже.
Схема II
Реагенты и условия: (a) Ac2О/H2О2; (b) HNО3/H2SО4; (c) R1-NH2; (d) L2.
Схема, приведенная выше, изображает альтернативный путь получения промежуточного соединения 6, полезного для получения соединений согласно настоящему изобретению. В стадии (a) N-оксид соединения 9 получают обработкой перекисью. N-оксид соединения 10 затем обрабатывают азотной кислотой, чтобы получить нитросоединение 11. Группу L1 в соединении 11 заменяют желаемым амином R1-NH2, получая соединение 12, и затем группу L2 вводят на стадии (d), чтобы получить промежуточное соединение 6. Соединение 6 может затем использоваться для получения соединений по изобретению согласно общей Схеме I, приведенной выше, и Примерам, представленным ниже.
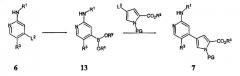
Схема III
Схема III, представленная выше, демонстрирует альтернативный способ получения соединения 7 из соединения 6. В этом способе группу L2 пирридинила 6 заменяют подходящей бороновой кислотой или ее эфирным производным, получая соединение 13, причем Rx и Ry имеют значения, как определено ниже для соединений формулы А. Это боронатное звено затем заменяют удаляемой группой L3 пиррола, изображенного выше, причем L3 является подходящей удаляемой группой с получением соединения 7. Соединение 7 затем используют, чтобы получить соединения согласно настоящему изобретению способами, сформулированными выше в Схемах I и II, описанными в разделе Примеров, и способами, известными специалисту в данной области техники.
Для специалиста очевидно, что различные соединения по изобретению могут быть получены согласно общему способу Схем I, II и III и Примерам синтеза, сформулированным ниже.
Согласно другому варианту осуществления настоящее изобретение относится к соединению формулы A:
или его соли, в которой:
PG обозначает подходящую аминозащитную группу;
Rz обозначает подходящую защитную группу карбоксилата и
Rх и Ry независимо обозначают водород или в случае необходимости замещенную
С1-6 алифатическую группу или
Rх и Ry вместе образуют в случае необходимости замещенное 5-7-членное кольцо.
Подходящие аминозащитные группы известны в уровне техники и включают описанные подробно в Protecting Groups in Organic Synthesis, Theodora W. Greene and Peter G. M. Wuts, 1991, опубликованном John Wiley and Sons. В некоторых вариантах осуществления группа PG соединения A обозначает алкил или арилсульфонил. Примеры таких групп включают метилсульфонил, тозил, нозил, брозил и 2,4,6-триметилбензолсульфонил ("Мts"). Другие такие группы включают Bn, PMB, Ms, Тs, SiR3, MOM, BOM, Tr, Ac, CO2R, CH2OCH2CH2Si(CH3)3.
Подходящие защитные группы карбоксилата известны в уровне техники и описаны подробно в Protecting Groups in Organic Synthesis, Theodora W. Greene and Peter G. M. Wuts, 3rd Edition, 1999, опубликованном John Wiley and Sons. В некоторых вариантах осуществления группа Rz соединения A обозначает в случае необходимости замещенную С1-6 алифатическую группу или в случае необходимости замещенный арил. Примеры подходящих групп Rz включают метил, этил, пропил, изопропил, бутил, изобутил, бензил и фенил, причем каждая группа может замещена.
В некоторых вариантах осуществления одна или обе группы Rх и Ry обозначают водород.
В других вариантах осуществления Rх и Ry вместе образуют в случае необходимости замещенное 5-6-членное кольцо. В других вариантах осуществления Rх и Ry вместе образуют 4,4,5,5-тетраметилдиоксаборолановое звено. Другие подходящие боронатные производные, рассматриваемые в соответствии с настоящим изобретением, включают бороновую кислоту, B(О-С1-10-алифатическую группу)2 и B(О-арил)2.
Согласно еще одному варианту осуществления настоящее изобретение относится к соединению формулы B:
или его соли, в которой:
R1 обозначает С1-6-алифатическую группу, причем R1 может быть замещен заместителями в числе до 2 групп, независимо выбранными из -OR или -C1-3 галогеналкила;
каждый R независимо обозначает водород или С1-4-алифатическую группу;
R3 обозначает водород, С1-3-алифатическую группу, фтор или хлор и
L2 обозначает подходящую удаляемую группу.
В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы B, как определено в целом и в классах и подклассах, описанных выше и здесь, в которой L2 не обозначает йод, когда R3 обозначает хлор и R1 обозначает изопропил.
Подходящая удаляемая группа представляет собой радикал, который легко заменяется желаемым химическим звеном. Таким образом, выбор определенной подходящей удаляемой группы основывается на ее способности к легкой замене на химическое звено формулы A. Подходящие удаляемые группы известны в уровне техники, например, см., "Advanced Organic Chemistry," Jerry March, 5th Ed., pp. 351-357, John Wiley and Sons, N.Y. Такие удаляемые группы включают, но не ограничены ими, галоген, алкокси, сульфонилокси, в случае необходимости замещенный алкилсульфонил, в случае необходимости замещенный алкенилсульфонил, в случае необходимости замещенный арилсульфонил и диазоний. Примеры подходящих удаляемых групп включают хлор, йод, бром, фтор, метансульфонил (метилсульфонил), тозил, трифлат, нитро-фенилсульфонил (нозил) и бром-фенилсульфонил (брозил). В некоторых вариантах осуществления группа L2 в формуле B обозначает йод.
Согласно альтернативному варианту осуществления подходящая удаляемая группа может быть получена in situ в реакционной среде. Например, L2 в соединении формулы B может быть получена in situ от предшественника этого соединения формулы B, причем указанный предшественник содержит группу, которая легко заменяется группой L2 in situ. В частном случае такой замены указанный предшественник соединения формулы B содержит группу (например, хлор или гидроксильную группу), которая in situ заменяется группой L2, такую как йод. Источник йода может быть, например, йодидом натрия. Такая генерация in situ подходящей удаляемой группы известна в уровне техники, например, см., "Advanced Organic Chemistry," Jerry March, pp. 430-431,5th Ed., John Wiley and Sons, N. Y.
Согласно некоторым вариантам осуществления звено R1 формулы B представляет собой С1-4-алифатическую группу, в случае необходимости замещенную -OR или -C1-3 галогеналкилом. В некоторых вариантах осуществления звено R1 формулы B обозначает С1-4-алифатическую группу, в случае необходимости замещенную -ОН, -CH2F, -CHF2 или -CF3. В других вариантах осуществления звено R1 формулы B обозначает С1-4-алифатическую группу, в случае необходимости замещенную -ОН. В других вариантах осуществления R1 является незамещенным.
Согласно другому варианту осуществления звено R1 формулы B обозначает изопропил, 2-бутил, циклопропил или этил, причем каждое звено в случае необходимости замещено -ОН или -CF3.
В других вариантах осуществления звено R3 формулы B обозначает водород, метил или хлор.
Соединение формулы B может быть получено из соединения формулы B':
или его соли, в которой:
R3 обозначает водород, С1-3-алифатическую группу, фтор или хлор и
L1 и L2 каждый независимо обозначают подходящую удаляемую группу.
В некоторых вариантах осуществления настоящее изобретение относится к соединению формулы B', как определено в целом и в классах и подклассах, описанных выше и здесь, в которой L2 не обозначает боронатное звено, когда R3 обозначает хлор и R1 обозначает фтор.
В некоторых вариантах осуществления изобретение относится к соединению B', в котором L2 обозначает -B(ORx)(ORy). В других вариантах осуществления одна или обе группы Rx и Ry обозначают водород. В других вариантах осуществления Rx и Ry вместе образуют в случае необходимости замещенное 5-6-членное кольцо. В других вариантах осуществления Rx и Ry вместе образуют 4,4,5,5-тетраметилдиоксаборолановое звено.
Как описано выше, подходящая удаляемая группа представляет собой радикал, который легко заменяется желаемым химическим звеном. Подходящие удаляемые группы известны в уровне техники, например, см., "Advanced Organic Chemistry," Jerry March, 5th Ed., pp. 351-357, John Wiley and Sons, N.Y. Такие удаляемые группы включают, но не ограничены ими, галоген, алкокси, сульфонилокси, в случае необходимости замещенный алкилсульфонил, в случае необходимости замещенный алкенилсульфонил, в случае необходимости замещенный арилсульфонил и диазоний. Примеры подходящих удаляемых групп включают хлор, йод, бром, фтор, метансульфонил (метилсульфонил), тозил, трифлат, нитро-фенилсульфонил (нозил) и бром-фенилсульфонил (брозил). В некоторых вар