Стабилизированные соединения эксендина-4
Иллюстрации
Показать всеВ данном изобретении предлагаются композиции, содержащие стабилизированный эксендин-4(1-39) и родственные соединения. В изобретении описаны стабилизированные агонисты эксендина-4, которые содержат, по меньшей мере, один модифицированный аминокислотный остаток, в частности в положении Asn28 молекулы эксендина-4(1-39). Изобретение также относится к способам получения и применения стабилизированных соединений эксендина, таким как для лечения диабета. 3 н. и 12 з.п. ф-лы, 9 ил., 2 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение относится к стабилизованным соединениям эксендина-4 и родственным молекулам. В одном аспекте изобретение относится к стабилизированным агонистам эксендина-4, которые содержат, по меньшей мере, один модифицированный аминокислотный остаток, в частности в положениях Gln13, Met14, Trp25 или Asn28 молекулы эксендина-4(1-39). Предпочтительными модификациями являются дезаминированные, гидролизованные, окисленные или изомеризованные продукты реакций определенных аминокислотных остатков, соответствующих тем же самым положениям в молекуле эксендина-4(1-39). Также предлагаются способы получения и применения стабилизированных соединений эксендина. Изобретение имеет широкий спектр применений и предлагает соединения эксендина-4, обладающие большей стабильностью по сравнению с предыдущими композициями эксендина-4.
УРОВЕНЬ ТЕХНИКИ
Ряд гормонов, которые понижают уровни глюкозы в крови, высвобождаются из слизистой оболочки желудочно-кишечного тракта в ответ на присутствие и поглощение питательных веществ в кишечнике. Гормоны включают гастрин, секретин, глюкозозависимый инсулинотропный полипептид (GIP) и глюкагон-подобный пептид-1 (GLP-1). Наиболее эффективным известным веществом является GLP-1 (Orskov, 1992, Diabetologia 35: 701-711). Глюкагон-подобный пептид 1 (GLP-1) является продуктом проглюкагона, пептида из 180 аминокислот (Drucker, 1998, Diabetes 47: 159-169). Полная последовательность проглюкагона содержит 29-аминокислотную последовательность глюкагона, 36- или 37-аминокислотную последовательность GLP-1 и 34-аминокислотную последовательность глюкагон-подобного пептида-2 (GLP-2), кишечнотропного пептида. GLP-1 имеет ряд функций. Он является физиологическим гормоном, который усиливает влияние на секрецию инсулина у здоровых людей и поэтому является гормоном инкретином. Кроме того, GLP-1 также снижает концентрации глюкагона, замедляет опорожнение желудка, стимулирует биосинтез (про)инсулина и усиливает чувствительность к инсулину (Nauck, 1997, Horm. Metab. Res. 47: 1253-1258). Пептид также повышает способность β-клеток распознавать и отвечать на глюкозу у субъектов с нарушенной толерантностью к глюкозе (Byrne, 1998, Eur. J. Clin. Invest. 28: 72-78). Инсулинотропное действие GLP-1 у людей увеличивает скорость исчезновения глюкозы частично вследствие повышенных уровней инсулина, а частично вследствие повышенной чувствительности к инсулину (D'Alessio, 1994, Eur. J. Clin. Invest. 28: 72-78). Это ставит GLP-1 на одно из первых мест в качестве многообещающего средства для лечения диабета типа II. Обнаружено, что активными фрагментами GLP-1 являются GLP-1(7-36) и GLP-1(7-37). Однако основной фармакологической проблемой в случае нативного GLP-1 является его короткое время полужизни. У человека и крыс GLP-1 быстро разрушается дипептидилпептидазой-IV (DPP-IV) до GLP-1(9-36)амида, действующего в качестве эндогенного антагониста рецептора GLP-1. Предложено несколько методик для того, чтобы обойти данную проблему, при этом в некоторых используют ингибиторы DPP-IV, а в других резистентные к DPP-IV аналоги GLP-1(7-36)амида.
Эксендины, другая группа пептидов, которые снижают уровни глюкозы в крови, имеют некоторое сходство последовательностей (53%) с GLP-1[7-36]NH2 (Goke et al., 1993, J. Biol. Chem. 268: 19650-55). Эксендины обнаружены в яде Helodermatidae или ядозубов. Эксендин-3 присутствует в яде Heloderma horridum, мексиканского ядозуба, а эксендин-4 присутствует в яде Heloderma suspectum, ядозуба желатье. Эксендин-4 отличается от эксендина-3 только по положениям два и три. кДНК, кодирующая белок-предшественник эксендина-4, 47-аминокислотный пептид, слитый с аминоконцом эксендина-4, клонирована и секвенирована (Pohl et al., 1998, J. Biol. Chem. 273: 9778-9784 и WО 98/35033).
Эксендин-4 является сильным агонистом рецептора GLP-1 на изолированных клетках инсулиномы крыс (Goke et al., 1993, J. Biol. Chem. 268: 19650-55). Эксендин-4, вводимый системно, снижает уровни глюкозы в крови на 40% у диабетических мышей db/db (WO99/07404). Недавно Grieg et al. (1999, Diabetologia 42: 45-50) показали длительное действие, понижающее уровень глюкозы в крови, при внутрибрюшинной инъекции эксендина-4 один раз в сутки диабетическим мышам ob/ob. В патенте США No. 5424286 описано, что значительная часть N-концевой последовательности необходима для того, чтобы сохранить инсулинотропное действие (эксендин-4(1-31) и
γ31-эксендин-4(1-31)), тогда как укороченный на N-конце эксендин (эксендин-4(9-39)) обладает ингибирующими свойствами.
Было предположено применение эксендина-3, эксендина-4 и агонистов эксендина для лечения сахарного диабета, снижения моторики желудка и замедления опорожнения желудка и предотвращения гипергликемии (патент США No. 5424286, WО 98/05351), а также для снижения потребления пищи (WО 98/30231). Были предложены способы получения новых соединений путем модификации нативных последовательностей эксендина. Один способ заключается в связывании липофильных заместителей с молекулой, например, как описано в WO 99/43708, в которой заявлены производные эксендина как раз с одним липофильным заместителем, связанным с C-концевым аминокислотным остатком.
Основной способ заключался в разработке аналогов эксендина, характеризующихся аминокислотными заменами и/или C-концевым укорочением нативной последовательности эксендина-4. Данный способ представлен соединениями, предложенными в WO 99/07404, WO 99/25727 и WO 99/25728.
В WO 99/07404 описаны агонисты эксендина, имеющие общую формулу I, которая определяет пептидную последовательность из 39 аминокислотных остатков с Gly Thr в положениях 4-5, Ser Lys Gln в положениях 11-13, Glu Glu Glu Ala Val Arg Leu в положениях 15-21, Leu Lys Asn Gly Gly в положениях 26-30, Ser Ser Gly Ala в положениях 32-35, и в которой оставшиеся положения могут быть заняты аминокислотными остатками эксендина дикого типа или могут быть заняты определенными аминокислотными заменами. Формула I не охватывает агонисты или аналоги эксендина, имеющие конкретные аминокислотные замены и/или являющихся конъюгатами, которые приведены в данном описании, такие как новые соединения desPro36-эксендин-4(1-39), эксендин-4(1-39)-K6 или desPro36-эксендин-4(1-39)-K6.
В WO 99/25727 раскрыты агонисты эксендина, имеющие общую формулу I, которая определяет пептидную последовательность от 28 до 38 аминокислотных остатков с Gly в положении 4 и Ala в положении 18, и в которой остальные положения могут быть заняты аминокислотными остатками эксендина дикого типа или могут быть заняты указанными аминокислотными заменами. Формула I не включает в себя последовательность пептида, имеющую Ser в качестве C-концевой аминокислоты, и агонисты или аналоги эксендина, имеющие конкретные делеции аминокислот и/или являющиеся конъюгатами, которые приведены в данном описании, такие как новые соединения desPro36-эксендин-4(1-39), эксендин-4(1-39)-K6 или desPro36-эксендин-4(1-39)-K6. Кроме того, формула II в WO 99/25727 определяет пептидную последовательность, сходную с последовательностью формулы I, но включая производные эксендина, имеющие C(1-10)алканольный или циклоалкилалканоильный заместитель на лизине в положении 27 или 28.
При лечении несоответствующих постпрандиальных уровней глюкозы в крови соединения вводят часто, например один, два или три раза в сутки.
В WO 99/25728 описаны агонисты эксендина, имеющие формулу I, которая определяет пептидную последовательность от 28 до 39 аминокислотных остатков с фиксированным Ala в положении 18 и в которой остальные положения могут быть заняты аминокислотными остатками эксендина дикого типа или могут быть заняты указанными аминокислотными заменами. Все указанные агонисты эксендина соответствовали укороченному аналогу эксендина, имеющему различную степень аминокислотных замен. Пептидные последовательности от 34 до 38 аминокислотных остатков не имеют Ser на C-конце. Пептидная последовательность из 39 аминокислотных остатков может иметь либо Ser, либо Tyr на C-конце, но не имеет других остатков. Агонисты или аналоги эксендина, имеющие конкретные делеции аминокислот и/или являющиеся конъюгатами согласно изобретению, описанному в данной публикации, не входят в формулу I. Кроме того, формула II определяет пептидную последовательность, сходную с последовательностью формулы I, но включая производные эксендина, имеющие C(1-10)-алканоильный или циклоалкилалканоильный заместитель на лизине в положении 27 или 28.
В WO 99/46283 (опубликована 16.09.99) описаны конъюгаты пептидов, содержащие фармакологически активный пептид X и стабилизирующую пептидную последовательность Z из 4-20 аминокислотных остатков, ковалентно связанную с X, при этом указанные конъюгаты характеризуются тем, что имеют увеличенное время полужизни по сравнению со временем полужизни X. X может представлять собой эксендин-4 или эксендин-3.
Было бы желательно иметь композиции эксендина, которые могут обеспечивать лучшую стабильность, чем стабильность предыдущих соединений. Кроме того, было бы желательно иметь композиции эксендина, которые могут не поддаваться деградации. Такие композиции были бы особенно полезны в условиях, когда предполагаются значительные периоды времени хранения и/или когда существует риск нежелательных реакций окисления, гидролиза или дезаминирования.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение в общем относится к стабилизированным соединениям эксендина-4 и родственным композициям. В одном аспекте изобретение относится к стабилизированным соединениям эксендина, в частности агонистам эксендина-4, которые содержат, по меньшей мере, один модифицированный аминокислотный остаток в положениях Gln13, Met14, Trp25 или Asn28 молекулы эксендина-4(1-39). Также предлагаются способы получения и применения стабилизированных композиций эксендина-4. Изобретение имеет широкий спектр применений, включая получение композиций эксендина-4 с лучшими свойствами стабильности и хранения по сравнению с предшествующими композициями эксендина-4 и родственными соединениями.
Авторы обнаружили, что можно стабилизировать соединения эксендина-4 и родственные композиции путем модификации в них отдельных аминокислот эксендина. Предпочтительными модификациями согласно изобретению являются дезаминированные, гидролизованные, окисленные или изомеризованные продукты реакций определенных аминокислотных остатков молекулы эксендина-4(1-39). Такие соединения легко можно получить с помощью одного или комбинации стандартных способов, включая воздействие на эксендин-4(1-39) фармакологически приемлемыми способами приготовления композиции, воздействуя на молекулу потенциально химически активными условиями, такими как контакт с водой, кислородом, светом, нагреванием или тому подобным, или иным образом обеспечивая условия, приводящие к спонтанной или полуспонтанной деградации аминокислот, соответствующих, по меньшей мере, одной из Gln13, Met14, Trp25 или Asn28 молекулы эксендина-4(1-39).
Практическое осуществление предпочтительных вариантов изобретения обеспечивает существенные преимущества. Например, применение изобретения в состоянии обеспечить стабилизированные соединения эксендина-4, которые отличаются более надежной активностью, в частности, на протяжении более длительных периодов хранения. Такие стабилизированные молекулы эксендина-4 и родственные композиции могут способствовать медицинским применениям, включая клинические исследования и другие применения, благодаря обеспечению более воспроизводимой и постоянной активности агониста. Данный отличительный признак изобретения особенно важен в том случае, когда необходимо большое количество препаратов эксендина-4 (партии). То есть, стабилизируя соединения эксендина-4 и родственные молекулы согласно изобретению, в настоящее время можно повысить соответствие партий между собой.
Кроме того, применение изобретения теперь может обеспечить постоянное дозирование композиций эксендина-4 и родственных молекул. То есть, стабилизированные соединения согласно изобретению менее подвержены деградации и, следовательно, могут обеспечивать более надежную терапевтическую активность. Данный отличительный признак изобретения особенно важен в том случае, когда требуется получить эксендин-4 и родственные молекулы, обладающие сравнительно постоянной активностью или хорошей стабильностью при среднем или крупномасштабном получении.
Фраза «соединение эксендина-4 или родственная молекула», включая множественные формы, означает эксендин-4(1-39) или его вариант, аналог или производное, которые определены в данной заявке. Иллюстративными примерами являются эксендин-4(1-39) и его производные, которые содержат делецию примерно от 1 до 5 аминокислот, которые соответствуют положениям 34, 35, 36, 37 или 38 эксендина-4. Необязательно такие производные, кроме того, содержат, по меньшей мере, один пептид Z, который определен в данном описании. Такие соединения или молекулы «стабилизируют» согласно изобретению (например, стабилизированное соединение эксендина-4(1-39)) посредством модификации, по меньшей мере, одного из аминокислотных остатков: Gln13, Met14, Trp25 или Asn28 молекулы эксендина-4(1-39). Предпочтительно модифицируют одну или две таких аминокислоты, которые приведены в описании, хотя для предполагаемого применения может подходить большее количество аминокислот.
Соответственно, в одном варианте осуществления изобретения предлагается соединение, которое включает в себя, по меньшей мере, один стабилизированный эксендин-4(1-39), предпочтительно один, два или три эксендина-4(1-39), предпочтительно один такой стабилизированный эксендин-4(1-39). В одном варианте соединение содержит:
a) делецию 0-5 аминокислот в положениях, соответствующих положениям 34-38 эксендина-4(1-39),
b) необязательно, по меньшей мере, одну пептидную последовательность Z, содержащую 4-20 аминокислотных единиц, ковалентно связанную с указанным соединением; и, по меньшей мере, один из следующих остатков:
i) остаток Asn, имеющий дезаминированную боковую цепь, остаток Asn, имеющий гидролизованную боковую цепь или структурный изомер остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленный остаток метионина, соответствующий положению 14 эксендина-4,
iii) окисленный остаток триптофана, соответствующий положению 25 эксендина-4,
iv) дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4,
и его фармацевтически приемлемую соль или сольват.
В одном варианте вышеуказанного соединения стабилизированный эксендин-4(1-39) содержит, по меньшей мере, один остаток L-аминокислоты или, по меньшей мере, один остаток D-аминокислоты. Альтернативно, соединение содержит комбинации L- и D-аминокислотных остатков.
В другом аспекте данное изобретение относится к соединению, которое включает в себя, по меньшей мере, одну молекулу стабилизированного эксендина-4(1-39), предпочтительно две, три или четыре молекулы стабилизированного эксендина-4(1-39), более предпочтительно одну такую молекулу стабилизированного эксендина-4(1-39). В одном варианте соединение содержит, по меньшей мере, один из остатков:
i) остаток Asn, имеющий дезаминированную боковую цепь, остаток Asn, имеющий гидролизованную боковую цепь, или структурный изомер остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленный остаток метионина, соответствующий положению 14 эксендина-4,
iii) окисленный остаток триптофана, соответствующий положению 25 эксендина-4,
iv) дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4;
и его фармацевтически приемлемую соль или сольват.
Кроме того, предлагаются фармацевтически приемлемые композиции, которые содержат, по меньшей мере, одну, предпочтительно две, три или четыре молекулы стабилизированного эксендина-4(1-39), более предпочтительно одно из таких соединений. Примеры таких композиций приведены ниже.
В другом аспекте изобретения предлагается способ получения композиции стабилизированного эксендина-4 или родственной молекулы, которые указаны в данном описании. В одном варианте способ включает в себя, по меньшей мере, одну из следующих стадий:
a) получение эксендина-4(1-39) или его варианта, аналога или производного; и
b) инкубацию эксендина-4(1-39) или его варианта, аналога или производного в условиях, достаточных для введения в него, по меньшей мере, одной из следующих аминокислот:
i) остатка Asn, имеющего дезаминированную боковую цепь, остатка Asn, имеющего гидролизованную боковую цепь, или структурного изомера остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленного остатка метионина, соответствующего положению 14 эксендина-4,
iii) окисленного остатка триптофана, соответствующего положению 25 эксендина-4,
iv) дезаминированного или гидролизованного Gln, соответствующего положению 13 эксендина-4; и
ее фармацевтически приемлемой соли или сольвата.
Часто будет предпочтительно получать молекулы стабилизированного эксендина-4 согласно изобретению синтетически или полусинтетически. Пример такого способа описан ниже и включает в себя использование методики синтеза пептидов Меррифилда.
В конкретных вариантах указанные выше способы, кроме того, включают в себя стадию выявления присутствия или отсутствия, по меньшей мере, одной из аминокислот (i)-(iv). Альтернативно или дополнительно способ может включать в себя идентификацию, по меньшей мере, одной из аминокислот (i)-(iv) в композиции. Способы выявления и идентификации модифицированных аминокислот обсуждаются ниже.
В другом варианте изобретения охарактеризован способ получения стабилизированного соединения эксендина-4 и родственных молекул, раскрытых в данном описании. Типичные способы включают в себя, по меньшей мере, одну из следующих стадий:
a) получение эксендина-4(1-39) или его варианта, аналога или производного,
b) осуществление контакта эксендина-4(1-39) или его варианта, аналога или производного, по меньшей мере, с одним фармацевтически приемлемым носителем или наполнителем для получения смеси; и
c) инкубацию смеси в условиях, достаточных для введения в соединение, по меньшей мере, одной из следующих аминокислот:
i) остатка Asn, имеющего дезаминированную боковую цепь, остатка Asn, имеющего гидролизованную боковую цепь, или структурного изомера остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленного остатка метионина, соответствующего положению 14 эксендина-4,
iii) окисленного остатка триптофана, соответствующего положению 25 эксендина-4,
iv) дезаминированного или гидролизованного Gln, соответствующего положению 13 эксендина-4; и
ее фармацевтически приемлемой соли или сольвата.
Кроме того, такой способ также может включать в себя стадию выявления присутствия или отсутствия, по меньшей мере, одного из аминокислотных остатков (i)-(iv). Альтернативно или дополнительно способ может включать в себя идентификацию, по меньшей мере, одной из аминокислот (i)-(iv) в композиции.
В другом аспекте изобретение относится к способу стабилизации эксендина-4(1-39) или его варианта, аналога или производного. В одном варианте способ включает в себя, по меньшей мере, одну из следующих стадий:
a) получение эксендина-4(1-39) или его варианта, производного или аналога; и
b) инкубацию эксендина-4(1-39) или его варианта, производного или аналога в условиях, достаточных для введения в него, по меньшей мере, одного из следующих аминокислотных остатков:
i) остатка Asn, имеющего дезаминированную боковую цепь, остатка Asn, имеющего гидролизованную боковую цепь, или структурного изомера остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленного остатка метионина, соответствующего положению 14 эксендина-4,
iii) окисленного остатка триптофана, соответствующего положению 25 эксендина-4,
iv) дезаминированного или гидролизованного Gln, соответствующего положению 13 эксендина-4; и
его фармацевтически приемлемой соли или сольвата.
В другом аспекте изобретение относится к способу лечения диабета типа 1 или типа 2, синдрома резистентности к инсулину, нарушенной толерантности к глюкозе (IGT), ожирения, нарушений питания, гипергликемии, метаболических расстройств и заболевания желудка. В одном варианте способ включает в себя введение терапевтически эффективного количества, по меньшей мере, одного стабилизированного соединения эксендина-4 или родственных молекул, раскрытых в данном описании.
Изобретение также относится к способу лечения патологических состояний, связанных с повышенными уровнями глюкозы в крови. В одном варианте способ включает в себя введение терапевтически эффективного количества, по меньшей мере, одного из стабилизированных соединений эксендина-4 или родственных молекул, раскрытых в данном описании.
Также предлагается способ регуляции уровней глюкозы в крови. В одном варианте способ включает в себя введение терапевтически эффективного количества, по меньшей мере, одного из стабилизированных соединений эксендина-4 или родственных молекул, раскрытых в данном описании.
Изобретение также относится к способу регуляции опустошения желудка. В одном варианте способ включает в себя введение терапевтически эффективного количества, по меньшей мере, одного из стабилизированных соединений эксендина-4 или родственных молекул, раскрытых в данном описании.
Данное изобретение также относится к способу стимуляции высвобождения инсулина у млекопитающего. В одном варианте способ включает в себя введение эффективного инсулинотропного количества, по меньшей мере, одного из стабилизированных соединений эксендина-4, раскрытых в данном описании.
Кроме того, предлагается способ снижения уровня глюкозы в крови у млекопитающего. В одном варианте способ включает в себя введение некоторого количества, по меньшей мере, одного из стабилизированных соединений эксендина-4 или родственных молекул, описанных в данной заявке, в количестве, эффективном для снижения уровня глюкозы в крови у указанного млекопитающего.
Изобретение также относится к способу снижения уровня липидов в плазме у млекопитающего. В одном примере способ включает в себя введение некоторого количества, по меньшей мере, одного из стабилизированных соединений эксендина-4, описанных в данной заявке, в количестве, эффективном для снижения уровня липидов в плазме у указанного млекопитающего.
Также предлагается способ снижения уровня смертности и заболеваемости после инфаркта миокарда у млекопитающего. В одном варианте способ включает в себя введение некоторого количества, по меньшей мере, одного из стабилизированных соединений эксендина-4, раскрытых в данном описании, в количестве, эффективном для снижения смертности и заболеваемости после инфаркта миокарда.
Также предлагается способ стимуляции высвобождения инсулина у млекопитающего. В одном варианте способ включает в себя введение эффективного инсулинотропного количества, по меньшей мере, одного из стабилизированных соединений эксендина-4, предложенных в данном изобретении.
Предпочтительно, млекопитающим, указанным в каждом из вышеупомянутых способов, является примат, предпочтительно человек, нуждающийся в лечении.
ФИГУРЫ
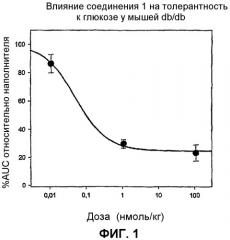
На фиг.1 показано влияние соединения 1 на толерантность к глюкозе у мышей.
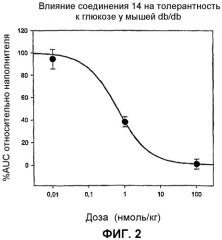
На фиг.2 показано влияние соединения 14 на толерантность к глюкозе у мышей.
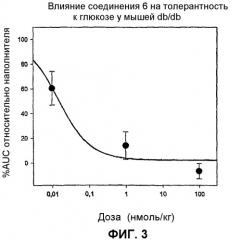
На фиг.3 показано влияние соединения 6 на толерантность к глюкозе у мышей.
На фиг.4 показано влияние соединения 7 на толерантность к глюкозе у мышей.
На фиг.5 показано влияние соединения 1 на толерантность к глюкозе у мышей.
На фиг.6 показано влияние соединения 5 на толерантность к глюкозе у мышей.
На фиг.7 показано влияние соединения 2 на толерантность к глюкозе у мышей.
На фиг.8 изображено влияние соединений 1, 8, 9, 10 и 11 на уровни глюкозы в крови у мышей.
На фиг.9 показаны последовательности соединения 1 (des Pro36-эксендин-4(1-39)-K6) и стабилизированных соединений соединения 1, а именно соединений 2, 3, 4, 5, 6, 7, 11, 12, 13 и 14, а также стабилизированных соединений эксендина-4(1-39), а именно соединений 8, 9 и 10.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как обсуждалось, изобретение относится к стабилизированным агонистам эксендина, которые содержат, по меньшей мере, один модифицированный аминокислотный остаток, в частности, в положениях Gln13, Met14, Trp25 или Asn28 молекулы эксендина-4(1-39). Предпочтительными модификациями являются дезаминированные, гидролизованные, окисленные или изомеризованные продукты реакций определенных аминокислотных остатков молекулы эксендина-4(1-39). Также предлагаются способы получения и применения стабилизированных соединений эксендина.
Предпочтительные стабилизированные соединения эксендина-4(1-39) и их фармацевтически приемлемые соли содержат:
a) делецию 0-5 аминокислот в положениях, соответствующих положениям 34-38 эксендина-4,
b) необязательно, по меньшей мере, одну пептидную последовательность Z, содержащую 4-20 аминокислотных единиц, ковалентно связанную с указанным вариантом; и, по меньшей мере, один из следующих остатков:
i) остаток Asn, имеющий дезаминированную боковую цепь, остаток Asn, имеющий гидролизованную боковую цепь или структурный изомер остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленный остаток метионина, соответствующий положению 14 эксендина-4,
iii) окисленный остаток триптофана, соответствующий положению 25 эксендина-4,
iv) дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4,
и его фармацевтически приемлемую соль или сольват.
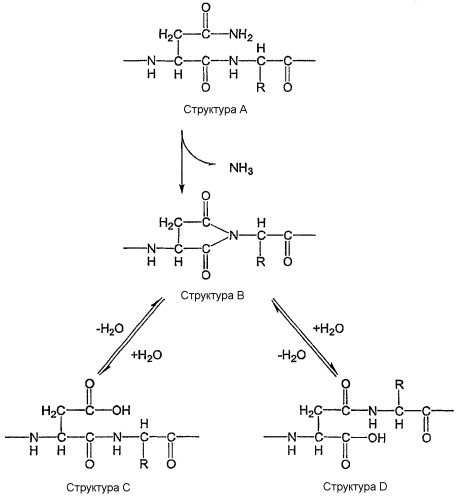
В одном варианте остатком Asn является остаток α-аспартата (Asp) или β-аспартата (изоаспартил) или остатком Asn является циклический имид. В другом варианте окисленным остатком метионина является метионинилсульфоксид или метионинилсульфон. В тех вариантах, в которых циклический имид получен из остатка Asp или Gln, циклический продукт в данном описании иногда называют аспартимидом или глутимидом, соответственно.
Альтернативно или дополнительно окисленный остаток триптофана включает окисленную 3H-индол-3-ильную группу. Другие примеры включают окисленный остаток триптофана, который представляет собой N-формилкинуренин (NFK), 3-гидроксикинуренин (3-OH-KYN), гидрокситриптофан (HTRP) или кинуренин (KYN).
В вариантах, в которых стабилизированное соединение эксендина или родственная композиция содержит, по меньшей мере, один пептид Z и, предпочтительно, один-два таких пептида, Z содержит, по меньшей мере, одну аминокислотную единицу Lys, обычно примерно от 4 до 20 аминокислотных единиц Lys, предпочтительно примерно 6 аминокислотных единиц Lys.
В вариантах, в которых стабилизированное соединение эксендина-4 содержит пептид Z, данный пептид ковалентно связан пептидной связью. Например, Z ковалентно связан со стабилизированным соединением эксендина-4(1-39) по C-концевой карбонильной функции.
Более конкретные стабилизированные соединения эксендина-4(1-39) согласно изобретению представлены следующими последовательностями:
des Pro36[Asp28]эксендин-4(1-39),
des Pro36[изоAsp28]эксендин-4(1-39),
des Pro36[циклический имид28]эксендин-4(1-39),
des Pro36[Met(О)14]эксендин-4(1-39),
des Pro36[Trp(O2)25]эксендин-4(1-39),
des Pro36[Met(O)14, Asp28]эксендин-4(1-39),
des Pro36[Met(O)14, изоAsp28]эксендин-4(1-39),
des Pro36[Met(O)14, циклический имид28]эксендин-4(1-39),
des Pro36[Met(O)14, Trp(O2)25]эксендин-4(1-39),
des Pro36 [Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39),
des Pro36[Met(О)14, Trp(О2)25, изоAsp2B]эксендин-4(1-39),
des Pro36[Met(О)14, Trp(О2)25, циклический имид28]эксендин-4(1-39)
и их фармацевтически приемлемая соль или сольват.
Что касается любого из вышеуказанных соединений эксендина-4(1-39), то соединения, кроме того, могут содержать дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4.
В одном варианте вышеуказанных соединений каждая последовательность связана на N- или C-конце со следующей группой: -Lys6-NH2. Предпочтительно группа связана с C-концом последовательности.
Дополнительные конкретные стабилизированные соединения эксендина-4(1-39) включают в себя следующие последовательности:
H-(Lys)6-des Pro36[Asp28]эксендин-4(1-39)-Lys6-NH2,
des Asp28Pro36, Pro37, Pro38эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5 des Pro36, Pro37, Pro38[Asp28]эксендин-4(1-39)-NH2,
des Pro36, Pro37, Pro38[Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36[циклический имид28]эксендин-4(1-39)-Lys6-NH2,
des Pro36, Pro37, Pro38[циклический имид28]эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[циклический имид28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[циклический имид28]эксендин-4(1-39)-NH2,
des Pro36, Pro37, Pro38[циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6 des Pro36, Pro37, Pro38[циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36[Trp(O2)25, Asp28]эксендин-4(1-39)-Lys6-NH2,
H-des Asp28Pro36, Pro37, Pro38[Trp(O2)25]эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Trp(O2)25, Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Trp(O2)25, Asp28]эксендин-4(1-39)-NH2,
des Pro36, Pro37, Pro38[Trp(O2)25, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Trp(O2)25, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Trp(O2)25, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36[Trp(O2)25, циклический имид28]эксендин-4(1-39)-Lys6-NH2,
des циклический имид28 Pro36, Pro37, Pro38[Trp(O2)25]эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Trp(O2)25, циклический имид28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Trp(O2)25, циклический имид28]эксендин-4(1-39)-
NH2,
des Pro36, Pro37, Pro38[Trp(O2)25, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Trp(O2)25, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Trp(O2)25, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36[Met(O)14, Asp28]эксендин-4(1-39)-Lys6-NH2,
des Met(О)14Asp28Pro36, Pro37, Pro38эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, Asp28]эксендин-4(1-39)-NH2,
des Pro36, Pro37, Pro38[Met(O)14, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5 des Pro36, Pro37, Pro38[Met(O)14, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Lys6-des Pro36[Met(O)14, циклический имид28]эксендин-4(1-39)-Lys6-NH2,
des Pro36, Pro37, Pro38[Met(O)14, циклический имид28]эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, циклический имид28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, циклический имид28]эксендин-4(1-39)-
NH2,
des Pro36, Pro37, Pro38[Met(O)14, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-Lys6-des Pro36[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39)-Lys6-NH2,
H-des Asp28 Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25]эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39)-NH2,
des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39)-(Lys)6-NH2,
H-Lys6-des Pro36[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)-Lys6-NH2,
des циклический имид28 Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25]эксендин-4(1-39)-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)-NH2,
des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-(Lys)6-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
H-Asn-(Glu)5-des Pro36, Pro37, Pro38[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)-(Lys)6-NH2,
и их фармацевтически приемлемая соль или сольват.
Что касается любого из вышеуказанных соединений эксендина-4(1-39), то соединения, кроме того, могут содержать дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4.
Как уже обсуждалось, отличительным признаком изобретения являются стабилизированные соединения эксендина-4(1-39), которые содержат, по меньшей мере, один из остатков:
i) остаток Asn, имеющий дезаминированную боковую цепь, остаток Asn, имеющий гидролизованную боковую цепь, или структурный изомер остатка Asp, где остаток Asn или Asp соответствует положению 28 эксендина-4,
ii) окисленный остаток метионина, соответствующий положению 14 эксендина-4,
iii) окисленный остаток триптофана, соответствующий положению 25 эксендина-4,
iv) дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4,
и их фармацевтически приемлемые соли или сольваты.
Соли и сольваты
Также предполагаются фармацевтически приемлемые соли или сольваты таких соединений. Примеры таких стабилизированных соединений эксендина-4(1-39) включают в себя следующие последовательности:
[Asp28]эксендин-4(1-39),
[изоAsp28]эксендин-4(1-39),
[циклический имид28]эксендин-4(1-39),
[Met(O)14]эксендин-4(1-39),
[Trp(O2)25]эксендин-4(1-39),
[Met(O)14, Asp28]эксендин-4(1-39),
[Met(O)14, изоAsp28]эксендин-4(1-39),
[Met(O)14, циклический имид28]эксендин-4(1-39),
[Met(O)14, Trp(O2)25]эксендин-4(1-39),
[Trp(O2)25, Asp28]эксендин-4(1-39),
[Trp(O2)25, изоAsp28]эксендин-4(1-39),
[Trp(O2)25, циклический имид28]эксендин-4(1-39),
[Met(O)14, Trp(O2)25, Asp28]эксендин-4(1-39),
[Met(O)14, Trp(O2)25, изоAsp28]эксендин-4(1-39), или
[Met(O)14, Trp(O2)25, циклический имид28]эксендин-4(1-39)
и их фармацевтически приемлемые соли или сольваты.
Что касается любого из вышеуказанных соединений эксендина-4(1-39), то соединения, кроме того, могут содержать дезаминированный или гидролизованный Gln, соответствующий положению 13 эксендина-4.
L- и D-варианты
Стабилизированные соединения эксендина-4(1-39), предложенные в данном описании, включая их варианты, аналоги и производные, могут характеризоваться, по меньшей мере, одной аминокислотой в L- или D-конфигурации (или как в D-, так и в L-формах). В вариантах, в которых, по меньшей мере, один из аминокислотных остатков дезаминирован, стабилизированное соединение эксендина-4(1-39) может иметь, по меньшей мере, один аминокислотный остаток в L-форме, по