Композиция и способ регулирования активности естественных клеток-киллеров
Иллюстрации
Показать всеНастоящее изобретение относится к иммунологии и биотехнологии. Предложен способ получения антитела для связывания с NK-клетками, которое перекрестно реагирует с продуктами гена KIR2DL1 и KIR2DL2/3 и нейтрализует ингибиторную активность таких KIR. Указанный способ включает отбор таких антител, которые перекрестно реагируют по меньшей мере с продуктами гена KIR2DL1 и KIR2DL2/3, способны восстанавливать лизис NK клетками Cw3+ или Cw4+ клеток-мишеней и связываются с клетками NK или полипептидом KIR примата. Описаны антитела, полученные таким способом, и их производные, где антитело сшито с токсином, радионуклеидом, распознаваемой группировкой, твердым носителем или ПЭГ. Использование изобретения обеспечивает получение единичного типа антител, который регулирует активность клеток NK разного типа, обеспечивает усиление их цитотоксичности, что может найти применение в терапии, для повышения у индивидуумов активности или цитотоксичности клеток NK без предварительного определения у индивидуума типа HLA. 3 н. и 4 з.п. ф-лы, 13 ил., 4 табл.
Реферат
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к антителам, фрагментам антител и их производным, которые перекрестно реагируют с двумя или более ингибиторными рецепторами, имеющимися на поверхности естественных клеток-киллеров (клеток NK), и усиливают цитотоксичность клеток NK у индивидуумов-млекопитающих или в биологическом образце. Изобретение относится также к способам получения таких антител, фрагментов, вариантов и производных; к фармацевтическим композициям, их содержащим; и к применению таких молекул и композиций, в частности в терапии, для повышения активности или цитотоксичности клеток NK у индивидуумов.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Клетки - естественные убийцы, киллеры (natural killer cells, NK cells) - это субпопуляция лимфоцитов, участвующих в нетрадиционном (ненаследуемом) иммунитете. Клетки NK могут быть получены различными известными в данной области способами - такими, как получение из проб крови, цитоферез, сборы и т.д.
Характеристики и биологические свойства клеток NK включают экспрессию поверхностных антигенов, в том числе CD16, CD56 и/или CD57; отсутствие на клеточной поверхности комплекса Т-клеточных рецепторов (TCR) альфа/бета или гамма/дельта; способность связываться с клетками, которые не экспрессируют «свои» антигены главного комплекса тканевой совместимости и антиген гистосовместимости (антигены MHC/HLA), и убивать эти клетки путем активации специфических цитолитических ферментов; способность убивать опухолевые клетки или другие больные клетки, экспрессирующие активирующий клетки NK рецептор-лиганд; способность высвобождать цитокины, стимулирующие или ингибирующие иммунную реакцию; и способность претерпевать множественные циклы клеточного деления и производить дочерние клетки с биологическими свойствами, одинаковыми со свойствами родительских клеток.
В контексте настоящего изобретения «активные» клетки NK означают биологически активные клетки NK, конкретнее клетки NK, способные лизировать клетки-мишени. Например, «активная» клетка NK способна убивать клетки, которые экспрессируют активирующий клетки NK рецептор-лиганд и не могут экспрессировать «свои» антигены MHC/HLA (KIR-несовместимые клетки).
На основе биологических свойств клеток NK в данной области были предложены разнообразные терапевтические и вакцинные стратегии, рассчитанные на модуляцию клеток NK. Однако активность клеток NK регулируется сложным механизмом, который включает как стимулирующие, так и ингибирующие сигналы. Поэтому для эффективной терапии, опосредованной клетками NK, могут потребоваться и стимуляция этих клеток, и нейтрализация ингибирующих сигналов.
Существует негативная регуляция клеток NK специфическими для 1 класса главного комплекса тканевой совместимости (major histocompatibility complex, MHC) ингибиторными рецепторами (Кärrе и др., 1986; Öhlén и др., 1989). Эти специфические рецепторы связываются с полиморфными детерминантами молекул I класса MHC или антигеном гистосовместимости (HLA), находящимися на других клетках, и ингибируют лизис клетками NK. У человека группы аллелей HLA I класса распознаются некоторыми представителями семейства рецепторов, называемых «киллерные lg-подобные рецепторы» (killer Ig-like receptors, KIR).
Рецепторы KIR - это большое семейство рецепторов, имеющихся на определенных подтипах лимфоцитов, в том числе на клетках NK. Номенклатура KIR основана на числе внеклеточных доменов (KIR2D или KIR3D) и на том, длинный ли (KIR2DL или KIR3DL) или короткий (KIR2DS или KIR3DS) цитоплазматический хвост. У людей наличие или отсутствие данного KIR меняется от одной клетки NK к другой в пределах популяции клеток NK, имеющихся у данного индивидуума. У человеческой популяции имеется также относительно высокий уровень полиморфизма молекул KIR, причем определенные молекулы KIR имеются у некоторых индивидуумов, но не у всех. Некоторые продукты гена KIR стимулируют активность лимфоцитов, связываясь с подходящим лигандом. Все KIR с подтвержденной стимулирующей активностью имеют короткий цитоплазматический хвост с заряженным трансмембранным участком, который ассоциирован с адапторной молекулой, имеющей иммуностимулирующий лейтмотив (immunostimulatory motif, ITAM). Другие продукты гена KIR по своей природе являются ингибирующими. Все KIR с подтвержденной ингибиторной активностью имеют длинный цитоплазматический хвост, и оказывается, что они взаимодействуют с различными подтипами антигенов HLA, в зависимости от подтипа KIR. Во внутрицитоплазматической части ингибиторных KIR проявляются один или несколько ингибиторных лейтмотивов, которые используют фосфатазы. Известные ингибиторные рецепторы KIR включают представителей подсемейств KIR2DL и KIR3DL. Рецепторы KIR, имеющие два домена Ig (KIR2D), идентифицируют аллотипы HLA-C: KIR2DL2 (первоначально его обозначали р58.2) или близко родственный продукт гена KIR2DL3 распознают эпитоп, общий в аллотипах группы 2 HLA-C (Сw1, 3, 7 и 8), тогда как KIR2DL1 (р58.1) распознает эпитоп, общий в аллотипах реципрокной группы 1 HLA-C (Cw2, 4, 5 и 6). Распознавание KIR2DL1 определяется наличием остатка Lys в положении 80 аллелей HLA-C. Распознавание KIR2DL2 и KIR2DL3 определяется наличием остатка Asn в положении 80. Важно то, что подавляющее большинство аллелей HLA-C имеет в положении 80 либо остаток Asn, либо остаток Lys. Один KIR с тремя доменами Ig - KIR3DL1 (р70) распознает эпитоп, общий в аллелях HLA-Bw4. Наконец, гомодимер молекул с тремя доменами Ig - KIR3DL2 (р140) распознает HLA-A3 и HLA-A11.
Хотя ингибиторные KIR и другие ингибиторные рецепторы I класса (Moretta и др., 1997; Valiante и др., 1997а; Lanier, 1998) могут совместно экспрессироваться клетками NK, в наборе клеток NK каждого данного индивидуума имеются клетки, экспрессирующие одиночный KIR, и поэтому соответствующие клетки NK блокируются только клетками, экспрессирующими специфическую группу аллелей I класса.
Было установлено, что популяция клеток NK или клоны, которые не соответствуют KIR, т.е. популяция клеток NK, которые экспрессируют KIR, не совместимые с молекулами HLA хозяина, являются наиболее возможными медиаторами анти-лейкемического действия трансплантата, наблюдаемого при аллогенной трансплантации (Ruggeri и др., 2002). Одним из путей воспроизведения этого эффекта у данного индивидуума могло бы быть использование реагентов, блокирующих взаимодействие KIR/HLA.
Было показано, что специфические к KIR2DL1 моноклональные антитела блокируют взаимодействие KIR2DL1 с аллелями Cw4 (или подобными им) (Moretta и др., 1993). Были также описаны моноклональные антитела к KIR2DL2/3, блокирующие взаимодействие KIR2DL2/3 с аллелями HLACw3 (или подобными им) (Moretta и др., 1993). Однако применение таких реагентов в клинических ситуациях потребовало бы разработки двух терапевтических моноклональных антител (monoclonal antibodies, mAb) для лечения всех пациентов, вне зависимости от того, экспрессировал ли данный пациент аллели HLA-C 1-го класса или 2-го класса. Более того, перед принятием решения о том, какой тип терапевтических антител использовать, необходимо было бы предварительно определить, какой тип HLA экспрессировал каждый пациент. Это привело бы к сильному удорожанию лечения.
Watzl и др. (// Tissue Antigens. 2000. Т.56. С.240) получили перекрестно реагирующие антитела, распознающие множественные изотипы KIR, но эти антитела не обладали усиливающим действием на активность клеток NK. Spaggiara G.M. и др. (// Blood. 2002. Т.100. С.4098-4107) выполнили опыты с использованием многочисленных моноклональных антител к различным KIR. Было показано, что один из этих типов антител, а именно NKVSF1, распознает общий эпитоп в CD158a (KIR2DL1), CD158b (KIR2DL2) и р50.3 (KIR2DS4). Не было высказано предположение, что NKVSF1 может усиливать активность клеток NK, и не предполагалось, что эти антитела могут быть использованы как терапевтическое средство. Поэтому практические и эффективные подходы к модуляции активности клеток до сих пор не были доступны в данной области, и для этого все еще требуется специфическое по отношению к аллелям HLA воздействие с помощью специфических реагентов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение ныне предусматривает новые антитела, композиции и способы, которые преодолевают существующие в настоящее время трудности в активации клеток NK и обеспечивают выгодные особенности и преимущества. В одном приводимом в качестве примера аспекте изобретение предусматривает единичный тип антител, усиливающий активацию человеческих клеток NK фактически у всех людей. Более конкретно, изобретение предусматривает новые специфические антитела, перекрестно реагирующие с различными группами ингибиторных KIR и нейтрализующие их ингибиторные сигналы, что приводит к усилению цитотоксичности у тех клеток NK, которые экспрессируют такие ингибиторные рецепторы KIR. Эта способность к перекрестной реакции со многими продуктами генов KIR позволяет эффективно использовать антитела настоящего изобретения для повышения активности клеток NK у большинства человеческих индивидуумов, без затруднений и затрат, связанных с предварительным определением у индивидуума типа HLA.
В первом аспекте изобретение предусматривает антитела, фрагменты антител и производные любых из них, причем указанное антитело, фрагмент или производное перекрестно реагирует, по меньшей мере, с двумя ингибиторными рецепторами KIR на поверхности клеток NK, нейтрализует ингибиторные сигналы клеток NK и усиливает активность клеток NK. Более предпочтительно антитело связывается с общим детерминантом рецепторов KIR2DL человека. Еще конкретнее, антитела согласно настоящему изобретению связываются, по меньшей мере, с рецепторами KIR2DL1, KIR2DL2 и KKIR2DL3. Для целей настоящего изобретения термин «KIR2DL2/3» относится к любому из рецепторов KIR2DL2 и KIR2DL3 или к ним обоим. Эти два рецептора имеют очень высокую степень гомологии, являются, по-видимому, аллельными формами одного и того же гена и в данной области считаются взаимозаменяемыми. Поэтому для целей настоящего изобретения считается, что KIR2DL2/3 - это одиночная молекула ингибиторного KIR, и поэтому антитела, которые перекрестно реагируют только с KIR2DL2 и KIR2DL3 и не реагируют ни с каким из других ингибиторных рецепторов KIR, не входят в круг охвата настоящего изобретения.
Антитела согласно настоящему изобретению специфически ингибируют связывание молекул МНС или HLA, по меньшей мере, с двумя ингибиторными рецепторами KIR и способствуют активности клеток NK. Под термином «нейтрализуют ингибиторную активность KIR», как он использован здесь, подразумеваются оба вида активности. Способность антител согласно настоящему изобретению «способствовать активности клеток NK», «способствовать цитотоксичности клеток NK», «помогать клеткам NK», «усиливать активность клеток NK», «усиливать цитотоксичность клеток NK» или «придавать силу клеткам NK» в контексте настоящего изобретения означает, что антитела дают возможность клеткам NK экспрессировать на своей поверхности ингибиторный рецептор KIR, чтобы они были способны лизировать клетки, экспрессирующие на своей поверхности соответствующий лиганд для этого конкретного ингибиторного рецептора KIR (например, конкретный антиген HLA). В конкретном аспекте изобретение предусматривает антитела, которые специфически ингибируют связывание молекул HLA-C с рецепторами KIR2DL1 и KIR2DL2/3. В другом конкретном аспекте изобретение предусматривает антитела, которые способствуют активности клеток NK in vivo.
Вследствие того, что, по меньшей мере, примерно у 90% человеческой популяции имеется, по меньшей мере, один рецептор KIR2DL1 или KIR2DL2/3, наиболее предпочтительные антитела настоящего изобретения способны помогать активности клеток NK, направленной на большинство клеток, ассоциированных с аллотипами HLA-C, соответственно с аллотипами HLA-C группы 1 и аллотипами HLA-C группы 2. Так, композиции настоящего изобретения могут быть применены для активации или усиления клеток NK у большинства человеческих индивидуумов, обычно у приблизительно 90% человеческих индивидуумов или больше. Поэтому единственная композиция с антителами в соответствии с настоящим изобретением может быть применена для лечения большинства человеческих индивидуумов, и необходимость определять аллельные группы или применять коктейли антител возникает редко.
Изобретение впервые демонстрирует, что можно получить перекрестно-реактивные и нейтрализующие антитела к ингибиторным KIR и что такие антитела обеспечивают эффективную активацию клеток NK в широком диапазоне человеческих групп.
Поэтому конкретный объект настоящего изобретения составляют антитела, причем указанные антитела специфически связываются и с человеческим рецептором KIR2DL1, и с человеческим рецептором KID2DL2/3 и отменяют опосредованное этими KIR ингибирование цитотоксичности клеток NK. В одном из вариантов осуществления настоящего изобретения антитела конкурируют с моноклональными антителами DF-200, продуцируемыми гибридомами DF-200. Указанные антитела, конкурирующие с антителами DF-200, сами могут не являться антителами DF-200.
В другом варианте осуществления антитела конкурируют с моноклональными антителами NKVSF1, причем антитела, конкурирующие с NKVSF1, могут (но не обязательно) не являться антителами NKVSF1.
В другом варианте осуществления антитела конкурируют с антителами 1-7F9.
Предпочтительно указанными антителами являются химерные антитела, «гуманизированные» антитела или человеческие антитела.
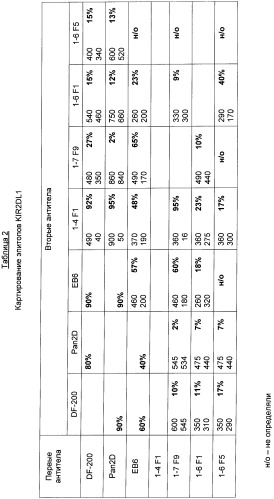
Термин «конкурирует с», когда он относится к конкретным моноклональным антителам (например, DF-200, NKVSF1, 1-7F9, ЕВ6, GL183), означает, что антитела конкурируют с моноклональными антителами (например, DF-200, NKVSF1, 1-7F9, ЕВ6, GL183) в анализе на связывание с использованием либо рекомбинантных молекул KIR, либо экспрессируемых на поверхности молекул KIR. Например, если антитела снижают связывание DF-200 с молекулой KIR в анализе на связывание, антитела «конкурируют» с DF-200. Антитела, которые «конкурируют» с DF-200, могут конкурировать с DF-200 за связывание с человеческим рецептором KIR2DL1, человеческим рецептором KIR2DL2/3 или с обоими человеческими рецепторами - и KIR2DL1, и KIR2DL2/3.
В предпочтительном варианте осуществления изобретение предусматривает антитела, связывающиеся с человеческими рецепторами - и с KIR2DL1, и с KIR2DL2/3, отменяющие опосредованное этими KIR ингибирование цитотоксичности клеток NK и конкурирующие с DF-200, 1-7F9 или NKVSF1 за связывание с человеческим рецептором KIR2DL1, человеческим рецептором KIR2DL2/3 или с обоими человеческими рецепторами - и KIR2DL1, и KIR2DL2/3. По усмотрению, этими антителами не являются NKVSF1. По усмотрению, указанными антителами являются химерные, человеческие или «гуманизированные» антитела.
В другом варианте осуществления изобретение предусматривает антитела, связывающиеся с человеческими рецепторами - и с KIR2DL1, и с KIR2DL2/3, отменяющие опосредованную этими KIR цитотоксичность клеток NK и конкурирующие с ЕВ6 за связывание с человеческим рецептором KIR2DL1, конкурирующие с GL183 за связывание с человеческим рецептором KIR2DL2/3, или же конкурирующие и с ЕВ6 за связывание с человеческим рецептором KIR2DL1, и с GL183 за связывание с человеческим рецептором KIR2DL2/3. По усмотрению, указанными антителами не являются NKVSF1; по усмотрению, указанными антителами не являются DF-200. По усмотрению, указанными антителами являются химерные, человеческие или «гуманизированные» антитела.
В полезном аспекте изобретение предусматривает антитела, конкурирующие с DF-200 и различающие на молекуле KIR в значительной степени такие же или в основном такие же, или просто такие же, как на моноклональных антителах DF-200, эпитопы или «эпитопные центры», связывающиеся с ними или имеют к ним иммуноспецифичность. Предпочтительно указанной молекулой KIR может быть человеческий рецептор KIR2DL1 или человеческий рецептор KIR2DL2/3.
Конкретный объект изобретения составляют антитела, причем указанные антитела связываются с общим детерминантом, присутствующим в человеческих рецепторах и KIR2DL1, и KIR2DL2/3, и отменяют опосредованное этими KIR ингибирование цитотоксичности клеток NK. Антитела более специфично связываются по существу с таким же эпитопом на KIR, как и на моноклональных антителах DF-200, продуцируемых гибридомами DF-200, или на антителах NKVSF1, продуцируемых гибридомами NKVSF1, причем антитела не являются NKVSF1.
В предпочтительной форме осуществления антителами согласно настоящему изобретению являются моноклональные антитела. Наиболее предпочтительными антителами согласно настоящему изобретению являются моноклональные антитела DF-200, продуцируемые гибридомами DF-200.
Продуцирующие антитела DF-200 гибридомы были депонированы в коллекции культур CNCM под идентификационным шифром "DF-200" (DF200), регистрационным номером CNCM I-3224, зарегистрированы 10 июня 2004 г., Collection Nationale de Cultures de Microorganismes, Institut Pasteur, 25, Rue du Docteur Roux, F-75724 Paris Cedex 15, France. Антитела NKVSF1 производятся фирмой Serotec (Cergy Sainte-Christophe, France), № по каталогу МСА2243. Антитела NKVSF1 здесь носят также обозначение pan2D mAb.
Изобретение предусматривает также функциональные фрагменты и производные описанных здесь антител, имеющие по существу такую же антигенную специфичность и активность (т.е. те, которые могут перекрестно реагировать с родительскими антителами и которые усиливают цитотоксическую активность клеток NK, экспрессирующих ингибиторные рецепторы KIR), включающие (но не ограничивающиеся ими) фрагмент Fab, фрагмент Fab'2, иммуноадгезин, димерные антитела (diabody), CDR и ScFv. Кроме того, антитела согласно настоящему изобретению могут быть гуманизированными, человеческими или химерными.
Изобретение предусматривает также производные антител, представляющие собой антитела по настоящему изобретению, конъюгированные или ковалентно сшитые с токсином, радионуклидом, распознаваемой частью молекулы (например, с флуорофором) или с твердым носителем.
Изобретение предусматривает также фармацевтические композиции, содержащие антитела, как они раскрыты выше, их фрагменты или производные любых из них. Соответственно с этим изобретение относится также к применению антител, как они здесь раскрыты, в способе производства лекарственного средства. В предпочтительных вариантах осуществления указанные лекарственное средство или фармацевтическая композиция предназначены для лечения рака или другого пролиферативного расстройства, инфекции, или для применения в трансплантации.
В другом варианте осуществления изобретение предусматривает композицию, содержащую антитела, которые связываются с продуктами, по меньшей мере, двух различных генов человеческих ингибиторных рецепторов KIR, причем указанные антитела способны нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в клетках NK, экспрессирующих, по меньшей мере, один из указанных двух различных человеческих ингибиторных рецепторов KIR, при этом указанные антитела включены внутрь липосом. По усмотрению, указанная композиция может содержать дополнительное вещество, выбранное из молекулы нуклеиновой кислоты для доставки генов в целях генной терапии; молекулы нуклеиновой кислоты для доставки антисмысловой РНК, интерферирующей РНК (RNAi) или малой интерферирующей РНК (siRNA) для супрессирования гена в клетках NK; или токсина или лекарства для адресованного уничтожения клеток NK, дополнительно включенное в указанные липосомы.
Изобретение предусматривает также способы регулирования активности клеток NK человека in vitro, ex vivo или in vivo, состоящие в контактировании клеток NK человека с эффективным количеством антител настоящего изобретения, фрагментов таких антител, производных каждого из них или с фармацевтической композицией, содержащей, по меньшей мере, одно из упомянутого. Предпочтительные способы состоят во введении эффективного количества фармацевтических композиций согласно настоящему изобретению и направлены на повышение цитотоксической активности клеток NK человека, наиболее предпочтительно ex vivo или in vivo, у индивидуума, имеющего рак, инфекционное заболевание или иммунное заболевание.
В дальнейших аспектах изобретение предусматривает гибридомы, которые содержат:
(a) В-клетки из хозяина-млекопитающего (обычно хозяин-млекопитающее, не является человеком), иммунизированные антигеном, содержащим эпитоп, имеющийся на полипептиде ингибиторного KIR, слитые с
(b) бессмертными клетками (например, клетками миеломы), причем указанные гибридомы продуцируют моноклональные антитела, связывающиеся, по меньшей мере, с двумя различными человеческими ингибиторными рецепторами KIR и способные, по меньшей мере, существенно нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующие указанные, по меньшей мере, два различных человеческих ингибиторных рецептора KIR.
По усмотрению, указанные гибридомы могут не продуцировать моноклональные антитела NKVSF1. Предпочтительно, чтобы указанные антитела связывались с рецепторами KIR2DL1 и KIR2DL2/3. Предпочтительно указанные антитела связываются с общим детерминантом, присутствующим на KIR2DL1 и KIR2DL2/3. Предпочтительно указанные гибридомы продуцируют антитела, которые ингибируют связывание молекулы аллели HLA-C, имеющей в положении 80 остаток Lys, с человеческим рецептором KIR2DL1 и связывание молекулы аллели HLA-C, имеющей в положении 80 остаток Asn, с человеческими рецепторами KIR2DL2/3. Предпочтительно, чтобы указанные гибридомы продуцировали антитела, связывающиеся по существу с таким же эпитопом, как и моноклональные антитела DF-200, продуцируемые гибридомами DF-200, либо на KIR2DL1, либо на KIR2DL2/3, либо и на KIR2DL1, и на KIR2DL2/3. Пример таких гибридом - DF-200.
Изобретение предусматривает также способы продуцирования антител, которые перекрестно реагируют с несколькими продуктами гена KIR2DL и которые нейтрализуют ингибиторную активность таких KIR, причем способ включает следующие этапы:
а) иммунизацию млекопитающего (не человека) иммуногеном, содержащим полипептид KIR2DL;
b) получение от иммунизированного млекопитающего антител, причем антитела связываются с полипептидом KIR2DL;
c) отбор среди антител этапа (b) тех, которые перекрестно реагируют, по меньшей мере, с двумя различными продуктами гена KIR2DL; и
d) отбор среди антител этапа (с) тех, которые усиливают активность клеток NK.
В одном из вариантов осуществления настоящего изобретения указанным млекопитающим (не человеком) является трансгенное животное, сконструированное так, чтобы экспрессировать набор человеческих антител (например, это млекопитающее (не человек), содержащее локусы человеческого иммуноглобулина и делеции в нативном гене иммуноглобулина, - такое, как Xenomouse™ (Abgenix - Fremont, CA, USA), или млекопитающее (не человек), содержащее минилокус из генов, кодирующих человеческий Ig, - такое как HuMab-mouse™ (Medarex - Princeton, NJ, USA)). По усмотрению, способ дополнительно включает отбор антител, которые связываются с клетками NK или полипептидом KIR примата, преимущественно обезьяны Cynomolgus. По усмотрению, изобретение может дополнительно включать способ оценки антител, где продуцированные согласно приведенному выше способу антитела вводят примату, предпочтительно обезьяне Cynomolgus, причем предпочтительно обезьяну наблюдают на предмет наличия или отсутствия признаков токсичности антител.
Изобретение также предусматривает способ получения антител, которые связываются, по меньшей мере, с двумя различными продуктами генов человеческих ингибиторных рецепторов KIR, причем указанные антитела способны нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующих указанные, по меньшей мере, два различных продукта генов человеческих ингибиторных рецепторов KIR, при этом указанный способ включает следующие этапы:
a) иммунизацию млекопитающего (не человека) иммуногеном, содержащим полипептид ингибиторного KIR;
b) получение антител от иммунизированного животного, причем антитела связываются с полипептидом KIR;
c) отбор антител этапа (b), которые перекрестно реагируют, по меньшей мере, с двумя различными продуктами генов человеческих ингибиторных рецепторов KIR, и
d) отбор антител этапа (с), способных нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующих указанные, по меньшей мере, два различных продукта генов человеческих ингибиторных рецепторов KIR, причем порядок этапов (с) и (d) может быть по усмотрению изменен, и по усмотрению может быть повторено один или более раз любое число этапов.
Предпочтительно, чтобы использованный для иммунизации полипептид ингибиторного KIR был полипептидом KIR2DL и отобранные в этапе (с) антитела перекрестно реагировали, по меньшей мере, с KIR2DL1 и KIR2DL2/3. Предпочтительно, чтобы указанные антитела распознавали общий детерминант, имеющийся, по меньшей мере, на двух различных продуктах генов рецепторов KIR; наиболее предпочтительно указанными KIR являются KIR2DL1 и KIR2DL2/3. По усмотрению, указанный способ дополнительно включает отбор антител, связывающихся с клетками NK или полипептидом KIR примата, предпочтительно обезьяны Cynomolgus. По усмотрению, изобретение дополнительно включает способ оценки антител, где продуцированные согласно приведенному выше способу антитела вводят примату, предпочтительно обезьяне Cynomolgus, причем предпочтительно обезьяну наблюдают на предмет наличия или отсутствия признаков токсичности антител.
По усмотрению, в описанных выше способах антитела, отобранные в этапах (с) или (d), не являются NKVSF1. Предпочтительно, чтобы антитела, полученные на этапе (b), в описанных выше способах представляли собой моноклональные антитела. Предпочтительно, чтобы антитела, отобранные в этапе (с) в описанных выше способах, ингибировали связывание аллельной молекулы HLA-C, имеющей в положении 80 остаток Lys, с человеческим рецептором KIR2DL1 и связывание аллельной молекулы HLA-C, имеющей в положении 80 остаток Asn, с человеческими рецепторами KIR2DL2/3. Предпочтительно, чтобы антитела, отобранные в этапе (d) в описанных выше способах, вызывали усиление цитотоксичности клеток NK - например, любое существенное усиление или, по меньшей мере, усиление цитотоксичности клеток NK, по меньшей мере, на 5%, 10%, 20%, 30% или более - например, усиление адресованной цитотоксичности клеток NK, по меньшей мере, приблизительно на 50%, (например, по меньшей мере, приблизительно на 60%, по меньшей мере, приблизительно на 70%, по меньшей мере, приблизительно на 80%, по меньшей мере, приблизительно на 85%, по меньшей мере, приблизительно на 90% или, по меньшей мере, на 95% (то есть усиление цитотоксичности клеток NK, например, на приблизительно от 65% до 100%)). Предпочтительно, чтобы антитела связывались по существу с тем же эпитопом, как и моноклональное антитело DF-200, на KIR2DL1 и/или KIR2DL2/3. По усмотрению, указанные способы также или альтернативно содержат дополнительный этап создания фрагментов отобранных моноклональных антител, создания производных отобранных моноклональных антител (например, путем конъюгации с радионуклидом, цитотоксическим агентом, репортерной молекулой или подобными им) или создания производных фрагментов антител - либо полученных из таких моноклональных антител, либо таких, которые содержат (аминокислотные) последовательности, соответствующие последовательностям таких моноклональных антител.
Изобретение далее предусматривает способ получения антител, связывающихся, по меньшей мере, с двумя различными продуктами генов человеческих ингибиторных рецепторов KIR, причем указанные антитела способны нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующих указанные, по меньшей мере, два различных продукта генов человеческих ингибиторных рецепторов KIR, при этом способ включает следующие этапы:
а) отбор, из библиотеки или набора, моноклональных антител или фрагмента моноклональных антител, которые перекрестно реагируют, по меньшей мере, с двумя различными продуктами гена человеческого ингибиторного рецептора KIR2DL, и
b) отбор антител стадии (а), способных нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующих указанные, по меньшей мере, два различных продукта гена человеческого ингибиторного рецептора KIR2DL. Предпочтительно, чтобы антитела связывались с общим детерминантом, присутствующим в рецепторах KIR2DL1 и KIR2DL2/3. По усмотрению, антитела, отобранные на этапе (b), могут не являться NKVSF1. Предпочтительно антитела, отобранные в этапе (b), ингибируют связывание аллельной молекулы HLA-C, имеющей в положении 80 остаток Lys, с человеческим рецептором KIR2DL1 и связывание аллельной молекулы HLA-C, имеющей в положении 80 остаток Asn, с человеческими рецепторами KIR2DL2/3. Предпочтительно, чтобы антитела, отобранные в этапе (b), вызывали усиление цитотоксичности клеток NK - например, любое существенное усиление или, по меньшей мере, усиление цитотоксичности клеток NK, по меньшей мере, на 5%, 10%, 20%, 30% или более - например, усиление адресованной цитотоксичности клеток NK, по меньшей мере, приблизительно на 50% (например, усиление цитотоксичности клеток NK, по меньшей мере, приблизительно на 60%, по меньшей мере, приблизительно на 70%, по меньшей мере, приблизительно на 80%, по меньшей мере, приблизительно на 85%, по меньшей мере, приблизительно на 90% или, по меньшей мере, на 95% (то есть, например, приблизительно на 65-100%)). Предпочтительно, чтобы антитела связывались по существу с тем же эпитопом, как и моноклональное антитело DF-200, на KIR2DL1 и/или KIR2DL2/3. По усмотрению, способ содержит дополнительный этап создания фрагментов отобранных моноклональных антител, создания производных отобранных моноклональных антител или создания производных фрагментов отобранных моноклональных антител.
Кроме того, изобретение предусматривает способ получения антител, которые связываются, по меньшей мере, с двумя различными продуктами генов человеческих ингибиторных рецепторов KIR, причем указанные антитела способны нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующих указанные, по меньшей мере, два различных продукта генов человеческих ингибиторных рецепторов KIR, при этом способ включает следующие этапы:
a) культивирование гибридом согласно настоящему изобретению в условиях, допускающих продуцирование моноклональных антител, и
b) отделение моноклональных антител от гибридом. По усмотрению, способ может содержать дополнительный этап создания фрагментов указанных моноклональных антител, создания производных моноклональных антител или создания производных таких фрагментов моноклональных антител. Предпочтительно, чтобы антитела связывались с общим детерминантом, присутствующим на KIR2DL1 и/или KIR2DL2/3.
Настоящим изобретением предусматривается также способ получения антител, которые связываются, по меньшей мере, с двумя различными продуктами генов человеческих ингибиторных рецепторов KIR, причем указанные антитела способны нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в популяции клеток NK, экспрессирующих указанные, по меньшей мере, два различных продукта генов человеческих ингибиторных рецепторов KIR, при этом указанный способ включает следующие этапы:
a) выделение из гибридом согласно настоящему изобретению нуклеиновой кислоты, кодирующей указанные моноклональные антитела;
b) по усмотрению, модификацию нуклеиновой кислоты таким образом, чтобы получить модифицированную нуклеиновую кислоту, содержащую последовательность, которая кодирует модифицированное или видоизмененное антитело, содержащее аминокислотную последовательность, которая соответствует функциональной последовательности моноклонального антитела или по существу подобна ей (например, идентична такой последовательности, по меньшей мере, приблизительно на 65%, по меньшей мере, приблизительно на 75%, по меньшей мере, приблизительно на 85%, по меньшей мере, приблизительно на 90%, по меньшей мере, приблизительно на 95% (так, как приблизительно на 70-99%)), выбранное из «гуманизированного» антитела, химерного антитела, одноцепочечного антитела, иммунореактивного фрагмента антитела или из слитого белка, содержащего такой иммунореактивный фрагмент;
c) вставку нуклеиновой кислоты или модифицированной нуклеиновой кислоты (или родственной нуклеиновой кислоты, кодирующей такую же аминокислотную последовательность) в экспрессирующий вектор, причем кодируемое антитело или кодируемый фрагмент антитела способен экспрессироваться, когда экспрессирующий вектор присутствует в клетке-хозяине, выращенной в подходящих условиях;
d) трансфицирование клетки-хозяина экспрессирующим вектором, причем клетка-хозяин не продуцирует иным способом белок иммуноглобулина;
e) культивирование трансфицированной клетки-хозяина в условиях, которые вызывают экспрессию антитела или фрагмента антитела; и
f) выделение антитела или фрагмента антитела, продуцированного указанной клеткой-хозяином. Предпочтительно, чтобы антитело связывалось с общим детерминантом, присутствующим на KIR2DL1 и KIR2DL2/3.
Следует принять во внимание, что изобретение также предусматривает композицию, содержащую антитела, связывающиеся, по меньшей мере, с двумя различными продуктами генов человеческих ингибиторных рецепторов KIR, причем указанные антитела способны нейтрализовать опосредованное KIR ингибирование цитотоксичности клеток NK в клетках NK, экспрессирующих хотя бы один из указанных двух различных человеческих ингибиторных рецепторов KIR, при этом антитела присутствуют в количестве, эффективном для заметного усиления цитотоксичности клеток NK у пациента или в биологическом образце, содержащем клетки NK; и фармацевтически приемлемый носитель или наполнитель. Предпочтительно, чтобы антитела связывались с общим детерминантом, имеющимся на KIR2DL1 и KIR2DL2/3. Композиция может по усмотрению дополнительно содержать второе терапевтическое средство, выбранное, например, из иммуномодулирующего средства, гормонального средства, химиотерапевтического средства, антиангиогенного средства, апоптозного средства, второго антитела, связывающегося с ингибиторным рецептором KIR и ингибирующего его действие, анти-инфекционного средства, адресующего средства или вспомогательного средства. Полезные иммуномодулирующие средства могут быть выбраны из IL-1 альфа, IL-1бета, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-11, IL-12, IL-13, IL-15, IL-21, TGF-бета, GM-CSF, M-CSF, G-CSF, TNF-альфа, TNF-бета, LAF, TCGF, BCGF, TRF, BAF, BDG, MP, LIF, OSM, TMF, PDGF, ИФН-альфа, ИФН-бета или ИФН-гамма. Примеры указанных химиотерапевтических средств включают алкилирующие агенты, антиметаболиты, цитотоксичные антибиотики, адриамицин, дактиномицин, митомицин, карминомицин, дауномицин, доксорубицин, тамоксифен, таксол, таксотер, винкристин, винбластин, винорелбин, этопозид (VP-16), 5-фторурацил (5FU), цитозин-арабинозид, циклофосфамид, тиотера, метотрексат, камптотецин, актиномицин-D, митомицин С, цисплатин (цис-DDP), аминоптерин, комбретастатин(ы), другие алкалоиды барвинка и их производные или предшественники. Примеры гормональных средств включают лейпрорелин, гозерелин, трипторелин, бузерелин, тамоксифен, торемифен, флутамид, нилутамид, кипротерон, бикалутамид, анастрозол, экземестан, летрозол, фадрозол медрокси, хлормадинон, мегестрол, другие агонисты Гонадотропин-высвобождающего гормона (LHRH, Luteinizing Hormone Releasing Hormone), другие анти-эстрогены, другие анти-андрогены, другие ингибиторы ароматазы и другие прогестагены. Предпочтительно, чтобы вторым антителом, связывающимся с ингибиторным рецептором KIR и ингибирующим его действие, было антитело или его фрагмент, которые связываются с таким эпитопом ингибиторного рецептора KIR, который отличается от эпитопа, связываемого указанным антителом, связывающимся с общим детерминантом, имеющимся, по меньшей мере, на двух различных продуктах гена человеческого ингибиторного рецептора KIR.
Далее изобретение предусматривает способ заметного усиления активности клеток NK у нуждающегося в этом пациента, включающий этап введения пациенту композиции в соответствии с настоящим изобретением. Пациентом, нуждающимся в усилении активности клеток NK, может быть любой пациент, имеющий заболевание или расстройство, при которых такое усиление может способствовать терапевтическому действию, усиливать и/или индуцировать терапевтическое действие (или способствует терапевтическому действию, усиливает и/или индуцирует терапевтическое действие, по меньшей мере, у значительной части пациентов с заболеванием или нарушением, или у лиц по существу с такими же характеристиками, как у пациентов, как может быть определено, например, клиническими испытаниями). Пациент, нуждающийся в таком лечении, может иметь, например, р