Способы лечения или профилактики аутоиммунных заболеваний с помощью соединений 2,4-пиримидиндиамина
Иллюстрации
Показать всеИзобретение относится к 2,4-пиримидиндиаминам, таким как N4-(4-Хлор-3-метоксифенил)-5-фтор-N2-[3-(N-метиламино)карбонилметиленоксифенил]-2,4-пиримидиндиамин, N4-(3-хлор-4-метоксикарбонилметиленоксифенил)-5-фтор-N2-[3-(N-метиламино)карбонилметиленоксифенил] -2,4-пиримидиндиамин, N4-[3-хлор-4-(N-метиламино)карбонилметиленоксифенил]-5-фтор-N2-[3-(N-метиламино)карбонилметиленоксифенил]-2,4-пиримидиндиамин, N4-[3-хлор-4-(2-гидроксиэтиленокси)фенил]-5-фтор-N2-[3-(N-метиламино)карбонилметиленоксифенил]-2,4-пиримидиндиамин, и другим соединениям, указанным в п.1 формулы настоящего изобретения в качестве ингибиторов Syk-киназы, а также к фармацевтическим композициям на их основе и их применению. Соединения могут найти применение для лечения таких аутоимуных заболеваний, как системная красная волчанка, ревматоидный артрит и др. 5 н. и 7 з.п. ф-лы, 16 ил. 11 табл.
Реферат
1. Перекрестные ссылки на «родственные» заявки
Согласно § 119(e) части 35 Свода Законов США (United States Code - U.S.C.) настоящая заявка является превалирующей по отношению к следующим заявкам: регистрационный номер 60/399 673, дата подачи 29 июля 2002 года; регистрационный номер 60/443 949, дата подачи 31 января 2003 года и регистрационный номер 60/452 339, дата подачи 6 марта 2003 года.
2. Область изобретения
Настоящее изобретение относится в целом к соединениям 2,4-пиримидинаминов, фармацевтическим композициям, содержащим указанные соединения, промежуточным соединениям и синтетическим способам производства указанных соединений и способам применения этих соединений и композиций в различных областях, например при лечении или профилактике аутоиммунных заболеваний и/или симптомов, связанных с этими заболеваниями.
3. Предпосылки к созданию изобретения
Перекрестное связывание Fc-рецепторов, таких, например, как рецептор с высоким сродством к IgE (FcεRI) и/или рецептор с высоким сродством к IgG (FcγRI), активирует сигнальный каскад в мастоцитах, базофилах и других иммунных клетках, в результате чего происходит выделение химических медиаторов, ответственных за различные неблагоприятные события. Например, такое перекрестное связывание приводит к выделению преформированных медиаторов реакций анафилактической гиперчувствительности I типа (немедленная реакция), таких как гистамин, из зон накопления в гранулах посредством дегрануляции. Оно также приводит к синтезу и выделению других медиаторов, включая лейкотриены, простагландины и факторы активации тромбоцитов (PAF), которые играют важную роль в воспалительных реакциях. Дополнительные медиаторы, которые синтезируются и выделяются в результате перекрестного связывания Fc-рецепторов, включают в себя цитокины и оксид азота.
Сигнальный каскад или каскады, активированные в результате перекрестного связывания Fc-рецепторов, как, например, FcεRI и/или FcγRI, включает в себя набор клеточных протеинов. Одними из наиболее важных распространителей межклеточных сигналов являются тирозинкиназы. Важной тирозинкиназой, участвующей в установлении сигнальных путей трансдукции, связанных с перекрестным связыванием рецепторов FcεRI и/или FcγRI, а также других каскадов передачи сигналов, является Syk-киназа (см. обзор в Valent et al., 2002, Intl. J. Hematol. 75(4):257-362).
Поскольку медиаторы, выделенные в результате перекрестного связывания рецепторов FcεRI и FcγRI, являются ответственными за проявление многочисленных неблагоприятных явлений или играют в этом важную роль, крайне желательно иметь в наличии соединения, способные ингибировать сигнальный каскад или каскады, ответственные за их выделение. Более того, ввиду критической роли Syk-киназы в сигнальном каскаде (каскадах) этих и других рецепторов наличие соединений, способных ингибировать Syk-киназу, также очень желательно.
4. Краткое описание изобретения
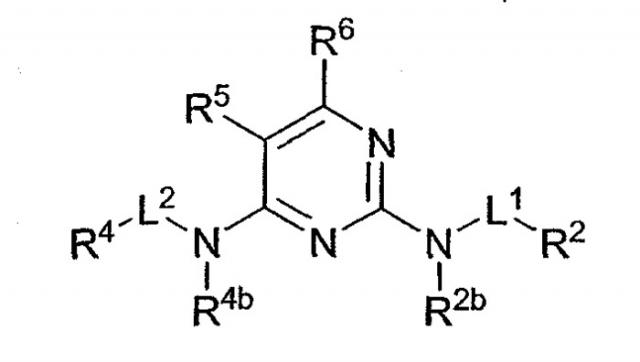
Одним из аспектов настоящего изобретения является предложение новых соединений 2,4-пиримидинаминов, которые, как будет подробно описано ниже, проявляют биологическую активность в ряде направлений. Эти соединения в целом состоят из 2,4-пиримидинаминного «ядра», которое имеет следующую структуру и систему нумерации:
Указанные соединения согласно настоящему изобретению замещаются в месте присоединения азота (N2) к атому C2 с целью образования вторичного амина и могут быть далее замещены в одном или нескольких положениях: в месте присоединения азота (N4) к атому C4, C5 и/или C6. При замещении в узле N4 заместитель образует вторичный амин. Заместитель в узле N2, а также возможные заместители в других положениях могут сильно отличаться по природе и физико-химическим свойствам. Например, заместитель (заместители) может представлять собой разветвленный, неразветвленный или циклический алкил, разветвленный, неразветвленный или циклический гетероалкил или комбинацию этих групп. Эти группы замещения могут в дальнейшем быть замещены, как подробно описано ниже.
Заместители N2 и/или N4 могут присоединяться непосредственно к соответствующим атомам азота или могут быть отделены от соответствующих атомов азота посредством линкеров, которые могут быть одинаковыми или различными. Природа линкеров может широко варьироваться и может включать в себя практически любую комбинацию атомов или групп, подходящую для разделения одной части молекулы от другой. Например, линкером может являться мост из ациклического углеводорода (например, насыщенный или ненасыщенный алкен-, как, например, метан-, этан-, этен-, пропан-, 1-пропен-, бутан-, 1-бутен-, 2-бутен, 1,3-бутадиен- и им подобные), мост из моноциклического или полициклического углеводорода (например, 1,2-бензол-, 2,3-нафталин- и им подобные), простой ациклический гетероатомный мост или гетероалкилдиильный мост (например,-О -, -S-, -S-O-, -NH-, -PH-, -C(O)-, -C(O)NH-, -S(O)-, -S(O)2-, -S(O)NH-, -S(O)2NH-, -O-CH2-, -CH2-O-CH2-, -O-CH=CH-CH2- и им подобные), моноциклический или полициклический гетероарильный мост (например, 3,4-фуран-, пиридин-, тиофен-, пиперидин-, пиперазин-, пиразидин-, пирролидин- и им подобные) или комбинации перечисленных мостов.
Заместители в положениях N2, N4, C5 и/или C6, а также потенциальные линкеры могут в дальнейшем быть замещены одной или несколькими идентичными или различными группами замещения. Природа этих групп замещения может меняться в широких пределах. Неограниченный ряд примеров подходящих групп замещения включает в себя разветвленные, неразветвленные и циклические алкилы, моно- и полициклические арилы, разветвленные, неразветвленные и циклические гетероалкилы, моно- и полициклические гетероарилы, галогенидуглеводороды, разветвленные, неразветвленные и циклические галогенидалкилы, гидроксилы, оксогруппы, триоксогруппы, разветвленные, неразветвленные и циклические алкоксигруппы, разветвленные, неразветвленные и циклические галогенидалкоксигруппы, трифторметоксигруппы, моно- и полициклические арилоксигруппы, моно- и полициклические гетероарилоксигруппы, эфиры, спирты, сульфиды, тиоэфиры, сульфанилы (тиолы), имины, азогруппы, азиды, амины (первичные, вторичные и третичные), нитрилы (любые изомеры), цианаты (любые изомеры), тиоцианаты (любые изомеры), нитрозогруппы, нитрогруппы, диазы, сульфоксиды, сульфонилы, сульфоновые кислоты, сульфамиды, сульфоноамиды, эфиры сульфаминовой кислоты, альдегиды, кетоны, карбоновые кислоты, сложные эфиры, амиды, амидины, формадины, аминокислоты, ацетилены, карбаматы, лактоны, лактамы, глюкозиды, глюконуриды, сульфоны, кетали, ацетали, тиокетали, оксимы, оксаминовые кислоты, эфиры оксаминовых кислот и т.д., а также комбинации указанных групп. Группы замещения, имеющие функциональную реакционноспособность, могут быть защищенными или незащищенными, что хорошо известно из предшествующих работ.
В одном из иллюстрационных примеров соединения 2,4-пиримидинаминов согласно настоящему изобретению представляют собой соединения с нижеприведенной структурной формулой (I):
включая их соли, гидраты, сольваты и N-оксиды, в которой структурные звенья L1 и L2, каждое в отдельности независимо друг от друга, выбраны из групп, содержащих прямую связь и линкер;
R2 выбран из группы, содержащей (C1-C6) алкил, который может быть замещен одной или несколькими идентичными или различными группами R8; (C3-C8) циклоалкил, который может быть замещен одной или несколькими идентичными или различными группами R8; циклогексил, который может быть замещен одной или несколькими идентичными или различными группами R8; циклогетероалкил с 3-8 членами, который может быть замещен одной или несколькими идентичными или различными группами R8; (C5-C15) арил, который может быть замещен одной или несколькими идентичными или различными группами R8; фенил, который может быть замещен одной или несколькими идентичными или различными группами R8 и гетероарил с 5-15 членами, который может быть замещен одной или несколькими идентичными или различными группами R8;
R4 выбран из группы, содержащей водород, (C1-C6) алкил, который может быть замещен одной или несколькими идентичными или различными группами R8; (C3-C8) циклоалкил, который может быть замещен одной или несколькими идентичными или различными группами R8; циклогексил, который может быть замещен одной или несколькими идентичными или различными группами R8; циклогетероалкил с 3-8 членами, который может быть замещен одной или несколькими идентичными или различными группами R8; (C5-C15) арил, который может быть замещен одной или несколькими идентичными или различными группами R8; фенил, который может быть замещен одной или несколькими идентичными или различными группами R8; и гетероарил с 5-15 членами, который может быть замещен одной или несколькими идентичными или различными группами R8;
R5 выбран из группы, содержащей R6, (C1-C6) алкил, который может быть замещен одной или несколькими идентичными или различными группами R8; (C1-C4) алканил, который может быть замещен одной или несколькими идентичными или различными группами R8; (C2-C4) алкенил, который может быть замещен одной или несколькими идентичными или различными группами R8 и (C2-C4) алкинил, который может быть замещен одной или несколькими идентичными или различными группами R8;
Каждая из групп R6 независимо выбрана из группы, содержащей водород, электроотрицательную группу, -ORd, -SRd, (C1-C3) галогенидалкилоксигруппу, (C1-C3) пергалогенидоалкилоксигруппу, -NRcRc, галоген, (C1-C3) галогенидалкил, (C1-C3) пергалоидоалкил, -CF3, -CH2CF3, -CF2CF3, -CN, -NC, -OCN, -SCN, -NO, -NO2, -N3, -S(O)Rd, -S(O)2Rd, -S(O)2ORd, -S(O)NRcRc; -S(O)2NRcRc, -OS(O)Rd, -OS(O)2Rd, -OS(O)2ORd, -OS(O)NRcRc, -OS(O)2NRcRc, -C(O)Rd, -C(O)ORd, -C(O)NRcRc, -C(NH)NRcRc, -OC(O)Rd, -SC(O)Rd, -OC(O)ORd, -SC(O)ORd, -OC(O)NRcRc, -SC(O)NRcRc, -OC(NH)NRcRc, -SC(NH)NRcRc, -[NHC(O)]nRd, -[NHC(O)]nORd, -[NHC(O)]nNRcRc и -[NHC(NH)]nNRcRc, (C5-C10) арил с возможным замещением одной или несколькими идентичными или различными группами R8, фенил с возможным замещением одной или несколькими идентичными или различными группами R8, (C6-C16) арилалкил с возможным замещением одной или несколькими идентичными или различными группами R8, 5-10-членный гетероарил с возможным замещением одной или несколькими идентичными или различными группами R8 и 6-16-членный гетероарилалкил с возможным замещением одной или несколькими идентичными или различными группами R8;
R8 выбран из группы, содержащей Ra, Rb, в которой группа Ra может быть замещена одной или несколькими идентичными или различными группами Ra или Rb, группа -ORa может быть замещена одной или несколькими идентичными или различными группами Ra или Rb, -B(ORa)2, -B(NRcRc)2, -(CH2)m-Rb, -(CHRa)m-Rb, -O-(CH2)m-Rb, -S-(CH2)m-Rb, -O-CHRaRb, -O-CRa(Rb)2, -O-(CHRa)m-Rb,
-O-(CH2)m-CH[(CH2)mRb]Rb, -S-(CHRa)m-Rb, -C(O)NH-(CH2)m-Rb,
-C(O)NH-(CHRa)m-Rb, -O-(CH2)m-C(O)NH-(CH2)m-Rb,
-S-(CH2)m-C(O)NH-(CH2)m-Rb, -O-(CHRa)m-C(O)NH-(CHRa)m-Rb,
-S-(CHRa)m-C(O)NH-(CHRa)m-Rb, -NH-(CH2)m-Rb, -NH-(CHRa)m-Rb,
-NH[(CH2)mRb], -N[(CH2)mRb]2, -NH-C(O)-NH-(CH2)m-Rb,
-NH-C(O)-(CH2)m-CHRbRb и -NH-(CH2)m-C(O)-NH-(CH2)m-Rb;
каждая из групп Ra независимо выбрана из группы, содержащей водород, (C1-C6) алкил, (C3-C8) циклоалкил, циклогексил, (C4-C11) циклоалкилалкил, (C5-C10) арил, фенил, (C6-C16) арилалкил, бензил, 2-6-членный гетероалкил, 3-8-членный циклогетероалкил, морфолинил, пиперазинил, гомопиперазинил, пиперидинил, 4-11-членный циклогетероалкилалкил, 5-10-членный гетероарил и 6-16-членный гетероарилалкил;
каждая из групп Rb представляет собой подходящую группу, которая выбрана из группы, содержащей =O, -ORd, (C1-C3) галогенидалкилоксигруппу, -OCF3, =S, -SRd, =NRd, =NORd, -NRcRc, галоген, -CF3, -CN, -NC, -OCN, -SCN, -NO, -NO2, =N2, -N3, -S(O)Rd, -S(O)2Rd, -S(O)2ORd, -S(O)NRcRc, -S(O)2NRcRc, -OS(O)Rd, -OS(O)2Rd, -OS(O)2ORd, -OS(O)2NRcRc, -C(O)Rd, -C(O)ORd, -C(O)NRcRc, -C(NH)NRcRc, -C(NRa)NRcRc, -C(NOH)Ra, -C(NOH)NRcRc, -OC(O)Rd, -OC(O)ORd, -OC(O)NRcRc, -OC(NH)NRcRc, -OC(NRa)NRcRc, -[NHC(O)]nRd, -[NRaC(O)]nRd, -[NHC(O)]nORd, -[NRaC(O)]nORd, -[NHC(O)]nNRcRc, -[NRaC(O)]nNRcRc, -[NHC(NH)]nNRcRc и -[NRaC(NRa)]nNRcRc;
каждая из групп Rc отдельно пре дставляет собой защитную группу или Ra, или, наоборот, каждая из групп Rc берется совместно с атомом азота, к которому она присоединена, с целью формирования 5-8-членного циклогетероалкила или гетероарила, которые могут включать в себя один или несколько идентичных или различных дополнительных гетероатомов и которые могут замещаться одной или несколькими идентичными или различными группами Ra или подходящими группами Rb;
каждая Rd группа отдельно представляет собой защитную группу или Ra;
каждый параметр m отдельно представляет собой целое число от 1 до 3; и
каждый параметр n отдельно представляет собой целое число от 0 до 3.
Другой аспект настоящего изобретения заключается в предложении пролекарств соединений 2,4-пиримидинаминов. Подобные пролекарства могут быть активными в виде их пролекарств или же неактивными до момента превращения в активную лекарственную форму при определенных физиологических или иных условиях применения. В пролекартвах согласно настоящему изобретению одна или несколько функциональных групп соединений 2,4-пиримидинаминов включены в прокомпоненты (promoieties), которые отщепляются от молекулы при условиях применения обычно путем гидролиза, ферментативного расщепления или другого механизма расщепления с образованием функциональных групп. Например, первичные или вторичные аминогруппы могут быть включены в амидный прокомпонент, который расщепляется при условиях применения с образованием первичной или вторичной аминогруппы. Таким образом, пролекарства согласно настоящему изобретению включают в себя особые виды защитных групп, которые называются «прогруппы» (“progroups”) и маскируют одну или несколько функциональных групп соединений 2,4-пиримидинаминов, которые расщепляются при условиях применения с образованием активных лекарственных соединений 2,4-пиримидинаминов. Функциональные группы, входящие в состав соединений 2,4-пиримидинаминов, которые могут быть замаскированы с помощью прогрупп с целью включения в прокомпонент, включают в себя, не ограничиваясь ими, амины (первичные и вторичные), гидроксилы, сульфанилы (тиолы), карбоксилы, карбонилы, фенолы, катехолы, диолы, алкины, фосфаты и пр. В настоящее время известно огромное количество прогрупп, подходящих для маскировки указанных функциональных групп с целью образования прокомпонентов, способных расщепляться при условиях применения. Все эти прогруппы, сами по себе или в комбинациях, могут быть включены в пролекарства согласно настоящему изобретению. Конкретные примеры прокомпонентов, образующих первичные или вторичные аминогруппы, которые могут быть включены в пролекарства согласно настоящему изобретению, включают в себя, не ограничиваясь ими, следующие группы: амиды, карбаматы, имины, мочевины, фосфенилы, фосфорилы и сульфенилы. Конкретные примеры прокомпонентов, образующих сульфанильные группы, которые могут быть включены в пролекарства согласно настоящему изобретению, включают в себя, не ограничиваясь ими, следующие группы: тиоэфиры, например, S-метилпроизводные (монотио-, дитио-, окситио-, аминотиоацетали, силиловые тиоэфиры, сложные тиоэфиры, тиокарбонаты, тиокарбаматы, асимметричные дисульфиды и т.д. Конкретные примеры прокомпонентов, образующих в результате расщепления гидроксильные группы, которые могут быть включены в пролекарства согласно настоящему изобретению, включают в себя, не ограничиваясь ими, следующие группы: сульфонаты, сложные эфиры и карбонаты. Конкретные примеры прокомпонентов, образующих карбоксильные группы, которые могут быть включены в пролекарства согласно настоящему изобретению, включают в себя, не ограничиваясь ими, следующие группы: сложные эфиры (включая сложные силиловые эфиры, эфиры оксаминовой кислоты и тиоэфиры), амиды и гидразиды.
В одном из иллюстративных примеров пролекарства согласно настоящему изобретению представляют собой соединения со структурной формулой (I), в которой защитная группа Rc и Rd является прогруппой.
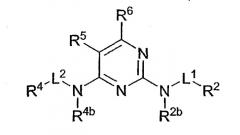
Замещение атомов водорода, присоединенных к N2 и N4 в 2,4-пиримидинаминах, имеющих структурную формулу (I), заместителями оказывает неблагоприятное воздействие на активность соединений. Однако и это будет оценено специалистами - эти атомы азота могут быть включены в прокомпоненты, которые при условиях применения расщепляются и образуют 2,4-пиримидинамины согласно структурной формуле (I). Таким образом, как показано в другом иллюстративном примере, пролекарства согласно настоящему изобретению представляют собой соединения со следующей структурной формулой (II):
включая их соли, гидраты, сольваты и N-оксиды, в которых
R2, R4, R5, R6, L1 и L2 - группы, указанные ранее при описании формулы (I); и
каждая из групп R2b и R4b в отдельности и независимо одна от другой является прогруппой.
Следующий аспект настоящего изобретения заключается в предложении композиций, содержащих одно или несколько соединений и/или пролекарств согласно настоящему изобретению, а также соответствующий носитель, наполнитель или разжижитель. Точная природа носителя, наполнителя или разжижителя будет зависеть от желаемого использования данной композиции - от веществ, применяемых в ветеринарной практике, до веществ, применяемых для лечения человека.
Еще один аспект настоящего изобретения заключается в предложении промежуточных соединений, используемых при синтезе соединений 2,4-пиримидинамина и пролекарств согласно настоящему изобретению. В одном из примеров промежуточные соединения представлены 4-пиримидинаминами со структурной формулой (III):
включая их соли, гидраты, сольваты и N-оксиды, в которых R4, R5, R6 и L2 представляют собой группы, описанные ранее при определении структурной формулы (I); LG представляет собой замещаемую группу, например -S(O)2Me, -SMe или галогеновые группы (т.е. F, Cl, Br, I); и R4c представляет собой водород или прогруппу.
В другом примере промежуточные соединения представлены 2-пиримидинаминами согласно структурной формуле (IV):
включая их соли, гидраты, сольваты и N-оксиды, в которых R2, R5, R6 и L1 представляют собой группы, описанные ранее при определении структурной формулы (I); LG представляет собой замещаемую группу, например -S(O)2Me, -SMe или галогеновые группы (т.е. F, Cl, Br, I); и R2c представляет собой водород или прогруппу.
В еще одном примере промежуточные соединения представлены 4-амино- или 4-гидрокси-2-пиримидинаминами в соответствии со структурной формулой (V):
включая их соли, гидраты, сольваты и N-оксиды, в которых R2, R5, R6 и L1 представляют собой группы, описанные ранее при определении структурной формулы (I); R7 представляет собой амино- или гидроксильную группу и R2c представляет собой водород или прогруппу.
В последующем примере промежуточные соединения представлены N4-замещенными цитозинами в соответствии со структурной формулой (VI):
включая их соли, гидраты, сольваты и N-оксиды, в которых R4, R5, R6 и L2 представляют собой группы, описанные ранее при определении структурной формулы (I); и R4c представляет собой водород или прогруппу.
Еще один аспект настоящего изобретения заключается в предложении способов синтеза соединений 2,4-пиридинаминов и пролекарств согласно настоящему изобретению. В одном из примеров указанный способ предполагает реакцию 4-пиримидинаминов со структурной формулой (III) с амином, имеющим формулу HR2cN-L1-R2, где L1, R2 и R2c представляют собой группы, указанные ранее при описании структурной формулы (IV), с целью образования 2,4-пиримидинамина, имеющего структурную формулу (I), или пролекарства в соответствии со структурной формулой (II).
В другом примере указанный способ предполагает реакцию 2-пиримидинаминов со структурной формулой (IV) с амином, имеющим формулу R4-L2-NHR4c, в которой L4, R4 и R4c представляют собой группы, указанные ранее при описании структурной формулы (III), с целью образования 2,4-пиримидинаминов, имеющего структурную формулу (I), или пролекарства в соответствии со структурной формулой (II).
В еще одном примере указанный способ предполагает реакцию 4-амино-2-пиримидинаминов со структурной формулой (V) (в которой R7 является аминогруппой) с амином, имеющим формулу R4-L2-NHR4c, в которой L4, R4 и R4c представляют собой группы, указанные ранее при описании структурной формулы (III), с целью образования 2,4-пиримидинамина, имеющего структурную формулу (I), или пролекарства в соответствии со структурной формулой (II). В альтернативном варианте, 4-амино-2-пиримидинамин может реагировать с соединением, имеющим формулу R4-L2-LG, в которой R4 и L2 представляют собой группы, указанные ранее при описании структурной формулы (I), и LG представляет собой замещаемую группу.
В еще одном примере указанный способ предполагает реакцию галогенирования 4-гидрокси-2-пиримидинамина со структурной формулой (V) (R7 является гидроксильной группой) с целью образования 2-пиримидинамина со структурной формулой (IV), с последующей реакцией указанного пиримидинамина с соответствующим амином, как указано выше.
В еще одном примере указанный способ предполагает реакцию галогенирования N4-замещенного цитозина со структурной формулой (VI) с целью образования 4-пиримидинамина со структурной формулой (III) с последующей реакцией указанного пиримидинамина с соответствующим амином, как указано выше.
Соединения 2,4-пиримидинаминов согласно настоящему изобретению являются мощными ингибиторами дегрануляции иммунных клеток, таких как мастоциты, базофилы, нейтрофилы и/или эозинофилы. Таким образом, еще один аспект настоящего изобретения заключается в предложении способов регуляции и, в частности, ингибирования дегрануляции таких клеток. Предлагаемый способ в целом заключается в приведении дегранулируемой клетки в контакт с соединением 2,4-пиримидинаминов или пролекарства согласно настоящему изобретению либо соответствующей соли, гидрата, сольвата, N-оксида указанных соединений и/или их комбинации в количестве, достаточном для эффективной регуляции или ингибирования дегрануляции клетки. Указанный способ может применяться in vitro или in vivo как тактика лечения или профилактики заболеваний, характеризуемых клеточной дегрануляцией, обусловленных ею или связанных с ней.
Не претендуя на связь с какой-либо теорией, объясняющей принцип действия, имеющиеся в наличии биохимические данные подтверждают, что соединения 2,4-пиримидинаминов оказывают ингибирующий эффект на дегрануляцию, по крайней мере частично, за счет блокирования и ингибирования каскада передачи сигналов (каскадов), инициированного в результате перекрестного связывания Fc-рецепторов с высокой степенью сродства к IgE (“FcεRI”) рецепторам и/или IgG (“FcγRI”) рецепторам. На самом деле соединения 2,4-пиримидинамина являются мощными ингибиторами дегрануляции, опосредованной и FcεRI-, и FcγRI- рецепторами. Как следствие этого соединения 2,4-пиримидина могут использоваться для ингибирования сигнальных каскадов указанных Fc-рецепторов в клетках любых типов, экспрессирующих такие FcεRI- и/или FcγRI-рецепторы, включая, но не ограничиваясь ими, следующие клетки: макрофаги, мастоциты, базофилы, нейтрофилы и/или эозинофилы.
Указанные способы также позволяют регулировать и, в частности, ингибировать процессы, протекающие в прямом направлении, которые являются результатом активации таких сигнальных каскадов Fc-рецепторов. Такие прямые процессы включают в себя, не ограничиваясь ими, следующие; FcεRI- и/или FcγRI- опосредованную дегрануляцию, производство цитокина и/или производство и/или выделение медиаторов липидов, таких как лейкотриены и простагландины. Указанный способ в целом заключается в приведении клетки из категории описанных выше, экспрессирующей Fc-рецептор, в контакт с соединением 2,4-пиримидинаминов или пролекарством согласно настоящему изобретению, либо соответствующей солью, гидратом, сольватом, N-оксида указанных соединений и/или их комбинаций, в количестве, достаточном для эффективной регуляции или ингибирования сигнального каскада Fc-рецепторов и/или прямого процесса, затронутого активацией этого сигнального каскада. Указанный способ может применяться in vitro или in vivo в качестве тактики лечения или профилактики заболеваний, характеризуемых, обусловленных или связанных с сигнальным каскадом Fc-рецепторов, как, например, заболеваний, обусловленных выделением химических медиаторов гранул в процессе дергануляции, выделением и/или синтезом цитокинов, и/или выделением и/или синтезом медиаторов липидов, таких как, например, лейкотриенов и простагландинов.
Еще один аспект настоящего изобретения заключается в предложении способов лечения и/или профилактики заболеваний, характеризуемых, обусловленных или связанных с выделением химических медиаторов в результате активирования сигнальных каскадов Fc-рецепторов, таких, например, как сигнальные каскады FcεRI- и/или FcγRI-рецепторов. Эти способы могут применяться как на животных, так и на людях. Указанные способы в целом заключаются во введении животным или человеку соединения 2,4-пиримидинаминов или пролекарства согласно настоящему изобретению либо соответствующей соли, гидрата, сольвата, N-оксида указанных соединений и/или их комбинации в количестве, достаточном для эффективного лечения или предотвращения заболевания. Как обсуждалось выше, активация сигнального каскада FcεRI- или FcγRI-рецепторов в определенных иммунных клетках приводит к выделению и/или синтезу различных химических веществ, которые являются фармакологическими медиаторами широкого диапазона заболеваний. Любые из этих заболеваний могут лечиться или быть предотвращены в соответствии со способами согласно настоящему изобретению.
Например, в мастоцитах и базофилах активация сигнального каскада FcεRI- или FcγRI-рецепторов приводит к немедленному (т.e. в течение 1-3 мин с момента акцивации рецепторов) выделению преформированных медиаторов атопических реакций и/или реакций гиперчувствительности I типа (например, гистамина, протеаз, как, например, триптазы, и т.д.) посредством процесса дегрануляции. Такие атопические реакции и/или реакции гиперчувствительности I типа включают в себя, не ограничиваясь ими анафилактические реакции на окружающую среду и другим аллергенам (например, пыльцу, яд насекомых и/или животных, пищу, лекарства, контрастную краску и т.д.), анафилактоидная реакция, сенная лихорадка, аллергический конъюнктивит, аллергический ринит, аллергическая астма, атопический дерматит, экзема, крапивница, нарушение функции слизистой оболочки, тканей, а также ряд желудочно-кишечных расстройств.
Вслед за немедленным выделением преформированных медиаторов посредством дегрануляции происходит выделение и/или синтез ряда других химических медиаторов, включая, среди прочих, фактор активации тромбоцитов (PAF), простагландины и лейкотриены (например, LTC4), а также синтез de novo и выделение цитокинов, как, например, TNFα, IL-4, IL-5, IL-6, IL-13 и т.д. Первый их этих двух процессов происходит примерно через 3-30 мин после активации рецепторов; последующий - примерно через 30 мин - 7 ч после активации рецепторов. Эти медиаторы “поздней стадии” считаются частично ответственными за хронические симптомы перечисленных выше атопической реакции и реакции гиперчувствительности I типа и вдобавок являются химическими медиатороами воспалений и воспалительных заболеваний (т.е. остеоартрит, воспалительная болезнь кишечника, язвенный колит, болезнь Крона, идиопатическая воспалительная болезнь кишечника, синдром повышенной раздражимости желудка, спастический колит и т.д.), слабое рубцевание (т.е. склеродерма, выраженный фиброз, образование келоидов, послеоперационные рубцы, фиброз легких, спазм сосудов, мигрень, реперфузионная травма и пост-инфаркт миокарда) и синдром Шегрена. Все эти заболевания могут лечиться или быть предотвращены в соответствии со способами согласно настоящему изобретению.
Дополнительные болезни, которые можно лечить или предотвратить с помощью способов согласно настоящему изобретению, включают в себя болезни, связанные с патологией базофильных клеток и/или мастоцитов. Примеры таких заболеваний включают в себя, не ограничиваясь ими, болезни кожи, как, например, склеродерма, болезни сердца, как, например, инфаркт миокарда, болезни легких, как, например, изменения или преобразования мышц легких или хроническое обструктивное заболевание легких (СOPD), и болезни кишечника, как, например, синдром воспаления кишечника (спастический колит).
Соединения 2,4-пиримидинаминов согласно настоящему изобретению также являются мощными ингибиторами тирозинкиназы и, в частности, Syk-киназы. Таким образом, еще один аспект настоящего изобретения заключается в предложении способов регуляции и, в частности, ингибирования активности Syk-киназы. Способ в целом заключается в приведении Syk-киназы или клетки, содержащей Syk-киназу, в контакт с соединением 2,4-пиримидинаминов или пролекарства согласно настоящему изобретению либо с соответствующей солью, гидратом, сольватом, N-оксидом указанных соединений и/или их композицией в количестве, достаточном для эффективной регуляции или ингибирования активности Syk-киназы. В одном из примеров Syk-киназа представлена в качестве изолированной или рекомбинантной Syk-киназы. В другом примере Syk-киназа представлена в качестве эндогенной или рекомбинантной Syk-киназы, экспрессированной клеткой, как, например, в случае мастоцита или базофила. Способ может применяться in vitro или in vivo в качестве тактики лечения или профилактики заболеваний, характеризуемых, обусловленных или связанных с активностью Syk-киназы.
Не ограничиваясь какой-либо одной теорией, объясняющей принцип действия, считается, что соединения 2,4-пиримидинаминов согласно настоящему изобретению оказывают ингибирующий эффект на дегрануляцию клеток и/или выделение других химических медиаторов преимущественно за счет ингибирования Syk-киназы, которая активируется посредством гомодимера гамма-цепи рецептора FcεRI (см., например, фиг.2). Этот гомодимер гамма-цепи является общим для других Fc-рецепторов, включая FcγRI, FcγRIII и FcαRI. Для всех этих рецепторов процесс внутриклеточной передачи сигналов опосредован общим гомодимером гамма-цепи. Связывание и агрегация этих рецепторов приводит к рекрутингу и активации тирозинкиназ, как, например, Syk-киназы. В результате этих общих сигнальных действий указанные соединения 2,4-пиримидинаминов могут использоваться для регуляции и, в частности, ингибирования сигнальных каскадов Fc-рецепторов с гомодимерами гамма-цепи, как, например, FcεRI, FcγRI, FcγRIII и FcαRI, а также реакций клеток, полученных посредством этих рецепторов.
Известно, что Syk-киназа играет критическую роль в других сигнальных каскадах. Например, Syk-киназа является эффектором сигналов рецепторов В-клеток (ВCR) (Turner et al., 2000, Immunology Today 21:148-154) и является существенным компонентом сигнального пути бэта(1), бэта(2) и бэта(3)-интегрина в нейтрофилах (Mocsai et al., 2002, Immunity 16:547-558). Поскольку указанные соединения 2,4-пиримидинаминов являются мощными ингибиторами Syk-киназы, их можно использовать для регуляции, в частности ингибирования, любых сигнальных каскадов, в которых Syk-киназа играет роль, например, в сигнальных каскадах Fc-рецепторов, BCR и интегрина, а также реакций клеток, полученных посредством этих рецепторов. Регуляция или ингибирование конкретной реакции клетки частично зависят от конкретного типа клетки и сигнального каскада рецепторов и хорошо известны в литературе. Некоторые из примеров реакций клеток, которые можно регулировать или ингибировать посредством соединений 2,4-пиримидинаминов, включают в себя респираторный всплеск, клеточную адгезию, дегрануляцию клеток, распространение клеток, миграцию клеток, фагоцитоз (например, в макрофагах), поток ионов кальция (например, в мастоцитах, базофилах, нейтрофилах, эозинофилах и B-клетках), агрегацию тромбоцитов и созревание клеток (например, в B-клетках).
Таким образом, еще один аспект настоящего изобретения заключается в предложении способов регуляции, в частности ингибирования, каскадов передачи сигналов, в которых участвует Syk-киназа. Способ в целом заключается в приведении Syk-зависимого рецептора или клетки, экспрессирующей Syk-зависимый рецептор, в контакт с соединением 2,4-пиримидинаминов или пролекарства согласно настоящему изобретению либо соответствующей соли, гидрата, сольвата, N-оксида указанных соединений и/или их комбинации в количестве, достаточном для эффективной регуляции или ингибирования каскада передачи сигналов. Указанные способы могут также использоваться для регуляции и, в частности, ингибирования прямых процессов или реакций клеток, полученных в результате активации конкретного Syk-зависимого каскада передачи сигналов. Способы можно использовать для регуляции любых каскадов передачи сигналов, в которых роль Syk-киназы неизвестна или же установлена позже. Способы могут использоваться in vitro или in vivo в качестве тактики лечения и профилактики заболеваний, характеризуемых, обусловленных или связанных с активацией Syk-зависимого каскада передачи сигналов. Некоторые примеры таких заболеваний включают болезни, описанные ранее.
Данные, полученные в результате клеточного анализа, в совокупности с данными, полученными на животных, также подтверждают, что соединения 2,4-пиримидинаминов в соответствии с настоящим изобретением могут быть использованы для лечения или профилактики аутоиммунных заболеваний и/или симптомов этих заболеваний. Соответствующие способы в целом включают в себя введение пациенту, страдающему аутоиммунным заболеванием или находящемуся под угрозой развития аутоиммунного заболевания, 2,4-пиримидиндиамина или пролекарства согласно настоящему изобретению или же приемлемой соли, N-оксида, гидрата, сольвата или их комбинации в количестве, эффективном для лечения или профилактики аутоиммунного заболевания и/или связанных с ним симптомов. Аутоиммунные заболевания, поддающиеся лечению или профилактике с помощью соединений 2,4-пиримидинаминов, включают в себя заболевания, зачастую ассоциируемые с реакциями нон-анафилактической гиперчувствительности (II, III и/или IV типа), и/или заболевания, опосредованные, по крайней мере частично, активацией сигнального каскада FcγR в моноцитах. Такого рода аутоиммунные заболевания включают в себя, не ограничиваясь ими, заболевания, часто характеризуемые как аутоиммунные расстройства отдельного органа или единого типа клеток, а также заболевания, часто характеризуемые как включающие в себя системные ау