Биологически активные производные пептида vapeehptllteaplnpk
Иллюстрации
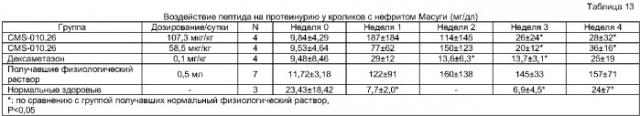
Показать всеИзобретение относится к биотехнологии и представляет собой по существу чистый пептид для модулирования иммунной системы, характеризуемый аминокислотной последовательностью VAPEEHPTLLTEAPLNPK, а также фармацевтическую композицию, содержащую указанный пептид. Изобретение позволяет модулировать иммунную активность, выбранную из группы, состоящей из подавления трансформации Т-лимфоцитов, подавления активности NK-клеток и подавления образования антител. 4 н. и 3 з.п. ф-лы, 5 ил., 15 табл.
Реферат
Предпосылки изобретения
Область изобретения
Настоящее изобретение относится к коротким пептидам и к их применению. В частности, настоящее изобретение относится к коротким пептидам с различными видами биологической активности.
Описание уровня техники
Пептиды известны в области лечения заболеваний и в качестве фармацевтических композиций. Например, в патенте США № 6191113 описан пептид с активностью в качестве ингибитора роста гладкомышечных клеток и, следовательно, приемлемый для профилактики и лечения ассоциированных с ростом гладкомышечных клеток патологических состояний, таких как атеросклероз, рестеноз после ангиопластики, сужение просвета после трансплантации кровеносных сосудов и гладкомышечная саркома. В патенте США 6184208 описан другой пептид, для которого обнаружено, что он модулирует физиологические процессы, такие как увеличение активности зоны эпителиального роста и роста волос. Кроме того, в публикации PCT № WO 03/006492 и в патентной заявке США № 10/237405 выдвигают предположение, что определенные пептиды и их фармацевтические композиции являются биологически активными и способны модулировать иммунные ответы.
Таким образом, целью настоящего изобретения является предоставление короткого пептида или пептидов с биологической активностью.
Сущность изобретения
Один из аспектов настоящего изобретения относится к пептидам, полученным из пептида CMS-010, содержащего 18 аминокислот (VAPEEHPTLLTEAPLNPK) (SEQ ID № 1), у которого обнаружено наличие биологической активности, где указанные пептиды не содержат последовательность пептида CMS-010. С целью тестирования образцы этих пептидов химически синтезировали из L-аминокислот. Дополнительные аспекты настоящего изобретения относятся к выделенному или очищенному пептиду, содержащему выбранную из SEQ ID № 2-31 последовательность, по существу состоящему или состоящему из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010 (SEQ ID № 1). Другой аспект относится к по существу чистым пептидам, содержащим выбранные из SEQ ID № 2-31 пептиды, где указанные пептиды не содержат последовательность пептида CMS-010.
Другой аспект настоящего изобретения представляет собой введение пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, по существу состоящего или состоящего из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, где воздействия указанного введения выбраны из группы, состоящей из подавления трансформации иммунных клеток, подавления активности NK-клеток, увеличения активности NK-клеток, подавления образования антител in vivo, подавления клеточной пролиферации, подавления роста опухоли, ослабления нефрита и уменьшения протеинурии. В некоторых вариантах осуществления подавление трансформации иммунных клеток представляет собой подавление трансформации Т-лимфоцитов посредством ConA in vitro. В некоторых вариантах осуществления подавление трансформации иммунных клеток представляет собой подавление трансформации Т-лимфоцитов in vivo. В некоторых вариантах осуществления подавление клеточной пролиферации представляет собой подавление развития клеток саркомы in vivo. В некоторых вариантах осуществления ослабление нефрита представляет собой ослабление нефрита, обусловленного антителами к почечным эпитопам.
Дополнительные аспекты настоящего изобретения относятся к пептиду, содержащему выбранную из SEQ ID № 2-31 последовательность, по существу состоящему или состоящему из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, состоящего из L-аминокислот. В некоторых вариантах осуществления пептид, содержащий выбранную из SEQ ID № 2-31 последовательность, по существу состоящий или состоящий из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, находится по существу в чистой форме.
Другой аспект настоящего изобретения относится к фармацевтическим композициям, содержащим пептид, который содержит выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность CMS-010. В некоторых вариантах осуществления фармацевтические композиции, содержащие пептид, который содержит выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010, содержат состоящие из L-аминокислот пептиды.
Еще одним аспектом настоящего изобретения являются способы получения фармацевтической композиции, предусматривающие получение пептида, который содержит выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010, и смешивание пептида с фармацевтически приемлемым носителем.
Еще одним аспектом настоящего изобретения являются способы уменьшения воздействий заболевания человека, включающие введение фармацевтически эффективных доз пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010. В некоторых вариантах осуществления указанный человек страдает от клеточно-пролиферативного и/или иммунологического нарушения. В некоторых вариантах осуществления клеточно-пролиферативное нарушение представляет собой злокачественную опухоль, саркому и/или опухоль.
Дополнительным аспектом настоящего изобретения является способ модулирования иммунной системы индивидуума, включающий введение фармацевтически эффективной дозы пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010.
Другим аспектом настоящего изобретения является применение пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010, в качестве фармацевтического препарата. В некоторых вариантах осуществления пептид применяют для лечения болезненного состояния в форме клеточно-пролиферативного нарушения и/или иммунологического нарушения. В некоторых вариантах осуществления подвергаемым лечению клеточно-пролиферативным нарушением является саркома.
Еще одним аспектом настоящего изобретения является применение пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010, в качестве модулятора иммунной системы. В некоторых вариантах осуществления модулирование иммунной системы представляет собой увеличение или подавление активности NK-клеток.
Дополнительным аспектом настоящего изобретения является применение пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, где указанный пептид не содержит последовательность пептида CMS-010, в качестве питательной добавки.
Другим аспектом настоящего изобретения является молекула, содержащая улучшенное производное пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, содержащее улучшающую молекулу, функционально связанную с указанным пептидом, где улучшающая молекула увеличивает терапевтическую эффективность указанного пептида и где указанный пептид не содержит последовательность пептида CMS-010.
Краткое описание чертежей
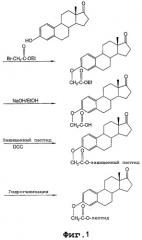
Каждая из пяти фигур иллюстративно демонстрирует химические реакции связывания пептидов со стероидными молекулами.
На фигуре 1 представлен ряд химических реакций связывания ковалентной связью пептида с молекулой эстрона.
На фигуре 2 представлен второй альтернативный ряд реакций для получения таких же связей, что и на фигуре 1.
Фигура 3 включает ряд химических реакций, предназначенных для связывания ковалентной связью пептида с молекулой эстрадиола.
Фигура 4 включает второй ряд химических реакций для получения таких же связей, что и на фигуре 3.
На фигуре 5 представлен способ связывания ковалентной связью пептида с молекулой гидрокортизона.
Подробное описание предпочтительного варианта осуществления
I. ВВЕДЕНИЕ
Обнаружено, что пептид CMS-010 (SEQ ID № 1) с последовательностью VAPEEHPTLLTEAPLNPK обладает биологической иммунорегулирующей активностью (U.S. Patent Application №10/178684) и имеет терапевтический потенциал для применения у человека. Настоящее изобретение относится к фрагментам и производным CMS-010 с биологической активностью. В конкретных вариантах осуществления настоящее изобретение относится к фрагментам и производным с последовательностями, представленными как SEQ ID № 2-31. В некоторых вариантах осуществления фрагменты могут иметь заместители и/или дополнительные молекулярные группы или могут быть функциональными производными VAPEEHPTLLTEAPLNPK (CMS-010). Применения фрагментов и производных CMS-010 включают регуляцию клеток и тканей. Фрагменты и производные CMS-010 могут быть включены в состав фармацевтических препаратов и питательных добавок.
Понятно, что в качестве другого способа практического осуществления настоящего изобретения возможно добавление дополнительных аминокислот к N-концу или C-концу пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, по существу состоящего или состоящего из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональных производных. В таких вариантах осуществления пептид, содержащий выбранную из SEQ ID № 2-31 последовательность, по существу состоящий или состоящий из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность CMS-010, и его функциональные производные сохраняют одно или несколько описанных здесь терапевтических или функциональных свойств. Например, в некоторых вариантах осуществления к описанному пептиду может быть добавлена одна или две аминокислоты без влияния на его биологическую функцию. В некоторых вариантах осуществления молекулы меньших размеров, содержащие некоторую часть VAPEEHPTLLTEAPLNPK (CMS-010), содержат единственный фрагмент последовательности, полученный из VAPEEHPTLLTEAPLNPK (CMS-010). В других вариантах осуществления молекулы меньших размеров, содержащие некоторую часть VAPEEHPTLLTEAPLNPK (CMS-010), содержат два или более фрагментов последовательности, полученных из отдельных, несмежных фрагментов VAPEEHPTLLTEAPLNPK (CMS-010). Например, в некоторых вариантах осуществления молекулы меньших размеров, содержащие некоторую часть VAPEEHPTLLTEAPLNPK (CMS-010), содержат последовательность, находящуюся вблизи N-конца VAPEEHPTLLTEAPLNPK (CMS-010), а также последовательность, находящуюся вблизи C-конца VAPEEHPTLLTEAPLNPK (CMS-010) без какой-либо промежуточной последовательности, находящейся между этими последовательностями в VAPEEHPTLLTEAPLNPK (CMS-010). В дополнительных вариантах осуществления возможно добавление трех или четырех аминокислот с сохранением функции пептида, выбранного из группы, состоящей из фрагментов CMS-010 (VAPEEHPTLLTEAPLNPK) (где указанные фрагменты не содержат последовательность CMS-010) и его функциональных производных. Все они относятся к вариантам одного и того же пептида. Кроме того, для практического осуществления другого аспекта настоящего изобретения можно использовать производные пептида, такие как производные с консервативной заменой одной аминокислоты на другую из того же функционального класса. Например, в пептидах с неполярными или гидрофобными боковыми цепями возможна замена одной боковой группы на другую без снижения биологической активности. В некоторых вариантах осуществления из последовательности фрагмента пептида CMS-010 можно удалить одну, две или более аминокислот, и, несмотря на это, все еще сохранится активность исходного пептидного фрагмента. Например, фрагмент пептида CMS-010 длиной десять аминокислот ресинтезируют без 5-й аминокислоты с N-конца последовательности. Таким образом, в полученном варианте длиной 9 аминокислот 4-я аминокислота с N-конца ковалентно связана с 6-й аминокислотой с N-конца исходной последовательности, и в то же время он обладает той же активностью, что и исходный фрагмент пептида из десяти аминокислот. В некоторых вариантах осуществления, где две или более аминокислоты удалены из последовательности фрагмента пептида CMS-010, удаленные аминокислоты в исходной последовательности фрагмента пептида являются соседними друг с другом. В других вариантах осуществления, где из последовательности фрагмента пептида CMS-010 удалены две или более аминокислоты, аминокислоты не являются в исходной последовательности фрагмента пептида соседними друг с другом, а точнее отделены друг от друга в исходной последовательности аминокислотами, которые сохраняются в укороченном варианте пептида. В дополнительных вариантах осуществления, где из фрагмента пептида CMS-010 удалены три или более аминокислоты, некоторые удаленные из исходной последовательности аминокислоты являются соседними друг с другом, в то время как одна или несколько аминокислот, удаленных из первоначальной последовательности, не являются соседними с какими-либо другими удаленными из исходной последовательности аминокислотами. В дополнительных вариантах осуществления этого изобретения в пептид для формирования вариантов может быть встроена последовательность линкера/спейсера, но варианты все еще сохраняют активную функциональную группу как в исходном пептиде, используемом в этом исследовании. Они также являются рассматриваемыми вариантами пептидов. Как применяют здесь, аналог пептида включает пептиды с молекулами аминокислот, имитирующими структуру природных аминокислот, например аналог с отличающейся структурой основной цепи, или замещенный D-аминокислотами. В качестве дополнительного примера, хотя аминокислоты, которые применяют для синтеза пептидов, находятся в их оптической изомерной L-форме, пептиды с одной или несколькими аминокислотами в последовательности, замещенными D-формами, могут обладать сходными видами биологической активности. Как используют в формуле изобретения, термин "функциональное производное" включает фрагменты, варианты, аналоги или химические производные пептида.
"По существу чистый пептид" относится к пептидам со степенью очистки, по меньшей мере, 10% мас./мас., более предпочтительно 20%, еще более предпочтительно 60% и значительно более предпочтительно более чем на 90% очищенным. В самом предпочтительном варианте осуществления степень очистки составляет более чем 99%. По существу, чистый пептид можно использовать для получения фармацевтических и питательных препаратов, которые, как описано далее, могут представлять собой комплексные смеси.
"Модулирование" относится к воздействию на клетки, обусловленному введением или воздействием пептидов по настоящему изобретению, где введение или воздействие пептидов на клетки приводит к изменениям активности клеток. Изменения могут представлять собой увеличение или подавление активности клетки. Увеличение или подавление активности клетки может представлять собой увеличение или подавление скорости деления клетки и репликации, увеличение или подавление реакции клетки на другие факторы и/или увеличение или подавление уровня продукции и/или секреции клеткой белков или веществ.
"Клеточная пролиферация" относится к увеличению количества существующих клеток и может быть следствием трансформации или иммортализации клетки. Нарушения клеточной пролиферации включают в качестве неограничивающих примеров злокачественные опухоли, доброкачественные опухоли, опухоли и саркомы и могут включать любое количество клеток. "Иммунологические нарушения" относятся к нарушению функции или повреждающей функции иммунных клеток или другой части иммунной системы. Такие нарушения могут быть вызваны подавлением активности клетки или молекулы или увеличением активности клетки или молекулы.
Применение в фармацевтических препаратах пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, по существу состоящего или состоящего из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональных производных, можно использовать в качестве возможного лечения иммунологических нарушений или заболеваний. Препараты могут содержать пептид, содержащий выбранную из SEQ ID № 2-31 последовательность, по существу состоящий или состоящий из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональные производные, смешанные с другими активными или неактивными компонентами, включая другие пептиды, например, к тому же препарату можно добавить от двух до нескольких (например, 3-5) пептидов с другими ингредиентами или без других ингредиентов. Альтернативно, пептид, содержащий выбранную из SEQ ID № 2-31 последовательность, по существу состоящий или состоящий из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональные производные можно использовать для получения препарата совместно с не перечисленными здесь пептидами. Они могут быть введены внутривенно, внутримышечно, внутрикожно, подкожно или интрадермально. Способ введения также может представлять собой внутриартериальную инъекцию, которая ведет непосредственно к пораженному органу. Другими способами введения являются трансдермальный, ингаляционный в виде порошка или аэрозоля и другие формы доставки, известные специалистам в данной области. Препараты также можно принимать перорально, и они могут содержать носители, которые можно использовать для предотвращения переваривания пептида в желудке после перорального применения, или любые другие носители, известные в данной области (носители для трансдермальной доставки, например, такие как липосомы).
Как применяют здесь, термин "гибридный пептид" используют в отношении пептидов, содержащих дополнительные пептиды, встроенные в исходный биологически активный пептид с указанной выше последовательностью или его функциональные производные, но все еще сохраняющих по существу сходную активность. Дополнительные пептиды включают лидерные пептиды, например, содержащие аминокислотную последовательность, которую узнают одна или несколько прокариотических или эукариотических клеток в качестве сигнала для секреции гибридного белка во внешнюю среду или в клетку. Секреция может быть прямой или непрямой посредством секреторных везикул.
Как применяют здесь, терминология "по существу состоящий из" относится к пептиду или полипептиду, содержащему выбранную из SEQ ID № 2-31 последовательность, по существу состоящему или состоящему из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональным производным с дополнительными аминокислотами на C-конце и/или N-конце и которые сохраняют один или несколько видов активности указанных пептидов, приведенных здесь. Таким образом, в качестве неограничивающего примера, где активность пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, по существу, состоящего или состоящего из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональных производных относится к лечению и/или профилактике клеточно-пролиферативных или иммунологических нарушений или заболеваний, пептид или полипептид, "по существу состоящий" из пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, по существу, состоящего или состоящего из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональных производных, обладает активностью в отношении лечения и/или профилактики нарушений или заболеваний, как представлено здесь в отношении этого пептида, и сам по себе не обладает какими-либо характеристиками (т.е. до модификации посредством присоединения одной или нескольких биологически активных молекул), которые существенно снижают способность пептида или полипептида к лечению или профилактике клеточно-пролиферативных или иммунологических нарушений или которые приводят к существенным изменениям основных и новых характеристик пептида в качестве лечебного и/или профилактического средства для указанных выше нарушений или заболеваний. Таким образом, в предыдущем примере природный полноразмерный полипептид, который обладает исходной активностью, отличной от лечения и/или профилактики клеточно-пролиферативных или иммунологических нарушений, и который где-либо содержит выбранную из SEQ ID № 2-31 последовательность, по существу, состоит или состоит из выбранной из SEQ ID № 2-31 последовательности (но не содержит последовательность CMS-010), и его функциональные производные не являются пептидом или полипептидом "по существу состоящим из" пептида, который содержит выбранную из SEQ ID № 2-31 последовательность, по существу состоит или состоит из выбранной из SEQ ID № 2-31 последовательности, и его функциональных производных, последовательность которого содержит природный полноразмерный полипептид. Также в предыдущем примере полученный способами генетической инженерии пептид или полипептид, который обладает исходной активностью, отличной от лечения или профилактики клеточно-пролиферативных или иммунологических нарушений, но включает аминокислотную последовательность пептида, который где-либо содержит выбранную из SEQ ID № 2-31 последовательность, по существу состоит или состоит из выбранной из SEQ ID № 2-31 последовательности (но не содержит последовательность CMS-010), и его функциональных производных, не будет являться пептидом или полипептидом "по существу состоящим из" пептида, который содержит выбранную из SEQ ID № 2-31 последовательность, по существу состоит или состоит из выбранной из SEQ ID № 2-31 последовательности (но не содержит последовательность CMS-010), и его функциональных производных, последовательность которых входит в полученный способами генетической инженерии пептид или полипептид.
Специалисты в данной области легко могут определить, состоит ли пептид или полипептид по существу из пептида, содержащего выбранную из SEQ ID № 2-31 последовательность, по существу состоящего или состоящего из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональных производных по указанным выше определениям посредством измерения активности пептида или полипептида с применением анализов лечения или профилактики клеточно-пролиферативных или иммунологических нарушений, которые предоставлены здесь в отношении фрагментов и производных пептида VAPEEHPTLLTEAPLNPK (CMS-010).
В предпочтительном варианте осуществления терминология "по существу состоящий из" также может относиться к пептидам или полипептидам, которые имеют менее 5 аминокислотных остатков дополнительно к пептиду, содержащему выбранную из SEQ ID № 2-31 последовательность, по существу состоящему или состоящему из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональным производным. В более предпочтительном варианте осуществления указанная выше терминология относится к пептидам с 2 аминокислотными остатками дополнительно к пептиду, содержащему выбранную из SEQ ID № 2-31 последовательность, по существу состоящему или состоящему из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональным производным. В еще более предпочтительном варианте осуществления указанная выше терминология относится к пептиду с одним аминокислотным остатком дополнительно к пептиду, содержащему выбранную из SEQ ID № 2-31 последовательность, по существу состоящему или состоящему из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональным производным.
Фармацевтический препарат может включать любой из известных фармацевтических носителей. Примеры приемлемых носителей включают любой из известных специалистам в данной области стандартных фармацевтически приемлемых носителей. Они включают в качестве неограничивающих примеров физиологический солевой раствор, воду, эмульсии, включая смеси масла и воды или триглицеридные эмульсии, и другие типы средств, наполнителей, покрытых оболочкой таблеток и капсул. Приемлемый носитель можно выбирать на основании способа введения фармацевтической композиции.
Пептид, выбранный из группы, содержащей выбранную из SEQ ID № 2-31 последовательность, по существу состоящей или состоящей из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональные производные можно вводить посредством внутривенной инъекции, внутримышечной инъекции, внутрибрюшинной инъекции, подкожной инъекции и подкожной имплантации. Также пептид можно вводить в любой форме для перорального введения, такой как таблетка, капсула, суспензия, раствор, и т.д., в обычной форме без модификации или в форме с замедленным высвобождением, или с желудочно-кишечной защитой или без нее. Кроме того, пептид можно применять в любой форме для местного применения, такой как мазь, крем, гель и т.д., с любым вспомогательным устройством для трансдермального применения или без него. Пептид можно также представить в виде его генетической последовательности и клонировать в экспрессирующую систему отдельно или в сочетании с последовательностями других пептидов для получения молекулы конечного пептида для использования активности пептида, как описано здесь.
Доза каждого пептида может составлять 1 нг - 10 г на кг массы тела. Предпочтительной для инъекционного способа введения является доза 10 нг - 10 мг на кг, а более предпочтительно 1 мкг - 1 мг на кг. Однако эффективная доза может составлять ниже 1 нг на кг массы тела вследствие того, что один или несколько пептидов могут действовать через рецепторы, которые индуцируют каскад нормального физиологического ответа. Альтернативно, один или несколько пептидов могут непосредственно быть инициаторами целого каскада реакций. Для перорального приема количество может составлять 1 нг - 10 г на кг массы тела в сутки, более предпочтительно 0,1 мкг - 1 г на кг массы тела в сутки и еще более предпочтительно 1 мкг - 10 мг в сутки.
II. ГЕННАЯ ТЕРАПИЯ И СПОСОБ ЛЕЧЕНИЯ
Генную терапию на основе указанных выше последовательностей пептидов осуществляют посредством конструирования последовательности нуклеиновой кислоты, которая кодирует один из этих пептидов. Нуклеиновую кислоту можно химически синтезировать и функционально лигировать с промотором, и клонировать в экспрессирующий вектор. Затем для экспрессии в клетках человека в качестве формы генной терапии экспрессирующий вектор вводят в организм человека. Как применяют здесь, термин "генетические векторы" включает эти экспрессирующие векторы. Векторы, которые можно использовать для генной терапии, включают аденоассоциированный вирус (Mizuno, M. et al. (1998). Jpn J Cancer Res 89, 76-80), векторы LNSX (Miller, A. D. et al. (1993) Methods Enzymol 217, 581-599) и лентивирус (Goldman, M. J. et al. (1997) Hum Gene Ther 8, 2261-2268).
Другие носители для доставки пептида включают векторы, кодирующие желательный пептид, которые можно перенести в организм, способный к репликации в организме хозяина, которому хотят ввести пептид, без значительных вредных воздействий на здоровье организма хозяина. Например, экспрессирующие векторы можно перенести в организм, который не является патогенным для организма хозяина, которому хотят ввести пептид. В некоторых вариантах осуществления экспрессирующий вектор продуцирует желательный пептид в бактериальном или грибковом организме, который не обладает значительными вредными воздействиями на здоровье организма хозяина, которому вводят пептид. Например, экспрессирующим вектором, кодирующим желательный пептид, может быть экспрессирующий вектор, который продуцирует желательный пептид в организме, таком как лактобактерия, E. Coli или дрожжи. В одном варианте осуществления экспрессирующий вектор продуцирует желательный пептид в микроорганизме, который в норме находится в кишечнике млекопитающих или микроорганизме, к которому толерантен пищеварительный тракт млекопитающих. Некоторые виды бактерий, в которых желательный пептид может быть экспрессирован, включают в качестве неограничивающих примеров виды Lactobacillus, такие как L. acidophilus, L. amylovorus, L. casei, L. crispatus, L. gallinarum, L. gasseri, L. johnsonii, L. paracasei, L. plantarum, L. reuteri, L. rhamnosus или другие; виды Bifidobacterium, такие как B. adolescentis, B. animalus, B. bifidum, B. breve, B. infantis, B. lactis, B. longum или другие; Enterococcus faecalis или Ent. facium; Sporolactobacillus inulinus; Bacillus subtilis или Bacillus cereus; Escherichia coli; Propionibacterium freudenreichii; или Saccharomyces cerevisiae или Saccharomyces boulardii.
Химически синтезированные или полученные другими способами, включающими в качестве неограничивающих примеров обратную транскрипцию мРНК с получением молекул кДНК, последовательности нуклеиновых кислот, которые кодируют любой из пептидов по настоящему изобретению, известными специалистам в данной области способами генетической инженерии встраивают в экспрессирующий вектор для переноса гена в желательные организмы. Экспрессирующие векторы могут представлять собой ДНК-векторы или РНК-векторы. Например, экспрессирующие векторы могут быть основаны на плазмидных или вирусных генетических элементах. Экспрессирующие векторы могут представлять собой векторы, которые реплицируются экстрахромосомно, или векторы, которые встраиваются в хромосому.
Экспрессирующие векторы содержат промотор, функционально связанный с нуклеиновой кислотой, кодирующей пептид по настоящему изобретению. Промотор может представлять собой регулируемый промотор, такой как индуцируемый промотор, или конститутивный промотор. В некоторых вариантах осуществления для получения желательного уровня экспрессии пептида промотор можно выбирать. Кроме того, если необходимо, экспрессирующие векторы могут содержать другие последовательности для обеспечения продукции, презентации и/или секреции пептидов. В некоторых вариантах осуществления нуклеиновая кислота, кодирующая пептид по настоящему изобретению, функционально связана с последовательностью нуклеиновой кислоты, которая направляет секрецию пептида. Например, нуклеиновая кислота, кодирующая пептид по настоящему изобретению, может быть функционально связана с нуклеиновой кислотой, кодирующей сигнальный пептид.
В некоторых вариантах осуществления экспрессирующие векторы, сконструированные для кодирования пептидов по настоящему изобретению, могут представлять собой экспрессирующие векторы, адаптированные для экспрессии пептида по настоящему изобретению в составляющих нормальную флору кишечника млекопитающих бактериальных видах, таких как виды Lactobacillus и Bacillus subtilis. Примеры таких экспрессирующих векторов можно найти в патентах США № 6100388, выданном Casas, и № 5728571, выданном Bellini соответственно. Таким образом, эти документы специально включены сюда в качестве ссылок в полном объеме. Следует понимать, что можно использовать любой экспрессирующий вектор, который облегчает экспрессию пептида по настоящему изобретению в организме, который не является вредным для здоровья организма хозяина, которому вводят пептид.
В некоторых вариантах осуществления экспрессирующие векторы, которые сконструированы для кодирования пептидов по настоящему изобретению, могут представлять собой экспрессирующие векторы, адаптированные для экспрессии пептида по настоящему изобретению в высокоустойчивых в кишечнике млекопитающих дрожжевых видах, таких как Saccharomyces cerevisiae; или предпочтительно Saccharomyces boulardii, которые могут колонизировать кишечник человека и которые применяют для лечения определенных форм диареи. Можно применять дрожжевые экспрессирующие векторы, которые конститутивно экспрессируют гетерологичные белки и пептиды, являются высокостабильными, поэтому хорошо переносятся в дочерние клетки при митозе и мейозе и могут содержать кодирующую сигнальный пептид или пептиды последовательность, обеспечивающую высокий уровень секреции рекомбинантного белка. Пример такого дрожжевого вектора приведен в патенте США № 6391585, выданном Jang et al., который таким образом специально включен сюда в качестве ссылки в полном объеме.
Экспрессирующие векторы, кодирующие пептиды по настоящему изобретению, можно вводить в организм, предназначенный для экспрессии пептидов, посредством известных в данной области способов. Эти способы включают традиционные способы трансформации бактерий, дрожжей или других микроорганизмов с применением, например, компетентных вследствие применения химического способа бактериальных клеток, трансформации посредством электропорации или ацетата лития (для дрожжей), а также современных достижений в области трансформации бактериальных видов, устойчивых к таким процедурам. В некоторых вариантах осуществления экспрессирующие векторы вводят в лактобактерии, известные как устойчивые к трансформации, с применением способа, описанного Leer et al. (WO 95/35389), описание которого включено сюда в качестве ссылки в полном объеме. Введенные последовательности могут встраиваться в хромосомную ДНК микроорганизмов или могут оставаться в качестве внехромосомных ДНК-элементов.
Затем для осуществления непрерывной иммунотерапии такие полученные способами генной инженерии микроорганизмы, содержащие экспрессирующий вектор, можно инокулировать в пищеварительный тракт, влагалище, трахею и т.д. В некоторых вариантах осуществления организмы, экспрессирующие пептиды по настоящему изобретению, принимают внутрь в неактивной форме или предпочтительно в живой форме. В кишечнике эти микроорганизмы продуцируют указанные пептиды, высвобождают их в просвет посредством секреции или лизиса микроорганизма или другим способом предоставляют пептиды хозяину, после чего пептиды осуществляют предназначенное для них действие в отношении организма хозяина. В других вариантах осуществления пептиды предоставляются хозяину на слизистых оболочках носовых ходов, влагалища или тонкого кишечника.
Другой способ лечения представляет собой применение липосом в качестве способа доставки конкретной нуклеиновой кислоты в клетки организма человека. Нуклеиновую кислоту (такую как экспрессирующий вектор, содержащий последовательность нуклеиновой кислоты, кодирующую пептид, содержащий выбранную из SEQ ID № 2-31 последовательность, по существу состоящий или состоящий из выбранной из SEQ ID № 2-31 последовательности, где указанный пептид не содержит последовательность пептида CMS-010, и его функциональные производные) помещают в среду, которая облегчает клеточное узнавание и встраивание в хромосому, как описано в Gao, X. and Huang, L. (1995) Gene Ther 2, 710-722 и патенте США 6207456. Альтернативно, сам пептид можно инкапсулировать в липосому и доставлять непосредственно с применением способа, описанного в патенте США 6245427. Все указанные выше научные публикации и патенты включены сюда в качестве ссылок в полном объеме.
Последовательности нуклеиновых кислот, приемлемые для генной терапии и способа лечения, указанных выше, включают последовательности, кодирующие эти пептиды и их функциональные производные. Любую из многочисленных последовательностей нуклеиновых кислот можно применять для кодирования этих пептидов и их производных на основании вырожденности системы кодонов.
Следующие ниже ссылки включены сюда в качестве ссылок в полном объеме.
1. Principles of Pre-clinical Research of New Drugs, People's Republic of China. 1993, 7:134-135 Shuyun Xu, Rulian Bian, Xiu Chen. Methodology of pharmacological experiment. People's Health Publishing House. 1991, 1221-1234.
2. Principle of new drug research in pre-clinic issued by Ministry of Health, People's Republic of China. 1993, 7:140.
3. Jinsheng He, Ruizhu Li, Tingyi Zong. The study on MTT reduction method of testing NK cell activity. China Immunology Journal. 1996, 1(6):356-358.
4. Quan Wang. Modern medical experiment method. People's Health Publishing House. 1998, 482-483.
5. Principle of new drug research in pre-clinic issued by Ministry of Health, People's Republic of China. 1993, 7:141.
6. Principle of new drug research in pre-clinic issued by Ministry of Health, People's Republic of China. 1993, 7:132-133.
7. Principle of new drug research in pre-clinic issued by Ministry of Health, People's Republic of China. 1993, 7:128-129.
8. Yuanpei Zhang, Huaide Su. Pharmacological experiment (second edition). People's Health Publishing House. 1998, 137-138.
9. Jiatai Li, clinical pharmacology (second edition). People's Health Publishing House. 1998, 1338-1339.
III. ПЕПТИДНЫЕ КОНЪЮГАТЫ И ПРЕПАРАТЫ С ПЕПТИДАМИ, СОДЕРЖАЩИМИ ВЫБРАННУЮ ИЗ SEQ I