Композитный материал, упаковка и носитель, выполненные на основе композитного материала, и способ получения композитного материала
Иллюстрации
Показать всеИзобретение относится к олигодинамическому композитному материалу, представляющему собой слой полимерного материала с электретными свойствами, в объеме которого, с выходом на одну рабочую поверхность электретного материала, расположен один первый дискретный элемент, выполненный из частиц металлов с различной работой выхода электронов и способных проявлять олигодинамическое действие. Композитный материал может также содержать другие дискретные элементы, представляющие собой дозатор лекарств или средства абсорбции. Композитный материал отличается высокой эффективностью за счет эффекта синергизма электретного материала и металла, проявляющего олигодинамическое действие. 16 з.п. ф-лы, 4 ил. 1 табл.
Реферат
Изобретение относится к области композитных материалов, а также устройств, выполненных на основе указанных композитных материалов, и может быть использовано в медицине, лечебной косметологии, гигиене и санитарии, в производстве носителей и упаковок лекарственной, оздоравливающей, косметической, пищевой, парфюмерной продукции, в производстве бытовых приборов и потребительских товаров, как материал самостоятельных элементов или элементов, включенных в состав более сложных устройств.
В дальнейшем будут использованы следующие основные термины:
Олигодинамическое действие - влияние очень малых концентраций положительных ионов (главным образом металлов, например Cu, Ag, Au и др.) на живые организмы. При олигодинамическом действии ионы металлов концентрируются на поверхности биологического объекта, что обусловливает блокирование свободных карбонильных и сульфогидрильных групп поверхностных структур. Олигодинамическое действие распространяется на ферментные системы, а также на активность неорганических катализаторов. К олигодинамическому действию относят и влияние отрицательных ионов, способных инактивировать ферментные системы.
Электреты - диэлектрики, сохраняющие поляризованное состояние длительное время после снятия внешнего воздействия, вызвавшего поляризацию. Практически все известные органические и неорганические диэлектрики могут быть переведены в электретное состояние. Все электреты имеют стабильный поверхностный заряд ~10-8 к/см2. Их используют как источники постоянного электрического поля (микрофоны и телефоны, вибродатчики, генераторы и т.п.), также в электрометрах, вольтметрах, в устройствах дозиметрии, электрической памяти, как фокусирующие устройства в барометрах, гигрометрах и газовых фильтрах, и др. Перспективные исследования по использованию электретов проводят в стоматологии, травматологии, ортопедии, хирургии, кардиохирургии, косметологии и других областях.
Диэлектрическая электроника - область физики, занимающаяся исследованием и практическим применением явлений, связанных с протеканием электрических токов в диэлектриках. Исследования тонких диэлектрических пленок показали, что при контакте с металлом в диэлектрик переходят электроны или дырки, в результате чего у контакта в тонком слое диэлектрика возникают в заметном количестве свободные носители заряда.
Работа выхода - энергия, затрачиваемая на удаление электрона из твердого тела или жидкости в вакуум.
Интегральная схема - интегральная микросхема, микроминиатюрное электронное устройство, все или часть элементов которого нераздельно связаны конструктивно и соединены между собой электрически. В качестве материалов применяют алюминий, золото, титан, нихром, окись тантала, моноокись кремния, титанат бария, окись олова и другие.
Эффект синергизма - суммарный эффект воздействия материала, в частности, на биологические ткани и гидрофильные среды, превышающий эффективность его отдельных компонентов
Биологически активное вещество - вещество, вырабатываемое организмом или получаемое им извне и оказывающее либо стимулирующее, либо подавляющее воздействие на происходящие в организме процессы. К ним относятся биолины, гормоны, ингибиторы, ферменты, фитогормоны, биогенные стимуляторы, пептиды и др.
Из существующего уровня техники известны различные композитные материалы, в частности, содержащие металлы с олигодинамическими свойствами.
Известен серебросодержащий материал из микрокристаллической целлюлозы, который изготавливают путем пропитки целлюлозного материала водным раствором AgNO3, с дополнительной обработкой смесью аммиака и глицерина (RU, 2256675). Данный материал может быть использован только для медицинских повязок и не редко вызывает раздражение раневой поверхности, аллергию, так как содержит продукты термохимического разложения химических реактивов и самой микрокристаллической целлюлозы.
Известно раневое покрытие, содержащее один или более компонентов, состоящих из водорастворимых полимеров класса полисахаридов и их производных, составляющих основу композиции, в композицию также введены частицы благородных металлов с размерами до 100 нм в количестве 0,001-3% (RU, 2006120301). Предложен также перевязочный материал с нанесением серебра в вакууме (RU 56493). В качестве недостатка вышеуказанных материалов следует отметить недостаточную биологическую активность к патогенной флоре.
Также известен способ введения в организм человека или животного лекарств или других веществ, включающий дистанционное разрушение путем СВЧ-воздействия оболочки предварительно введенной в организм микрокапсулы, состоящей из внутренней полости, содержащей вещество, предназначенное для введения в организм, и оболочки в виде полимерной пленки, выполненной из n разнозаряженных полиэлектролитных слоев, между которыми расположены от 1 до n-1 слоя наночастиц металлов или оксидов Fe, или Au, или Ag, или Ni, или Со (RU, 2006121560). Недостатком способа является сложность изготовления и возможный вред от СВЧ-воздействия на организм человека или животного.
Предложено устройство для физического воздействия на организм человека через зоны акупунктуры (RU, 2112497). Средство включает два электрода. Корпус катода выполнен в виде пустотелой цилиндрической капсулы из медного сплава - латуни или оловянистой бронзы. В торцевых частях капсулы размещены электреты, а между ними помещена смесь минералов Корпус анода выполнен в виде пустотелой капсулы из сплава цинк-свинец-олово. К недостаткам устройства относятся его громоздкость, дороговизна, высокое содержание вредных примесей олова и свинца.
Известен пленочный материал на полиэфирной основе с наноразмерным металлическим покрытием (RU, 2295448). Материал обеспечивает повышение удельной электрической емкости конденсатора и используется только для производства анодов электролитических конденсаторов.
Известен пористый губчатый целлюлозный материл для лечения ран и ожогов, содержащий цинк, медь, селен и/или железо в количествах от 0,1 мкг/г сухого материала (RU, 2281088, FI, 20011232, US, 60/297269).
Предложен фармацевтический препарат для чрескожного введения, который включает подложку и адгезивный слой, содержащий хлорид металла, адгезив, соединение пропинилфенетиламина и его гидрохлорида, где адгезивный слой подвергнут поперечной сшивке (RU, 2006119611, JP, 2005-165051) и другие.
Из существующего уровня техники известны бытовые ионаторы воды, например, содержащий источник питания, соединенный через электрическую схему с электродами, погружаемыми в воду, по крайней мере, один из которых, анод выполнен серебряным (Кульский Л.А. Серебряная вода. Киев: Наукова думка, 1982, с.115-121.). К типичным недостаткам подобных устройств относятся привязанность его к электрической сети, невозможность использования в автономном режиме в полевых условиях, невысокий уровень электробезопасности. Из общих недостатков вышеприведенных примеров можно отметить узость практического применения и большие трудозатраты на их изготовление.
Предложено использование электрета в качестве медицинского пластыря для физиотерапевтического лечения и ухода за больными (RU, 94020964). Несмотря на положительные результаты применения, этот материал не обладает высокой биологической эффективностью, в частности, из-за отсутствия олигодинамического эффекта.
Известен материал на основе тканых и нетканых материалов, содержащий наночастицы серебра, железа, алюминия, меди (RU, 2314834). Этот материал может содержать дополнительный слой, который в свою очередь может содержать лекарственные вещества, Но биологическая активность материала не высока из-за отсутствия электретных свойств, что значительно сужает область его применения.
Наиболее близким техническим решением является устройство для заживления ран, содержащие пленочное покрытие на пластичной основе из металлической фольги, на которое нанесено электретное покрытие стехиометрического состава Ta2O5 (RU, 2001114454). Способ получения и состав данного устройства вполне отвечают заявленным целям по его ограниченному применению, однако отсутствует биологически значимый эффект взаимодействия между частицами металлов, имеющих разную работу выхода электронов.
Техническая задача, решаемая посредством разработанного изобретения, состоит в создании нового композиционного материала, обладающего широким диапазоном применения в различных областях деятельности человека.
Технический результат, получаемый при реализации разработанного изобретения, состоит в эффекте синергизма - сверхсуммарном биологическом эффекте действия разработанного композитного материала, который превышает эффективность его отдельных компонентов, что значительно расширяет функциональные возможности устройств, созданных на основе этого материала.
Устройства, созданные на основе разработанного композиционного материала, служат источником снижения дефицита важных микроэлементов в организме, отличаются от аналогов высокой эффективностью за счет эффекта синергизма при отсутствии внешних источников электропитания, высокой электробезопасностью, миниатюрностью, универсальностью и широтой практического применения, низкой себестоимостью при серийном производстве, комфортны при эксплуатации, обладают улучшенными санитарно-гигиеническими и противоэпидемическими свойствами, легко дезинфицируются.
Для достижения указанного технического результата предложено использовать композитный материал, характеризуемый наличием слоя материала с электретными свойствами, в объеме которого, с выходом, по меньшей мере, на одну рабочую поверхность электретного материала, расположен, по меньшей мере, один первый дискретный элемент, выполненный из частиц металлов, предпочтительно, наноразмеров, с различной работой выхода электронов и способных проявлять олигодинамическое действие. При создании первого дискретного элемента предпочтительно использованы металлы, выбранные из числа металлов, необходимых для полноценной жизнедеятельности живого организма. Однако возможно введение в состав первого дискретного элемента и других металлов. Композитный материал может дополнительно содержать слой изоляционного материала (в частности, диоксид кремния), расположенный между слоем материала с электретными свойствами и первым дискретным элементом. Также композитный материал может дополнительно содержать расположенный в слое материала с электретными свойствами с выходом на его рабочую поверхность, по меньшей мере, один второй дискретный элемент, представляющий собой носитель - дозатор лекарств, биологически активных веществ, микроэлементов, штаммов бактерий, ароматических веществ. В некоторых случаях реализации первый дискретный элемент может быть расположен во втором дискретном элементе. Второй дискретный элемент может быть выполнен с выходом на вторую поверхность материала с электретными свойствами. Также композитный материал может дополнительно содержать расположенный в слое материала с электретными свойствами с выходом на его рабочую поверхность, по меньшей мере, один третий дискретный элемент, представляющий собой средство избирательной абсорбции с развитой поверхностью в составе рабочей поверхности, которая соединена сквозным отверстием с противоположной стороной материала с электретными свойствами. В некоторых случаях реализации первый дискретный элемент расположен в объеме третьего дискретного элемента с выходом на рабочую поверхность. Третий дискретный элемент может содержать компонент, способный сорбировать влагу из атмосферы. Третий и первый дискретный элемент могут быть выполнены с выходом на вторую поверхность материала с электретными свойствами. Минимальная толщина слоев композитного материала составляет 50 нм. Максимальная толщина слоев, преимущественно, составляет 40 мкм. Для удобства использования материал с электретными свойствами может иметь основу. Предпочтительно использовать клеевую основу, биологически совместимую с тканями живого организма Указанная биологически совместимая клеевая основа может быть выполнена из растворимого полимера. Также может быть использована бумажная или тканевая основа.
Указанный технический результат может быть достигнут и при использовании различной упаковки, характеризуемой тем, что она, по меньшей мере, частично выполнена из вышеприведенного композиционного материала.
Указанный технический результат может быть достигнут и при использовании различного носителя, характеризуемого тем, что он, по меньшей мере, частично выполнен из приведенного выше композиционного материала.
Указанный технический результат может быть достигнут и при использовании способа получения вышеприведенного композиционного материала, характеризуемого тем, что дискретные элементы формируют путем локального нанесения на материал с электретными свойствами компонентов дискретных элементов в сочетании с предварительной или последующей перфорацией материала. В одном из вариантов реализации компоненты наносят путем напыления компонентов под вакуумом.
Предлагаемый композитный материал получил название «Новафор» («Novafor», далее NF). Каждый из элементов материала NF может быть создан с использованием нанотехнологий, а также быть перфорированным, содержать сквозные отверстия и/или быть растворимым, и/или иметь биологически совместимую гипоаллергенную клеевую основу, например, из полиакрилатных соединений, для склеивания вышеуказанных слоев, и/или иметь дополнительную бумажную/тканевую основу.
Ионы металлов из слоя дискретных элементов и молекулы биологически активных веществ из участков носителей-дозаторов диффундируют через электролит в контактные среды и депонируются там в концентрациях, допустимых для наружного (накожного), а также внутреннего применения, включая аспирацию при распылении жидкостей и паров. Металлы с олигодинамическими свойствами выбирают, преимущественно, из ряда микроэлементов, важных для полноценной жизнедеятельности человека, многих представителей животного и растительного мира.
Слой дискретных элементов содержит, преимущественно, наноразмерные частицы металлов, которые могут располагаться с возможностью взаимной диффузии, за счет чего возрастает концентрация ионов металлов в электролите. В сочетании с электрическим полем, создаваемым слоем электрета, существенно повышается эффективность прямого оздоравливающего, обеззараживающего, обезболивающего, иммуностимулирующего воздействия при непосредственном контакте с устройством из материала NF, а также при использовании его с лекарственной или иной начинкой дискретных элементов (вкраплений) носителя-дозатора для профилактики и комбинированной фармакотерапии широкого спектра заболеваний.
К дополнительным эффектам устройств из пленочного материала NF для наружного применения можно отнести локальное согревание, нормализацию обменных процессов, улучшение кровообращения, рефлексотерапевтическое воздействие на биологически активные зоны и биологически активные точки в местах применения.
Материал NF может быть компонентом приборов диэлектрической электроники, радиоэлектроники, триботехники, а также найти применение в других промышленных областях.
Таким образом, универсальный композитный материал NF способен эффективно генерировать в заданном направлении ионы металлов, абсорбировать в участки с развитой поверхностью некоторые вещества из контактных сред в присутствии электролита, а также дозированно перемещать в контактные среды биологически активные вещества, содержащиеся в носителях-дозаторах основы материала, обладающей свойствами электрета и, соответственно, являющейся источником постоянного электрического поля. Наличие постоянного электрического поля обеспечивает повышенную активность металлов и биологически активных веществ.
Существенным отличием заявленного материала от известных является то, что суммарный биологический эффект предлагаемого композитного материала превышает эффективность его отдельных компонентов, и это значительно расширяет функциональные возможности устройств, созданных на его основе. Универсальный композитный материал NF способен эффективно генерировать в заданном направлении ионы металлов, обладающих олигодинамическим действием, абсорбировать в участки с повышенной адсорбцией определенные вещества из контактных сред в присутствии электролита, а также ускоренно перемещать в контактные среды биологически активные вещества, содержащиеся в носителе-дозаторе основы материала, обладающей свойствами электрета и, соответственно, являющейся источником постоянного электрического поля. Наличие в материале постоянного электрического поля обеспечивает повышенную активность металлов и биологически активных веществ в области рабочей поверхности материала, их эффективный перенос в контактирующие среды, при аппликации материала на кожные или слизистые покровы в качестве внутридермальной или трансдермальной терапевтической системы, при контакте с жидкостями (вода, кожные и слизистые секреты, а также напитки и т.п.), влагосодержащими субстанциями (текучие лекарства и биологически активные вещества, пища, включая замороженную и т.п.); а также водорастворимыми субстанциями (мелкодисперсные лечебные, биологически-активные порошки, твердые растворы и т.п.) за счет участков с повышенной адсорбцией, содержащих компонент, растворяющийся за счет поглощения влаги из атмосферы, который смачивает контактирующие поверхности и растворяет активные субстанции между ними. При фиксации рабочей поверхности материала на любой другой поверхности, доступ к атмосферной влаге происходит через сквозные отверстия, которые соединены с вкраплениями материала. Биологическая активность материала в присутствии любой электролитической жидкости повышается и за счет взаимодействия между частицами металлов, имеющих разную работу выхода электронов.
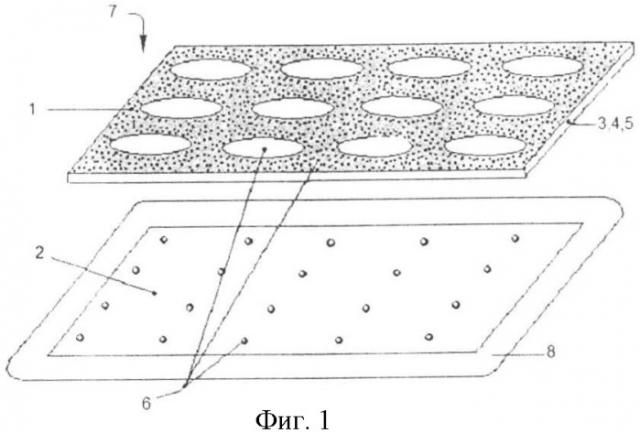
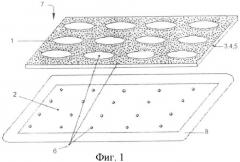
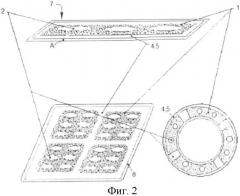
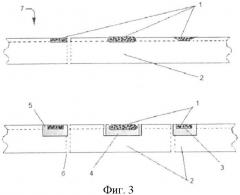
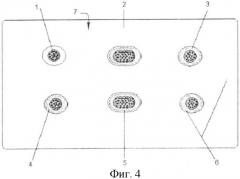
На Фиг.1 представлен вариант композиционного материала NF с разделением слоев, на Фиг.2 - вариант материала в виде ленты, квадрата и круга, на фиг.3 - вид в разрезе основных элементов, на Фиг.4 - вид рабочей поверхности; форма всех элементов условна. При этом использованы следующие обозначения: дискретный слой 1, состоящий из частиц или сплавов биологически совместимых металлов, слой 2 электрета, слой 3 изолятора, расположенный между основными слоями 1 и 2, элемент - дозатор (вкрапление) 4 с выходом на рабочую поверхность материала, дискретный элемент (вкрапление) 5, способное к избирательной абсорбции, сквозные отверстия 6 между слоями; рабочая поверхность 7 материала; клеящий слой 8.
При необходимости (на графическом материале не показаны) устройство может дополнительно содержать энергоснабжающие компоненты и/или интегральные микросхемы, и/или индикаторы, соединенные с устройством. Ниже рассматриваются основные варианты способов получения материала NF.
В зависимости от экономической и технологической целесообразности, для получения слоя 2 и дополнительных элементов 3, 4 и 5 используют любые подходящие материалы синтетического, природного происхождения или их производные, например, полимеры, выбранные из группы, содержащей поливинилхлорид, полиметилметакрилат, полиэтилентерефталат, поликарбонат, полиамид, полиэтилен, полипропилен, полиэфир, фторопласт и многие другие, а также сополимеры, например, сополимер N-окси-1,4-этиленпиперазина и (N-карбокси)-1,4-этиленпиперазиния бромида, с добавлением, например, хлопчатобумажного, вискозного волокна или их смесей и т.п.
Технология приготовления материала может включать этапы: получения раствора полимера-носителя, распределения в нем биологически активных веществ и/или лекарственных препаратов, разлива полученной массы на основу и/или гидрофобную подложку в присутствии, например, сильного постоянного электрического поля, напылением частиц металлов, с последующим высушиванием при временном и температурном режиме, определяемом видом пленок, перфорации, резки, стерилизации и герметичной упаковки. Для изготовления предлагаемого материала могут использоваться и готовые электретные пленки, включая пленки, содержащие металлонаполненные полимеры. В зависимости от способов получения электретов, характеристик наносимых металлов и дополнительных элементов, материалу присваиваются соответствующие классификационные индексы (табл.).
| Таблица | ||
| Классификационные индексы материала Novafor* | ||
| По свойствам слоя 1: | монометаллический | - |
| биметаллический | В | |
| полиметаллический | В+ | |
| По способам получения слоя 2; в основном, являются: | коронноэлектретом | Ko |
| электроэлектретом | Е | |
| фотоэлектретом | F | |
| лазероэлектретом | L | |
| термоэлектретом | Т | |
| радиоэлектретом | Re | |
| трибоэлектретом | Tr | |
| магнетоэлектретом | Me | |
| криоэлектретом | Kr | |
| механоэлектретом | М | |
| комбинацией электретов | С | |
| По наличию дополнительных элементов; содержат | дискретный слой 3 | I |
| вкрапления 4 | D | |
| вкрапления 5 | А | |
| По наличию клеевой | содержат клеевую основу | K |
| основы: | не содержат | - |
| По растворимости: | растворимы | Н |
| нерастворимы | - | |
| По конфигурации: | пленочные (листовые или фигурные) | Р |
| односторонние | V | |
| двухсторонние | W | |
| нитевидные (прямые или фигурные) | N | |
| в виде рулона или «сандвича» | S | |
| * Примечание: все материалы пригодны для использования в медицинских и гигиенических целях, для контакта с пищевыми продуктами, а также проходят контроль по ГОСТ 25209-82 (Пластмассы и пленки полимерные. Методы определения поверхностных зарядов электретов). |
Для изготовления электретов предложен ряд способов (P.W.Chudleigh, Mechanism of Charge Transfer to a Polymer Surface by a Conducting Liquid Contact, 21 Appl. Phys. Lett., 547-548, Dec 1,1972; P.W.Chudleigh, Charging of Polymer Foils Using Liquid Contacts, 47 J. Appl. Phys., 4475-4483, October 1976; US 4215682; US 4588537; US 4798850; US 5280406; US 5411576 A; US 5496507 A; WO 97/07272 Al; US 5908598 A; RU 2189850; RU 2260866; RU 2266771; RU 2298245; RU 2002119973 и др.).
Также известно, что эффективным с практической точки зрения является метод получения композитов, синтезируемых на основе микрочастиц термопластичных полимеров, покрытых наночастицами металла. Такой подход позволяет получить наиболее равномерное распределение металла в матрице полимера при последующем получении материала (Анисимов А.Ю., Грехова О.Б. Электрическая проводимость и физико-механические характеристики никель-наполненных олигомер-олигомерных композиционных материалов. // Журн. прикладн. химии, 1998. Т.71. №10. С.1713-1716.). Приемлемы способы, которые позволяют наносить частицы металлов слоя 1 и дополнительных элементов на слой 2, например, с помощью экструзионного ламинирования; напыления на горячем расплаве биосовместимого клея, который наносят на слой 2 в количестве 5-20 г/м2; с использованием вакуумно-плазменной технологии, способом распылительной сушки; совмещения методов гелиографии, или флексографии, или офсетной печати (предпочтительно, с разрешением до 1 мкм) с методами испарения и сублимации металлов под вакуумом, а также другими методами. В частности, известен метод нанесения металлов в вакуумной камере с использованием магнетронного напыления (RU, 2314834).
Предлагаемый материал производят с использованием в качестве этапа одного или нескольких из вышеперечисленных способов. Способ может включать обработку материала лазером, имеющим мощность, равную 1,5-300 Вт, с последующей перфорацией и резкой материала. Для нанесения на материал используются как металлы, предложенные ранее (RU, 2299057), так и другие, обладающие выраженным олигодинамическим действием. Дополнительные элементы материала 4 и 5 формируют путем нанесения на металлонаполненные электретные пленки соответствующих мелкодисперсных составов, растворов с предварительной или последующей перфорацией материала. Технология получения материала NF и его элементов может иметь дополнительные особенности, определяемые назначением материала. Лечебный материал NF высоко эффективен при лечении раневых поверхностей, ссадин, ожогов, стимуляции пролиферативных процессов в ранах, может использоваться в качестве противоболевых стимуляторов, индивидуальных средств для оказания первой медицинской помощи в виде, например, салфеток, пластырей и т.п. Материал не вызывает аллергических реакций при длительном наложении на раневую поверхность. Возможность дополнительного содержания слоев позволяет улучшить его сорбционные свойства при лечении ран с раневым экссудатом, материал не присыхает к ранам, может безболезненно наноситься и сниматься. Пленки, пластыри, комбинированные повязки или тампоны NF актуальны для активной локальной диффузии препаратов, которые в зависимости от биологически активных вкраплений, в ряде случаев способны заменять инъекции в качестве гигиенически безопасного аналога. Исходя из состава вкраплений, NF может обладать усиленными анальгетическим, противовоспалительным, заживляющим, антимутагенным, антихолестериновым, иммуномодулирующим, детоксирующим, гормонотерапевтическим мембранопротекторным, антиоксидантным и другими эффектами. Такие формы выпуска более безопасны по сравнению с аналогичными препаратами в виде таблеток. Возможен выпуск растворимых капсул NF, содержащих вещества с вышеуказанными эффектами или с содержанием сбалансированных добавок активных микроэлементов, витаминов, провитаминов, фитонцидов, гормонов и т.п.
Известно, что действующее вещество дня внутридермального или трансдермального введения должно обладать целым комплексом необходимых качеств: способностью проникать через кожу, не ухудшая характеристики прилипания клеящего компонента материала, не вызывая раздражения кожи и аллергических реакций, обладать хорошими фармакокинетическими и фармакодинамическими характеристиками, характеристиками метаболизма, которые удовлетворительно согласуются с терапевтическим действием при непрерывном введении, а также обладать относительно широким спектром терапевтического действия. В настоящее время существует длинный перечень фармацевтических веществ, которые вводят чрескожным и/или внутрикожным путем.
Приемлемые антимикробные или антибактериальные соединения могут быть выбраны из следующих: триклозан, неомицин, клиндамицин, полимиксин, бацитрацин, пероксид бензоила, пероксид водорода, тетрациклины, такие как доксициклин или миноциклин, сульфамидные препараты, такие как сульфацетамид, пенициллины, цефалоспорины, такие как цефалексин, и хинолоны, такие как ломефлоксацин, олфлоксацин или тровафлоксацин. Подходящие противоболевые средства выбирают, например, из следующих: лидокаин, тримекаин, диклофенак, кетопрофен, ибупрофен и др. Приемлемые противогрибковые соединения выбирают из следующих: фарнезол, клотримазол, кетоконаэол, эконазол, флуконазол, увдециленат цинка или кальция, увдециленовая кислота, гидрохлорид бутенафина, олаимин циклопирокса, нитрат миконазола, сулконазол, нистатин и гидрохлорид тербинафина. Подходящие противовоспалительные соединения выбирают из следующих: стероидные средства, выбранные из гидрокортизона, ацетонида флуоцинолона, галцинонида, пропионата галобетазола, пропионата клобетазола, дипропионата бетаметазона, валерата бетаметазона и ацетонида триамцинолона и нестероидные противовоспалительные средства, выбранные из ибупрофена, кетопрофена, напроксена, алоэ вера, корня канадской ивы; цинка и аллантоина. Подходящие антивирусные соединения, выбирают из тамвира, ацикловира и пенцикловира.
Изобретение иллюстрировано следующими примерами, не исчерпывающими области применения материала
Пример 1. Исследования проводили в условиях амбулаторного приема на базе медпункта СПб НПИГИ. Для опытной группы использовали перфорированный пленочный материал Novafor BKoDAKPV (см. табл.1.) с содержанием на рабочей поверхности наночастиц серебра и меди в соотношении 10:3. Дополнительным носителем лекарственных средств являлись хлопковискозные вкрапления на перфорированной электретной полиэтиленовой пленке (толщиной 40 мкм), которые были пропитаны водным раствором полиэтиленгликолей с молекулярным весом 200-2000 и лекарственными препаратами антисептического и анестезирующего действия с вариантами допустимого содержания на носителе: полиэтиленгликолей 10-30 мг/см2; антисептиков 0,03-1,0 мг/см2 (в частности, использовали триклозан 0,1 мг/см2) и анестетиков 0,05-1,2 мг/см2 (в частности, использовали 0,5% раствор гидрохлорида лидокаина (содержание лидокаина 0,5 мг/см2). Хлопковискозные вкрапления (25-120 г/м2) обеспечивали сорбционную способность материала не ниже 8 г/г. Размер отверстий 6 не менее 0,3 мм. Перфорация материала выполнена в виде сквозных каналов, суммарная площадь отверстий которых составляет от 10% до 40% общей площади. Наличие сквозных каналов было способно обеспечить отток, например, раневого экссудата в хлопковискозные вкрапления. Материал использовали в виде прозрачной пленки размером 3,5×7,0 см в герметичной стерильной упаковке по 5 шт. Каждая из пластинок содержала открытые электретные промежутки на рабочей поверхности площадью 0,5 см2. Зону задержки роста микроорганизмов определяли методом дисков по наиболее распространенному виду инфекции - золотистому стафилококку. Поглотительную способность определяли сравнением веса сухого и влажного материала. Стерильность определяли микробиологическим методом по подавлению роста колоний микроорганизмов в чашке Петри с агар-агаром, на поверхности которого располагали образец рабочей поверхности материала.
В опытной группе 7 амбулаторных пациентов, из них 3 мужчин и 4 женщины в возрасте от 22 до 57 лет с последствиями бытовых травм: небольшими ранами, ссадинами, ожогами II-IIIa степени (два случая).
В контрольной группе 5 амбулаторных пациентов, из них 2 мужчин и 3 женщины в возрасте от 24 до 42 лет с ранами и ссадинами, которым проводили традиционную терапию раневого процесса с ежедневной сменой асептических ватно-марлевых повязок, пропитанных триклозаном (0,8 мг/см2) и 2% раствором гидрохлорида лидокаина. В контрольной группе повязки применяли на площади от 0,3 до 1% поверхности тела.
Лечение в обеих группах начинали на 2-4 сутки после травмы (в момент первого обращения), продолжительность лечения составляла от 3 до 12 суток.
В опытной группе повязку из материала NF применяли на площади от 0,5 до 2% поверхности тела. Перевязки проводили каждые 3 дня до полной эпителизации ран. При поверхностных ожогах, когда количество раневого отделяемого значительно уменьшалось, повязку оставляли на ране до полной эпителизации. Повязку начинали применять в первую фазу раневого процесса. На фоне лечения уже к 3 суткам (после первой перевязки) значительно уменьшились явления перифокального воспаления, а при ожогах II-IIIa степени сформировался сухой струп. Раневое отделяемое впитывалось сорбционным слоем и высыхало. При ожогах II-IIIa степени после отторжения струпа повязку оставляли на ране до полной эпителизации и самостоятельного отделения покрытия, при этом сроки эпителизации составили в среднем 10 суток после травмы. В опытной группе нагноений под повязкой не отмечалось, количество стафилококков на раневых поверхностях составляло 1-2% от исходной популяции, в то время как в контрольной группе эта величина достигала 15-17%, у двух пациентов было отмечено нагноение ссадин. Не осложненная эпителизация раневых поверхностей на 6 день лечения отмечена у 73% пациентов опытной группы и у 58% пациентов контрольной группы. В опытной группе 65% случаев применения боли уменьшались через 20-40 минут и в 85% случаев боли прекращались через 2-3 часа. В опытной группе эти показатели составили, соответственно, 41% и 68%.
Испытания показали, что при использовании материала эффективно купируются явления воспаления в ране и болевой синдром, небольшие раневые поверхности и ссадины ускоренно эпителизируются. За счет выраженных сорбционных свойств рабочей поверхности материала в комплексе с действием полиэтиленгликолей и наночастиц металлов под повязкой при ожогах II-IIIa степени быстро формируется сухой струп, покрытие обладает отчетливыми антибактериальными свойствами и позволяет в значительной степени купировать болевой синдром, благодаря воздействию олигодинамических и электретных свойств материала в сочетании с триклозаном (0,1 мг/см2) и лидокаином (0,5 мг/см2).
Было установлено, что вышеуказанное сочетание свойств материала позволяет эффективно использовать минимальные терапевтические дозы этих дополнительных лечебных препаратов, значительно снижая риск развития лекарственных интоксикаций и аллергических проявлений у пациентов. Материал способен обеспечивать проникновение через кожу максимально возможного количества действующих веществ. Материал хорошо прилежит к раневой поверхности, при его использовании сохраняется визуальный контроль течения раневого процесса за счет прозрачности материала, обеспечен микроотток раневого экссудата через материал, не требуется ежедневной замены, существенно уменьшены трудозатраты при перевязке пациентов, экономично расходуется перевязочный материал. Сроки замены повязок пролонгируются и, соответственно, раневые поверхности в меньшей степени подвержены травматизации. У исследуемых не выявлено каких-либо аллергических реакций и побочных эффектов. Материал NF в вице прозрачной пленки размером 3,5×7,0 см в герметичной стерильной упаковке по 5 шт. наиболее удобен при лечении небольших раневых поверхностей, обширных ссадин, при ожогах II-IIIa степени, а также может быть целесообразен в комплексной терапии трофических язв, пролежней в стадии грануляции и т.п. Материал легко и атравматично снимается после пропитки обычными антисептиками. Микробной загрязненности ран не отмечено. Использование пленочного материала NF не препятствует применению водорастворимых мазей или растворов поверх материала. За счет содержания наночастиц металлов с олигодинамическими свойствами материал обладает улучшенными противоэпидемическими и санитарно-гигиеническими свойствами, обладает хорошей переносимостью кожей, физической и химической стабильностью при длительном хранении и применении, а также имеет хорошие адгезивные свойства. Хранится в стерильной упаковке, удобен в применении.
Пример 2. Исследовательская задача заключалась в создании эффективной и недорогой продукции, являющейся альтернативной или дополнительной по отношению к существующим антиперспирантам-дезодорантам.
Исследования проводились в амбулаторных условиях на базе медпункта спортивного лагеря СПб НПИГИ. Использовался материал Novafor BLPV (см. табл.1.) с содержанием на рабочей поверхности электретной полиметилметакрилатной пленки (толщиной 30 мкм) наночастиц серебра и цинка в соотношении 10:1. А хлопковискозные вкрапления (120 г/м2), имеющие выходы на рабочую поверхность материала, обеспечивали сорбционную способность материала. Перфорация материала выполнена в виде сквозных каналов, суммарная площадь отверстий которых составляла от 30% общей площади. Размер отверстий не менее 0,5 мм. Материал использовали в виде полупрозрачных пленочных наклеек размером 4,5×4,5 см в герметичной стерильной упаковке по 2 шт.Предположительно, что такой материал обладает антимикробной, сорбционной и дезодорирующей активностью.
Эффективность использования материала NF определяли в сравнении с плацебо органолептическими тестами (на образование запахов) в группе из 17 здоровых волонтеров, из них 6 мужчин и 11 женщин, средний возраст 29,5 лет. В качестве плацебо использовали перфорированную неметаллизированную неэлектретную полиметилметакрилатную пленку с хлопковискозными вкраплениями (120 г/м2), размером 4,5×4,5 см в герметичной стерильной упаковке по 2 шт.
Испытуемым было предложено побрить или эпилировать аксиллярные области (области подмышечных в