Агент для снижения инсулинорезистентности
Иллюстрации
Показать всеИзобретение относится к агенту для ингибирования продукции адипоцитокинов, в частности адипоцитокинов, которые вызывают инсулинорезистентность, и для предотвращения возникновения патологического состояния, вызываемого инсулинорезистентностью. Агент содержит 9,19-циклостан-3-ол, или 24-метилен-9,19-циклостан-3-ол, или экстракт органическим растворителем, экстракт горячей водой растения семейства Liliaceae или Gramineae, или его фракцию, которые содержат указанное соединение в качестве активного ингредиента. 5 н. и 2 з.п. ф-лы, 1 ил., 3 табл.
Реферат
Область техники
Настоящее изобретение относится к агенту для снижения инсулинорезистентности, который содержит соединение, имеющее циклоланостановый скелет в качестве активного ингредиента, и содержащим его пищевому продукту или напитку. В частности, настоящее изобретение относится к агенту для снижения инсулинорезистентности, который способен контролировать продукцию адипоцитокинов, являющихся факторами, вовлеченными в начало и обострение патологического процесса, в котором играет роль резистентность к инсулину, таких как свободные жирные кислоты, ингибитор активатора плазминогена, фактор некроза опухоли, белок-1 хемоаттрактант моноцитов и резистин, и относится к содержащим его пищевому продукту или напитку.
Уровень техники
Инсулин относится к гормонам, производимым β-клетками в островках Лангерганса поджелудочной железы, и играет важную роль в поддержании гомеостаза живого организма путем воздействия на метаболизм липидов и белков, а также на метаболизм сахаров через инсулиновые рецепторы, присутствующие в тканях-мишенях инсулина, таких как скелетные мышцы, печень и жировая ткань. Примеры воздействий инсулина на соответствующие ткани-мишени включают усиление абсорбции глюкозы из крови в мышечные клетки и адипоциты, усиление продукции гликогена в печени и мышечной ткани, ингибирование глюконеогенеза в печени, усиление потребления глюкозы и синтеза жирных кислот в адипоцитах и ингибирование деградации липидов.
Инсулинорезистентность означает состояние, при котором клетки, органы или индивидуумы требуют большего количества инсулина, чем обычно его требуется для получения соответствующих эффектов инсулина, а именно означает состояние нарушенных эффектов инсулина, в котором снижена чувствительность к инсулину. По результатам предыдущих эпидемиологических исследований гипертензия, диабет, гиперлипидемия (гипертриглицеридемия и гипо-HDL-холестеринемия), ожирение и т.п. считаются патологическими состояниями на основе инсулинорезистентности. Инсулинорезистентность является причиной недостаточного действия инсулина в метаболизме сахара, приводит к компенсаторной гиперинсулинемии для поддержания уровня сахара в крови, в результате чего возникают гипергликемия и непереносимость глюкозы, а также ухудшается диабет вследствие истощения панкреатических β-клеток. Кроме того, гиперинсулинемия увеличивает активацию симпатических нервов и усиливает поглощение натрия почками, что является причиной гипертензии, и также индуцирует постпрандиальную гиперлипидемию и гиперурикемию, увеличение уровня ингибитора-1 активатора плазминогена (PAI-1) и т.п.
При этом инсулинорезистентность индуцирует аномальный метаболизм липидов, вызываемый недостаточным действием инсулина, и уровень свободных жирных кислот (FFA), высвобождаемых из адипоцитов, увеличивается в печени, усиливая синтез триглицерида (TG), что приводит к гипертриглицеридемии. Кроме того, активность липопротеиновой липазы (LPL), обычно имеющей высокую чувствительность к инсулину, является сниженной при состоянии инсулинорезистентности, так что расщепление TG является сниженным и гипертриглицеридемия дополнительно усиливается. Кроме того, при развитии диабета возникают осложнения, такие как ретинопатия, нефропатия и гангрена, вызываемые ангиопатией, так что развивается сердечный инфаркт и мозговой инфаркт, являющиеся атеросклеротическими заболеваниями, а гипертензия осложняет сердечно-сосудистые заболевания. Описанная выше резистентность к инсулину считается в значительной степени вовлеченной в ухудшение осложненного патологического состояния (непатентный документ 1).
Недавно из результатов анализа органспецифической экспрессии генов было выявлено, что различные физиологически активные вещества секретируются жировой тканью и жировая ткань, поэтому, считается не только энергосохраняющей тканью, но также и наиболее крупным органом эндокринной системы в живом организме. Эндокринные факторы, полученные из жировой ткани, в общем называются адипоцитокинами и играют важную роль в поддержании гомеостаза в метаболизме. Однако полагают, что в случае ожирения, то есть состояния, при котором жиры накапливаются, продуцируется и секретируется излишнее или слишком маленькое количество адипоцитокинов, а баланс адипоцитокинов разрушается, что приводит к инсулинорезистентности.
Адипоцитокины классифицируются на две группы: одну, которая увеличивает чувствительность к инсулину; и одну, которая вызывает резистентность к инсулину, представительные примеры первой группы включают адипонектин, лектин, АМРК (АМФ-зависимую протеинкиназу) и т.п. В частности, было опубликовано, что адипонектин обладает эффектом сокращения инсулинорезистентности и эффектом ингибирования глюконеогенеза в печени (непатентный документ 2).
В это же время примеры адипоцитокинов, которые вызывают резистентность к инсулину, включают фактор-α некроза опухоли (TNF-α), белок-1 хемоаттрактант моноцитов (МСР-1), являющийся своего рода воспалительным хемокином, и резистин в дополнение к вышеупомянутым FFA и PAI-1. В частности, было опубликовано, что TNF-α способен вызывать резистентность к инсулину посредством ингибирования фосфорилирования тирозина инсулинового рецептора и IRS1 (субстрата-1 инсулинового рецептора) в механизме передачи инсулинового сигнала, таким образом, что ослабляется эффект инсулина. Кроме того, было опубликовано, что при состоянии инсулинорезистентности уровень МСР-1 в живом организме увеличен, а мРНК GLUT4 (переносчика-4 глюкозы), который является носителем в переносе глюкозы, PPARγ (рецептор-γ активатора пролиферации пероксисом), который является внутриядерным рецептором, β3AR (β3-адренергический рецептор), который является катехоламиновым рецептором адипоцитов β-типа, и аР2 (связывающий жирные кислоты белок-2 адипоцитов), который является связывающим жирные кислоты белком, являются сниженными. Таким образом, считается, что МСР-1 является причиной снижения чувствительности к инсулину (непатентные документы 3, 4 и 5).
В качестве агентов для снижения инсулинорезистентности были разработаны бигуанидные агенты, которые ингибируют глюконеогенез в основном в печени, и тиазолидиновые производные, улучшающие чувствительность к инсулину мышечной и жировой тканей. Эти агенты уже разрешены к применению в качестве лекарственных средств при диабете и также используются при лечении атеросклероза. Считается, что тиазолидиновые производные, представленные троглитазоном и пиоглитазоном, действуют как лиганды рецептора активатора пролиферации пероксисом (PPAR), являющегося внутриядерным транскрипционным фактором рецепторного типа, усиливая дифференцировку адипоцитов, таким образом снижая инсулинорезистентность.
В дополнение в качестве агентов для снижения инсулинорезистентности были раскрыты агент для снижения инсулинорезистентности, содержащий адипонектин или его гены, в качестве активного ингредиента (патентный документ 1), профилактический и/или терапевтический агент против заболеваний, вызванных инсулинорезистентностью, содержащий вещество, имеющее сродство к 3 подтипу бомбезинового рецептора (BRS-3) в качестве активного ингредиента (патентный документ 2), агент, снижающий уровень свободных жирных кислот (FFA), содержащий пиррольное производное в качестве активного ингредиента (патентный документ 3) и т.п. Кроме того, в качестве агентов, содержащих вещество, полученное из пищевого продукта или напитка, в качестве активного ингредиента, были раскрыты состав для снижения инсулинорезистентности, содержащий уксусную кислоту и ее ион или соль в качестве активного ингредиента (патентный документ 4), агент для снижения инсулинорезистентности, содержащий нелетучее масло, содержащее определенный диглицерид и/или моноглицерид (патентный документ 5) и т.п.
Про растительные стерины, такие как β-ситостерин, кампестерин и стигмастерин, известно, что они обладают эффектом снижения уровня холестерина в крови посредством ингибирования абсорбции холестерина, а их практическое применение было ограничено попыткой добавления их в виде масляной композиции в пищевое масло. Кроме того, были раскрыты агент против ожирения и агент, улучшающий метаболизм липидов, содержащие холестеноновое соединение в качестве активного ингредиента, которое синтезируется посредством использования растительных стеринов, таких как β-ситостерин и кампестерин в качестве исходного вещества (патентные документы 6-8 и непатентный документ 6).
Кроме того, были раскрыты усилитель секреции адипонектина, содержащий экстракт из по меньшей мере одного из рисовых отрубей, грибов шимей, хризантемы, ржи, белой березы и испанского жасмина (Alpinia zeumber) и тритерпен циклоартанового ряда или циклоартенол и/или (24S)-24,25-дигидроксициклоартанол, которые являются производными тритерпенов циклоартанового ряда (патентный документ 9).
Род Aloe в семействе Liliaceae представляет собой группу растений, включающих алоэ вера (Aloe barbadensis Miller), алоэ древовидное (Aloe arborescens Miller var. natalensis Berger) и т.п., и из опыта известно, что они обладают различным действием. Например, раскрытыми являются агенты, улучшающие иммуносупрессию, содержащие бутанольную фракцию экстракта алоэ или алоин (патентный документ 10), агент, относящийся к снижению уровня глюкозы в крови (патентные документы 11-14), агент для профилактики и снижения ожирения (патентный документ 15) и т.п., но эффект на снижение инсулинорезистентности растений, принадлежащих к роду Aloe, не был опубликован.
[Патентный документ 1] международная публикация №WO2003/63894, брошюра
[Патентный документ 2] патент Японии, опубликованный под №10-298100
[Патентный документ 3] патент Японии, опубликованный под №08-12573
[Патентный документ 4] патент Японии, опубликованный под №2002-193797
[Патентный документ 5] патент Японии, опубликованный под №2001-247473
[Патентный документ 6] патент Японии, опубликованный под №07-165587
[Патентный документ 7] патент Японии, опубликованный под №11-193296
[Патентный документ 8] патент Японии, опубликованный под №2001-240544
[Патентный документ 9] патент Японии, опубликованный под №2005-68132
[Патентный документ 10] патент Японии, опубликованный под №08-208495
[Патентный документ 11] патент Японии, опубликованный под №59-214741
[Патентный документ 12] патент Японии, опубликованный под №2003-286185
[Патентный документ 13] патент США №4598069
[Патентный документ 14] публикация патентной заявки США №2003/0207818
[Патентный документ 15] патент Японии, опубликованный под №2000-319190
[Непатентный документ 1] Insulin resistance and lifestyle-related diseases, Ed. Kazuaki Shimamoto, Shindan to Chiryosha, 2003, p.1-5
[Непатентный документ 2] Adiposcience, vol. 1, NO. 3, 2004, p.247-257
[Непатентный документ 3] Proceedings of the National Academy of Sciences, vol. 100, 2003, p.7265-7270
[Непатентный документ 4] Nature, vol. 389, 1997, p.610-614
[Непатентный документ 5] The Netherlands Journal of Medicine, vol. 6, NO. 6, 2003, p.194-212
[Непатентный документ 6] Hormone Metabolism Research, vol. 37, 2005, p.79-83
Раскрытие изобретения
При применении бигуанидного агента, который является повсеместно используемым агентом для снижения инсулинорезистентности, может произойти нарушение функций желудочно-кишечного тракта и редко - молочный ацидоз. Кроме того, тиазолидиновое производное, которое является агентом того же типа, может иногда вызвать серьезные побочные эффекты, такие как задержка жидкости, увеличение веса тела и дисфункция печени, так что их применение требует дополнительного наблюдения. Далее, для инсулинорезистентности при заболеваниях, не относящихся к диабету или гипергликемии, трудно на практике использовать противодиабетические агенты. При этих обстоятельствах желательна разработка активного начала, которое является абсолютно безопасным, может приниматься ежедневно и способно снижать инсулинорезистентность с наименьшими возможными болевыми ощущениями.
В свете вышеупомянутых проблем, авторы настоящего изобретения изучали механизмы связанных с образом жизни болезней, вызываемых инсулинорезистентностью, таких как гипертензия, диабет, гиперлипидемия (гипертриглицеридемия и гипо-HDL-холестеринемия) и ожирение, и исследовали агент, относящийся к предотвращению, улучшению и т.п. связанных с образом жизни болезней, а именно агент для снижения инсулинорезистентности. Авторы настоящего изобретения обратили внимание на адипоцитокины, являющиеся факторами, вовлеченными в начало и развитие инсулинорезистентности, и тщательно исследовали новое действующее вещество, способное снижать инсулинорезистентность путем контролирования вышеупомянутых факторов. В результате авторы настоящего изобретения обнаружили, что соединения, имеющие циклоланостановый скелет, способны контролировать продукцию адипоцитокинов, таких как свободные жирные кислоты, TNF-α и МСР-1, в частности, их эффекта достаточно для снижения продукции адипоцитокинов, которые вызывают инсулинорезистентность, таким образом, снижая инсулинорезистентность.
В отношении вышеупомянутых эффектов настоящего изобретения патентный документ 9 описывает только предотвращающий эффект растительного экстракта на дифференцировку культивируемых адипоцитов, путь синтеза тритерпенового производного циклоартанового типа и усиливающий эффект эргостерина на секрецию адипонектина, но не описывает усиливающий эффект тритерпена циклоартанового типа или циклоартенола, который является его производным, на секрецию адипонектина. В дополнение, совсем не был описан и раскрыт понижающий эффект активного ингредиента настоящего изобретения на инсулинорезистентность.
В дополнение, авторы настоящего изобретения обнаружили, что соединение, имеющее циклоланостановый скелет, напрямую снижает инсулинорезистентность без вмешательства в свойство секреции инсулина и т.п., с помощью исследования инсулинового теста толерантности (тест инсулинового стресса), в дополнение к методу клэмпа глюкозы, методу постоянной инфузии глюкозы (SSPG) и методу минимальной модели, которые являются повсеместно используемыми способами оценки инсулинорезистентности.
Такой инсулиновый тест толерантности не был проведен в вышеупомянутых патентных документах 1-5. Авторы настоящего изобретения обнаружили эффект, обладающий большим преимуществом в отношении снижения инсулинорезистентности без влияния на секрецию инсулина по сравнению с общеизвестными эффектами снижения инсулинорезистентности, и создали настоящее изобретение.
Целью настоящего изобретения является предоставление агента для снижения инсулинорезистентности, который содержит соединение, имеющее циклоланостановый скелет в качестве активного ингредиента. В дополнение, другим объектом настоящего изобретения является предоставление физиологически функционального пищевого продукта или напитка, содержащих агент для снижения инсулинорезистентности, таких как пищевой продукт, воздействующий на состояние здоровья.
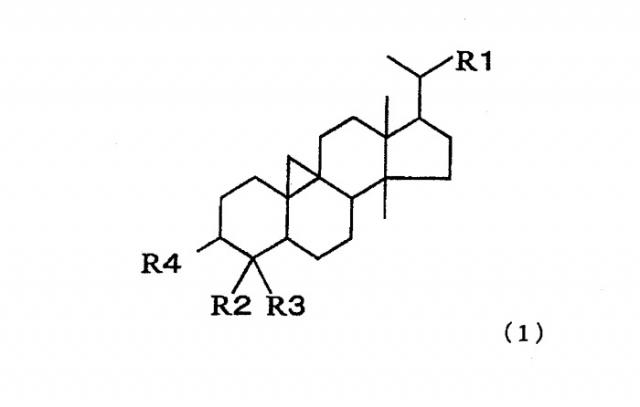
Первым изобретением настоящей заявки для разрешения вышеупомянутых проблем является агент для снижения инсулинорезистентности, содержащий соединение, представленное следующей общей формулой (1), в качестве активного ингредиента
(В формуле R1 представляет алкильную группу или алкенильную группу, содержащую 1 или 2 двойные связи, или замещенные алкильную или алкенильную группу, содержащую 1 или 2 гидроксильные группы и/или карбонильные группы, которая имеет прямую или разветвленную цепь, содержащую от 6 до 8 атомов углерода, R2 и R3, каждый независимо, представляет атом водорода или метильную группу, и R4 образует С=О с атомом углерода в составе кольца или является группой, представленной одной из следующих формул)
В дополнение, следующие пункты с (1) по (3) являются предпочтительными вариантами осуществления настоящего изобретения.
1) Вышеупомянутый R1 представлен любой из следующих формул, вышеупомянутые R2 и R3, оба, являются метильными группами, и вышеупомянутый R4 является гидроксильной группой
-СН2-СН2-СН2-СН(СН3)2
-СН2-СН2-CHRa-С(СН3)2Rb
(где Ra является любым из атома водорода, гидроксильной или метильной групп, а Rb является атомом водорода или гидроксильной группой)
-СН2-СН2-СН(СН2СН3)-СН(СН3)2
-СН2-СН2-CHRc-С(СН3)=СН2
(где Rc является любым из атома водорода, гидроксильной или метильной групп)
-СН2-СН2-С(=О)-С(СН3)=СН2
-СН2-СН2-С(=СН2)-СН(СН3)2
-СН2-СН2-СН=С(СН3)2
-СН2-СН=С(СН3)-СН(СН3)2
-СН2-СН2-С(=СНСН3)-СН(СН3)2.
2) Вышеупомянутое соединение по 1) является 9,19-циклоланостан-3-олом или 24-метилен-9,19-циклоланостан-3-олом.
3) Вышеупомянутое соединение по 1) или 2), содержащееся в количестве, по меньшей мере, 0,001% по массе.
Вторым изобретением настоящей заявки для разрешения вышеупомянутых проблем является агент для снижения инсулинорезистентности, который содержит экстракт растения органическим растворителем, или экстракт растения горячей водой, содержащий соединение, представленное следующей общей формулой (1), или его фракцию в качестве активного ингредиента, где экстракт растения органическим растворителем, или экстракт растения горячей водой, или его фракция содержат, по меньшей мере, 0,001% по сухой массе соединения, представленного следующей общей формулой (1)
(В формуле R1 представляет алкильную группу или алкенильную группу, содержащую 1 или 2 двойные связи, или замещенные алкильную или алкенильную группу, содержащую 1 или 2 гидроксильные группы и/или карбонильные группы, которые имеют прямую или разветвленную цепь, содержащую от 6 до 8 атомов углерода, R2 и R3, каждый независимо, представляет атом водорода или метильную группу, и R4 образует С=О с атомом углерода в составе кольца или является группой, представленной одной из следующих формул)
Кроме того, следующие пункты от 4) до 6) являются предпочтительными вариантами осуществления настоящего изобретения.
4) Вышеупомянутое растение принадлежит к семейству Liliaceae или Gramineae.
5) Вышеупомянутый R1 представлен одной из следующих формул, вышеупомянутые R2 и R3, оба, являются метильными группами и вышеупомянутый R4 является гидроксильной группой
-СН2-СН2-СН2-СН(СН3)2
-СН2-СН2-CHRa-С(СН3)2Rb
(где Ra является любым из атома водорода, гидроксильной или метильной групп, а Rb является атомом водорода или гидроксильной группой)
-СН2-СН2-СН(СН2СН3)-СН(СН3)2
-СН2-СН2-CHRc-С(СН3)=СН2
(где Rc является любым из атома водорода, гидроксильной или метильной групп)
-СН2-СН2-С(=О)-С(СН3)=СН2
-СН2-СН2-С(=СН2)-СН(СН3)2
-СН2-СН2-СН=С(СН3)2
-СН2-СН=С(СН3)-СН(СН3)2
-СН2-СН2-С(=СНСН3)-СН(СН3)2.
6) Вышеупомянутое соединение по 5) является 9,19-циклоланостан-3-олом или 24-метилен-9,19-циклоланостан-3-олом.
Третьим изобретением настоящей заявки для разрешения вышеупомянутых проблем являются пищевой продукт или напиток, содержащие агент для снижения инсулинорезистентности, по первому и второму изобретению.
В дополнение, следующий пункт 7) является предпочтительным вариантом осуществления настоящего изобретения.
7) Пищевой продукт или напиток содержат 0,0001% по сухой массе или более соединения, представленного вышеупомянутой общей формулой (1).
Четвертым изобретением настоящей заявки для разрешения вышеупомянутых проблем является применение соединения, представленного вышеупомянутой общей формулой (1), или экстракта растения органическим растворителем, или экстракта растения горячей водой, содержащего, по меньшей мере, 0,001% по сухой массе соединения, или его фракции в производстве агента для снижения инсулинорезистентности.
Пятым изобретением настоящей заявки для разрешения вышеупомянутых проблем является способ снижения инсулинорезистентности, включающий введение соединения, представленного вышеупомянутой общей формулой (1), или экстракта растения органическим растворителем, или экстракта растения горячей водой, содержащего, по меньшей мере, 0,001% по сухой массе соединений, или его фракции пациенту, у которого должна быть снижена инсулинорезистентность.
В вышеупомянутом применении и способе настоящего изобретения предпочтительный вариант соединения, представленного вышеупомянутой общей формулой (1), является тем же самым, что и соединение второго аспекта настоящего изобретения.
Агент для снижения инсулинорезистентности настоящего изобретения и пищевой продукт или напиток, содержащие его, могут быть безопасно введены или приняты внутрь и обладают профилактическими эффектами на болезни, связанные с образом жизни, которые, как считается, вызывают инсулинорезистентность. Кроме того, активный ингредиент агента для снижения инсулинорезистентности настоящего изобретения может быть легко получен из растения семейства Liliaceae, такого как алоэ вера (Aloe barbadensis Miller), которое является легкодоступным и, как известно из эмпирического опыта, может быть безопасно принято внутрь.
Краткое описание чертежей
На чертеже представлен график, показывающий изменение уровня содержания глюкозы в крови в инсулиновом тесте толерантности.
Лучший вариант осуществления изобретения
Далее будет приведено подробное описание предпочтительных вариантов осуществления настоящего изобретения. Однако настоящее изобретение не ограничено следующими предпочтительными вариантами осуществления и может быть свободно модифицировано в объеме настоящего изобретения. В дополнение, используемое здесь процентное содержание указывает массу, если особо не оговорено другое.
Соединение, используемое как активный ингредиент агента для снижения инсулинорезистентности (далее именуемое «агент настоящего изобретения») настоящего изобретения, включает любые соединения и производные, если они имеют структуру, представленную вышеупомянутой общей формулой (1), и обладают эффектом снижения инсулинорезистентности (далее также именуемое «соединение настоящего изобретения»).
Наиболее предпочтительным является, чтобы чистота соединения настоящего изобретения, используемого в качестве активного ингредиента агента для снижения инсулинорезистентности настоящего изобретения, была 100%. Однако чистота соответственно может находиться в пределах, в которых агент обладает эффектом снижения инсулинорезистентности.
Кроме того, композиция, используемая в качестве активного ингредиента агента для снижения инсулинорезистентности настоящего изобретения (далее также именуемая «композиция настоящего изобретения»), является экстрактом растения семейства Liliaceae или Gramineae или его фракцией, содержащими, по меньшей мере, 0,001% по сухой массе или больше, предпочтительно, 0,01% по сухой массе или больше и, более предпочтительно, 0,1% по сухой массе или больше вышеупомянутого соединения, представленного общей формулой (1). Верхняя граница содержания соединения настоящего изобретения конкретно не ограничена, и она может быть равна, например, предпочтительно, 10% по массе или 50% по массе, 70% по массе или 90% по массе.
В настоящем изобретении сухая масса означает массу, измеренную после высушивания соединения посредством способа сушки, определенного в «тесте потери веса», являющегося общим тестовым способом, описанным в Japanese Pharmacopoeia, 14th Revision (March 30, 2001, the Ministry of Health, Labor and Welfare, Ministerial Notification No.111). Например, масса соединения настоящего изобретения может быть определена этим способом так: примерно 1 г соединения настоящего изобретения измеряли и высушивали при 105°С в течение 4 часов; и получившийся материал остужали в эксикаторе; и массу соединения взвешивали на весах.
По варианту осуществления настоящего изобретения агент для снижения инсулинорезистентности настоящего изобретения и содержащие его пищевой продукт или напиток содержат соединение, имеющее циклоланостановый скелет, которое обладает эффектом снижения инсулинорезистентности, в качестве активного ингредиента. Циклоланостановый скелет является соединением, представленным следующей общей формулой (2)
Конкретные примеры соединения, имеющего циклоланостановый скелет, включают соединения, представленные вышеупомянутой общей формулой (1). Количество двойных связей, присутствующих в соединении, имеющем циклоланостановый скелет, не является конкретно ограниченным. Далее, число двойных связей, присутствующих в кольце, также не является конкретно ограниченным. Когда присутствуют одна или две двойные связи, они могут быть сопряжены. Агент и пищевой продукт или напиток настоящего изобретения могут содержать два или более типов соединений настоящего изобретения.
В соединении настоящего изобретения вышеупомянутой общей формулы (1) R1 является алкильной группой или алкенильной группой, содержащей 1 или 2 двойные связи, которая имеет прямую или разветвленную цепь, содержащую от 6 до 8 атомов углерода, или замещенной алкильной или алкенильной группой, в которой один или два атома водорода алкильной или алкенильной группы замещены гидроксильными группами и/или карбонильными группами, R2 и R3, каждый независимо, являются атомами водорода или метильными группами, и R4 образует С=О с атомом углерода в составе кольца или является группой, представленной одной из следующих формул
В вышеупомянутой общей формуле (1) R1 предпочтительно является любой из групп, представленных следующими формулами:
(i) -СН2-СН2-СН2-СН(СН3)2
(ii) -СН2-СН2-CHRa-С(СН3)2Rb
(где Ra является любым из атома водорода, гидроксильной или метильной групп, а Rb является атомом водорода или гидроксильной группой)
(iii) -СН2-СН2-СН(СН2СН3)-СН(СН3)2
(iv) -СН2-СН2-CHRc-С(СН3)=СН2
(где Rc является любым из атома водорода, гидроксильной или метильной групп)
(v) -СН2-СН2-С(=О)-С(СН3)=СН2
(vi) -СН2-СН2-С(=СН2)-СН(СН3)2
(vii) -СН2-СН2-СН=С(СН3)2
(viii) -СН2-СН=С(СН3)-СН(СН3)2
(ix) -СН2-СН2-С(=СНСН3)-СН(СН3)2.
Далее, в вышеупомянутой общей формуле (1) предпочтительным является, чтобы R2 и R3, оба, являлись метильными группами, и вышеупомянутый R4 являлся гидроксильной группой. Наиболее предпочтительными соединениями являются те, что представлены следующими формулами: 9,19-циклоланостан-3-олом (формулой (3)) и 24-метилен-9,19-циклоланостан-3-олом (формулой (4))
То есть 9,19-циклоланостан-3-ол является соединением, представленным вышеупомянутой общей формулой (1), где R2 и R3 являются метильными группами и R4 является гидроксильной группой, а R1 является группой, представленной вышеупомянутой формулой (i). Далее, 24-метилен-9,19-циклоланостан-3-ол является соединением, представленным вышеупомянутой общей формулой (1), где R2 и R3 являются метильными группами и R4 является гидроксильной группой, а R1 является группой, представленной вышеупомянутой формулой (vi).
Соединение настоящего изобретения может являться циклоартенолом (формула (5)) или 24-метилцилклоартанолом (формула (7)). Оба эти соединения являются соединениями, представленными вышеупомянутой общей формулой (1), где R2 и R3 являются метильными группами и R4 является гидроксильной группой, а R1 является группой, представленной вышеупомянутой формулой (vii), в циклоартеноле или группой, представленной вышеупомянутой формулой (ii) (Ra=CH3, Rb=H), в 24-метилциклоартаноле.
Соединение настоящего изобретения может быть получено химическим синтезом с помощью известного способа получения. Например, способы получения циклоартенола (формула (5)) и 24-метиленциклоартанола (общепринятое название для 24-метилен-9,19-циклоланостан-3-ола) (формула (4)) были раскрыты в патенте Японии, опубликованном под №57-018617, способ получения ферулата циклоартенола (формула (6)) из γ-оризанола и способ синтеза соединения с применением его гидролизата в качестве исходного вещества раскрыты в патенте Японии, опубликованном под №2003-277269. Далее, когда R1 фрагмент из общей формулы (1) содержит двойную связь, можно получить различные производные соединения при использовании методики превращения двойной связи в альдегид с помощью реакции разложения под воздействием озона и связывания фосфоната с ним, методики добавления водорода к двойной связи или методики окисления двойной связи озоном и превращения ее в альдегид или кислоту. Далее, способы получения не являются ограниченными только методами химического синтеза, и соединения могут быть получены с помощью биологических методов посредством использования микроорганизмов и т.п. В качестве альтернативы они могут быть получены посредством использования ферментов, полученных из микроорганизмов.
Агент для снижения инсулинорезистентности настоящего изобретения и пищевой продукт или напиток, содержащие его, могут содержать один тип, или два, или больше произвольно выбранных типов вышеупомянутых соединений.
Известно, что соединения, имеющие циклоланостановый скелет, содержатся в растениях семейств Liliaceae, Leguminosae, Gramineae, Solanaceae, Musaceae и т.д. (см. Phytochemistry, U.S.A., 1977, Vol.16, p.140-141; Handbook of phytochemical constituents of GRAS herbs and other economic plants, 1992, U.S.A., CRS Press; Hager's Handbuch der Pharmazeutischen Praxis, Vols. 2-6, 1969-1979, Germany, Springer-Verlag Berlin). Соответственно, соединения могут быть получены посредством экстракции из этих растений, их части или гомогената с использованием способа, такого как экстракция органическим растворителем или экстракция горячей водой, и концентрирования их.
Конкретные примеры растения, принадлежащего к семейству Liliaceae, включают растения, принадлежащие родам Aloe или Allium. Примеры растений рода Aloe включают алоэ вера (Aloe barbadensis Miller), Aloe ferox Miller, Aloe africana Miller, Aloe arborescen Miller var. natalensis Berger, Aloe spicata Baker и т.д. В производстве соединения настоящего изобретения или состава, содержащего его, хотя можно использовать целое растение, предпочтительным является использование его мезофилла (прозрачной гелеобразной части). Такое растение или его часть разрушают с использованием гомогенизатора и т.п., и таким образом превращают его в жидкость, и экстрагируют соединение настоящего изобретения или состав, содержащий его, из продукта разрушения, используя органический растворитель или горячую воду. Примеры органического растворителя включают спирты, такие как метанол, этанол и бутанол; сложные эфиры, такие как метилацетат, этилацетат, пропилацетат и бутилацетат; кетоны, такие как ацетон и метилизобутилкетон; простые эфиры, такие как диэтиловый эфир и петролейный эфир; углеводороды, такие как гексан, циклогексан, толуол и бензол; галогенированные углеводороды, такие как четыреххлористый углерод, дихлорметан и хлороформ; гетероциклические соединения, такие как пиридин; гликоли, такие как этиленгликоль; многоатомные спирты, такие как полиэтиленгликоль; нитрильные растворители, такие как ацетонитрил, смеси этих соединений и т.д. Кроме того, эти растворители могут быть безводными или содержать воду. Среди этих растворителей предпочтительными являются смеси этилацетат/бутанол (3:1) и хлороформ/метанол (2:1).
В качестве способа экстракции может быть применен способ для обычной экстракции растительных компонентов. Обычно используемым является, например, нагревание с обратным холодильником от 1 до 300 массовых частей органического растворителя с 1 массовой частью свежего растения или высушенного растения до температуры кипения растворителя или ниже и перемешивание или встряхивание, или проведение экстракции ультразвуком при комнатной температуре. Экстракт-сырец можно получить отделением нерастворимых частей от экстракционной жидкости, используя подходящий способ, такой как фильтрование или центрифугирование.
Экстракт-сырец можно очистить с помощью различных типов хроматографии, таких как нормальная или обращенно-фазовая колоночная хроматография на силикагеле. Когда используется градиент смеси хлороформ/метанол в качестве элюирующего растворителя в нормально-фазовой колоночной хроматографии на силикагеле, соединение настоящего изобретения элюируется при соотношении хлороформ:метанол=примерно 25:1. Кроме того, при использовании смеси гексан/этилацетат (4:1) в качестве элюирующего растворителя в обращенно-фазовой колоночной хроматографии на силикагеле, соединение настоящего изобретения элюируется во фракции, элюируемой на ранней стадии. Полученная фракция может далее быть очищена с помощью ВЭЖХ или т.п.
Далее, соединение, используемое для настоящего изобретения, может также быть получено посредством химического синтеза или биологическими или ферментативными методами с использованием микроорганизмов, ферментов или т.п.
Действительно ли соединение или состав настоящего изобретения, полученные, как описано выше, содержат соединение настоящего изобретения, может быть подтверждено, например, с помощью масс-спектрометрии (МС), ядерного магнитного резонанса (ЯМР) или т.п.
Соединение настоящего изобретения может быть использовано в качестве активного ингредиента агента для снижения инсулинорезистентности настоящего изобретения и пищевого продукта или напитка, содержащего его, как оно есть. Далее, экстракт растения органическим растворителем, или экстракт растения горячей водой, содержащие соединение настоящего изобретения, или его фракции (далее именуемые «экстракт и т.д.») могут также быть использованы в качестве активного ингредиента агента для снижения инсулинорезистентности настоящего изобретения и пищи или напитка, содержащего его. В дополнение, когда алоэ вера используется в качестве растения семейства Liliaceae, предпочтительным является, чтобы общее содержание алоина и алоэ-эмодина, которые содержатся в большом количестве в коже листьев алоэ вера, являлось 5 ч/млн (частей на миллион) или меньше.
Вышеупомянутый экстракт и т.д., который содержится в агенте для снижения инсулинорезистентности, предпочтительно содержит, по меньшей мере, 0,001% по сухой массе, более предпочтительно, от 0,01 до 1% по сухой массе, особенно предпочтительно, от 0,05 до 1% по сухой массе соединения настоящего изобретения. Далее, вышеупомянутый экстракт и т.д., который содержится в пище или напитке, предпочтительно содержит, по меньшей мере, 0,0001% по сухой массе, более предпочтительно, от 0,001 до 1% по сухой массе, особенно предпочтительно, от 0,005 до 1% по сухой массе соединения настоящего изобретения. Вышеупомянутый экстракт и т.д. может содержать два или более типов соединения настоящего изобретения. Далее, вышеупомянутый экстракт и т.д. может являться раствором или может также быть лиофилизированным или высушенным распылением обычными методами и храниться или использоваться в виде порошка.
В качестве агента для снижения инсулинорезистентности настоящего изобретения соединение настоящего изобретения или композиция, содержащая его, такая как экстракт и т.п. как таковой, или они же, смешанные с фармацевтически приемлемым носителем, могут быть введены перорально или парентерально млекопитающему, включая человека. В агенте настоящего изобретения соединение может являться фармацевтически приемлемой солью. Примеры фармацевтически приемлемых солей включают как соли металлов (неорганические соли), так и органические соли, включающие, например, перечисленные в “Remington's Pharmaceutical Sciences,” 17th edition, p.1418, 1985. Конкретные примеры солей в